物质的除杂(提纯)检验(浙江省宁波市海曙区)
文档属性
| 名称 | 物质的除杂(提纯)检验(浙江省宁波市海曙区) |

|
|
| 格式 | rar | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2008-09-09 00:00:00 | ||
图片预览







文档简介
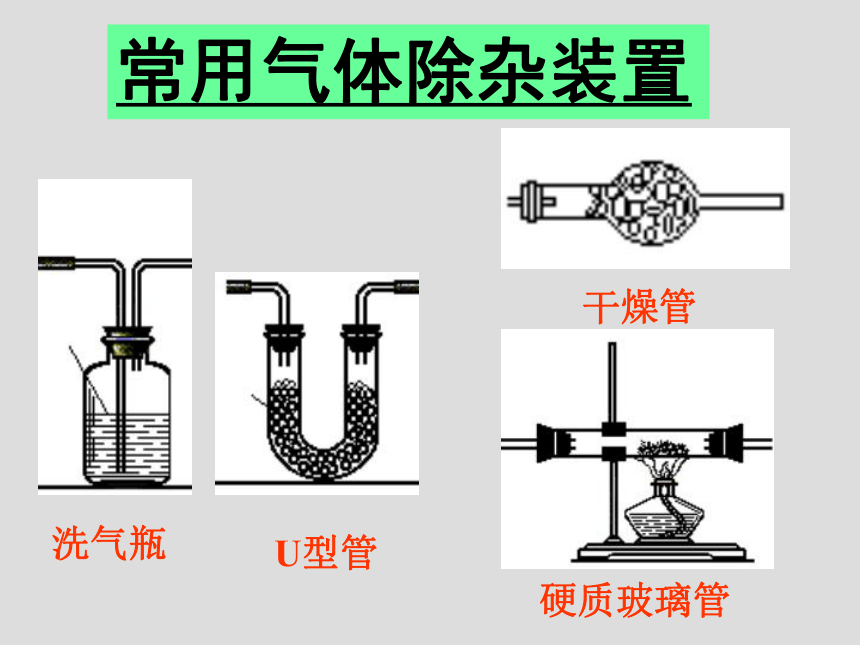
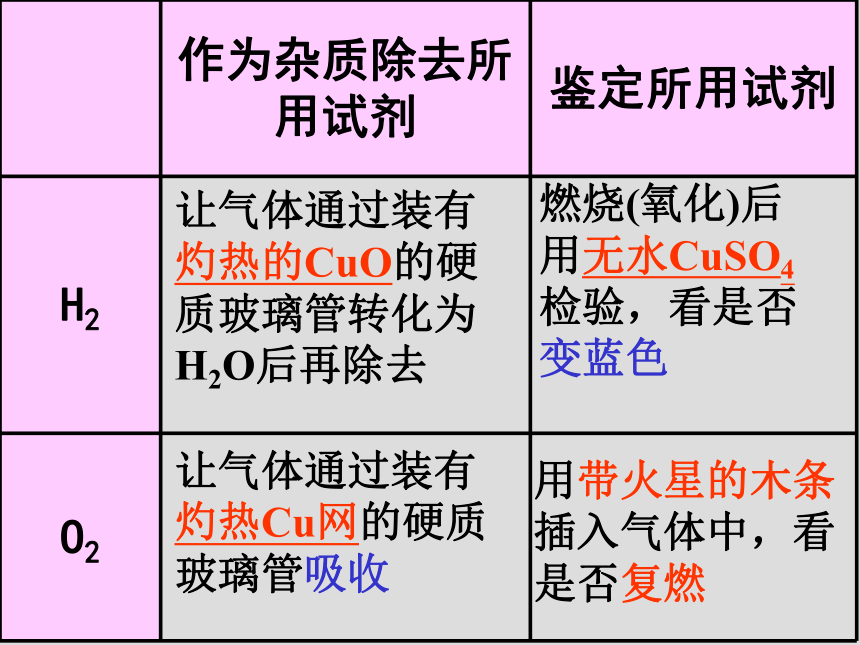
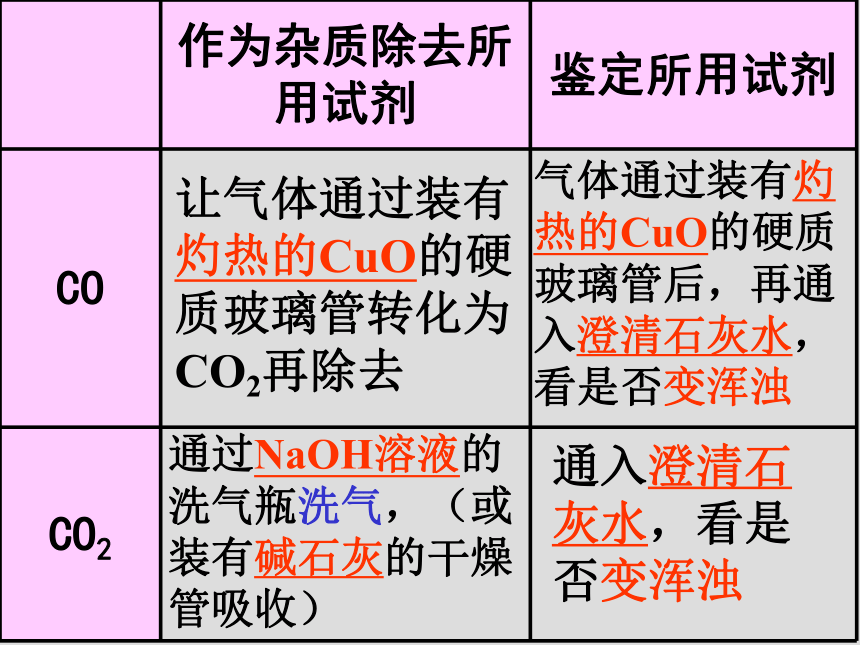
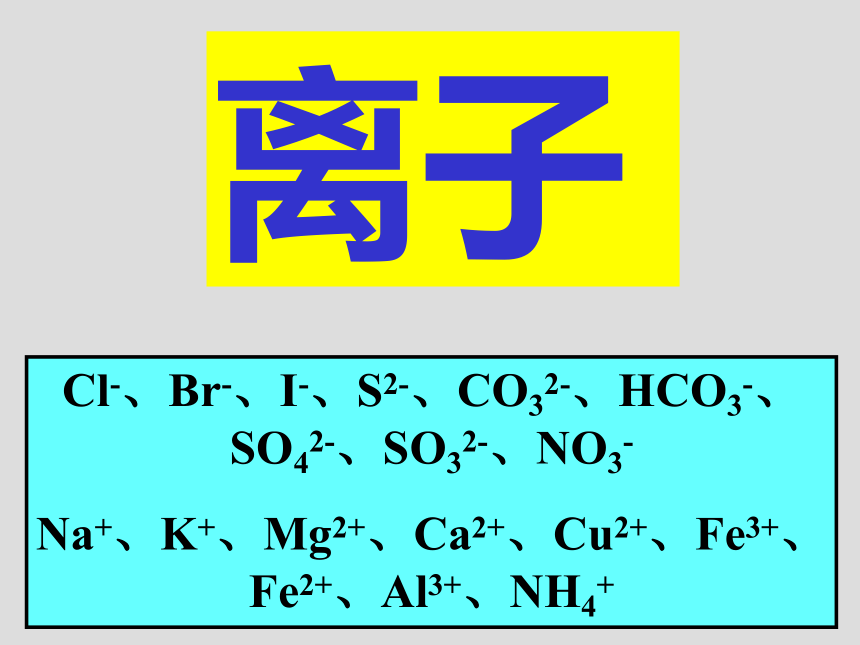
课件36张PPT。物质的除杂(提纯) 检 验气体H2、O2、N2、Cl2 CH4、C2H2、C2H4、NH3 、 HCl、H2S CO、CO2、NO、NO2 、 SO2常用气体除杂装置洗气瓶U型管干燥管硬质玻璃管让气体通过装有灼热的CuO的硬质玻璃管转化为H2O后再除去燃烧(氧化)后用无水CuSO4检验,看是否变蓝色让气体通过装有灼热Cu网的硬质玻璃管吸收用带火星的木条插入气体中,看是否复燃让气体通过装有灼热的CuO的硬质玻璃管转化为CO2再除去气体通过装有灼热的CuO的硬质玻璃管后,再通入澄清石灰水,看是否变浑浊通过NaOH溶液的洗气瓶洗气,(或装有碱石灰的干燥管吸收)通入澄清石灰水,看是否变浑浊通过NaOH溶液的洗气瓶洗气, (或通过装有××饱和溶液的洗气瓶洗气)通入品红溶液或(酸性KMnO4溶液) ,看是否褪色通过水的洗气瓶洗气,(或通过装有××饱和溶液的洗气瓶洗气)用湿润的蓝色石蕊试纸靠近气体,看是否变红色(或用蘸有浓氨水的玻璃棒靠近,看是否有大量白烟)通过装有水的洗气瓶洗气,(或通过装有稀H2SO4溶液的洗气瓶洗气)用湿润的红色石蕊试纸靠近气体,看是否变蓝色(或用蘸有浓盐酸的玻璃棒靠近,看是否有大量白烟)通过装有碱石灰的干燥管吸收,(或通过装有浓H2SO4的洗气瓶洗气)通过无水CuSO4 ,看是否变蓝色离子Cl-、Br-、I-、S2-、CO32-、HCO3-、SO42-、SO32-、NO3-
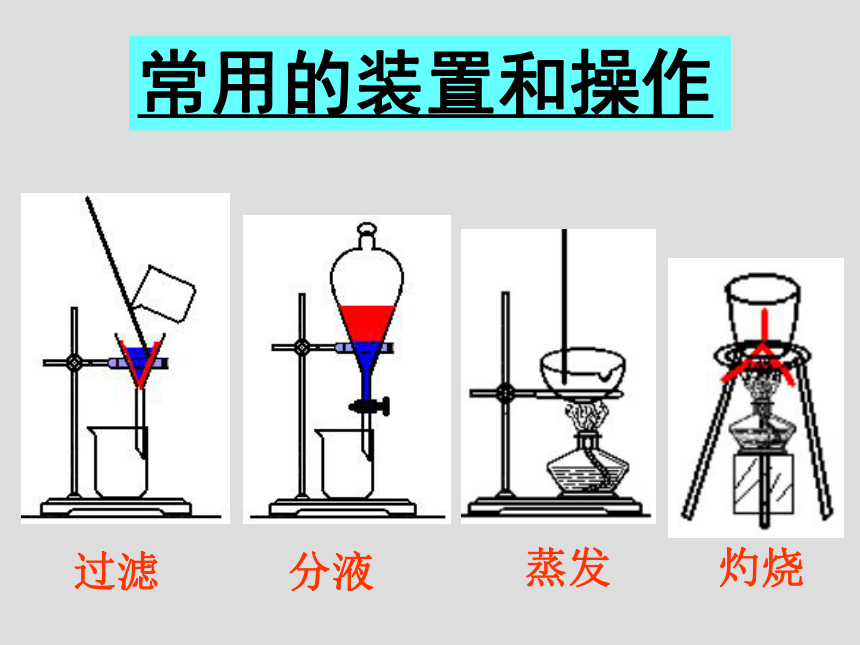
Na+、K+、Mg2+、Ca2+、Cu2+、Fe3+、Fe2+、Al3+、NH4+过滤分液蒸发灼烧常用的装置和操作加AgNO3溶液将其转化为沉淀,过滤除去加AgNO3溶液将其转化为沉淀,过滤除去;或加氯水转化为单质,再用有机溶剂萃取除去用稀HNO3酸化后,再加AgNO3溶液,看沉淀的颜色问题:1、如何除去NaCl固体中的NaBr、NaI?2、如何从海带中制取单质碘?加稀HCl,将其转化成气体除去;或加Ca2+使其转化为沉淀,过滤除去加稀HCl,将其转化成气体除去加稀HCl,有无色、无味的气体产生,将该气体通入澄清石灰水,变浑浊1、工业上在粗盐提纯的操作中有这样一步:向溶液中加入过量的纯碱,过滤。这步操作后再如何操作就可得到精制的食盐水了?2、如何除去混在KCl中的KHCO3,得到纯净的KCl。 问题:加Ba2+使其转化为沉淀,过滤除去先用稀HCl酸化,无明显现象,再加BaCl2溶液,看有无白色沉淀加稀HCl,将其转化成气体除去;或加Ca2+、Ba2+使其转化为沉淀,过滤除去先加BaCl2溶液,有白色沉淀,用盐酸酸化,沉淀消失,且有刺激性气体产生 实验室需要一些纯净的氯化钾。现有的氯化钾样品中含有少量的KI、K2SO4、NH4Cl,按照下列实验方案提纯氯化钾。问题:(1)固体应在 中加热;
(2)能否用Ba(OH)2代替BaCl2?理由。
(3)证明SO42-已完全沉淀的方法是 。
(4)过滤操作所使用的仪器为 。加浓H2SO4,同时加金属Cu,有红棕色气体产生加Cu2+, 使其转化为沉淀,过滤除去加Cu2+,有黑色沉淀生成;或加H+,有臭鸡蛋味产生 有一溶液中,存在着K+、NH4+、SO42-、S2 -,Cl-。现要将其中的阴离子依次一一除去,应如何选择试剂?按怎样的顺序加入?最后溶液中的阴离子是什么?问题:焰色反应,焰色为黄色焰色反应,焰色为浅紫色(透过蓝色钴玻璃片观察)加CO32-, 使其转化为沉淀,过滤除去加OH-, 使其转化为沉淀,过滤除去焰色反应,
焰色为砖红色 某井水经测定,含有较多的Ca2+和Mg2+。请你选用较为价廉的药品除去水的Ca2+和Mg2+。问题: 粗盐中含有泥沙和CaCl2、MgSO4等杂质。试从①NaOH溶液②Ba(OH)2溶液③Ca(OH)2溶液④K2CO3溶液⑤ Na2CO3溶液⑥ BaCl2溶液⑦ H2SO4溶液⑧ HCl溶液中,选择恰当的试剂,设计合理的顺序,对此粗盐进行提纯,你认为还需要什么试剂吗?问题:加OH-, 使其转化为沉淀,过滤除去;或转化。加OH-, 使其转化为沉淀,过滤除去;或转化。加SCN-离子的溶液,看溶液是否变血红色;或加苯酚溶液,变紫色加OH-, 出现白色沉淀,马上转变为灰绿色,最后变为红裼色。 某溶液含有较多的Na2SO4和少量的Fe2(SO4)3.若用该溶液制取芒硝,可供选择的操作有:①加适量H2SO4溶液,②加金属Na,③结晶,④加过量NaOH溶液,⑤加强热脱结晶水, ⑥过滤.正确的操作步骤是
(A)②⑥③ (B)④⑥①③ (C)④⑥③⑤ (D)②⑥①③⑤ 问题:通H2S(或加OH-),使其转化为沉淀,过滤除去本身有颜色,加NaOH溶液有蓝色沉淀通NH3(或加氨水),使其转化为沉淀,过滤除去逐滴加NaOH溶液有白色沉淀,继续加过量NaOH溶液,白色沉淀消失 为了除去酸性AlCl3溶液中的Cu2+,进行如下实验:(1)通入CO2气体;(2)加盐酸;(3)加过量的NaOH溶液;(4)加H2SO4;(5)过滤。以下步骤顺序和试剂正确的是
A、 (3)(5)(4)(5)(2) B、 (3)(5)(2) C、 (3)(5)(1)(2) D、(3)(5)(1)(5)(2)问题:加OH-,加热向试管中的试样中,加OH-,加热,用湿润的红色石蕊试纸靠近,变蓝色练习:1、请在下表中画出对应的连线,其中Ⅰ栏为含有杂质的试剂(括号内为杂质),Ⅱ为对应的除去杂质的试剂,Ⅲ为对应的除杂操作或仪器,Ⅳ为检验杂质是否已除干尽的试剂。CO2(HCl)SO2(HCl)H2S(HCl)CO2(SO2)Cl2(HCl)NO(NO2)2、下列气体中的杂质气体如何除去(括号中为杂质)?通过饱和NaHCO3溶液通过饱和NaHSO3溶液通过饱和NaHS溶液通过饱和NaCL溶液通过饱和NaHCO3溶液水FeCl3(FeCl2)FeCl2(FeCl3)通入适量Cl2
或加适量H2O2和HCl加入还原铁粉(或铁钉)和稀HCl3、下列物质中的杂质如何除去(括号中为杂质)?Na2CO3(NaHCO3)NaHCO3 ( Na2CO3 )给固体加强热到质量不再变化为止制成溶液,通足量的CO2,低温蒸干溶液得晶体4、为了除去酸性ZnCl2溶液中的FeCl3,可在加热搅拌时加入一种试剂,使溶液的pH升高,过滤后,再向滤液中加入适量的盐酸,该试剂是
A、KOH B、K2CO3
C、ZnSO4 D、Zn(OH)2若是CaCl2溶液中有FeCl3、CuCl2溶液中有FeCl3应加什么物质? 5、有一种工业废水,已知其中含有多量的FeSO4,少量的Ag+、Na+、污泥,试设计一个既经济又合理的方法回收金属银和硫酸亚铁晶体,分步列出实验步骤,说明每一步骤的目的。 6、下列实验方案的目的,是将某废液中含有的Cu2+、Zn2+、K+、Na+、NO3-、Br-等离子进行分离,并制得Br2的CCl4溶液,金属铜,KNO3晶体,NaCl晶体和皓矾。(1)请在下列表中填写各操作步骤①~⑧所加的试剂名称和用量,以及分离方法(可重复使用)。如该操作步骤不需要加试剂或分离,请在格中划一斜线。(2)上述分离方法中不需要玻璃棒的是:
Na+、K+、Mg2+、Ca2+、Cu2+、Fe3+、Fe2+、Al3+、NH4+过滤分液蒸发灼烧常用的装置和操作加AgNO3溶液将其转化为沉淀,过滤除去加AgNO3溶液将其转化为沉淀,过滤除去;或加氯水转化为单质,再用有机溶剂萃取除去用稀HNO3酸化后,再加AgNO3溶液,看沉淀的颜色问题:1、如何除去NaCl固体中的NaBr、NaI?2、如何从海带中制取单质碘?加稀HCl,将其转化成气体除去;或加Ca2+使其转化为沉淀,过滤除去加稀HCl,将其转化成气体除去加稀HCl,有无色、无味的气体产生,将该气体通入澄清石灰水,变浑浊1、工业上在粗盐提纯的操作中有这样一步:向溶液中加入过量的纯碱,过滤。这步操作后再如何操作就可得到精制的食盐水了?2、如何除去混在KCl中的KHCO3,得到纯净的KCl。 问题:加Ba2+使其转化为沉淀,过滤除去先用稀HCl酸化,无明显现象,再加BaCl2溶液,看有无白色沉淀加稀HCl,将其转化成气体除去;或加Ca2+、Ba2+使其转化为沉淀,过滤除去先加BaCl2溶液,有白色沉淀,用盐酸酸化,沉淀消失,且有刺激性气体产生 实验室需要一些纯净的氯化钾。现有的氯化钾样品中含有少量的KI、K2SO4、NH4Cl,按照下列实验方案提纯氯化钾。问题:(1)固体应在 中加热;
(2)能否用Ba(OH)2代替BaCl2?理由。
(3)证明SO42-已完全沉淀的方法是 。
(4)过滤操作所使用的仪器为 。加浓H2SO4,同时加金属Cu,有红棕色气体产生加Cu2+, 使其转化为沉淀,过滤除去加Cu2+,有黑色沉淀生成;或加H+,有臭鸡蛋味产生 有一溶液中,存在着K+、NH4+、SO42-、S2 -,Cl-。现要将其中的阴离子依次一一除去,应如何选择试剂?按怎样的顺序加入?最后溶液中的阴离子是什么?问题:焰色反应,焰色为黄色焰色反应,焰色为浅紫色(透过蓝色钴玻璃片观察)加CO32-, 使其转化为沉淀,过滤除去加OH-, 使其转化为沉淀,过滤除去焰色反应,
焰色为砖红色 某井水经测定,含有较多的Ca2+和Mg2+。请你选用较为价廉的药品除去水的Ca2+和Mg2+。问题: 粗盐中含有泥沙和CaCl2、MgSO4等杂质。试从①NaOH溶液②Ba(OH)2溶液③Ca(OH)2溶液④K2CO3溶液⑤ Na2CO3溶液⑥ BaCl2溶液⑦ H2SO4溶液⑧ HCl溶液中,选择恰当的试剂,设计合理的顺序,对此粗盐进行提纯,你认为还需要什么试剂吗?问题:加OH-, 使其转化为沉淀,过滤除去;或转化。加OH-, 使其转化为沉淀,过滤除去;或转化。加SCN-离子的溶液,看溶液是否变血红色;或加苯酚溶液,变紫色加OH-, 出现白色沉淀,马上转变为灰绿色,最后变为红裼色。 某溶液含有较多的Na2SO4和少量的Fe2(SO4)3.若用该溶液制取芒硝,可供选择的操作有:①加适量H2SO4溶液,②加金属Na,③结晶,④加过量NaOH溶液,⑤加强热脱结晶水, ⑥过滤.正确的操作步骤是
(A)②⑥③ (B)④⑥①③ (C)④⑥③⑤ (D)②⑥①③⑤ 问题:通H2S(或加OH-),使其转化为沉淀,过滤除去本身有颜色,加NaOH溶液有蓝色沉淀通NH3(或加氨水),使其转化为沉淀,过滤除去逐滴加NaOH溶液有白色沉淀,继续加过量NaOH溶液,白色沉淀消失 为了除去酸性AlCl3溶液中的Cu2+,进行如下实验:(1)通入CO2气体;(2)加盐酸;(3)加过量的NaOH溶液;(4)加H2SO4;(5)过滤。以下步骤顺序和试剂正确的是
A、 (3)(5)(4)(5)(2) B、 (3)(5)(2) C、 (3)(5)(1)(2) D、(3)(5)(1)(5)(2)问题:加OH-,加热向试管中的试样中,加OH-,加热,用湿润的红色石蕊试纸靠近,变蓝色练习:1、请在下表中画出对应的连线,其中Ⅰ栏为含有杂质的试剂(括号内为杂质),Ⅱ为对应的除去杂质的试剂,Ⅲ为对应的除杂操作或仪器,Ⅳ为检验杂质是否已除干尽的试剂。CO2(HCl)SO2(HCl)H2S(HCl)CO2(SO2)Cl2(HCl)NO(NO2)2、下列气体中的杂质气体如何除去(括号中为杂质)?通过饱和NaHCO3溶液通过饱和NaHSO3溶液通过饱和NaHS溶液通过饱和NaCL溶液通过饱和NaHCO3溶液水FeCl3(FeCl2)FeCl2(FeCl3)通入适量Cl2
或加适量H2O2和HCl加入还原铁粉(或铁钉)和稀HCl3、下列物质中的杂质如何除去(括号中为杂质)?Na2CO3(NaHCO3)NaHCO3 ( Na2CO3 )给固体加强热到质量不再变化为止制成溶液,通足量的CO2,低温蒸干溶液得晶体4、为了除去酸性ZnCl2溶液中的FeCl3,可在加热搅拌时加入一种试剂,使溶液的pH升高,过滤后,再向滤液中加入适量的盐酸,该试剂是
A、KOH B、K2CO3
C、ZnSO4 D、Zn(OH)2若是CaCl2溶液中有FeCl3、CuCl2溶液中有FeCl3应加什么物质? 5、有一种工业废水,已知其中含有多量的FeSO4,少量的Ag+、Na+、污泥,试设计一个既经济又合理的方法回收金属银和硫酸亚铁晶体,分步列出实验步骤,说明每一步骤的目的。 6、下列实验方案的目的,是将某废液中含有的Cu2+、Zn2+、K+、Na+、NO3-、Br-等离子进行分离,并制得Br2的CCl4溶液,金属铜,KNO3晶体,NaCl晶体和皓矾。(1)请在下列表中填写各操作步骤①~⑧所加的试剂名称和用量,以及分离方法(可重复使用)。如该操作步骤不需要加试剂或分离,请在格中划一斜线。(2)上述分离方法中不需要玻璃棒的是:
