华师大版九年级下册 第三章 物质的转化和元素的循环 1.物质的转化(浙江省宁波市慈溪市)
文档属性
| 名称 | 华师大版九年级下册 第三章 物质的转化和元素的循环 1.物质的转化(浙江省宁波市慈溪市) |

|
|
| 格式 | rar | ||
| 文件大小 | 140.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2008-09-25 00:00:00 | ||
图片预览





文档简介
课件18张PPT。
思考:
请你仔细观察周围的各种物质,它们是从哪里来的?又会到哪里去?在这些过程中物质之间是否发生了转化?物质 根据组成
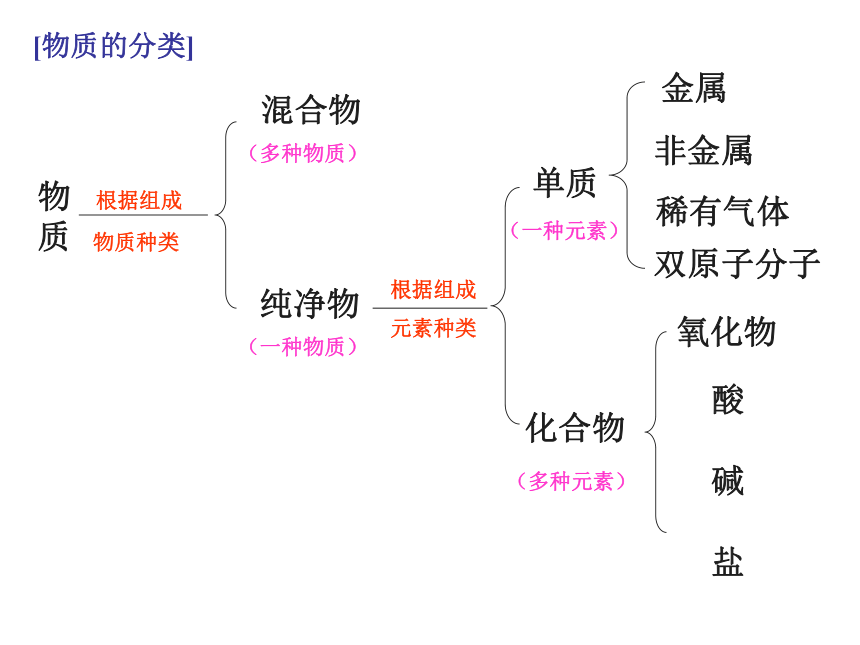
物质种类 混合物纯净物 根据组成
元素种类单质化合物 氧化物 酸碱盐金属非金属稀有气体双原子分子(多种物质)(一种物质)(一种元素)(多种元素)[物质的分类]二 单质、氧化物、酸(碱)之间的转化1.取一药匙硫黄,观察其外观: _____________________________________。
2.将硫黄放到燃烧匙中,在酒精灯上点燃硫黄,观察现象:___________________________________。
3.把燃烧着的硫黄放进盛的氧气的集气瓶内,观察现象:______________________________________
用化学方程式: _______________________。实验一:硫在空气及氧气中燃烧.swf淡黄色固体淡蓝色火焰,生成刺激性气味且有毒的气体蓝紫色火焰,生成刺激性气味且有毒的气体非金属单质与其化合物的转化酸雨当雨水被二氧化碳饱和时,略呈酸性,pH值为5.65。当大气被酸性气体污染时,pH值小于5.65的雨叫酸雨;pH值小于5.65的雪叫酸雪;在高空或高山上弥漫的雾,pH值小于5.65时叫酸雾。
煤中的硫燃烧生成_______,它在粉尘的催化作用下跟O2反应生成________,再与雨水结合生成硫酸。相关的化学方程式是:
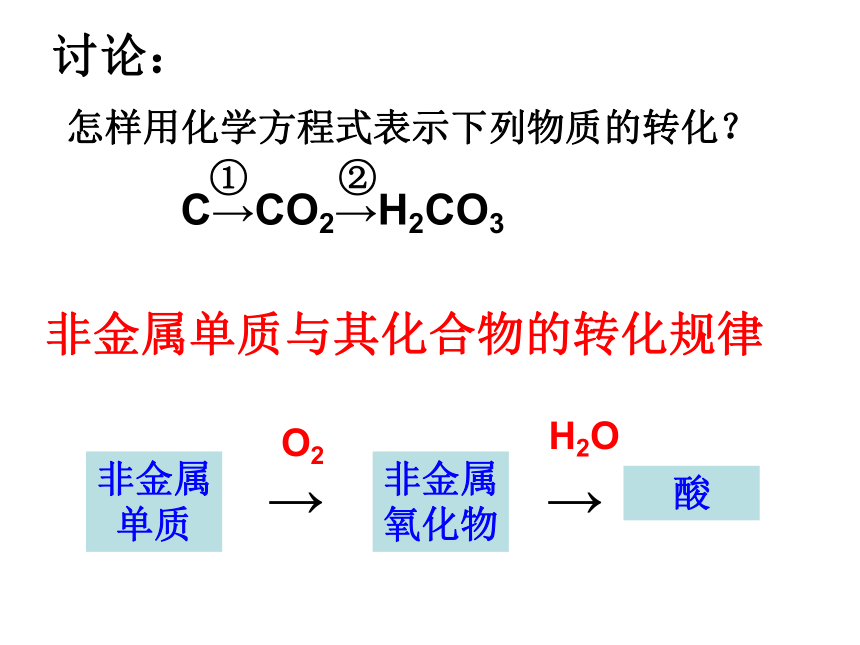
酸雨的形成SO2SO3SO3+ H2O = H2SO4怎样用化学方程式表示下列物质的转化?C→CO2→H2CO3①②非金属单质与其化合物的转化规律O2H2O讨论:你能用化学方程式来表示下列物质之间的转化吗?
O2H2O金属的氧化CuO + H2SO4 = CuSO4 + H2OCuSO4 +2NaOH = Cu(OH)2 ↓+Na2SO4钾钙钠的氧化物+水→碱K 2 O + H2O= 2KOH其他金属氧化物不溶于水,跟水不反应Ca O + H2O= Ca(OH)2Na 2 O + H2O= 2NaOH+ O2+ H2O金属1.Ca→CaO→Ca(OH)2 →CaCO32)CaO + H2O = Ca(OH)23)Ca(OH)2 + CO2 = CaCO3 + H2O讨论:分析下列物质的变化讨论:分析下列物质的变化2.C→CO2→H2CO3 →Na2CO32)CO2 + H2O = H2CO33)H2CO3 + 2NaOH = Na2CO3 + H2O+ O2+ H2O+ 酸金属+ H2O+ 碱非金属酸盐→→+ O21.2.1.金属 + 非金属 → 盐2.金属氧化物 + 非金属氧化物 → 盐3.酸 + 碱 → 盐 + H2O4.盐 + 盐→ 新盐 + 新盐2Fe + 3Cl2 = ==2FeCl3CaO + SiO2 == CaSiO3HCl + NaOH = NaOH + H2OAgNO3 + NaCl = NaNO3 + AgCl↓点燃?制盐常见的方法非金属氧化物 + 碱 → 盐 + H2O金属氧化物 + 酸 → 盐 + H2OFe2O3 + 6HCl = 2FeCl3 + 3H2OSO2+ 2NaOH= 2Na2SO3 + H2O5.6.金属 + 盐 → 新金属 + 盐金属 + 酸 → 盐 + H2Fe + CuSO4= Cu + FeSO4Zn + H2SO4= ZnSO4 + H2↑7.8.1.Zn + H2SO4 = ZnSO4 + H2↑
2.Zn + CuSO4 = ZnSO4 + Cu
3.ZnO + H2SO4 = ZnSO4 + H2O
4.Zn(OH)2 + H2SO4 = ZnSO4 + 2 H2O试设计制ZnSO4四种方法。你还有其它方法吗?P63练习4
思考:
请你仔细观察周围的各种物质,它们是从哪里来的?又会到哪里去?在这些过程中物质之间是否发生了转化?物质 根据组成
物质种类 混合物纯净物 根据组成
元素种类单质化合物 氧化物 酸碱盐金属非金属稀有气体双原子分子(多种物质)(一种物质)(一种元素)(多种元素)[物质的分类]二 单质、氧化物、酸(碱)之间的转化1.取一药匙硫黄,观察其外观: _____________________________________。
2.将硫黄放到燃烧匙中,在酒精灯上点燃硫黄,观察现象:___________________________________。
3.把燃烧着的硫黄放进盛的氧气的集气瓶内,观察现象:______________________________________
用化学方程式: _______________________。实验一:硫在空气及氧气中燃烧.swf淡黄色固体淡蓝色火焰,生成刺激性气味且有毒的气体蓝紫色火焰,生成刺激性气味且有毒的气体非金属单质与其化合物的转化酸雨当雨水被二氧化碳饱和时,略呈酸性,pH值为5.65。当大气被酸性气体污染时,pH值小于5.65的雨叫酸雨;pH值小于5.65的雪叫酸雪;在高空或高山上弥漫的雾,pH值小于5.65时叫酸雾。
煤中的硫燃烧生成_______,它在粉尘的催化作用下跟O2反应生成________,再与雨水结合生成硫酸。相关的化学方程式是:
酸雨的形成SO2SO3SO3+ H2O = H2SO4怎样用化学方程式表示下列物质的转化?C→CO2→H2CO3①②非金属单质与其化合物的转化规律O2H2O讨论:你能用化学方程式来表示下列物质之间的转化吗?
O2H2O金属的氧化CuO + H2SO4 = CuSO4 + H2OCuSO4 +2NaOH = Cu(OH)2 ↓+Na2SO4钾钙钠的氧化物+水→碱K 2 O + H2O= 2KOH其他金属氧化物不溶于水,跟水不反应Ca O + H2O= Ca(OH)2Na 2 O + H2O= 2NaOH+ O2+ H2O金属1.Ca→CaO→Ca(OH)2 →CaCO32)CaO + H2O = Ca(OH)23)Ca(OH)2 + CO2 = CaCO3 + H2O讨论:分析下列物质的变化讨论:分析下列物质的变化2.C→CO2→H2CO3 →Na2CO32)CO2 + H2O = H2CO33)H2CO3 + 2NaOH = Na2CO3 + H2O+ O2+ H2O+ 酸金属+ H2O+ 碱非金属酸盐→→+ O21.2.1.金属 + 非金属 → 盐2.金属氧化物 + 非金属氧化物 → 盐3.酸 + 碱 → 盐 + H2O4.盐 + 盐→ 新盐 + 新盐2Fe + 3Cl2 = ==2FeCl3CaO + SiO2 == CaSiO3HCl + NaOH = NaOH + H2OAgNO3 + NaCl = NaNO3 + AgCl↓点燃?制盐常见的方法非金属氧化物 + 碱 → 盐 + H2O金属氧化物 + 酸 → 盐 + H2OFe2O3 + 6HCl = 2FeCl3 + 3H2OSO2+ 2NaOH= 2Na2SO3 + H2O5.6.金属 + 盐 → 新金属 + 盐金属 + 酸 → 盐 + H2Fe + CuSO4= Cu + FeSO4Zn + H2SO4= ZnSO4 + H2↑7.8.1.Zn + H2SO4 = ZnSO4 + H2↑
2.Zn + CuSO4 = ZnSO4 + Cu
3.ZnO + H2SO4 = ZnSO4 + H2O
4.Zn(OH)2 + H2SO4 = ZnSO4 + 2 H2O试设计制ZnSO4四种方法。你还有其它方法吗?P63练习4
同课章节目录
- 第一章 宇宙的起源与演化
- 1 我们的宇宙
- 2 热大爆炸宇宙模型
- 3 恒星的一生
- 4 星际航行和空间技术
- 第二章 地球的演化和生物圈的形成
- 1 地球的演化
- 2 生命起源
- 3 生物进化
- 4 生态平衡
- 第三章 物质的转化和元素的循环
- 1 物质的转化
- 2 自然界中的碳循环和氧循环
- 3 自然界中的氮循环
- 第四章 健康与保健
- 1 健康、亚健康和疾病
- 2 运动与健康
- 3 免疫与健康
- 4 营养与健康
- 5 卫生与健康
- 6 环境与健康
- 第五章 生物的遗传和变异
- 1 生物的遗传
- 2 生物的变异
- 第六章 能源与社会
- 1 能源和能源的分类
- 2 太阳能的利用
- 3 核能的开发与放射性防护
- 4 新能源与可持续发展
- 第七章 科学与社会发展
- 1 科学就是力量
- 2 科学推动技术发展
- 3 科学技术推动经济增长
- 4 科学技术与可持续发展
