课题3 元素(33张PPT)
图片预览











文档简介
课件33张PPT。课题3
元 素一、元素
1.概念:_______(即_________)相同的一类原子的总称。
2.与化学变化的关系:在物质发生化学变化时,由于_______
_____不变,故化学反应前后元素的种类也不改变。
3.在地壳中的含量(质量分数):居前四位的元素依次是_____
___________。
4.元素的化学性质与原子结构的关系:元素的化学性质与其原子的核外电子排布,特别是_________________有关。质子数核电荷数原子的种类氧、硅、铝、铁最外层电子的数目【想一想】
具有相同质子数的粒子是否一定是同种元素的原子?
提示:具有相同质子数的原子一定属于同种元素,但具有相同质子数的粒子还可以是分子,有的分子如水分子(H2O)和原子如氖原子(Ne)都含有10个质子,但却不属于同种元素的原子。二、元素符号
1.书写:国际上统一采用元素_______名称的___________来表示元素。书写时注意:
(1)由一个字母表示的元素符号要_____。如__表示碳元素。
(2)由两个字母表示的元素符号,第一个字母要_____,第二个字母要_____。如铝元素的符号为___。拉丁文第一个字母大写C大写小写Al2.意义:
(1)宏观意义:表示_________。
(2)微观意义:表示这种元素的_________。一种元素一个原子氧元素一个氧原子【微点拨】
元素符号前面添加数字时,只具有微观意义,即表示几个原子。3.分类。
元素_____元素:铁、铝等
_______元素(包括稀有气体元素):氧、硅等金属非金属三、元素周期表
1.原子序数:元素周期表按元素原子_________递增的顺序给元素编的号。原子序数=_________=_______。
2.元素周期表的结构:
(1)横行(也叫周期):元素周期表共有7个周期。每周期(第一周期除外)以_____元素开始,再过渡到_______元素(终止于其中的_________元素)。
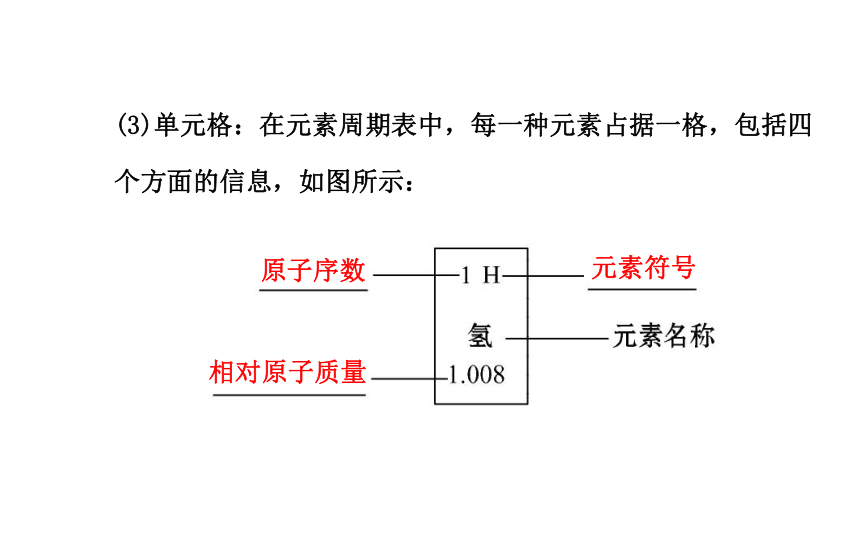
(2)纵行(也叫族):元素周期表共有18个纵行,16个族。核电荷数核电荷数质子数金属非金属稀有气体(3)单元格:在元素周期表中,每一种元素占据一格,包括四个方面的信息,如图所示:原子序数元素符号相对原子质量1.判断正误:
(1)元素是中子数相同的一类原子的总称。( )
提示:元素是以其原子中的质子数为标准进行分类的,而不是以其原子中的中子数为标准,原因是一种元素可能含有中子数不同的多种原子。
(2)地壳中含量最多的金属元素是氧元素。( )
提示:氧元素属于非金属元素,地壳中含量最多的金属元素是铝元素。××(3)元素符号是采用英文名称的第一个字母或另加第二个字母表示的。( )
提示:元素符号是采用拉丁文名称的第一个字母或另加第二个字母表示的。
(4)2O表示氧元素和2个氧原子。( )
提示:在元素符号前面添加数字后,不再表示某种元素,只表示几个原子。××2.碳元素和氧元素的根本区别是( )
A.质子数不同 B.相对原子质量不同
C.电子数不同 D.最外层电子数不同
【解析】选A。不同元素间最本质的区别是质子数不同。3.张杰通过广告了解到海产品、瘦肉、肝脏、牛奶、豆类、小米等食品可以为人体提供所需的锌。这里的“锌”是指( )
A.元素 B.原子 C.分子 D.离子
【解析】选A。食品中为人体提供所需的“锌”不是以分子、原子、离子等形式存在,这里所指的“锌”是强调存在的元素,与具体形态无关。4.下列元素名称与其对应的元素符号完全正确的是( )
A.氯cl B.氖Na C.镁Mg D.铜Ca
【解析】选C。用两个字母表示元素符号时应该第一个字母大写,第二个字母小写,故A项中氯元素的元素符号为Cl;B项中氖的元素符号和钠的元素符号混淆了,应为Ne;D项中铜和钙的元素符号混淆了,应为Cu。5.锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示:(1)锶属于____________(选填“金属”或“非金属”)元素。
(2)锶元素的原子序数为________________,相对原子质量为______________。
(3)图2所表示的粒子的化学符号是______________。【解析】(1)由锶元素的粒子结构示意图,可知其最外层电子数为2,符合金属元素的最外层电子数一般小于4的特点,可推测元素种类为金属元素;也可根据汉语名称“锶”,带“钅”字旁,故推测元素种类为金属元素;(2)由锶元素的粒子结构示意图和规律“原子序数=核内质子数=核外电子数=核电荷数”可知锶元素的原子序数为38;根据在元素周期表中显示的信息,可知其相对原子质量为87.62;(3)图2所表示的粒子为锶原子失去最外层电子所得的结构,根据失去的电子数为2,可知带2个单位正电荷;根据在元素周期表中显示的信息,可知其元素符号为Sr,故粒子符号为Sr2+。答案:(1)金属 (2)38 87.62 (3)Sr2+要点一 元素与原子的比较 【示范题1】下列关于元素与原子关系的叙述中,正确的是
( )
A.元素是原子的一个归类“集体”
B.同种元素的原子结构和质量完全相同
C.元素的种类取决于该元素原子的核外电子数
D.不同种元素的根本区别是核内中子数不同【解析】选A。本题考查的是元素与原子的关系,解题的关键是明确元素的分类依据。元素是同类原子的总称,因此两者属于整体与个体的关系,故A正确;同种元素原子的中子数可能不同,故同种元素的原子结构和质量不一定相同,B不正确;元素的种类取决于该元素原子的质子数,C不正确;不同种元素的原子核内中子数可能相同,而质子数不同,故不同种元素的根本区别是核内质子数不同,故D不正确。【特别提醒】
1.对元素概念中“同一类原子”的理解:
(1)质子数相同、中子数不同的原子,如:氢元素的三种原子(氕、氘、氚),质子数都为1,中子数分别为0,1,2。
(2)质子数相同的原子和离子,原子失去或得到电子得到的离子和原来的原子同属于同种元素,如Cl和Cl-都是氯元素。2.用元素描述物质组成时的注意事项:
(1)元素只有种类不同,而无数量多少。
(2)元素是宏观概念不能描述为“由某元素构成”。
(3)不能用宏观概念元素描述微观粒子。
以水为例,正确描述如下:水是由氢、氧两种元素组成的;水分子是由氢、氧两种原子构成的;每个水分子是由两个氢原子和一个氧原子构成的。要点二 元素周期表
1.元素周期表的结构:2.元素的排布规律:
(1)同一周期:电子层数相同,从左至右最外层上的电子数依次增加。
(2)同一族:最外层上的电子数相同,从上到下电子层数依次增加。【示范题2】“化学家的主要工作是耕耘元素周期表”。如图所示为元素周期表中部分元素的相关信息。请利用图示信息回答相关问题:(1)锂原子的核电荷数为______________。
(2)16号元素的原子在化学反应中比较容易________(填“得”或“失”)电子,该元素属于__________(填“金属”或“非金属”)元素。
(3)写出表中关于8号元素的一条信息:______________。【解析】本题考查元素周期表的应用。主要涉及原子序数、核电荷数、原子结构示意图等内容。(1)锂原子的原子序数是3,则核电荷数也是3。(2)16号元素的原子最外层有6个电子,在化学反应中容易得电子;该元素是硫元素,属于非金属元素。(3)8号元素是氧元素、质子数是8、有两个电子层、最外层有6个电子等,符合题意即可。
答案:(1)3 (2)得 非金属
(3)氧元素(或质子数是8或有两个电子层或最外层有6个电子等)【习题备选】钾在人体内起着调节体液平衡的作用,图A是钾元素在元素周期表中的相关信息。
(1)钾元素的相对原子质量为____________。
(2)图B是钾元素某种粒子的结构示意图,图中x=______,该粒子的符号为____________。【解析】本题考查学生的读图和分析能力。解答本题的关键有:(1)明确元素周期表中单元格包含的信息;(2)原子结构示意图的含义。从钾元素单元格中的信息可知,钾元素的相对原子质量为39.10;钾元素的原子序数是19,因此核内质子数也为19;由于该粒子的质子数比电子数多1,故带一个单位的正电荷。
答案:(1)39.10 (2)19 K+1.根据所学知识,在下图中写出有关符号所表示的意义。提示:元素符号一般表示两种意义,即一种元素和该元素的一个原子,图中“H”表示氢元素和一个氢原子;元素符号前面加了数字只表示微观意义,如“2H”表示两个氢原子。2.根据所学知识,将如下物质的组成与构成图填写完整。
提示:物质由元素组成,元素属于宏观概念,只有种类之分,没有数量之别;分子由原子构成,原子属于微观概念,既有种类之分,又有数量之别。
元 素一、元素
1.概念:_______(即_________)相同的一类原子的总称。
2.与化学变化的关系:在物质发生化学变化时,由于_______
_____不变,故化学反应前后元素的种类也不改变。
3.在地壳中的含量(质量分数):居前四位的元素依次是_____
___________。
4.元素的化学性质与原子结构的关系:元素的化学性质与其原子的核外电子排布,特别是_________________有关。质子数核电荷数原子的种类氧、硅、铝、铁最外层电子的数目【想一想】
具有相同质子数的粒子是否一定是同种元素的原子?
提示:具有相同质子数的原子一定属于同种元素,但具有相同质子数的粒子还可以是分子,有的分子如水分子(H2O)和原子如氖原子(Ne)都含有10个质子,但却不属于同种元素的原子。二、元素符号
1.书写:国际上统一采用元素_______名称的___________来表示元素。书写时注意:
(1)由一个字母表示的元素符号要_____。如__表示碳元素。
(2)由两个字母表示的元素符号,第一个字母要_____,第二个字母要_____。如铝元素的符号为___。拉丁文第一个字母大写C大写小写Al2.意义:
(1)宏观意义:表示_________。
(2)微观意义:表示这种元素的_________。一种元素一个原子氧元素一个氧原子【微点拨】
元素符号前面添加数字时,只具有微观意义,即表示几个原子。3.分类。
元素_____元素:铁、铝等
_______元素(包括稀有气体元素):氧、硅等金属非金属三、元素周期表
1.原子序数:元素周期表按元素原子_________递增的顺序给元素编的号。原子序数=_________=_______。
2.元素周期表的结构:
(1)横行(也叫周期):元素周期表共有7个周期。每周期(第一周期除外)以_____元素开始,再过渡到_______元素(终止于其中的_________元素)。
(2)纵行(也叫族):元素周期表共有18个纵行,16个族。核电荷数核电荷数质子数金属非金属稀有气体(3)单元格:在元素周期表中,每一种元素占据一格,包括四个方面的信息,如图所示:原子序数元素符号相对原子质量1.判断正误:
(1)元素是中子数相同的一类原子的总称。( )
提示:元素是以其原子中的质子数为标准进行分类的,而不是以其原子中的中子数为标准,原因是一种元素可能含有中子数不同的多种原子。
(2)地壳中含量最多的金属元素是氧元素。( )
提示:氧元素属于非金属元素,地壳中含量最多的金属元素是铝元素。××(3)元素符号是采用英文名称的第一个字母或另加第二个字母表示的。( )
提示:元素符号是采用拉丁文名称的第一个字母或另加第二个字母表示的。
(4)2O表示氧元素和2个氧原子。( )
提示:在元素符号前面添加数字后,不再表示某种元素,只表示几个原子。××2.碳元素和氧元素的根本区别是( )
A.质子数不同 B.相对原子质量不同
C.电子数不同 D.最外层电子数不同
【解析】选A。不同元素间最本质的区别是质子数不同。3.张杰通过广告了解到海产品、瘦肉、肝脏、牛奶、豆类、小米等食品可以为人体提供所需的锌。这里的“锌”是指( )
A.元素 B.原子 C.分子 D.离子
【解析】选A。食品中为人体提供所需的“锌”不是以分子、原子、离子等形式存在,这里所指的“锌”是强调存在的元素,与具体形态无关。4.下列元素名称与其对应的元素符号完全正确的是( )
A.氯cl B.氖Na C.镁Mg D.铜Ca
【解析】选C。用两个字母表示元素符号时应该第一个字母大写,第二个字母小写,故A项中氯元素的元素符号为Cl;B项中氖的元素符号和钠的元素符号混淆了,应为Ne;D项中铜和钙的元素符号混淆了,应为Cu。5.锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示:(1)锶属于____________(选填“金属”或“非金属”)元素。
(2)锶元素的原子序数为________________,相对原子质量为______________。
(3)图2所表示的粒子的化学符号是______________。【解析】(1)由锶元素的粒子结构示意图,可知其最外层电子数为2,符合金属元素的最外层电子数一般小于4的特点,可推测元素种类为金属元素;也可根据汉语名称“锶”,带“钅”字旁,故推测元素种类为金属元素;(2)由锶元素的粒子结构示意图和规律“原子序数=核内质子数=核外电子数=核电荷数”可知锶元素的原子序数为38;根据在元素周期表中显示的信息,可知其相对原子质量为87.62;(3)图2所表示的粒子为锶原子失去最外层电子所得的结构,根据失去的电子数为2,可知带2个单位正电荷;根据在元素周期表中显示的信息,可知其元素符号为Sr,故粒子符号为Sr2+。答案:(1)金属 (2)38 87.62 (3)Sr2+要点一 元素与原子的比较 【示范题1】下列关于元素与原子关系的叙述中,正确的是
( )
A.元素是原子的一个归类“集体”
B.同种元素的原子结构和质量完全相同
C.元素的种类取决于该元素原子的核外电子数
D.不同种元素的根本区别是核内中子数不同【解析】选A。本题考查的是元素与原子的关系,解题的关键是明确元素的分类依据。元素是同类原子的总称,因此两者属于整体与个体的关系,故A正确;同种元素原子的中子数可能不同,故同种元素的原子结构和质量不一定相同,B不正确;元素的种类取决于该元素原子的质子数,C不正确;不同种元素的原子核内中子数可能相同,而质子数不同,故不同种元素的根本区别是核内质子数不同,故D不正确。【特别提醒】
1.对元素概念中“同一类原子”的理解:
(1)质子数相同、中子数不同的原子,如:氢元素的三种原子(氕、氘、氚),质子数都为1,中子数分别为0,1,2。
(2)质子数相同的原子和离子,原子失去或得到电子得到的离子和原来的原子同属于同种元素,如Cl和Cl-都是氯元素。2.用元素描述物质组成时的注意事项:
(1)元素只有种类不同,而无数量多少。
(2)元素是宏观概念不能描述为“由某元素构成”。
(3)不能用宏观概念元素描述微观粒子。
以水为例,正确描述如下:水是由氢、氧两种元素组成的;水分子是由氢、氧两种原子构成的;每个水分子是由两个氢原子和一个氧原子构成的。要点二 元素周期表
1.元素周期表的结构:2.元素的排布规律:
(1)同一周期:电子层数相同,从左至右最外层上的电子数依次增加。
(2)同一族:最外层上的电子数相同,从上到下电子层数依次增加。【示范题2】“化学家的主要工作是耕耘元素周期表”。如图所示为元素周期表中部分元素的相关信息。请利用图示信息回答相关问题:(1)锂原子的核电荷数为______________。
(2)16号元素的原子在化学反应中比较容易________(填“得”或“失”)电子,该元素属于__________(填“金属”或“非金属”)元素。
(3)写出表中关于8号元素的一条信息:______________。【解析】本题考查元素周期表的应用。主要涉及原子序数、核电荷数、原子结构示意图等内容。(1)锂原子的原子序数是3,则核电荷数也是3。(2)16号元素的原子最外层有6个电子,在化学反应中容易得电子;该元素是硫元素,属于非金属元素。(3)8号元素是氧元素、质子数是8、有两个电子层、最外层有6个电子等,符合题意即可。
答案:(1)3 (2)得 非金属
(3)氧元素(或质子数是8或有两个电子层或最外层有6个电子等)【习题备选】钾在人体内起着调节体液平衡的作用,图A是钾元素在元素周期表中的相关信息。
(1)钾元素的相对原子质量为____________。
(2)图B是钾元素某种粒子的结构示意图,图中x=______,该粒子的符号为____________。【解析】本题考查学生的读图和分析能力。解答本题的关键有:(1)明确元素周期表中单元格包含的信息;(2)原子结构示意图的含义。从钾元素单元格中的信息可知,钾元素的相对原子质量为39.10;钾元素的原子序数是19,因此核内质子数也为19;由于该粒子的质子数比电子数多1,故带一个单位的正电荷。
答案:(1)39.10 (2)19 K+1.根据所学知识,在下图中写出有关符号所表示的意义。提示:元素符号一般表示两种意义,即一种元素和该元素的一个原子,图中“H”表示氢元素和一个氢原子;元素符号前面加了数字只表示微观意义,如“2H”表示两个氢原子。2.根据所学知识,将如下物质的组成与构成图填写完整。
提示:物质由元素组成,元素属于宏观概念,只有种类之分,没有数量之别;分子由原子构成,原子属于微观概念,既有种类之分,又有数量之别。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
