课题1 金刚石、石墨和C60(32张PPT)
文档属性
| 名称 | 课题1 金刚石、石墨和C60(32张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 761.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-03-17 00:00:00 | ||
图片预览










文档简介
课件32张PPT。第六单元 碳和碳的氧化物
课题1 金刚石、石墨和C60一、碳的单质
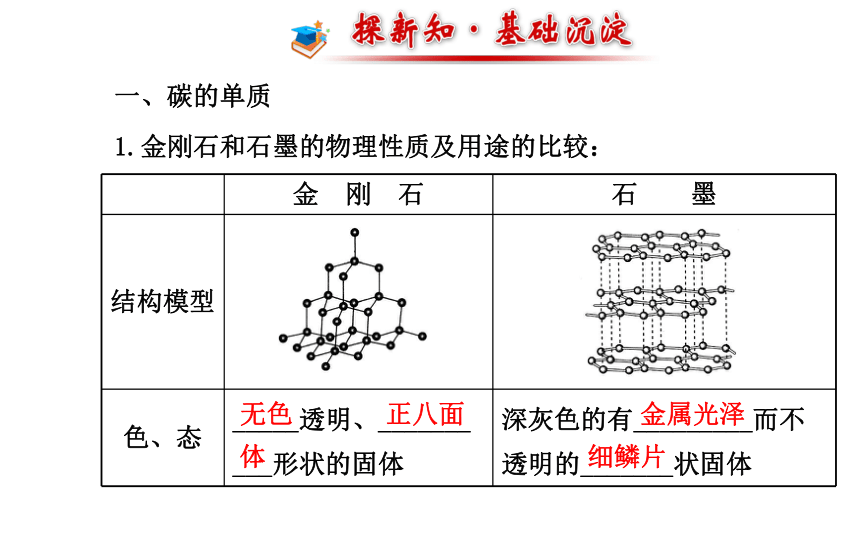
1.金刚石和石墨的物理性质及用途的比较:无色正八面体金属光泽细鳞片最硬很软不导电优良2.木炭和活性炭的吸附性:
(1)原因:由于木炭和活性炭具有_________的结构,因此它们都具有吸附性。
(2)应用。
①活性炭用在防毒面具中_________。
②制糖工业中也利用活性炭来_____以制白糖。
③城市污水、工业废水和饮用水在深度净化处理时用活性炭吸附。
④活性炭用来吸附装修产生的对人体有害的气体。疏松多孔吸附毒气脱色二、单质碳的化学性质
1.稳定性:常温下,碳的化学性质_______,受日光照射或与
空气、水分接触,都不易起变化。
2.可燃性:
(1)氧气充足时,碳充分燃烧,化学方程式为____________。
(2)氧气不足时,碳燃烧不充分,化学方程式为____________
____。C+O2 CO22C+O22CO不活泼3.还原性:
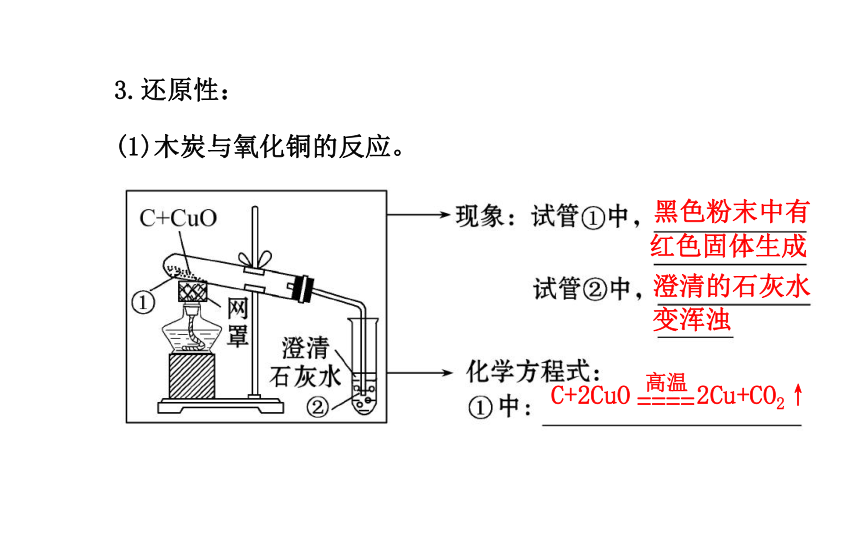
(1)木炭与氧化铜的反应。黑色粉末中有红色固体生成澄清的石灰水变浑浊C+2CuO 2Cu+CO2↑(2)还原反应:_______________________的反应。上述反应中木炭使氧化铜还原为铜,它具有_____性。
(3)用途。
①用于冶金工业。如焦炭能将氧化铁还原为铁,化学方程式为________________________。
②在高温条件下,碳能使二氧化碳转变成_________,化学方程式为_____________。含氧化合物里的氧被夺去还原3C+2Fe2O3 4Fe+3CO2↑一氧化碳CO2+C 2CO1.判断正误:
(1)碳的单质都是黑色固体。( )
提示:金刚石属于无色透明、正八面体形状的固体。
(2)由于金刚石和石墨是由同种元素组成的,所以它们的性质相同。( )
提示:由于构成它们的碳原子的排列方式不同,物理性质存在着很大差异。××(3)利用活性炭的吸附性净化水属于物理变化。( )
提示:活性炭的吸附性是利用了其疏松多孔的结构吸附色素及异味,吸附过程中没有其他物质生成,属于物理变化。
(4)碳在氧气中充分燃烧放出热量,不充分燃烧吸收热量。
( )
提示:无论碳是否充分燃烧都放出热量,只是前者比后者放出的热量多。√×2.防毒面具中用来除去有毒气体的物质是( )
A.焦炭 B.炭黑 C.活性炭 D.石墨
【解析】选C。活性炭具有很强的吸附性,能用作防毒面具里的滤毒罐来吸附毒气。3.用墨书写的字或绘的画能保存多年不褪色,是由于常温下
碳( )
A.化学性质不活泼 B.具有吸附性
C.具有还原性 D.具有氧化性
【解析】选A。墨的主要成分是碳单质,由于碳在常温下化学性质不活泼,所以用墨书写的字或绘的画能保存多年不褪色。4.将木炭和氧化铜的混合物均匀放在试管中加热。
(1)观察到的现象是________色的氧化铜最终变成________色的固体,将反应生成的气体通入澄清的石灰水中观察到的现象是_______________________。
(2)写出木炭与氧化铜反应的化学方程式_________________,
在反应中,氧化铜发生________反应。【解析】木炭和氧化铜在高温下反应生成铜与二氧化碳,会观察到黑色的氧化铜粉末最终变成红色固体,生成的二氧化碳气体能使澄清的石灰水变浑浊,在反应中氧化铜发生还原反应。
答案:(1)黑 红 澄清石灰水变浑浊
(2)C+2CuO 2Cu+CO2↑ 还原要点一 碳单质的组成、结构与性质的关系
分析下列金刚石和石墨的微观结构图,思考以下问题: 1.金刚石和石墨都由碳元素组成,但是物理性质却存在很大的差异,原因是什么?
提示:结构决定性质,两者物理性质的差异是由结构不同造成的。金刚石和石墨虽然都由碳原子构成,但碳原子排列方式不同。
2.在一定条件下,石墨可以转化为金刚石,该变化属于物理变化还是化学变化?
提示:石墨和金刚石结构不同,属于两种不同物质,故两者之间的转化,属于化学变化。【示范题1】金刚石、石墨和C60都是由碳元素组成的单质,下列说法正确的是( )
A.碳原子的排列方式相同
B.在氧气中充分燃烧时都生成二氧化碳
C.物理性质相同
D.一定条件下,石墨转化成金刚石是物理变化【解析】选B。碳原子以不同的排列方式,构成了金刚石、石墨和C60等物质,A不正确;金刚石、石墨和C60都是由碳元素组成的单质,在氧气中充分燃烧时都生成二氧化碳,B正确;金刚石、石墨和C60的物理性质不同,C不正确;石墨和金刚石是两种不同的物质,一定条件下,石墨转化成金刚石是化学变化,D不正确。【试题备选】如图是金刚石、石墨、C60、碳纳米管结构示意图,下列说法错误的是( )A.这4种物质完全燃烧后的产物都是CO2
B.这4种物质的物理性质有较大差异的原因是碳原子的排列方式不同
C.常温下C60和碳纳米管的化学性质很活泼
D.碳纳米管在室温下能贮存和凝聚大量的H2【解析】选C。金刚石、石墨、C60、碳纳米管都是由碳元素组成的单质,完全燃烧的产物都是二氧化碳,A说法正确;因为碳原子的排列方式不同,所以4种物质的物理性质有较大差异,B说法正确;常温下C60和碳纳米管的化学性质很稳定,C说法不正确;碳纳米管具有较大的表面积,在室温下能贮存和凝聚大量的氢气,D说法正确。要点二 碳单质的化学性质
1.碳的稳定性:常温下,碳的化学性质稳定,这种稳定性与碳原子的结构有关。碳原子最外层为4个电子,在化学反应中不容易得失电子,因此化学性质稳定。
2.碳的可燃性:碳在氧气是否充足的情况下,燃烧产物不同。氧气充足生成二氧化碳,氧气不足,生成一氧化碳。由于一氧化碳有毒,因此,我们在用煤炉或木炭取暖时,一定要注意空气流通。3.碳的还原性:高温条件下,碳可以与二氧化碳和氧化铜等物质发生还原反应。进行碳与氧化铜实验时要注意以下两点:
(1)实验时酒精灯加网罩的作用是集中酒精灯火焰以提高受热温度,也可改用酒精喷灯加热。
(2)为了防止水回流使试管炸裂,停止加热时应先将导管从石灰水中撤出,同时为了防止进入空气使生成的铜重新被氧化,应用弹簧夹夹紧橡皮管,待试管冷却后再把试管里的粉末倒出。【示范题2】下列说法中,正确的是( )
A.书写档案规定必须用碳素墨水,原因是碳单质常温下化学性质比较稳定
B.焦炭可以把铁从它的氧化物矿石里还原出来,是因为碳具有氧化性
C.用活性炭可除去硬水中的氯化钙杂质
D.木炭燃烧时可吸收大量的热【解析】选A。碳单质化学性质稳定,常温下不与其他物质发生化学反应;焦炭还原铁的氧化物得到铁是利用了其还原性;活性炭只能吸附水中的悬浮物和异味不能除去水中的可溶性杂质;木炭燃烧放出大量的热。【示范题3】如图是实验室木炭还原氧化铜的实验,请回答:(1)盛放氧化铜的试管内的现象是_______________________;
盛放石灰水的试管内的现象是______________。
(2)盛放氧化铜的试管内的反应的化学方程式为____________
_______________,在这个反应中______________发生还原反应,___________具有还原性。
(3)实验时,酒精灯上加网罩的目的是__________________。【解析】木炭与氧化铜在加热的条件下反应生成铜与二氧化碳,所以盛放氧化铜的试管中黑色粉末会逐渐变成亮红色,盛放石灰水的试管中会变浑浊;在反应中氧化铜失去氧发生还原反应,碳能夺取氧化铜的氧,具有还原性;反应需要的温度较高,酒精灯上加网罩是为了使火焰集中,提高温度。
答案:(1)黑色固体逐渐减少,产生红色固体
导气管口冒气泡,澄清石灰水逐渐变浑浊
(2)2CuO+C 2Cu+CO2↑ CuO C
(3)使酒精灯的火焰集中,提高加热温度【误区警示】“碳”≠“炭”
(1)“碳”是指碳元素,是“核电荷数为6的同一类原子的总称”,并不是具体指某种物质。如二氧化碳中的碳是指碳元素。
(2)“炭”是指具体的物质——由碳元素组成的部分物质,如木炭、焦炭、活性炭、炭黑等。1.请将下图中金刚石、石墨的结构、性质与用途用线连起来。提示:物质的结构决定其性质,性质决定物质的用途,金刚石是无色透明的,为正八面体结构,能用作装饰品,是最硬的物质,可镶在玻璃刀头上;石墨有优良的导电性,能作电极,在纸上划过可留下痕迹能制作铅笔芯,有滑腻感可用作润滑剂。2.请将下图中碳单质的化学性质及其相关化学方程式填写完整。提示:碳单质在常温下化学性质稳定,温度升高时活动性增强,具有可燃性和还原性,在氧气中完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳,在高温下能夺取氧化铜中的氧生成铜与二氧化碳。
课题1 金刚石、石墨和C60一、碳的单质
1.金刚石和石墨的物理性质及用途的比较:无色正八面体金属光泽细鳞片最硬很软不导电优良2.木炭和活性炭的吸附性:
(1)原因:由于木炭和活性炭具有_________的结构,因此它们都具有吸附性。
(2)应用。
①活性炭用在防毒面具中_________。
②制糖工业中也利用活性炭来_____以制白糖。
③城市污水、工业废水和饮用水在深度净化处理时用活性炭吸附。
④活性炭用来吸附装修产生的对人体有害的气体。疏松多孔吸附毒气脱色二、单质碳的化学性质
1.稳定性:常温下,碳的化学性质_______,受日光照射或与
空气、水分接触,都不易起变化。
2.可燃性:
(1)氧气充足时,碳充分燃烧,化学方程式为____________。
(2)氧气不足时,碳燃烧不充分,化学方程式为____________
____。C+O2 CO22C+O22CO不活泼3.还原性:
(1)木炭与氧化铜的反应。黑色粉末中有红色固体生成澄清的石灰水变浑浊C+2CuO 2Cu+CO2↑(2)还原反应:_______________________的反应。上述反应中木炭使氧化铜还原为铜,它具有_____性。
(3)用途。
①用于冶金工业。如焦炭能将氧化铁还原为铁,化学方程式为________________________。
②在高温条件下,碳能使二氧化碳转变成_________,化学方程式为_____________。含氧化合物里的氧被夺去还原3C+2Fe2O3 4Fe+3CO2↑一氧化碳CO2+C 2CO1.判断正误:
(1)碳的单质都是黑色固体。( )
提示:金刚石属于无色透明、正八面体形状的固体。
(2)由于金刚石和石墨是由同种元素组成的,所以它们的性质相同。( )
提示:由于构成它们的碳原子的排列方式不同,物理性质存在着很大差异。××(3)利用活性炭的吸附性净化水属于物理变化。( )
提示:活性炭的吸附性是利用了其疏松多孔的结构吸附色素及异味,吸附过程中没有其他物质生成,属于物理变化。
(4)碳在氧气中充分燃烧放出热量,不充分燃烧吸收热量。
( )
提示:无论碳是否充分燃烧都放出热量,只是前者比后者放出的热量多。√×2.防毒面具中用来除去有毒气体的物质是( )
A.焦炭 B.炭黑 C.活性炭 D.石墨
【解析】选C。活性炭具有很强的吸附性,能用作防毒面具里的滤毒罐来吸附毒气。3.用墨书写的字或绘的画能保存多年不褪色,是由于常温下
碳( )
A.化学性质不活泼 B.具有吸附性
C.具有还原性 D.具有氧化性
【解析】选A。墨的主要成分是碳单质,由于碳在常温下化学性质不活泼,所以用墨书写的字或绘的画能保存多年不褪色。4.将木炭和氧化铜的混合物均匀放在试管中加热。
(1)观察到的现象是________色的氧化铜最终变成________色的固体,将反应生成的气体通入澄清的石灰水中观察到的现象是_______________________。
(2)写出木炭与氧化铜反应的化学方程式_________________,
在反应中,氧化铜发生________反应。【解析】木炭和氧化铜在高温下反应生成铜与二氧化碳,会观察到黑色的氧化铜粉末最终变成红色固体,生成的二氧化碳气体能使澄清的石灰水变浑浊,在反应中氧化铜发生还原反应。
答案:(1)黑 红 澄清石灰水变浑浊
(2)C+2CuO 2Cu+CO2↑ 还原要点一 碳单质的组成、结构与性质的关系
分析下列金刚石和石墨的微观结构图,思考以下问题: 1.金刚石和石墨都由碳元素组成,但是物理性质却存在很大的差异,原因是什么?
提示:结构决定性质,两者物理性质的差异是由结构不同造成的。金刚石和石墨虽然都由碳原子构成,但碳原子排列方式不同。
2.在一定条件下,石墨可以转化为金刚石,该变化属于物理变化还是化学变化?
提示:石墨和金刚石结构不同,属于两种不同物质,故两者之间的转化,属于化学变化。【示范题1】金刚石、石墨和C60都是由碳元素组成的单质,下列说法正确的是( )
A.碳原子的排列方式相同
B.在氧气中充分燃烧时都生成二氧化碳
C.物理性质相同
D.一定条件下,石墨转化成金刚石是物理变化【解析】选B。碳原子以不同的排列方式,构成了金刚石、石墨和C60等物质,A不正确;金刚石、石墨和C60都是由碳元素组成的单质,在氧气中充分燃烧时都生成二氧化碳,B正确;金刚石、石墨和C60的物理性质不同,C不正确;石墨和金刚石是两种不同的物质,一定条件下,石墨转化成金刚石是化学变化,D不正确。【试题备选】如图是金刚石、石墨、C60、碳纳米管结构示意图,下列说法错误的是( )A.这4种物质完全燃烧后的产物都是CO2
B.这4种物质的物理性质有较大差异的原因是碳原子的排列方式不同
C.常温下C60和碳纳米管的化学性质很活泼
D.碳纳米管在室温下能贮存和凝聚大量的H2【解析】选C。金刚石、石墨、C60、碳纳米管都是由碳元素组成的单质,完全燃烧的产物都是二氧化碳,A说法正确;因为碳原子的排列方式不同,所以4种物质的物理性质有较大差异,B说法正确;常温下C60和碳纳米管的化学性质很稳定,C说法不正确;碳纳米管具有较大的表面积,在室温下能贮存和凝聚大量的氢气,D说法正确。要点二 碳单质的化学性质
1.碳的稳定性:常温下,碳的化学性质稳定,这种稳定性与碳原子的结构有关。碳原子最外层为4个电子,在化学反应中不容易得失电子,因此化学性质稳定。
2.碳的可燃性:碳在氧气是否充足的情况下,燃烧产物不同。氧气充足生成二氧化碳,氧气不足,生成一氧化碳。由于一氧化碳有毒,因此,我们在用煤炉或木炭取暖时,一定要注意空气流通。3.碳的还原性:高温条件下,碳可以与二氧化碳和氧化铜等物质发生还原反应。进行碳与氧化铜实验时要注意以下两点:
(1)实验时酒精灯加网罩的作用是集中酒精灯火焰以提高受热温度,也可改用酒精喷灯加热。
(2)为了防止水回流使试管炸裂,停止加热时应先将导管从石灰水中撤出,同时为了防止进入空气使生成的铜重新被氧化,应用弹簧夹夹紧橡皮管,待试管冷却后再把试管里的粉末倒出。【示范题2】下列说法中,正确的是( )
A.书写档案规定必须用碳素墨水,原因是碳单质常温下化学性质比较稳定
B.焦炭可以把铁从它的氧化物矿石里还原出来,是因为碳具有氧化性
C.用活性炭可除去硬水中的氯化钙杂质
D.木炭燃烧时可吸收大量的热【解析】选A。碳单质化学性质稳定,常温下不与其他物质发生化学反应;焦炭还原铁的氧化物得到铁是利用了其还原性;活性炭只能吸附水中的悬浮物和异味不能除去水中的可溶性杂质;木炭燃烧放出大量的热。【示范题3】如图是实验室木炭还原氧化铜的实验,请回答:(1)盛放氧化铜的试管内的现象是_______________________;
盛放石灰水的试管内的现象是______________。
(2)盛放氧化铜的试管内的反应的化学方程式为____________
_______________,在这个反应中______________发生还原反应,___________具有还原性。
(3)实验时,酒精灯上加网罩的目的是__________________。【解析】木炭与氧化铜在加热的条件下反应生成铜与二氧化碳,所以盛放氧化铜的试管中黑色粉末会逐渐变成亮红色,盛放石灰水的试管中会变浑浊;在反应中氧化铜失去氧发生还原反应,碳能夺取氧化铜的氧,具有还原性;反应需要的温度较高,酒精灯上加网罩是为了使火焰集中,提高温度。
答案:(1)黑色固体逐渐减少,产生红色固体
导气管口冒气泡,澄清石灰水逐渐变浑浊
(2)2CuO+C 2Cu+CO2↑ CuO C
(3)使酒精灯的火焰集中,提高加热温度【误区警示】“碳”≠“炭”
(1)“碳”是指碳元素,是“核电荷数为6的同一类原子的总称”,并不是具体指某种物质。如二氧化碳中的碳是指碳元素。
(2)“炭”是指具体的物质——由碳元素组成的部分物质,如木炭、焦炭、活性炭、炭黑等。1.请将下图中金刚石、石墨的结构、性质与用途用线连起来。提示:物质的结构决定其性质,性质决定物质的用途,金刚石是无色透明的,为正八面体结构,能用作装饰品,是最硬的物质,可镶在玻璃刀头上;石墨有优良的导电性,能作电极,在纸上划过可留下痕迹能制作铅笔芯,有滑腻感可用作润滑剂。2.请将下图中碳单质的化学性质及其相关化学方程式填写完整。提示:碳单质在常温下化学性质稳定,温度升高时活动性增强,具有可燃性和还原性,在氧气中完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳,在高温下能夺取氧化铜中的氧生成铜与二氧化碳。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
