化学能与电能课件(共24张PPT)
文档属性
| 名称 | 化学能与电能课件(共24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-04-05 00:00:00 | ||
图片预览





文档简介
课件24张PPT。化学能与电能人教版化学必修2第二章第2节生活处处离不开电问题初探1:你知道电能的来源吗?火力发电化石燃料
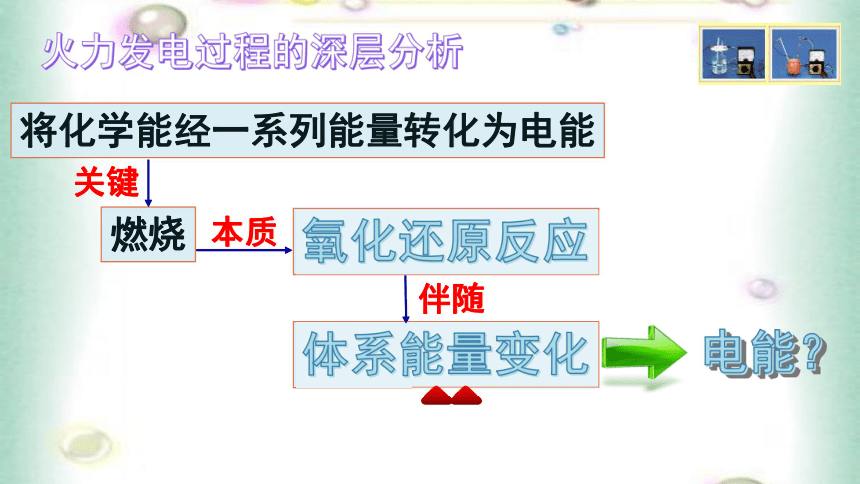
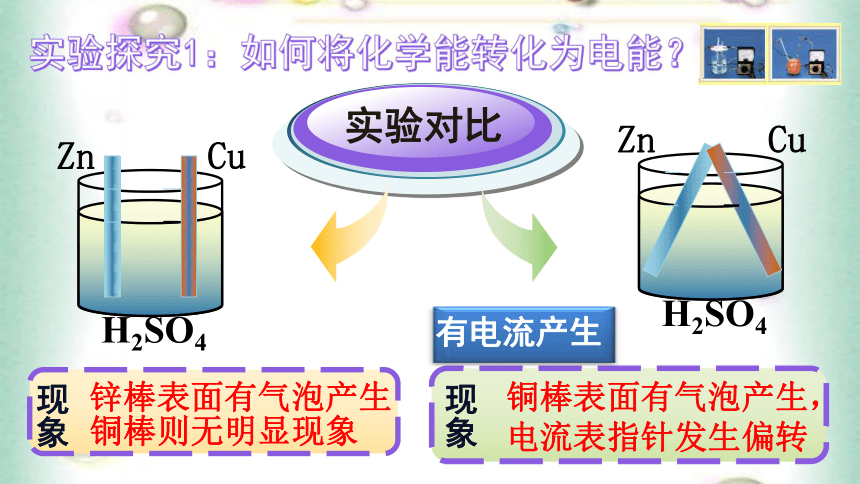
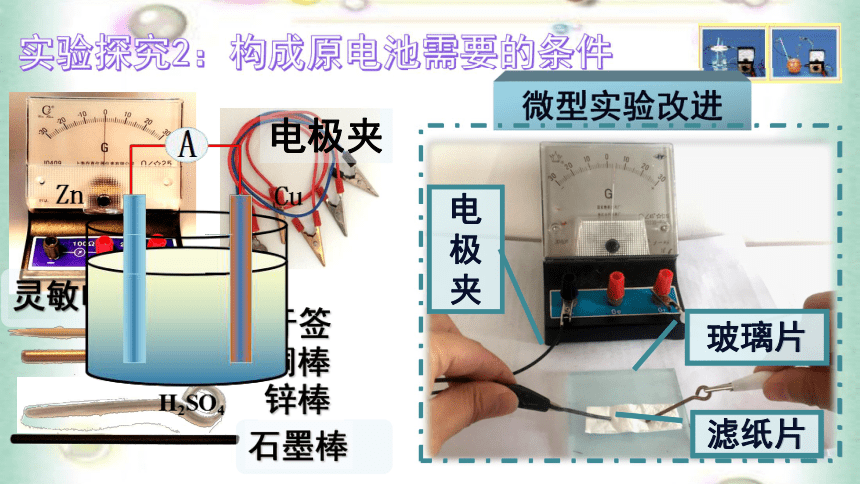
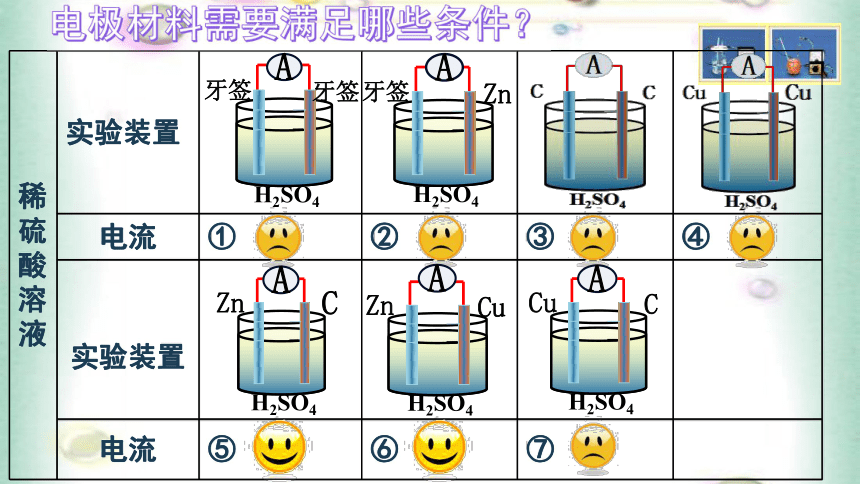
的化学能 机械能 热能电能直接转化?问题初探2:火力发电有哪些弊端呢?燃烧氧化还原反应将化学能经一系列能量转化为电能关键本质体系能量变化伴随火力发电过程的深层分析实验探究1:如何将化学能转化为电能?铜棒表面有气泡产生,电流表指针发生偏转现象1、原电池: 将化学能转变成电能的装置。化学能转化为电能实验探究2:构成原电池装置需要的条件用不同的电极材料完成实验实验探究2:构成原电池需要的条件微型实验改进玻璃片滤纸片电极夹电极材料铜棒牙签锌棒电极材料需要满足哪些条件?AAAA实验探究结果:构成原电池的电极条件电极为活泼性不同的导体活泼性不同的金属金属与非金属导体⑦能自发地发生氧化还原反应实验探究2:构成原电池装置需要的条件将滤纸上的液体替换为酒精两电极必须插在电解质溶液中A实验探究结果:构成原电池的液体条件这两套装置为何没有电流产生?没有构成闭合回路!2、构成原电池的条件
①具有活泼性不同的两个电极。
②两电极必须插在电解质溶液中。
③能自发地发生氧化还原反应。
④形成闭合回路。
两极一液一线一反应化学能转化为电能3、原电池原理:交流
讨论①导线上(外电路)电子的移动方向?
溶液中(内电路)离子的移动方向?
②你知道锌片和铜片上面发生哪些反应吗?电子移动方向:
锌片→铜片阴离子移向:锌片阳离子移向:铜片化学能转化为电能3、原电池原理:交流讨论电子移动方向:锌片→铜片
阴离子移向:锌片
阳离子移向:铜片阴离子移向的一极阳离子移向的一极 (锌):Zn – 2e- = Zn2+
(铜):2H+ +2e- = H2↑
电极
反应式反应本质:氧化还原反应还原反应氧化反应总反应:Zn+2H+= Zn2++H2↑正极负极还原剂(Zn)失去电子,发生氧化反应Zn2+氧化剂(H+)在铜极上得到电子,发生还原反应电子从锌极流出流入铜极.经外电路H+SO42-电流方向1、以下哪些装置可以形成原电池? +++2、写出电极反应式以及总反应,并判断正负极 负极(铜):Cu - 2e- = Cu2+正极(银):Ag+ + e- = AgCu + 2Ag+ = Cu2+ + 2Ag 正极(铁):2H++2e- =H2↑ 负极(锌):Zn -2e - = Zn2+ Zn+2H+=Zn2++H2↑请根据反应:Zn+Cu2+=Zn2++Cu设计原电池
画出装置图,写出电极反应式及产生的现象3、设计原电池 负极:Zn - 2e-?=Zn?2+?
正极:Cu2+?+2e-?=Cu 负极锌片溶解,正极上覆盖一层红色的铜。 作业1、完成全优练习册相应的内容
2、动手试试看,利用水果制作原电池,体验生活中的化学再见
的化学能 机械能 热能电能直接转化?问题初探2:火力发电有哪些弊端呢?燃烧氧化还原反应将化学能经一系列能量转化为电能关键本质体系能量变化伴随火力发电过程的深层分析实验探究1:如何将化学能转化为电能?铜棒表面有气泡产生,电流表指针发生偏转现象1、原电池: 将化学能转变成电能的装置。化学能转化为电能实验探究2:构成原电池装置需要的条件用不同的电极材料完成实验实验探究2:构成原电池需要的条件微型实验改进玻璃片滤纸片电极夹电极材料铜棒牙签锌棒电极材料需要满足哪些条件?AAAA实验探究结果:构成原电池的电极条件电极为活泼性不同的导体活泼性不同的金属金属与非金属导体⑦能自发地发生氧化还原反应实验探究2:构成原电池装置需要的条件将滤纸上的液体替换为酒精两电极必须插在电解质溶液中A实验探究结果:构成原电池的液体条件这两套装置为何没有电流产生?没有构成闭合回路!2、构成原电池的条件
①具有活泼性不同的两个电极。
②两电极必须插在电解质溶液中。
③能自发地发生氧化还原反应。
④形成闭合回路。
两极一液一线一反应化学能转化为电能3、原电池原理:交流
讨论①导线上(外电路)电子的移动方向?
溶液中(内电路)离子的移动方向?
②你知道锌片和铜片上面发生哪些反应吗?电子移动方向:
锌片→铜片阴离子移向:锌片阳离子移向:铜片化学能转化为电能3、原电池原理:交流讨论电子移动方向:锌片→铜片
阴离子移向:锌片
阳离子移向:铜片阴离子移向的一极阳离子移向的一极 (锌):Zn – 2e- = Zn2+
(铜):2H+ +2e- = H2↑
电极
反应式反应本质:氧化还原反应还原反应氧化反应总反应:Zn+2H+= Zn2++H2↑正极负极还原剂(Zn)失去电子,发生氧化反应Zn2+氧化剂(H+)在铜极上得到电子,发生还原反应电子从锌极流出流入铜极.经外电路H+SO42-电流方向1、以下哪些装置可以形成原电池? +++2、写出电极反应式以及总反应,并判断正负极 负极(铜):Cu - 2e- = Cu2+正极(银):Ag+ + e- = AgCu + 2Ag+ = Cu2+ + 2Ag 正极(铁):2H++2e- =H2↑ 负极(锌):Zn -2e - = Zn2+ Zn+2H+=Zn2++H2↑请根据反应:Zn+Cu2+=Zn2++Cu设计原电池
画出装置图,写出电极反应式及产生的现象3、设计原电池 负极:Zn - 2e-?=Zn?2+?
正极:Cu2+?+2e-?=Cu 负极锌片溶解,正极上覆盖一层红色的铜。 作业1、完成全优练习册相应的内容
2、动手试试看,利用水果制作原电池,体验生活中的化学再见
