人教版九年级化学下册教学课件:碱的化学性质复习 (共28张PPT)
文档属性
| 名称 | 人教版九年级化学下册教学课件:碱的化学性质复习 (共28张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-04-10 00:00:00 | ||
图片预览







文档简介
课件28张PPT。人教版化学九年级下册第十一单元复习课 碱的化学性质复习
重点:碱的化学性质
难点:实验探究NaOH的变质及变质程度 学习目标: 碱的化学性质1.你能说出哪些碱的名称?会写其化学式吗?氢氧化钠NaOH 氢氧化钙Ca(OH)2
氢氧化钾(KOH)、氨水(NH3.H2O)3.不同碱的化学性质为什么是相似的?不同碱的溶液里都含有OH-2.烧碱是碱吗?纯碱是碱吗?
生石灰是碱吗?熟石灰是碱吗?氢氧化钠俗称烧碱、火碱、苛性钠,有吸水性,固体会潮解,可作某些气体的干燥剂,易溶于水,溶解时会放热。
氢氧化钙俗称熟石灰或消石灰,微溶于水,其水溶液俗称石灰水练习:化合物的分类有酸、碱、盐、氧化物等,下列物质哪些是酸、碱、盐、氧化物?
盐 碱 酸 盐 氧化物碱的化学性质碱与指示剂反应碱与某些非金属氧化物反应碱与酸反应碱与某些盐反应碱的化学性质
一、碱与指示剂反应 碱能使紫色石蕊溶液变蓝色,
使无色酚酞溶液变红色。问题1 氢氧化钾溶液中含有哪些粒子?含有H2O、K+、OH-问题2 是哪种粒子能使无色酚酞溶液变红?你能设计实验证明吗?
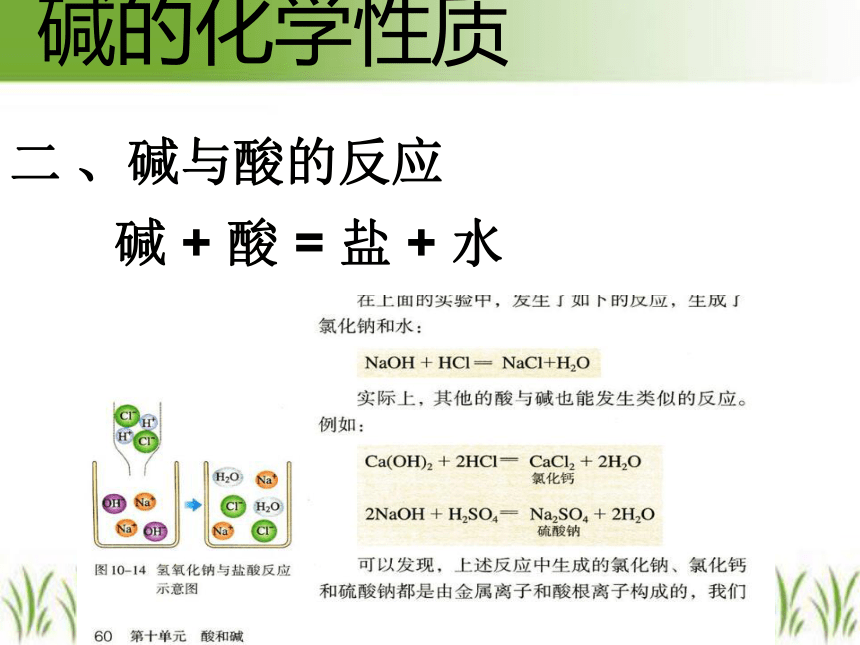
毕业综合训练册99页14题、95页例2碱的化学性质二 、碱与酸的反应NaOH与稀盐酸反应碱 + 酸 = 盐 + 水中和反应的实质酸溶液中的H+与碱溶液中的OH-结合成H2O。
2014福州15(3)某同学进
行图9所示实验,证明酸碱
发生反应的现象为:试管
中溶液由 色变为无色,
该反应的化学方程为 。实验后测得试管中溶液的pH=2,该溶液中的溶质有 (写化学式) 。练习红NaOH+HCl==NaCl+H2ONaCl、HCl碱的化学性质三 、碱与某些盐的反应碱 + 盐 = 另一种碱 + 另一种盐问题1:CuSO4溶液滴入NaOH溶液,观察到现象为 ,写出反应的化学方程式。CuSO4+2NaOH==Cu(OH)2↓+Na2SO4问题2:蓝色沉淀滴入稀盐酸,观察现象为 。写出反应的化学方程式.Cu(OH)2+2HCl==CuCl2+2H2O蓝色沉淀蓝色沉淀溶解哪一个是中和反应?CO32-Ca(OH)2溶液CaCO3Na+Na+OH-Ca2+OH-问:以上三个反应属于哪种反应类型?这类反应发生的条件是什么?属于复分解反应,酸碱盐之间发生反应,两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才能发生。化学反应向着离子浓度降低的方向进行。 碱的化学性质四 、碱与非金属氧化物反应碱 + 非金属氧化物 = 盐 + 水1、分别写出CO2通入澄清的石灰水、
NaOH溶液吸收CO2反应的化学方程式。
2、并仿照写出用氢氧化钠溶液吸收污染性气体二氧化硫的化学方程式1、分别写出CO2通入澄清的石灰水、
NaOH溶液与CO2反应的化学方程式。
2、并仿照写出用氢氧化钠溶液吸收污染性气体二氧化硫的化学方程式Ca(OH)2+CO2==CaCO3↓+H2O
2NaOH+CO2==Na2CO3+H2O
2NaOH+SO2==Na2SO3+H2O讨论:模考一探究题:用蜡烛代替红磷做验证空气组成的实验,请你设计方案除去集气瓶中蜡烛燃烧生的CO2,有同学选用了石灰水不得分,为什么要选用NaOH溶液呢?答案:因为Ca(OH)2的溶解度很小,石灰水的浓度低,不能有效吸收CO2,故要选用浓NaOH溶液。
因为NaOH溶液与CO2反应没有明显现象,而石灰水遇CO2变浑浊,故检验CO2要用澄清的石灰水。
所以检验CO2用澄清的石灰水,吸收CO2用NaOH溶液探究一如何验证一瓶NaOH溶液是否已经变质?
请选择不同类别的试剂,并写出化学方程式。1.稀盐酸3.CaCl2溶液2.Ca(OH)2溶液Na2CO3+2HCl==2NaCl+H2O+CO2↑Na2CO3+Ca(OH)2==CaCO3↓+2NaOHNa2CO3+CaCl2==CaCO3↓+2NaCl这瓶氢氧化钠溶液是全部变质还是部分变质呢?我的猜想 :②NaOH溶液部分变质①NaOH溶液全部变质全部变质:Na2CO3
部分变质:Na2CO3和NaOH想一想:我想知道探究二如果NaOH溶液全部变质,存在的溶质
有哪些?部分变质呢?下册78页用稀盐酸能判断NaOH是全部变质还是部分变质吗?1、加稀盐酸,没有气泡,则NaOH变有变质。
2、若NaOH部分变质,加过量稀盐酸,冒气泡,反应后溶液显酸性。
3、若NaOH全部变质,加过量稀盐酸,冒气泡,反应后溶液显酸性
所以用稀盐酸不能判断是否全部变质 Na2CO3+2HCl==2NaCl+H2O+CO2↑用Ca(OH)2溶液能判断NaOH溶液是全部变质还是部分变质吗?1、加石灰水,没有沉淀,则NaOH没有变质。
2、若NaOH部分变质,加过量石灰水,有沉淀,反应后溶液显碱性。
3、若NaOH全部变质,加过量石灰水,有沉淀,反应后溶液显碱性
所以用石灰水不能判断是否全部变质
Na2CO3+Ca(OH)2==CaCO3↓+2NaOHOH–Na+CO32-过量Ca(OH)2溶液CaCO3Na+Na+OH-Ca2+OH-Ca2+OH-Na+CO32-CaCO3Na+OH-Ca2+OH-OH-Ca2+OH-碱性碱性部分变质:Na2CO3和NaOH全部变质:Na2CO3OH-红色红色现象相同,不能用Ca(OH)2溶液和酚酞溶液。用CaCl2溶液能判断NaOH溶液是全部变质还是部分变质吗?1、加CaCl2溶液,没有沉淀,则NaOH没有变质。
2、若NaOH部分变质,加过量CaCl2溶液,有沉淀,反应后溶液显碱性(有NaOH,加酚酞试液显红色)。
3、若NaOH全部变质,加过量CaCl2溶液,有沉淀,反应后溶液显中性(无NaOH,加酚酞试液显无色)
所以用CaCl2溶液能判断是否全部变质
Na2CO3+CaCl2==CaCO3↓+2NaCl
OH–Na+CO32-过量CaCl2溶液CaCO3Na+Na+Cl-Ca2+Cl-Cl-Ca2+Cl-Na+CO32-CaCO3Na+Cl-Ca2+Cl-Cl-Ca2+Cl-碱性中性部分变质:Na2CO3和NaOH全部变质:Na2CO3红色无色现象不同,可以选择CaCl2溶液和酚酞溶液。 用CaCl2溶液能判断NaOH溶液是全部变质还是部分变质实验步骤:
1、加CaCl2溶液,没有沉淀,则NaOH没有变质。
2、加CaCl2溶液,有沉淀,滤出沉淀后的母液加无色酚酞试剂变红。 NaOH溶液部分变质,
3、 加CaCl2溶液,有沉淀,滤出沉淀后的母液加无色酚酞试剂不变色。 NaOH溶液全部变质,
所以用CaCl2溶液能判断是否全部变质
Na2CO3+CaCl2==CaCO3↓+2NaCl练习:毕业综合练册106页第3题探究实验:
分别用稀盐酸、澄清的石灰水、氯化钙溶液实验一瓶久置的氢氧化钠溶液是全部变质还是部分变质。
重点:碱的化学性质
难点:实验探究NaOH的变质及变质程度 学习目标: 碱的化学性质1.你能说出哪些碱的名称?会写其化学式吗?氢氧化钠NaOH 氢氧化钙Ca(OH)2
氢氧化钾(KOH)、氨水(NH3.H2O)3.不同碱的化学性质为什么是相似的?不同碱的溶液里都含有OH-2.烧碱是碱吗?纯碱是碱吗?
生石灰是碱吗?熟石灰是碱吗?氢氧化钠俗称烧碱、火碱、苛性钠,有吸水性,固体会潮解,可作某些气体的干燥剂,易溶于水,溶解时会放热。
氢氧化钙俗称熟石灰或消石灰,微溶于水,其水溶液俗称石灰水练习:化合物的分类有酸、碱、盐、氧化物等,下列物质哪些是酸、碱、盐、氧化物?
盐 碱 酸 盐 氧化物碱的化学性质碱与指示剂反应碱与某些非金属氧化物反应碱与酸反应碱与某些盐反应碱的化学性质
一、碱与指示剂反应 碱能使紫色石蕊溶液变蓝色,
使无色酚酞溶液变红色。问题1 氢氧化钾溶液中含有哪些粒子?含有H2O、K+、OH-问题2 是哪种粒子能使无色酚酞溶液变红?你能设计实验证明吗?
毕业综合训练册99页14题、95页例2碱的化学性质二 、碱与酸的反应NaOH与稀盐酸反应碱 + 酸 = 盐 + 水中和反应的实质酸溶液中的H+与碱溶液中的OH-结合成H2O。
2014福州15(3)某同学进
行图9所示实验,证明酸碱
发生反应的现象为:试管
中溶液由 色变为无色,
该反应的化学方程为 。实验后测得试管中溶液的pH=2,该溶液中的溶质有 (写化学式) 。练习红NaOH+HCl==NaCl+H2ONaCl、HCl碱的化学性质三 、碱与某些盐的反应碱 + 盐 = 另一种碱 + 另一种盐问题1:CuSO4溶液滴入NaOH溶液,观察到现象为 ,写出反应的化学方程式。CuSO4+2NaOH==Cu(OH)2↓+Na2SO4问题2:蓝色沉淀滴入稀盐酸,观察现象为 。写出反应的化学方程式.Cu(OH)2+2HCl==CuCl2+2H2O蓝色沉淀蓝色沉淀溶解哪一个是中和反应?CO32-Ca(OH)2溶液CaCO3Na+Na+OH-Ca2+OH-问:以上三个反应属于哪种反应类型?这类反应发生的条件是什么?属于复分解反应,酸碱盐之间发生反应,两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才能发生。化学反应向着离子浓度降低的方向进行。 碱的化学性质四 、碱与非金属氧化物反应碱 + 非金属氧化物 = 盐 + 水1、分别写出CO2通入澄清的石灰水、
NaOH溶液吸收CO2反应的化学方程式。
2、并仿照写出用氢氧化钠溶液吸收污染性气体二氧化硫的化学方程式1、分别写出CO2通入澄清的石灰水、
NaOH溶液与CO2反应的化学方程式。
2、并仿照写出用氢氧化钠溶液吸收污染性气体二氧化硫的化学方程式Ca(OH)2+CO2==CaCO3↓+H2O
2NaOH+CO2==Na2CO3+H2O
2NaOH+SO2==Na2SO3+H2O讨论:模考一探究题:用蜡烛代替红磷做验证空气组成的实验,请你设计方案除去集气瓶中蜡烛燃烧生的CO2,有同学选用了石灰水不得分,为什么要选用NaOH溶液呢?答案:因为Ca(OH)2的溶解度很小,石灰水的浓度低,不能有效吸收CO2,故要选用浓NaOH溶液。
因为NaOH溶液与CO2反应没有明显现象,而石灰水遇CO2变浑浊,故检验CO2要用澄清的石灰水。
所以检验CO2用澄清的石灰水,吸收CO2用NaOH溶液探究一如何验证一瓶NaOH溶液是否已经变质?
请选择不同类别的试剂,并写出化学方程式。1.稀盐酸3.CaCl2溶液2.Ca(OH)2溶液Na2CO3+2HCl==2NaCl+H2O+CO2↑Na2CO3+Ca(OH)2==CaCO3↓+2NaOHNa2CO3+CaCl2==CaCO3↓+2NaCl这瓶氢氧化钠溶液是全部变质还是部分变质呢?我的猜想 :②NaOH溶液部分变质①NaOH溶液全部变质全部变质:Na2CO3
部分变质:Na2CO3和NaOH想一想:我想知道探究二如果NaOH溶液全部变质,存在的溶质
有哪些?部分变质呢?下册78页用稀盐酸能判断NaOH是全部变质还是部分变质吗?1、加稀盐酸,没有气泡,则NaOH变有变质。
2、若NaOH部分变质,加过量稀盐酸,冒气泡,反应后溶液显酸性。
3、若NaOH全部变质,加过量稀盐酸,冒气泡,反应后溶液显酸性
所以用稀盐酸不能判断是否全部变质 Na2CO3+2HCl==2NaCl+H2O+CO2↑用Ca(OH)2溶液能判断NaOH溶液是全部变质还是部分变质吗?1、加石灰水,没有沉淀,则NaOH没有变质。
2、若NaOH部分变质,加过量石灰水,有沉淀,反应后溶液显碱性。
3、若NaOH全部变质,加过量石灰水,有沉淀,反应后溶液显碱性
所以用石灰水不能判断是否全部变质
Na2CO3+Ca(OH)2==CaCO3↓+2NaOHOH–Na+CO32-过量Ca(OH)2溶液CaCO3Na+Na+OH-Ca2+OH-Ca2+OH-Na+CO32-CaCO3Na+OH-Ca2+OH-OH-Ca2+OH-碱性碱性部分变质:Na2CO3和NaOH全部变质:Na2CO3OH-红色红色现象相同,不能用Ca(OH)2溶液和酚酞溶液。用CaCl2溶液能判断NaOH溶液是全部变质还是部分变质吗?1、加CaCl2溶液,没有沉淀,则NaOH没有变质。
2、若NaOH部分变质,加过量CaCl2溶液,有沉淀,反应后溶液显碱性(有NaOH,加酚酞试液显红色)。
3、若NaOH全部变质,加过量CaCl2溶液,有沉淀,反应后溶液显中性(无NaOH,加酚酞试液显无色)
所以用CaCl2溶液能判断是否全部变质
Na2CO3+CaCl2==CaCO3↓+2NaCl
OH–Na+CO32-过量CaCl2溶液CaCO3Na+Na+Cl-Ca2+Cl-Cl-Ca2+Cl-Na+CO32-CaCO3Na+Cl-Ca2+Cl-Cl-Ca2+Cl-碱性中性部分变质:Na2CO3和NaOH全部变质:Na2CO3红色无色现象不同,可以选择CaCl2溶液和酚酞溶液。 用CaCl2溶液能判断NaOH溶液是全部变质还是部分变质实验步骤:
1、加CaCl2溶液,没有沉淀,则NaOH没有变质。
2、加CaCl2溶液,有沉淀,滤出沉淀后的母液加无色酚酞试剂变红。 NaOH溶液部分变质,
3、 加CaCl2溶液,有沉淀,滤出沉淀后的母液加无色酚酞试剂不变色。 NaOH溶液全部变质,
所以用CaCl2溶液能判断是否全部变质
Na2CO3+CaCl2==CaCO3↓+2NaCl练习:毕业综合练册106页第3题探究实验:
分别用稀盐酸、澄清的石灰水、氯化钙溶液实验一瓶久置的氢氧化钠溶液是全部变质还是部分变质。
同课章节目录
