第2节 物质转化的规律
图片预览


文档简介
登陆21世纪教育 助您教考全无忧
第2节 物质转化的规律
联想情景导入
你一定非常熟悉明代诗人于谦所写的《石灰吟》吧。“千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间。”于谦在这首诗中真实地描写了从石灰石到碳酸钙的变化过程。自然界中的所有物质都在不停地发生变化,科学家常利用物质与物质之间的反应,制造出许多新的物质,使物质世界更加丰富多彩。那么,哪些种类的物质之间可以发生化学反应呢 物质之间的反应遵循怎样的规律呢
重点知识详解
一、非金属单质与其化合物的转化
1.非金属单质在氧气中燃烧可生成非金属氧化物;如将淡黄色的硫黄粉末在氧气中燃烧,产生明亮的蓝紫色火焰,生成一种无色有刺激性气味的二氧化硫气体。
S+O2SO2,
2.大部分的非金属氧化物可溶于水,生成对应的酸;如将二氧化碳通往紫色的石蕊试液,紫色的石蕊试液变红。将红色溶液加热,又变成原来的紫色。说明二氧化碳与水反应生成相应的酸。
CO2+H2O=H2CO3 H2CO3CO2↑+H2O
3.非金属氧化物可与碱反应生成相应的盐和水。
CO2+2NaOH=Na2CO3+H2O
4.非金属单质与其化合物转化的一般规律。
C→CO2→H2CO3
非金属单质非金属氧化物酸
二、金属单质与其化合物的转化21世纪教育网
1.金属与非金属可以相互反应,生成相应的盐。
S+FeFeS 2Fe+3Cl2FeCl3
2.金属与氧气可以相互反应,生成相应的金属氧化物。
3F2+2O2Fe3O4 2Mg+O22MgO
3.有些金属氧化物可以和水相互反应,生成相应的碱。
CaO+H2O=Ca(OH)2
4.金属氧化物与还原性物质发生氧化——还原反应,生成相应的金属。
C+2CuO=2Cu+CO2↑ CO+CuOCu+CO2
H2+CuOCu+H2O
三、化合物之间的相互转化21世纪教育网
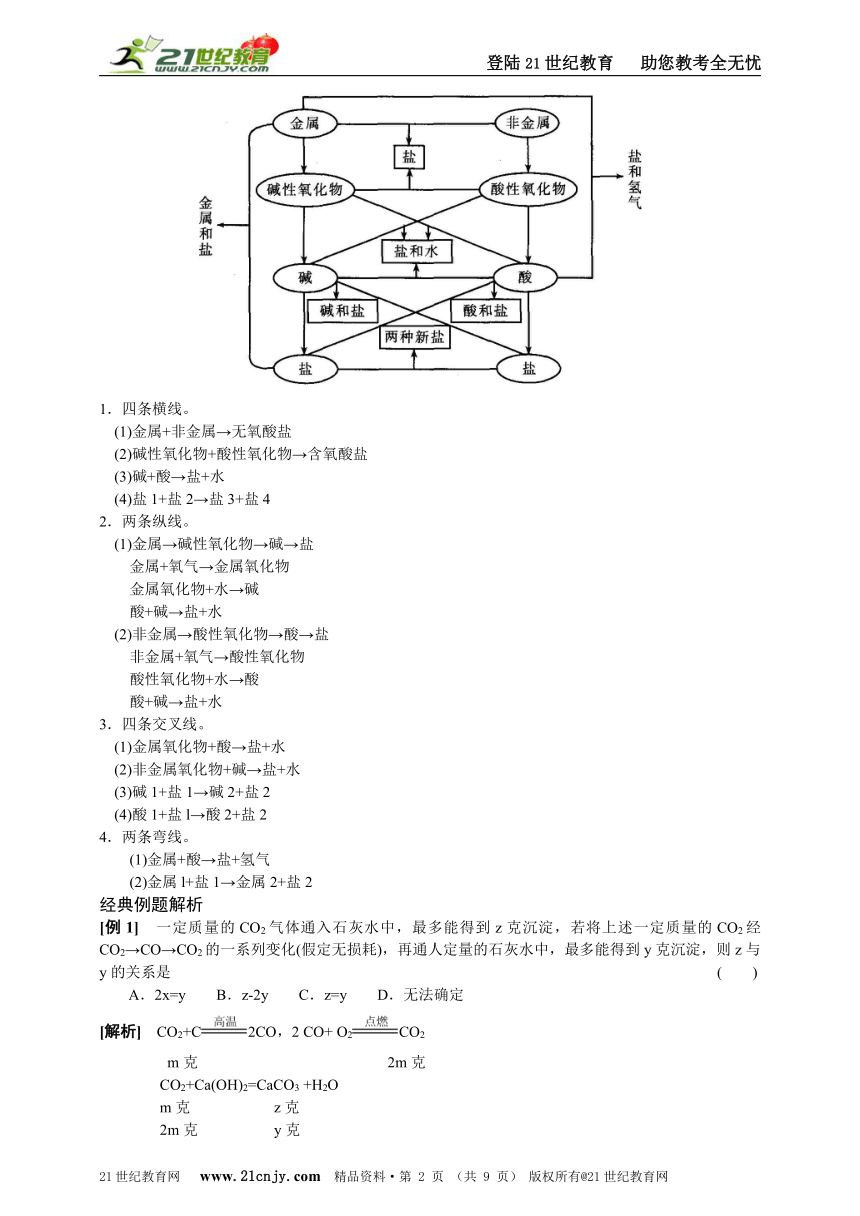
1.四条横线。
(1)金属+非金属→无氧酸盐
(2)碱性氧化物+酸性氧化物→含氧酸盐
(3)碱+酸→盐+水
(4)盐1+盐2→盐3+盐4
2.两条纵线。
(1)金属→碱性氧化物→碱→盐
金属+氧气→金属氧化物
金属氧化物+水→碱
酸+碱→盐+水21世纪教育网
(2)非金属→酸性氧化物→酸→盐
非金属+氧气→酸性氧化物
酸性氧化物+水→酸
酸+碱→盐+水
3.四条交叉线。
(1)金属氧化物+酸→盐+水
(2)非金属氧化物+碱→盐+水
(3)碱1+盐1→碱2+盐2
(4)酸1+盐l→酸2+盐2
4.两条弯线。
(1)金属+酸→盐+氢气
(2)金属l+盐1→金属2+盐2
经典例题解析
[例1] 一定质量的CO2气体通入石灰水中,最多能得到z克沉淀,若将上述一定质量的CO2经CO2→CO→CO2的一系列变化(假定无损耗),再通人定量的石灰水中,最多能得到y克沉淀,则z与y的关系是 ( )
A.2x=y B.z-2y C.z=y D.无法确定
[解析] CO2+C2CO,2 CO+ O2CO2
m克 2m克
CO2+Ca(OH)2=CaCO3 +H2O
m克 z克
2m克 y克
2x=y
[答案] A
[例2] 将一定质量的CaCO3和Cu粉置于同一敞口容器中,加热煅烧后使其完全反应,反应前后容器内的固体质量不变,则容器内CaCO3和Cu粉的质量比为 ( )
A.11:4 B.25:44 C.25:16 D.14:25
[解析] CaCO3加热会发生分解反应生成二氧化碳而失去质量,铜粉在受热的条件下,能与空气中的氧气结合生成氧化铜而增重,反应前后容器内的固体质量不变,说明CaCO3分解产生的CO2的质量恰好等于与铜粉反应氧气的质量。根据反应CaCO3CaO+CO2↑,2Cu+O22CuO,建立关系式可解。21世纪教育网
[答案] B21世纪教育网
[例3] 某无色气体可能含有H2、CO、CO2和N2中的一种或几种,当混合气体依次通过紫色石蕊试液时,紫色石蕊试液没有变色;通过灼热的氧化铜时有红色的铜生成;通过澄清的石灰水时,石灰水变浑浊。该气体一定含有,一定不含_______,可能含有_______。
[解析] 混合气体通过紫色石蕊试液时,石蕊不变色,说明没有CO2;通过灼热的氧化铜时有红色的铜生成,说明有H2或CO或H2、CO的混合气体;再根据通过澄清的石灰水时,石灰水变浑浊,推知肯定有CO2,而CO2是由CO和氧化铜反应生成的,由此推断一定有CO,H2和N2是否存在无法确定。21世纪教育网
[答案] CO CO2 H2和N2
[例4] 为鉴别硫酸钾、氢氧化钡、盐酸、氯化钾、氢氧化钾五种无色溶液,先加入一种试剂,鉴别出一种物质,并把未鉴别出的物质分为两组,再进行鉴别,填空回答:先加入一种 试剂就可以鉴别出 _______。把余下的四种物质分成两组,甲组是 _______,乙组是_______。在甲组中加入适量的_______或_______试剂就可以区别开来,在乙组中加入适量的或_______试剂就可以区别开来。
[解析] 硫酸钾、氢氧化钡、盐酸、氯化钾、氢氧化钾分别属于酸、碱、盐三类物质。硫酸钾、氯化钾属于盐,氢氧化钡、氢氧化钾属于碱,盐酸属于酸。取五种溶液少许,分别滴加紫色石蕊试液,使紫色石蕊试液变红色的是盐酸,使紫色石蕊试液变蓝色的是氢氧化钡、氢氧化钾,紫色石蕊试液不变色的是硫酸钾、氯化钾。这样,把未鉴别出的物质分为硫酸钾和氯化钾、氢氧化钡和氢氧化钾两组。SO42-和Ba2+相互结合生成不溶解于稀硝酸的白色沉淀。所以,硫酸钾和氯化钾可滴加含有Ba2+的溶液进行鉴别,氢氧化钡和氢氧化钾可滴加含有SO42-的物质进行鉴别。21世纪教育网
[答案] 石蕊盐酸硫酸钾和氯化钾 氢氧化钡和氢氧化钾 氯化钡 氢氧化钡硫酸硫酸钾
[例5] 有一包混合物,其中可能是含有碳酸氢铵、碳酸钙、炭粉、氧化铜、氧化铁中的一种或几种。现作如下实验,第一步:取样品,高温灼热后产生一种无色无味的气体,将该气体通入澄清的石灰水中,石灰水变浑浊;第二步:把足量稀盐酸滴入固体残留物后,残留物全部溶解,同时产生一种具有还原性的气体。试回答:21世纪教育网
①混合物中一定不含有的物质是_______。
②混合物中一定含有的物质是_______;在实验中肯定发生的反应化学方程式是____________________________。
③混合物中可能含有的物质是_______;为证明它是否存在,应采用的方法是_____________________。若确实有该物质存在,那么在第二步实验中,还可发生的化学反应有___________________________ (用化学方程式表示)。
[解析] 由第一步实验产生无色无味的气体可推知,混合物中肯定不存在碳酸氢铵。能使澄清的石灰水变浑浊的气体是二氧化碳,它可能来自于碳酸钙分解,也可能来自炭粉与氧化铜或炭粉与氧化铁反应后的产物,所以此时不能判断碳酸钙的存在,根据第二步实验加稀盐酸后残留物全部溶解,且有还原性气体产生,可知一定存在单质铁而无单质铜,因为炭与氧化铜反应的产物铜不溶于盐酸,进而推知原混合物中一定存在氧化铁和炭,而无氧化铜。
[答案] ①NH4HCO3和CuO ②C和Fe2O3 3C+2Fe2O34Fe+3CO2↑CO2+Ca(OH)2= CaCO3↓+H2O Fe+2HCl=FeCl2+H2↑ ③碳酸钙(或CaCO3)若证明存在碳酸钙,可取少量样品,加入适量的稀盐酸,若产生能使澄清石灰水变浑浊的气体,则证明存在碳酸钙,否则不含有碳酸钙CaCO3+2HCl=CaCl2+CO2↑+H2O
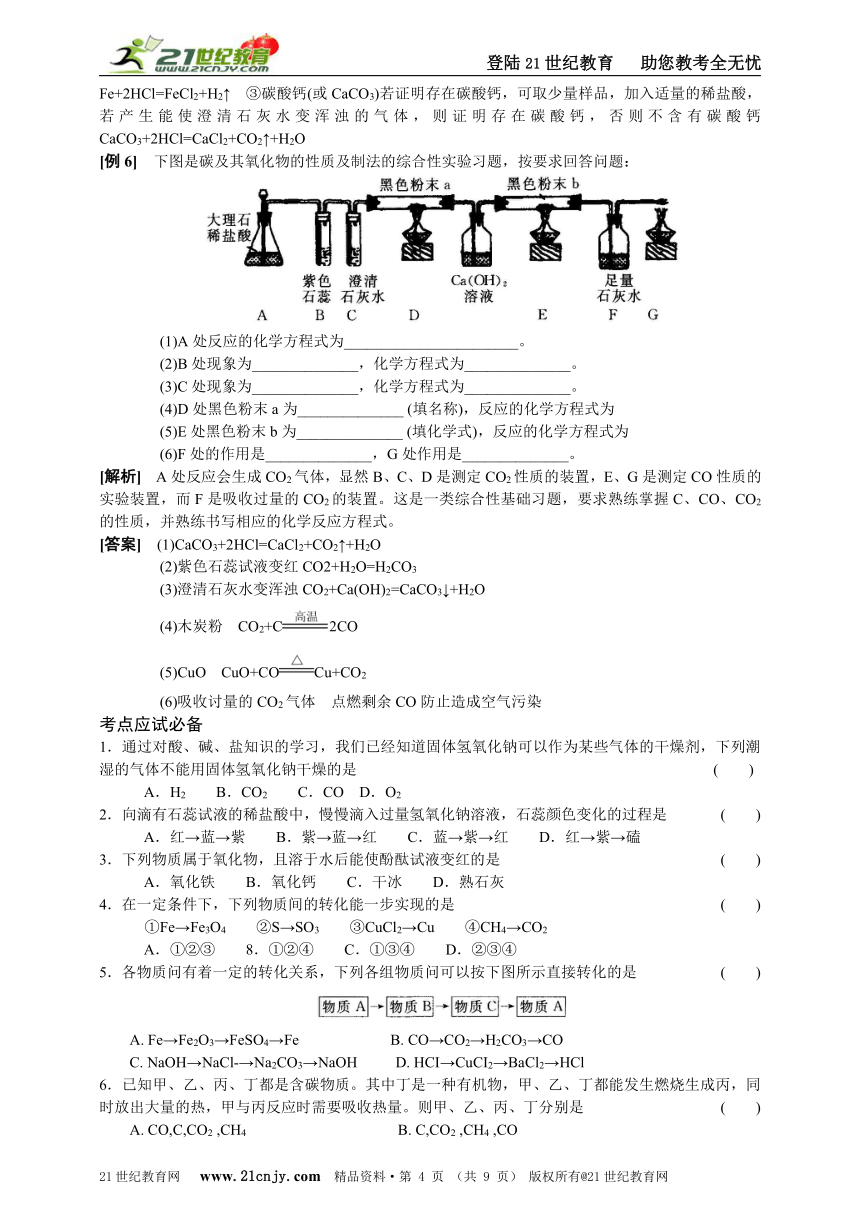
[例6] 下图是碳及其氧化物的性质及制法的综合性实验习题,按要求回答问题:21世纪教育网
(1)A处反应的化学方程式为 _______________________。
(2)B处现象为______________,化学方程式为______________。
(3)C处现象为______________,化学方程式为______________。
(4)D处黑色粉末a为______________ (填名称),反应的化学方程式为
(5)E处黑色粉末b为______________ (填化学式),反应的化学方程式为
(6)F处的作用是______________,G处作用是______________。
[解析] A处反应会生成CO2气体,显然B、C、D是测定CO2性质的装置,E、G是测定CO性质的实验装置,而F是吸收过量的CO2的装置。这是一类综合性基础习题,要求熟练掌握C、CO、CO2的性质,并熟练书写相应的化学反应方程式。21世纪教育网
[答案] (1)CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)紫色石蕊试液变红CO2+H2O=H2CO3
(3)澄清石灰水变浑浊CO2+Ca(OH)2=CaCO3↓+H2O
(4)木炭粉 CO2+C2CO
(5)CuO CuO+COCu+CO2
(6)吸收讨量的CO2气体 点燃剩余CO防止造成空气污染
考点应试必备
1.通过对酸、碱、盐知识的学习,我们已经知道固体氢氧化钠可以作为某些气体的干燥剂,下列潮湿的气体不能用固体氢氧化钠干燥的是 ( )
A.H2 B.CO2 C.CO D.O2
2.向滴有石蕊试液的稀盐酸中,慢慢滴入过量氢氧化钠溶液,石蕊颜色变化的过程是 ( )
A.红→蓝→紫 B.紫→蓝→红 C.蓝→紫→红 D.红→紫→磕
3.下列物质属于氧化物,且溶于水后能使酚酞试液变红的是 ( )
A.氧化铁 B.氧化钙 C.干冰 D.熟石灰
4.在一定条件下,下列物质间的转化能一步实现的是 ( )
①Fe→Fe3O4 ②S→SO3 ③CuCl2→Cu ④CH4→CO2
A.①②③ 8.①②④ C.①③④ D.②③④21世纪教育网
5.各物质问有着一定的转化关系,下列各组物质问可以按下图所示直接转化的是 ( )
A. Fe→Fe2O3→FeSO4→Fe B. CO→CO2→H2CO3→CO
C. NaOH→NaCl-→Na2CO3→NaOH D. HCI→CuCI2→BaCl2→HCl
6.已知甲、乙、丙、丁都是含碳物质。其中丁是一种有机物,甲、乙、丁都能发生燃烧生成丙,同时放出大量的热,甲与丙反应时需要吸收热量。则甲、乙、丙、丁分别是 ( )
A. CO,C,CO2 ,CH4 B. C,CO2 ,CH4 ,CO
C. C,CO,CO2 ,CH4 D. C,O2 ,CO2 ,CH4
7.我国已发射“嫦娥I号”卫星,卫星运载火箭的动力由高氯酸铵(NH4ClO3)分解提供。高氯酸铵分解有可能排入大气的物质是 ( )
A.H2O B.SO2 C.CO2 D.CO 21世纪教育网
8.下列物质循环过程中,不能经过一步反应实现的是 ( )
A.HCl—CuCl2 B.Na2SO4一NaCl
C.CO—CO2 D.Fe2O3—Fe(OH)3
9.某种牵牛花清晨呈粉红色,下午变为蓝紫色。原因是:清晨该牵牛花细胞内CO2含景较高,细胞液呈酸性;下午细胞内CO2含量较低。由此推测,该牵牛花中含有能变色的物质,这种物质的性质类似于 ( )
A.碘溶液 B.酚酞试液 C.石蕊试液 D.硫酸溶液
10.铜片在酒精灯上加热后表面变黑,有同学认为黑色物质是氧化铜(CuO),也有同学认为黑色物质是酒精不完全燃烧生成的炭黑(C)。下列试剂中,只要一步反应即可判断哪种观点正确的是 ( )
A.蒸馏水 B.稀硫酸 C.氯化钡溶液 D.氢氧化钠溶液
11.把含有少量氧化铜的铁粉加入稀盐酸中,加热充分反应后,发现铁粉有剩余。将溶液过滤,滤液中可能含有的溶质是 ( )
A.稀盐酸 B.氯化铜 C.氯化铁 D.氯化亚铁21世纪教育网
12.下列除杂(括号内是杂质)所选试剂合理的是 ( )
A.Cu(Fe) 稀盐酸
B.CO2气体(HCl) 氢氧化钠溶液
C.CuO(Cu) 稀硫酸
D.Na2SO4溶液 (Na2CO3) 氯化钡溶液
13.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如下图所示的四组实验方案,其中能达到目的的是 ( )
14.下列应用的原理用化学方程式表示正确的是 ( )
A.用适量的稀盐酸除铁锈 Fe2O3+6HCl=2FeCl2+3H2O
B.用一氧化碳作燃料 CO+O2CO2
C.高温煅烧石灰石制取生石灰 CaCO3CaO+CO2↑
D.用红磷燃烧测定空气中氧气含量P+O2P2O5
15.下列物质的转化能实现的是 ( )
A.H2SO4 HCl B.CO Na2CO3
C.Cu(OH)2 NaOH D.NaNO3 Ba(NO3)2
16.为防止水体污染并回收某种金属,某工厂向含有硫酸铜的废水中加入一定量的铁粉,充分反应后过滤、洗涤、干燥得滤渣,取少量滤渣向其中加入稀盐酸产生气泡。则滤渣中一定含有的物质是_________(填化学式),用化学方程式表示产生气泡的原因:___________________________。
17.1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔 在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。21世纪教育网
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH4)。反应化学方程式为 ____________________________________。
(2)用分别表示N2、H2、NH4。观察下图,写出符合在催化剂表面合成氨反应过程的顺序:________________________(将下面五张图按反应过程顺序用序号排列)。21世纪教育网
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程。在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O2的溶解,水膜呈中性。若空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式:_________________。在汽车排气管上安装尾气净化装置,可使尾气中的CO和NO在催化剂表面发生反应,产生两种空气组成的气体,写出该反应的化学方程式: 。
18.(1)2008年5月18日,奥运火炬在杭州传递。“祥云”火炬中的燃料含有C3H8,它燃烧的化学方程式是__________________________________。21世纪教育网
(2)某化工厂产生的废水中含有氢氟酸(HF),技术人员用熟石灰对废水进行处理,使其达标排放。写出该反应的化学方程式:__________________________________。
19.用木炭还原氧化铜的实验如下图。21世纪教育网
(1)酒精灯加网罩的目的_________________。
(2)刚开始预热,试管②中立即产生气泡,但澄清石灰水不变浑浊,原因是_________________。
(3)继续加热,观察到黑色粉末中出现红色物质,澄清石灰水逐渐变浑浊。请你写出带点部分的化学方程式:_________________、_________________。
(4)停止加热时,应先将导管从试管②中撤出,并用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出。这样操作的原因是_________________。
20.下图表示的是物质A—H相互间的关系(“→”表示物质间的转化关系,“——”表示两端的物质能发生化学反应)。A、G都是常见单质,气体C常用于灭火,D是纯碱,E是熟石灰,F是一种蓝色溶液,可用于配制农药波尔多液。请你回答:21世纪教育网
(1)C的化学式 __________,H可能是 __________。
(2)写出标号①、②、③、④的化学方程式:
① __________ __________;② __________ __________ ;
③ __________ __________;④ __________ __________。
21.小兵和小东是某校化学研究性学习小组的成员,他们在查阅资料时,发现单质碳能够在高温时与金属氧化物反应得到金属单质。于是,他们用木炭与CuO进行了如下的探究活动。请你参与他们的这次活动,并解决有关问题:
[提出问题] ,
木炭与氧化铜反应除生成单质铜外,另一种生成物是什么
[猜想与假设] 21世纪教育网
(1)可能是CO。(2)可能是CO2。
[设计实验方案]
(1)检验CO2的方法是_________________ 。
(2)为了检验CO2他们在互联网上用Google收集到这样一条信息:把滤纸浸泡在磷钼酸和氯化钯的黄色混合溶液中制成的试纸遇CO立即变成蓝色,而遇CO2不变色。
[实验与结论] 21世纪教育网
设计的实验装置图如下:
实验现象 实验结论
A中固体由黑色变成红色 有___________生成
B中黄色试纸没有变蓝 没有___________生成
C中______________________ 有CO2生成
22.2008年年初,我国南方出现了大面积的冰雪灾害,在除雪过程中,融雪剂发挥了很大的作用。某公司生产的融雪剂是由氯化钠、硝酸钠、氯化镁、硫酸铜中的两种或两种以上的物质组成的。小佳同学为探究其成分,设计并完成了以下实验:21世纪教育网
请你根据以上设计过程,完成下列空白:
(1)该融雪剂中一定含有________ (写化学式,下同),一定不含有________,可能含有________。
(2)在过滤后的滤液中加入硝酸银溶液发生反应的化学方程式是________ 。
23.新华网 杭州5月17日电(记者胡作华、傅丕毅)奥运圣火在浙江杭州传递的时间及路线将大幅精简。18日在杭州进行的圣火传递原定进行9小时53分钟。四川汶川发生强烈地震后,为了支援灾区,杭州市火炬传递将简化程序,传递时间压缩为3小时45分钟,而且传递沿途将重点安排赈灾内容。奥运“祥云”火炬在工艺上采用了高品质的铝合金外壳和中空塑件设计。请根据下列材料,回答有关问题:21世纪教育网
(1)铝合金材料中的铝是通过下列反应制得的:2Al2O3(熔融)4AI+3O2↑。其中,冰晶石作熔剂,可使Al2O3更易离解成自由离子。冰晶石的化学式为Na2AlF6,则其中氟元素的化合价为________。
(2)“祥云”火炬所用的燃料是丙烷(化学式为C3H8),它与甲烷(CH4)、丁烷(C4H10)属于同一系列的有机物一一烷烃。烷烃系列中还有戊烷(C5H12)、己烷(C6H14)等许多物质。根据上述几种烷烃的化学式与名称,可知分子中含两个碳原子的烷烃的化学式是 ____________________,所有烷烃中含氢量最高的物质是__________。
(3)丙烷完全燃烧后生成二氧化碳和水,则其化学反应方程式为 __________________ 。
(4)若将丙烷完全燃烧后产生的CO2气体,通入一定量的澄清石灰水中,产生的沉淀与通入CO2气体的质量关系如下图所示,则产生沉淀的最大质量是_____g,请计算原石灰水中所含溶质的质量。[已知:CaCO3+CO2+H2O=Ca(HCO3)2,Ca(HCO3)2易溶于水] 21世纪教育网
参考答案
1.B 2.D 3.B 4.C 5.D 6.C 7.A 8.D 9.C 10.B 11.D 12.A 13.D 14.C 15.A 16.Fe和Cu Fe+2HCl=FeCl2+H2↑ 17.(1)N2 +3H22NH4 (2)⑤④①②③ (3)H2O+CO2=H2CO3 2CO+2NON2+2CO2 18. (1)C3H8+5O23CO2+4H2O (2)Ca(OH)2+2HF=CaF2↓+2H2O 19.(1)提高酒精灯火焰的温度 (2)开始排出的是试管内的空气 (3)C+2CuO2Cu+CO2 CO2+Ca(OH)2=CaCO3↓+H2O (4)防止水倒流入试管,防止生成的铜被氧化 20.(1)CO2 HCl等(合理即可) (3)①2C+O22CO ②2NaOH+CO2=Na2CO3+H2O ③Na2CO3+Ca(OH)2=CaCO3↓+2NaOH ④Fe+CuSO4=Cu+FeSO4 21.[设计实验方案]:(1)将气体通入澄清石灰水,若澄清石灰水变浑浊,说明该气体是二氧化碳 (2)[实验与结论]:Cu CO通人澄清石灰水,澄清石灰水变浑浊22.(1)MgCl2 CuSO4 NaCl和NaNO3 (2)AgNO3+NaCl=AgCl++NaNO3 23.(1)-1价 (2)C2H6 甲烷(或CH4) (3) C3H8+5O23CO2+4H2O (4)10 7.49
高温、高压
催化剂
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网 www.21cnjy.com 精品资料·第 1 页 (共 9 页) 版权所有@21世纪教育网
第2节 物质转化的规律
联想情景导入
你一定非常熟悉明代诗人于谦所写的《石灰吟》吧。“千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间。”于谦在这首诗中真实地描写了从石灰石到碳酸钙的变化过程。自然界中的所有物质都在不停地发生变化,科学家常利用物质与物质之间的反应,制造出许多新的物质,使物质世界更加丰富多彩。那么,哪些种类的物质之间可以发生化学反应呢 物质之间的反应遵循怎样的规律呢
重点知识详解
一、非金属单质与其化合物的转化
1.非金属单质在氧气中燃烧可生成非金属氧化物;如将淡黄色的硫黄粉末在氧气中燃烧,产生明亮的蓝紫色火焰,生成一种无色有刺激性气味的二氧化硫气体。
S+O2SO2,
2.大部分的非金属氧化物可溶于水,生成对应的酸;如将二氧化碳通往紫色的石蕊试液,紫色的石蕊试液变红。将红色溶液加热,又变成原来的紫色。说明二氧化碳与水反应生成相应的酸。
CO2+H2O=H2CO3 H2CO3CO2↑+H2O
3.非金属氧化物可与碱反应生成相应的盐和水。
CO2+2NaOH=Na2CO3+H2O
4.非金属单质与其化合物转化的一般规律。
C→CO2→H2CO3
非金属单质非金属氧化物酸
二、金属单质与其化合物的转化21世纪教育网
1.金属与非金属可以相互反应,生成相应的盐。
S+FeFeS 2Fe+3Cl2FeCl3
2.金属与氧气可以相互反应,生成相应的金属氧化物。
3F2+2O2Fe3O4 2Mg+O22MgO
3.有些金属氧化物可以和水相互反应,生成相应的碱。
CaO+H2O=Ca(OH)2
4.金属氧化物与还原性物质发生氧化——还原反应,生成相应的金属。
C+2CuO=2Cu+CO2↑ CO+CuOCu+CO2
H2+CuOCu+H2O
三、化合物之间的相互转化21世纪教育网
1.四条横线。
(1)金属+非金属→无氧酸盐
(2)碱性氧化物+酸性氧化物→含氧酸盐
(3)碱+酸→盐+水
(4)盐1+盐2→盐3+盐4
2.两条纵线。
(1)金属→碱性氧化物→碱→盐
金属+氧气→金属氧化物
金属氧化物+水→碱
酸+碱→盐+水21世纪教育网
(2)非金属→酸性氧化物→酸→盐
非金属+氧气→酸性氧化物
酸性氧化物+水→酸
酸+碱→盐+水
3.四条交叉线。
(1)金属氧化物+酸→盐+水
(2)非金属氧化物+碱→盐+水
(3)碱1+盐1→碱2+盐2
(4)酸1+盐l→酸2+盐2
4.两条弯线。
(1)金属+酸→盐+氢气
(2)金属l+盐1→金属2+盐2
经典例题解析
[例1] 一定质量的CO2气体通入石灰水中,最多能得到z克沉淀,若将上述一定质量的CO2经CO2→CO→CO2的一系列变化(假定无损耗),再通人定量的石灰水中,最多能得到y克沉淀,则z与y的关系是 ( )
A.2x=y B.z-2y C.z=y D.无法确定
[解析] CO2+C2CO,2 CO+ O2CO2
m克 2m克
CO2+Ca(OH)2=CaCO3 +H2O
m克 z克
2m克 y克
2x=y
[答案] A
[例2] 将一定质量的CaCO3和Cu粉置于同一敞口容器中,加热煅烧后使其完全反应,反应前后容器内的固体质量不变,则容器内CaCO3和Cu粉的质量比为 ( )
A.11:4 B.25:44 C.25:16 D.14:25
[解析] CaCO3加热会发生分解反应生成二氧化碳而失去质量,铜粉在受热的条件下,能与空气中的氧气结合生成氧化铜而增重,反应前后容器内的固体质量不变,说明CaCO3分解产生的CO2的质量恰好等于与铜粉反应氧气的质量。根据反应CaCO3CaO+CO2↑,2Cu+O22CuO,建立关系式可解。21世纪教育网
[答案] B21世纪教育网
[例3] 某无色气体可能含有H2、CO、CO2和N2中的一种或几种,当混合气体依次通过紫色石蕊试液时,紫色石蕊试液没有变色;通过灼热的氧化铜时有红色的铜生成;通过澄清的石灰水时,石灰水变浑浊。该气体一定含有,一定不含_______,可能含有_______。
[解析] 混合气体通过紫色石蕊试液时,石蕊不变色,说明没有CO2;通过灼热的氧化铜时有红色的铜生成,说明有H2或CO或H2、CO的混合气体;再根据通过澄清的石灰水时,石灰水变浑浊,推知肯定有CO2,而CO2是由CO和氧化铜反应生成的,由此推断一定有CO,H2和N2是否存在无法确定。21世纪教育网
[答案] CO CO2 H2和N2
[例4] 为鉴别硫酸钾、氢氧化钡、盐酸、氯化钾、氢氧化钾五种无色溶液,先加入一种试剂,鉴别出一种物质,并把未鉴别出的物质分为两组,再进行鉴别,填空回答:先加入一种 试剂就可以鉴别出 _______。把余下的四种物质分成两组,甲组是 _______,乙组是_______。在甲组中加入适量的_______或_______试剂就可以区别开来,在乙组中加入适量的或_______试剂就可以区别开来。
[解析] 硫酸钾、氢氧化钡、盐酸、氯化钾、氢氧化钾分别属于酸、碱、盐三类物质。硫酸钾、氯化钾属于盐,氢氧化钡、氢氧化钾属于碱,盐酸属于酸。取五种溶液少许,分别滴加紫色石蕊试液,使紫色石蕊试液变红色的是盐酸,使紫色石蕊试液变蓝色的是氢氧化钡、氢氧化钾,紫色石蕊试液不变色的是硫酸钾、氯化钾。这样,把未鉴别出的物质分为硫酸钾和氯化钾、氢氧化钡和氢氧化钾两组。SO42-和Ba2+相互结合生成不溶解于稀硝酸的白色沉淀。所以,硫酸钾和氯化钾可滴加含有Ba2+的溶液进行鉴别,氢氧化钡和氢氧化钾可滴加含有SO42-的物质进行鉴别。21世纪教育网
[答案] 石蕊盐酸硫酸钾和氯化钾 氢氧化钡和氢氧化钾 氯化钡 氢氧化钡硫酸硫酸钾
[例5] 有一包混合物,其中可能是含有碳酸氢铵、碳酸钙、炭粉、氧化铜、氧化铁中的一种或几种。现作如下实验,第一步:取样品,高温灼热后产生一种无色无味的气体,将该气体通入澄清的石灰水中,石灰水变浑浊;第二步:把足量稀盐酸滴入固体残留物后,残留物全部溶解,同时产生一种具有还原性的气体。试回答:21世纪教育网
①混合物中一定不含有的物质是_______。
②混合物中一定含有的物质是_______;在实验中肯定发生的反应化学方程式是____________________________。
③混合物中可能含有的物质是_______;为证明它是否存在,应采用的方法是_____________________。若确实有该物质存在,那么在第二步实验中,还可发生的化学反应有___________________________ (用化学方程式表示)。
[解析] 由第一步实验产生无色无味的气体可推知,混合物中肯定不存在碳酸氢铵。能使澄清的石灰水变浑浊的气体是二氧化碳,它可能来自于碳酸钙分解,也可能来自炭粉与氧化铜或炭粉与氧化铁反应后的产物,所以此时不能判断碳酸钙的存在,根据第二步实验加稀盐酸后残留物全部溶解,且有还原性气体产生,可知一定存在单质铁而无单质铜,因为炭与氧化铜反应的产物铜不溶于盐酸,进而推知原混合物中一定存在氧化铁和炭,而无氧化铜。
[答案] ①NH4HCO3和CuO ②C和Fe2O3 3C+2Fe2O34Fe+3CO2↑CO2+Ca(OH)2= CaCO3↓+H2O Fe+2HCl=FeCl2+H2↑ ③碳酸钙(或CaCO3)若证明存在碳酸钙,可取少量样品,加入适量的稀盐酸,若产生能使澄清石灰水变浑浊的气体,则证明存在碳酸钙,否则不含有碳酸钙CaCO3+2HCl=CaCl2+CO2↑+H2O
[例6] 下图是碳及其氧化物的性质及制法的综合性实验习题,按要求回答问题:21世纪教育网
(1)A处反应的化学方程式为 _______________________。
(2)B处现象为______________,化学方程式为______________。
(3)C处现象为______________,化学方程式为______________。
(4)D处黑色粉末a为______________ (填名称),反应的化学方程式为
(5)E处黑色粉末b为______________ (填化学式),反应的化学方程式为
(6)F处的作用是______________,G处作用是______________。
[解析] A处反应会生成CO2气体,显然B、C、D是测定CO2性质的装置,E、G是测定CO性质的实验装置,而F是吸收过量的CO2的装置。这是一类综合性基础习题,要求熟练掌握C、CO、CO2的性质,并熟练书写相应的化学反应方程式。21世纪教育网
[答案] (1)CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)紫色石蕊试液变红CO2+H2O=H2CO3
(3)澄清石灰水变浑浊CO2+Ca(OH)2=CaCO3↓+H2O
(4)木炭粉 CO2+C2CO
(5)CuO CuO+COCu+CO2
(6)吸收讨量的CO2气体 点燃剩余CO防止造成空气污染
考点应试必备
1.通过对酸、碱、盐知识的学习,我们已经知道固体氢氧化钠可以作为某些气体的干燥剂,下列潮湿的气体不能用固体氢氧化钠干燥的是 ( )
A.H2 B.CO2 C.CO D.O2
2.向滴有石蕊试液的稀盐酸中,慢慢滴入过量氢氧化钠溶液,石蕊颜色变化的过程是 ( )
A.红→蓝→紫 B.紫→蓝→红 C.蓝→紫→红 D.红→紫→磕
3.下列物质属于氧化物,且溶于水后能使酚酞试液变红的是 ( )
A.氧化铁 B.氧化钙 C.干冰 D.熟石灰
4.在一定条件下,下列物质间的转化能一步实现的是 ( )
①Fe→Fe3O4 ②S→SO3 ③CuCl2→Cu ④CH4→CO2
A.①②③ 8.①②④ C.①③④ D.②③④21世纪教育网
5.各物质问有着一定的转化关系,下列各组物质问可以按下图所示直接转化的是 ( )
A. Fe→Fe2O3→FeSO4→Fe B. CO→CO2→H2CO3→CO
C. NaOH→NaCl-→Na2CO3→NaOH D. HCI→CuCI2→BaCl2→HCl
6.已知甲、乙、丙、丁都是含碳物质。其中丁是一种有机物,甲、乙、丁都能发生燃烧生成丙,同时放出大量的热,甲与丙反应时需要吸收热量。则甲、乙、丙、丁分别是 ( )
A. CO,C,CO2 ,CH4 B. C,CO2 ,CH4 ,CO
C. C,CO,CO2 ,CH4 D. C,O2 ,CO2 ,CH4
7.我国已发射“嫦娥I号”卫星,卫星运载火箭的动力由高氯酸铵(NH4ClO3)分解提供。高氯酸铵分解有可能排入大气的物质是 ( )
A.H2O B.SO2 C.CO2 D.CO 21世纪教育网
8.下列物质循环过程中,不能经过一步反应实现的是 ( )
A.HCl—CuCl2 B.Na2SO4一NaCl
C.CO—CO2 D.Fe2O3—Fe(OH)3
9.某种牵牛花清晨呈粉红色,下午变为蓝紫色。原因是:清晨该牵牛花细胞内CO2含景较高,细胞液呈酸性;下午细胞内CO2含量较低。由此推测,该牵牛花中含有能变色的物质,这种物质的性质类似于 ( )
A.碘溶液 B.酚酞试液 C.石蕊试液 D.硫酸溶液
10.铜片在酒精灯上加热后表面变黑,有同学认为黑色物质是氧化铜(CuO),也有同学认为黑色物质是酒精不完全燃烧生成的炭黑(C)。下列试剂中,只要一步反应即可判断哪种观点正确的是 ( )
A.蒸馏水 B.稀硫酸 C.氯化钡溶液 D.氢氧化钠溶液
11.把含有少量氧化铜的铁粉加入稀盐酸中,加热充分反应后,发现铁粉有剩余。将溶液过滤,滤液中可能含有的溶质是 ( )
A.稀盐酸 B.氯化铜 C.氯化铁 D.氯化亚铁21世纪教育网
12.下列除杂(括号内是杂质)所选试剂合理的是 ( )
A.Cu(Fe) 稀盐酸
B.CO2气体(HCl) 氢氧化钠溶液
C.CuO(Cu) 稀硫酸
D.Na2SO4溶液 (Na2CO3) 氯化钡溶液
13.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如下图所示的四组实验方案,其中能达到目的的是 ( )
14.下列应用的原理用化学方程式表示正确的是 ( )
A.用适量的稀盐酸除铁锈 Fe2O3+6HCl=2FeCl2+3H2O
B.用一氧化碳作燃料 CO+O2CO2
C.高温煅烧石灰石制取生石灰 CaCO3CaO+CO2↑
D.用红磷燃烧测定空气中氧气含量P+O2P2O5
15.下列物质的转化能实现的是 ( )
A.H2SO4 HCl B.CO Na2CO3
C.Cu(OH)2 NaOH D.NaNO3 Ba(NO3)2
16.为防止水体污染并回收某种金属,某工厂向含有硫酸铜的废水中加入一定量的铁粉,充分反应后过滤、洗涤、干燥得滤渣,取少量滤渣向其中加入稀盐酸产生气泡。则滤渣中一定含有的物质是_________(填化学式),用化学方程式表示产生气泡的原因:___________________________。
17.1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔 在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。21世纪教育网
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH4)。反应化学方程式为 ____________________________________。
(2)用分别表示N2、H2、NH4。观察下图,写出符合在催化剂表面合成氨反应过程的顺序:________________________(将下面五张图按反应过程顺序用序号排列)。21世纪教育网
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程。在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O2的溶解,水膜呈中性。若空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式:_________________。在汽车排气管上安装尾气净化装置,可使尾气中的CO和NO在催化剂表面发生反应,产生两种空气组成的气体,写出该反应的化学方程式: 。
18.(1)2008年5月18日,奥运火炬在杭州传递。“祥云”火炬中的燃料含有C3H8,它燃烧的化学方程式是__________________________________。21世纪教育网
(2)某化工厂产生的废水中含有氢氟酸(HF),技术人员用熟石灰对废水进行处理,使其达标排放。写出该反应的化学方程式:__________________________________。
19.用木炭还原氧化铜的实验如下图。21世纪教育网
(1)酒精灯加网罩的目的_________________。
(2)刚开始预热,试管②中立即产生气泡,但澄清石灰水不变浑浊,原因是_________________。
(3)继续加热,观察到黑色粉末中出现红色物质,澄清石灰水逐渐变浑浊。请你写出带点部分的化学方程式:_________________、_________________。
(4)停止加热时,应先将导管从试管②中撤出,并用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出。这样操作的原因是_________________。
20.下图表示的是物质A—H相互间的关系(“→”表示物质间的转化关系,“——”表示两端的物质能发生化学反应)。A、G都是常见单质,气体C常用于灭火,D是纯碱,E是熟石灰,F是一种蓝色溶液,可用于配制农药波尔多液。请你回答:21世纪教育网
(1)C的化学式 __________,H可能是 __________。
(2)写出标号①、②、③、④的化学方程式:
① __________ __________;② __________ __________ ;
③ __________ __________;④ __________ __________。
21.小兵和小东是某校化学研究性学习小组的成员,他们在查阅资料时,发现单质碳能够在高温时与金属氧化物反应得到金属单质。于是,他们用木炭与CuO进行了如下的探究活动。请你参与他们的这次活动,并解决有关问题:
[提出问题] ,
木炭与氧化铜反应除生成单质铜外,另一种生成物是什么
[猜想与假设] 21世纪教育网
(1)可能是CO。(2)可能是CO2。
[设计实验方案]
(1)检验CO2的方法是_________________ 。
(2)为了检验CO2他们在互联网上用Google收集到这样一条信息:把滤纸浸泡在磷钼酸和氯化钯的黄色混合溶液中制成的试纸遇CO立即变成蓝色,而遇CO2不变色。
[实验与结论] 21世纪教育网
设计的实验装置图如下:
实验现象 实验结论
A中固体由黑色变成红色 有___________生成
B中黄色试纸没有变蓝 没有___________生成
C中______________________ 有CO2生成
22.2008年年初,我国南方出现了大面积的冰雪灾害,在除雪过程中,融雪剂发挥了很大的作用。某公司生产的融雪剂是由氯化钠、硝酸钠、氯化镁、硫酸铜中的两种或两种以上的物质组成的。小佳同学为探究其成分,设计并完成了以下实验:21世纪教育网
请你根据以上设计过程,完成下列空白:
(1)该融雪剂中一定含有________ (写化学式,下同),一定不含有________,可能含有________。
(2)在过滤后的滤液中加入硝酸银溶液发生反应的化学方程式是________ 。
23.新华网 杭州5月17日电(记者胡作华、傅丕毅)奥运圣火在浙江杭州传递的时间及路线将大幅精简。18日在杭州进行的圣火传递原定进行9小时53分钟。四川汶川发生强烈地震后,为了支援灾区,杭州市火炬传递将简化程序,传递时间压缩为3小时45分钟,而且传递沿途将重点安排赈灾内容。奥运“祥云”火炬在工艺上采用了高品质的铝合金外壳和中空塑件设计。请根据下列材料,回答有关问题:21世纪教育网
(1)铝合金材料中的铝是通过下列反应制得的:2Al2O3(熔融)4AI+3O2↑。其中,冰晶石作熔剂,可使Al2O3更易离解成自由离子。冰晶石的化学式为Na2AlF6,则其中氟元素的化合价为________。
(2)“祥云”火炬所用的燃料是丙烷(化学式为C3H8),它与甲烷(CH4)、丁烷(C4H10)属于同一系列的有机物一一烷烃。烷烃系列中还有戊烷(C5H12)、己烷(C6H14)等许多物质。根据上述几种烷烃的化学式与名称,可知分子中含两个碳原子的烷烃的化学式是 ____________________,所有烷烃中含氢量最高的物质是__________。
(3)丙烷完全燃烧后生成二氧化碳和水,则其化学反应方程式为 __________________ 。
(4)若将丙烷完全燃烧后产生的CO2气体,通入一定量的澄清石灰水中,产生的沉淀与通入CO2气体的质量关系如下图所示,则产生沉淀的最大质量是_____g,请计算原石灰水中所含溶质的质量。[已知:CaCO3+CO2+H2O=Ca(HCO3)2,Ca(HCO3)2易溶于水] 21世纪教育网
参考答案
1.B 2.D 3.B 4.C 5.D 6.C 7.A 8.D 9.C 10.B 11.D 12.A 13.D 14.C 15.A 16.Fe和Cu Fe+2HCl=FeCl2+H2↑ 17.(1)N2 +3H22NH4 (2)⑤④①②③ (3)H2O+CO2=H2CO3 2CO+2NON2+2CO2 18. (1)C3H8+5O23CO2+4H2O (2)Ca(OH)2+2HF=CaF2↓+2H2O 19.(1)提高酒精灯火焰的温度 (2)开始排出的是试管内的空气 (3)C+2CuO2Cu+CO2 CO2+Ca(OH)2=CaCO3↓+H2O (4)防止水倒流入试管,防止生成的铜被氧化 20.(1)CO2 HCl等(合理即可) (3)①2C+O22CO ②2NaOH+CO2=Na2CO3+H2O ③Na2CO3+Ca(OH)2=CaCO3↓+2NaOH ④Fe+CuSO4=Cu+FeSO4 21.[设计实验方案]:(1)将气体通入澄清石灰水,若澄清石灰水变浑浊,说明该气体是二氧化碳 (2)[实验与结论]:Cu CO通人澄清石灰水,澄清石灰水变浑浊22.(1)MgCl2 CuSO4 NaCl和NaNO3 (2)AgNO3+NaCl=AgCl++NaNO3 23.(1)-1价 (2)C2H6 甲烷(或CH4) (3) C3H8+5O23CO2+4H2O (4)10 7.49
高温、高压
催化剂
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网 www.21cnjy.com 精品资料·第 1 页 (共 9 页) 版权所有@21世纪教育网
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
