浙江省2018年中考科学系统复习专题16溶液
文档属性
| 名称 | 浙江省2018年中考科学系统复习专题16溶液 |

|
|
| 格式 | zip | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2018-05-11 00:00:00 | ||
图片预览








文档简介
课件29张PPT。
考点一 溶液 悬浊液 乳浊液专题16 溶液考点二 固体物质的溶解度考点三 溶质质量分数考点一 溶液 悬浊液 乳浊液1. 知道溶液的组成(a)
2. 说明溶液的特点,区别溶液、悬浊液和乳浊液(b)
3. 区别饱和溶液与不饱和溶液(b)
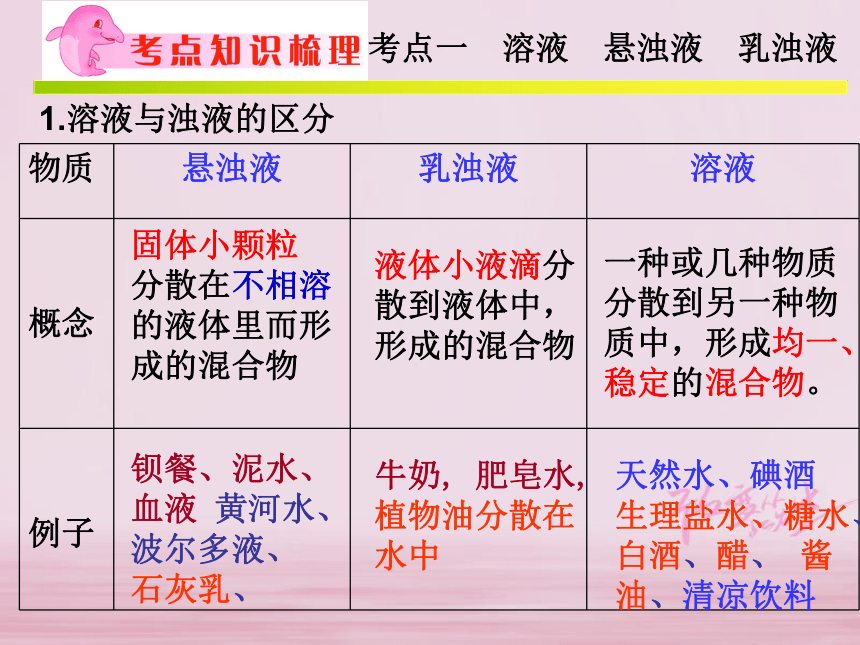
4. 列举影响物质溶解性的一些因素(a)1.溶液与浊液的区分固体小颗粒
分散在不相溶的液体里而形成的混合物液体小液滴分散到液体中,形成的混合物一种或几种物质 分散到另一种物 质中,形成均一、稳定的混合物。钡餐、泥水、
血液 黄河水、 波尔多液、 石灰乳、 天然水、碘酒
生理盐水、糖水、
白酒、醋、 酱油、清凉饮料牛奶, 肥皂水, 植物油分散在水中考点一 溶液 悬浊液 乳浊液1.溶液与浊液的区分考点一 溶液 悬浊液 乳浊液稳定:指条件不发生变化时 (如水分不蒸发,温度不改变),无论放置多久,溶质都不会分离出来均一:指各部分性质一样(密度一样),浓、稀一样。食盐水各部分咸味一样。糖水呢?各部分甜味一样均一的、稳定的、久置不分层的混合物
(不一定无色,不一定透明)2.溶液的特点:考点一 溶液 悬浊液 乳浊液不能溶于水的油污,可以用汽油、丙酮等有机溶剂去除 在一定温度下,在一定量的溶剂里不能继续溶解某种溶质的溶液称为这种溶质的饱和溶液。 (2). 不饱和溶液:
在一定温度下,在一定量的溶剂里 还能继续溶解某种溶质的溶液,称为这 种溶质的不饱和溶液。(1). 饱和溶液:其它溶质可溶溶解过程仍进行 V溶解 = V结晶3.如何判断溶液是否饱和?考点一 溶液 悬浊液 乳浊液饱和溶液不饱和溶液②升高温度(一般情况)②降低温度
??①增加溶剂①增加溶质③蒸发溶剂4.饱和溶液和不饱和溶液的相互转化注意:对少数溶液来说:例饱和石灰水与不饱和石灰水之间的转化条件(温度)则刚好相反
将不饱和溶液变为饱和溶液,最可靠的方法是( )
A 升高温度 B 降低温度
C 加入溶质 D 倒出溶剂
C考点一 溶液 悬浊液 乳浊液一种物质在另一种物质中溶解能力的大小。 6.影响物质溶解性的因素:(1)溶质、溶剂的性质(内因—决定因素)
(2)温度的影响(外因——影响因素)5.溶解性(定性):考点一 溶液 悬浊液 乳浊液练习4 在进行食盐、蔗糖和淀粉溶解性比较的实验时,不需要控制的条件是( )
A.溶质颗粒大小 B.溶剂的温度
C.溶剂的种类 D.溶剂的质量练一练A7.有的物质溶解时,会放出热量,使溶液温度升高,例如:浓硫酸、氢氧化钠固体;
有的物质溶解时,会吸收热量,使溶液温度降低,例如:硝酸铵练习5 【2017兰州】如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后U型管内液面a低于b,不符合上述实验现象的一组试剂是( )
A.生石灰和水 B.铁粉和稀盐酸
C.硝酸铵和水 D.纯碱和稀盐酸C练习1 【2017兰州】把少量下列物质分别放入水中,充分搅拌。可以得到溶液的是( )
A.面粉 B.苏打粉 C.花生油 D.牛奶(1)图中“?”是指 ;
(2)将5克食盐固体放入盛有20克蒸馏水的烧杯中, 充分搅拌后完全溶解。你是如何确定食盐固体“完全溶解”的? 。练习2B 溶剂烧杯底部观察不到食盐固体颗粒 练习3 下列有关溶液说法正确的是( )
A. 均一、稳定的液体一定是溶液
B. 饱和溶液降温析出晶体后的溶液一定是不饱和溶液
C. 饱和溶液的溶质质量分数一定比不饱和溶液的大
D. 一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液D考点二 固体物质的溶解度知道物质的溶解度的含义(不要求溶解度的计算)(a)是指在一定温度下,某种物质在100_g溶剂里达到饱和状态时所能溶解的溶质的质量.
2. 温度对溶解度的影响
大多数固体物质的溶解度随温度升高而增大,如:KNO3;
少数固体物质的溶解度受温度变化很小,如:NaCl;
极少数固体溶解度随温度升高而降低,如Ca(OH)2.
气体物质的溶解度随温度升高而减小。1. 溶解度考点二 固体物质的溶解度判断是非:
1、20℃时,10克食盐溶解在100克水中,
所以20℃时食盐的溶解度是10克。
2、100克水中溶解了36克食盐刚好达到饱和,
所以食盐的溶解度是36克。
3、在20℃时,100克水里最多溶解33.3克氯化
铵,则20℃氯化铵的溶解度是33.3。
4、50℃时,烧杯内水中最多溶有30克氯化钾,
所以氯化钾在水中的溶解度是30克。 5、在20℃时,100克硝酸钾饱和溶液里含硝酸
钾24克,则20℃硝酸钾的溶解度是24克。
6、在30℃时,100克水中加入40克氯化钾后达到
饱和溶液,则30℃时氯化钾的溶解度是40克。练习1 向常温下已饱和的石灰水中加少量的生石灰,溶液的质量随时间变化情况正确的是( )D练习2 (2016宁波)下表是不同温度时硝酸钾的溶解度,下列有关说法正确的是 ( )
A.硝酸钾的溶解度随温度的升高而增大
B.20℃时,100克水中溶解的硝酸钾越多溶解度就越大
C.40℃时,100克硝酸钾饱和溶液中含有硝酸钾63.9克
D.100℃时水中溶解的硝酸钾一定比80℃时水中溶解的硝酸钾多A 练习3 某同学为测定室温下Na2CO3的溶解度,在编号为A、B、C、D的四个烧杯中各加入室温下的水100 g,并分别加入取自实验室的Na2CO3固体,搅拌至充分溶解.实验数据记录如下表:分析上述数据可知,烧杯编号是 中的溶液是饱和溶液.室温下,Na2CO3的溶解度是 克.CD40考点三 溶质质量分数1. 说明溶液中溶质质量分数的意义(b)
2. 应用公式[溶质的质量分数=(溶质质量/溶液质量)×100%进行简单计算(c)
3. 按要求配制一定溶质质量分数的溶液,说明有关配制方案、步骤与操作方式(b)1.定义:是指溶液中溶质的质量与溶液的质量之比。2.公式: 适用任何溶液(m质必须是已溶解部分)15%的硫酸铜溶液的含义: 每100克硫酸铜溶液中有15克硫酸铜和85克水注意: 1.常用小数或百分数表示 2.溶质的质量与溶液质量的单位必须统一考点三 溶质质量分数
(1)计算:需食盐5克,水45毫升。
(2)称量:称量前,先将游码归零,调节平衡螺母至天平平衡;称量时左盘放食盐,右盘放砝码。量取45毫升的水,选用50mL的量筒;当倒入的水接近45mL时,改用胶头滴管加水;读数时,视线与凹液面最低处相平。
(3)溶解:用玻璃棒搅拌,可加快食盐的溶解。托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒
步骤所需仪器:3. 用食盐和水配制10%食盐水50克。考点三 溶质质量分数小明同学在实际操作中出现了如下操作,导致配制的氯化钠溶液质量分数偏小的有 .
A. 在托盘天平的左盘称取氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数
B. 氯化钠固体不纯
C. 量筒量取水前先用蒸馏水润洗
D. 将量筒中的水倒入烧杯时,有水洒出
E. 按照图B的方法读数;
F. 转移已配好的溶液时,有少量溶液洒落在瓶外
G. 盛装溶液的试剂瓶留有少量蒸馏水思考:ABEG.
(1)仪器:无需天平、药匙。
(2)计算时,关键要抓住稀释前后溶质质量不变。
(3)溶解时,不能在量筒中配制;要将浓硫酸沿杯壁或玻璃棒慢慢注入水中,并不断搅拌。
注意:(1)计算溶质质量分数时,留意有无未溶解的固体溶质。
(2)溶液稀释计算时,稀溶液的体积≠浓溶液的体积+加入的水的体积4.配制一定质量分数的稀硫酸需注意以下几点:考点三 溶质质量分数500ml
品名:盐酸
化学式:HC1
相对分子质量:36.5
密度:1.19g/ml
溶质质量分数:38%(1) HCl中氢元素和氯元素的质量比为 (结果用最简整数比表示)。
(2)这瓶盐酸溶液的质量为 g。
(3)现要配制3800g溶质质量分数为10%的稀盐酸,需要溶质质量分数为38%的浓盐酸的质量为 g,需要这种浓盐酸 瓶。
一瓶浓盐酸,标签如下:【答案】(1)2:71 (2)595 (3)1000 2练习1 已知20℃硝酸钾的溶解度为31.6g。在该温度下将40g硝酸钾放入100g水中,充分搅拌,则所得溶液中溶质的质量分数约为( )
A.24.0% B.28.6% C.31.6% D.40.0%A练习2 (2016绍兴)20℃时,向3个盛有50克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据回答。(l)实验所得3杯溶液中,属于不饱和溶液的是______(选填编号)。
(2)若将A杯中的溶液稀释成溶质的质量分数为0.9%的生理盐水,需加水_______克。
【答案:(1)A (2)941】练习3 (2016金华)A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入25g、10g、5g同种固体物质,充分溶解后,静置,现象如图所示,回答下列问题(填烧杯编号)
(1)A、B、C三只烧杯中的溶液一定是不饱和溶液的是 。 (2)A、B、C三只烧杯中溶液的溶质质量分数的大小关系是 。
【答案:(1)C (2)A≥B>C】练习5 “配制50 g 6%的氯化钠溶液”实验的部分操作如下图所示.(1)需要称取氯化钠的质量是 ,右边的托盘上需放左边的托盘相等质量的纸,其目的是 ;若称量时A出现了右盘略低的现象,接下来的具体操作是 .
(2)量取水时,应选用规格为50mL的量筒而不选用100mL的量筒,其目的是 ;
(3)C中用玻璃棒搅拌的作用是 .3g保持与左盘平衡右手轻拍持药匙的左手腕,将药匙中的药品添加到左盘中至天平平衡减少误差加快溶解速度1.D 2.C 3.B 4.D 5.C .6.D 7.C 8.B 9. (1)可能是(2)加快液面空气流速 10.(1)继续加KNO3固体(2)不饱和(3)降低温度(或蒸发水或加KNO3固体)
11.(1)CH4+2O2 CO2+2H2O(2)①氢氧化钠、尿素;②(或其他合理答案);③白色污染(或其他合理答案)【考点16综合训练答案】
考点一 溶液 悬浊液 乳浊液专题16 溶液考点二 固体物质的溶解度考点三 溶质质量分数考点一 溶液 悬浊液 乳浊液1. 知道溶液的组成(a)
2. 说明溶液的特点,区别溶液、悬浊液和乳浊液(b)
3. 区别饱和溶液与不饱和溶液(b)
4. 列举影响物质溶解性的一些因素(a)1.溶液与浊液的区分固体小颗粒
分散在不相溶的液体里而形成的混合物液体小液滴分散到液体中,形成的混合物一种或几种物质 分散到另一种物 质中,形成均一、稳定的混合物。钡餐、泥水、
血液 黄河水、 波尔多液、 石灰乳、 天然水、碘酒
生理盐水、糖水、
白酒、醋、 酱油、清凉饮料牛奶, 肥皂水, 植物油分散在水中考点一 溶液 悬浊液 乳浊液1.溶液与浊液的区分考点一 溶液 悬浊液 乳浊液稳定:指条件不发生变化时 (如水分不蒸发,温度不改变),无论放置多久,溶质都不会分离出来均一:指各部分性质一样(密度一样),浓、稀一样。食盐水各部分咸味一样。糖水呢?各部分甜味一样均一的、稳定的、久置不分层的混合物
(不一定无色,不一定透明)2.溶液的特点:考点一 溶液 悬浊液 乳浊液不能溶于水的油污,可以用汽油、丙酮等有机溶剂去除 在一定温度下,在一定量的溶剂里不能继续溶解某种溶质的溶液称为这种溶质的饱和溶液。 (2). 不饱和溶液:
在一定温度下,在一定量的溶剂里 还能继续溶解某种溶质的溶液,称为这 种溶质的不饱和溶液。(1). 饱和溶液:其它溶质可溶溶解过程仍进行 V溶解 = V结晶3.如何判断溶液是否饱和?考点一 溶液 悬浊液 乳浊液饱和溶液不饱和溶液②升高温度(一般情况)②降低温度
??①增加溶剂①增加溶质③蒸发溶剂4.饱和溶液和不饱和溶液的相互转化注意:对少数溶液来说:例饱和石灰水与不饱和石灰水之间的转化条件(温度)则刚好相反
将不饱和溶液变为饱和溶液,最可靠的方法是( )
A 升高温度 B 降低温度
C 加入溶质 D 倒出溶剂
C考点一 溶液 悬浊液 乳浊液一种物质在另一种物质中溶解能力的大小。 6.影响物质溶解性的因素:(1)溶质、溶剂的性质(内因—决定因素)
(2)温度的影响(外因——影响因素)5.溶解性(定性):考点一 溶液 悬浊液 乳浊液练习4 在进行食盐、蔗糖和淀粉溶解性比较的实验时,不需要控制的条件是( )
A.溶质颗粒大小 B.溶剂的温度
C.溶剂的种类 D.溶剂的质量练一练A7.有的物质溶解时,会放出热量,使溶液温度升高,例如:浓硫酸、氢氧化钠固体;
有的物质溶解时,会吸收热量,使溶液温度降低,例如:硝酸铵练习5 【2017兰州】如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后U型管内液面a低于b,不符合上述实验现象的一组试剂是( )
A.生石灰和水 B.铁粉和稀盐酸
C.硝酸铵和水 D.纯碱和稀盐酸C练习1 【2017兰州】把少量下列物质分别放入水中,充分搅拌。可以得到溶液的是( )
A.面粉 B.苏打粉 C.花生油 D.牛奶(1)图中“?”是指 ;
(2)将5克食盐固体放入盛有20克蒸馏水的烧杯中, 充分搅拌后完全溶解。你是如何确定食盐固体“完全溶解”的? 。练习2B 溶剂烧杯底部观察不到食盐固体颗粒 练习3 下列有关溶液说法正确的是( )
A. 均一、稳定的液体一定是溶液
B. 饱和溶液降温析出晶体后的溶液一定是不饱和溶液
C. 饱和溶液的溶质质量分数一定比不饱和溶液的大
D. 一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液D考点二 固体物质的溶解度知道物质的溶解度的含义(不要求溶解度的计算)(a)是指在一定温度下,某种物质在100_g溶剂里达到饱和状态时所能溶解的溶质的质量.
2. 温度对溶解度的影响
大多数固体物质的溶解度随温度升高而增大,如:KNO3;
少数固体物质的溶解度受温度变化很小,如:NaCl;
极少数固体溶解度随温度升高而降低,如Ca(OH)2.
气体物质的溶解度随温度升高而减小。1. 溶解度考点二 固体物质的溶解度判断是非:
1、20℃时,10克食盐溶解在100克水中,
所以20℃时食盐的溶解度是10克。
2、100克水中溶解了36克食盐刚好达到饱和,
所以食盐的溶解度是36克。
3、在20℃时,100克水里最多溶解33.3克氯化
铵,则20℃氯化铵的溶解度是33.3。
4、50℃时,烧杯内水中最多溶有30克氯化钾,
所以氯化钾在水中的溶解度是30克。 5、在20℃时,100克硝酸钾饱和溶液里含硝酸
钾24克,则20℃硝酸钾的溶解度是24克。
6、在30℃时,100克水中加入40克氯化钾后达到
饱和溶液,则30℃时氯化钾的溶解度是40克。练习1 向常温下已饱和的石灰水中加少量的生石灰,溶液的质量随时间变化情况正确的是( )D练习2 (2016宁波)下表是不同温度时硝酸钾的溶解度,下列有关说法正确的是 ( )
A.硝酸钾的溶解度随温度的升高而增大
B.20℃时,100克水中溶解的硝酸钾越多溶解度就越大
C.40℃时,100克硝酸钾饱和溶液中含有硝酸钾63.9克
D.100℃时水中溶解的硝酸钾一定比80℃时水中溶解的硝酸钾多A 练习3 某同学为测定室温下Na2CO3的溶解度,在编号为A、B、C、D的四个烧杯中各加入室温下的水100 g,并分别加入取自实验室的Na2CO3固体,搅拌至充分溶解.实验数据记录如下表:分析上述数据可知,烧杯编号是 中的溶液是饱和溶液.室温下,Na2CO3的溶解度是 克.CD40考点三 溶质质量分数1. 说明溶液中溶质质量分数的意义(b)
2. 应用公式[溶质的质量分数=(溶质质量/溶液质量)×100%进行简单计算(c)
3. 按要求配制一定溶质质量分数的溶液,说明有关配制方案、步骤与操作方式(b)1.定义:是指溶液中溶质的质量与溶液的质量之比。2.公式: 适用任何溶液(m质必须是已溶解部分)15%的硫酸铜溶液的含义: 每100克硫酸铜溶液中有15克硫酸铜和85克水注意: 1.常用小数或百分数表示 2.溶质的质量与溶液质量的单位必须统一考点三 溶质质量分数
(1)计算:需食盐5克,水45毫升。
(2)称量:称量前,先将游码归零,调节平衡螺母至天平平衡;称量时左盘放食盐,右盘放砝码。量取45毫升的水,选用50mL的量筒;当倒入的水接近45mL时,改用胶头滴管加水;读数时,视线与凹液面最低处相平。
(3)溶解:用玻璃棒搅拌,可加快食盐的溶解。托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒
步骤所需仪器:3. 用食盐和水配制10%食盐水50克。考点三 溶质质量分数小明同学在实际操作中出现了如下操作,导致配制的氯化钠溶液质量分数偏小的有 .
A. 在托盘天平的左盘称取氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数
B. 氯化钠固体不纯
C. 量筒量取水前先用蒸馏水润洗
D. 将量筒中的水倒入烧杯时,有水洒出
E. 按照图B的方法读数;
F. 转移已配好的溶液时,有少量溶液洒落在瓶外
G. 盛装溶液的试剂瓶留有少量蒸馏水思考:ABEG.
(1)仪器:无需天平、药匙。
(2)计算时,关键要抓住稀释前后溶质质量不变。
(3)溶解时,不能在量筒中配制;要将浓硫酸沿杯壁或玻璃棒慢慢注入水中,并不断搅拌。
注意:(1)计算溶质质量分数时,留意有无未溶解的固体溶质。
(2)溶液稀释计算时,稀溶液的体积≠浓溶液的体积+加入的水的体积4.配制一定质量分数的稀硫酸需注意以下几点:考点三 溶质质量分数500ml
品名:盐酸
化学式:HC1
相对分子质量:36.5
密度:1.19g/ml
溶质质量分数:38%(1) HCl中氢元素和氯元素的质量比为 (结果用最简整数比表示)。
(2)这瓶盐酸溶液的质量为 g。
(3)现要配制3800g溶质质量分数为10%的稀盐酸,需要溶质质量分数为38%的浓盐酸的质量为 g,需要这种浓盐酸 瓶。
一瓶浓盐酸,标签如下:【答案】(1)2:71 (2)595 (3)1000 2练习1 已知20℃硝酸钾的溶解度为31.6g。在该温度下将40g硝酸钾放入100g水中,充分搅拌,则所得溶液中溶质的质量分数约为( )
A.24.0% B.28.6% C.31.6% D.40.0%A练习2 (2016绍兴)20℃时,向3个盛有50克水的烧杯中,分别加入一定质量的氯化钠,并充分溶解。根据下表实验数据回答。(l)实验所得3杯溶液中,属于不饱和溶液的是______(选填编号)。
(2)若将A杯中的溶液稀释成溶质的质量分数为0.9%的生理盐水,需加水_______克。
【答案:(1)A (2)941】练习3 (2016金华)A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入25g、10g、5g同种固体物质,充分溶解后,静置,现象如图所示,回答下列问题(填烧杯编号)
(1)A、B、C三只烧杯中的溶液一定是不饱和溶液的是 。 (2)A、B、C三只烧杯中溶液的溶质质量分数的大小关系是 。
【答案:(1)C (2)A≥B>C】练习5 “配制50 g 6%的氯化钠溶液”实验的部分操作如下图所示.(1)需要称取氯化钠的质量是 ,右边的托盘上需放左边的托盘相等质量的纸,其目的是 ;若称量时A出现了右盘略低的现象,接下来的具体操作是 .
(2)量取水时,应选用规格为50mL的量筒而不选用100mL的量筒,其目的是 ;
(3)C中用玻璃棒搅拌的作用是 .3g保持与左盘平衡右手轻拍持药匙的左手腕,将药匙中的药品添加到左盘中至天平平衡减少误差加快溶解速度1.D 2.C 3.B 4.D 5.C .6.D 7.C 8.B 9. (1)可能是(2)加快液面空气流速 10.(1)继续加KNO3固体(2)不饱和(3)降低温度(或蒸发水或加KNO3固体)
11.(1)CH4+2O2 CO2+2H2O(2)①氢氧化钠、尿素;②(或其他合理答案);③白色污染(或其他合理答案)【考点16综合训练答案】
