浙江省2018年中考科学系统复习专题14物质的分类
文档属性
| 名称 | 浙江省2018年中考科学系统复习专题14物质的分类 |

|
|
| 格式 | zip | ||
| 文件大小 | 676.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2018-05-11 00:00:00 | ||
图片预览










文档简介
课件32张PPT。
考点一 物质的分类
考点二 纯净物和混合物
考点三 相对原子质量和相对分子质量
考点四 化学式
专题14 物质的分类1.根据物质的组成对常见的物质进行分类(c)
2.指认具体物质的类别(a)考点一 物质的分类 纯净物单 质化合物金属单质非金属单质(包括稀有气体单质)混合物 (含多种成分)物质 含一种成分含一种元素含多种元素氧化物酸:碱盐金属氧化物非金属氧化物无机化合物有机化合物一般不含碳 含碳二元一氧( 溶液 、浊液 、空气 、矿石、合金 )无机物 含碳的化合物(碳的氧化物、碳酸和碳酸盐除外)考点一 物质的分类1.物质分类及依据:结晶水合物属于纯净物,如CuSO4?5H2O等考点一 物质的分类2.氧化物与含氧化合物区分:氧化物属于含氧化合物,含氧化合物不一定是氧化物。3.结晶水合物是混合物吗?练习1 【2017德州】分类是研究物质的常用方法.右图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )
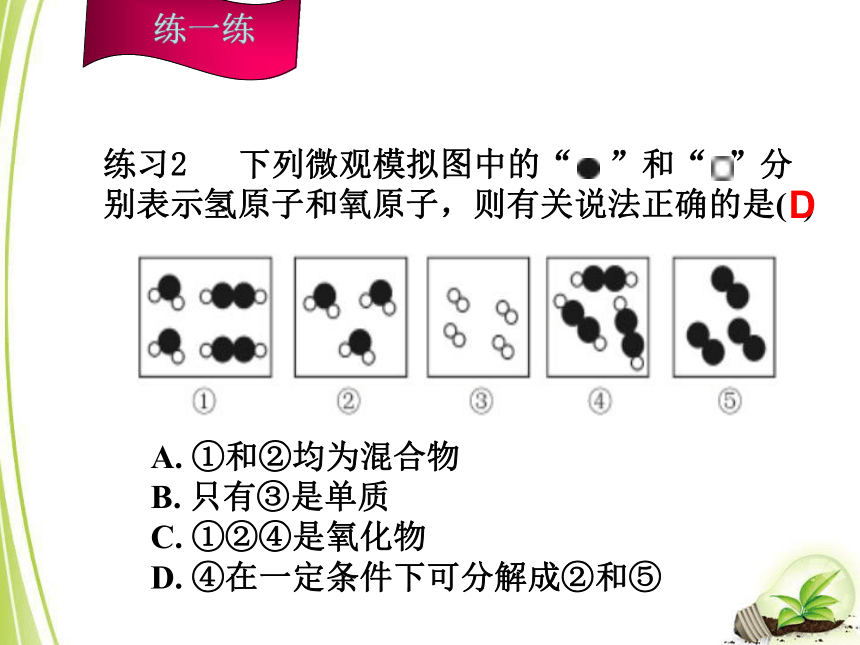
A.红磷 B.干冰 C.氯酸钾 D.食盐水B练习2 下列微观模拟图中的“ ”和“ ”分别表示氢原子和氧原子,则有关说法正确的是( )
A. ①和②均为混合物
B. 只有③是单质
C. ①②④是氧化物
D. ④在一定条件下可分解成②和⑤D练习3 有下列物质:
①液氧 ②净化的空气 ③五水合硫酸铜
④五氧化二磷 ⑤石灰石 ⑥生铁 ⑦ 干冰
⑧高锰酸钾 ⑨冰水混合物 ⑩碘酒。
试分类(填编号):
混合物: , 单质: ,
氧化物: ,化合物: . ②⑤⑩⑥①④⑦⑨③④⑦⑧⑨练习4 某校实验室将药品分类后放在不同的药品柜里,已存放的部分药品如下:
该实验室新购进部分生石灰和纯碱,应将它们分别放
在( )
A. ③和① B. ④和① C. ③和④ D. ①和②C考点二 纯净物和混合物
1.区别纯净物与混合物(b)
2.说明混合物分离的主要方法(过滤、蒸发)
及操作要点(b)
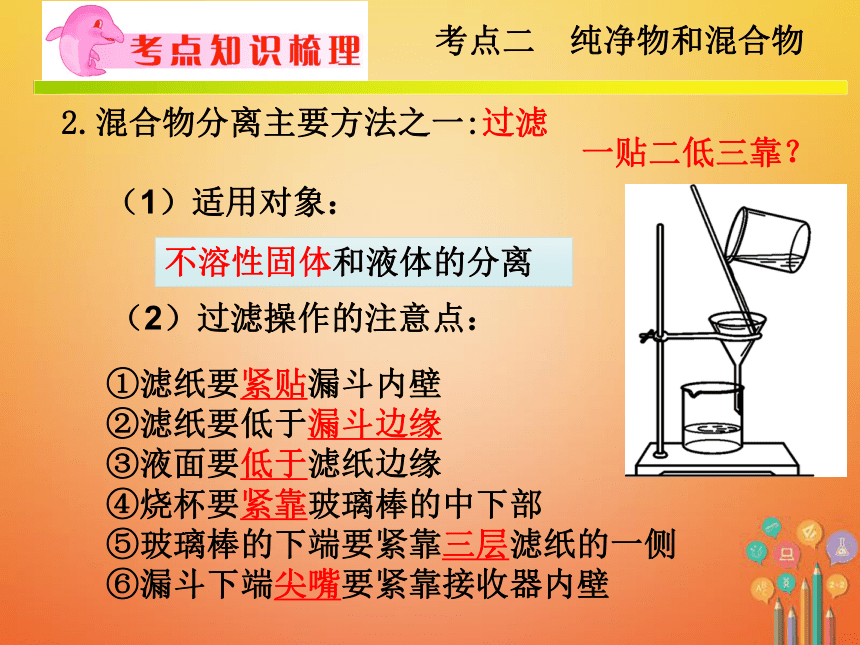
3.说明粗盐提纯的过程(b)1.区别纯净物与混合物考点二 纯净物和混合物2.混合物分离主要方法之一:过滤不溶性固体和液体的分离(1)适用对象:①滤纸要紧贴漏斗内壁
②滤纸要低于漏斗边缘
③液面要低于滤纸边缘
④烧杯要紧靠玻璃棒的中下部
⑤玻璃棒的下端要紧靠三层滤纸的一侧
⑥漏斗下端尖嘴要紧靠接收器内壁(2)过滤操作的注意点:一贴二低三靠?(3)生产实例①水厂用过滤池净水②生活中也可制作简易过滤器得到过滤水③制豆腐、榨汁机、除去粗盐中的泥沙④化学工业用压滤机等过滤设备分离固体和液体的
混合物考点二 纯净物和混合物2.混合物分离主要方法之一:过滤2.混合物分离主要方法之一:蒸发除去溶液中的溶剂(1)适用对象:①加热蒸发过程中应用 不断搅拌。
②当有 但还残留少量溶液时应停止加热,利用蒸发皿的 蒸发至干,以防飞溅。 (3)主要操作事项:玻璃棒较多固体析出余热(2)仪器:考点二 纯净物和混合物沸点不同的液体混合物的分离2.混合物分离主要方法之一:蒸馏(1)适用对象(2)小石子或碎瓷片的作用:(3)具体实例:防暴沸海水制淡水分离酒精和水石油分馏分离液态空气考点二 纯净物和混合物考点二 纯净物和混合物(1)步骤:粗盐溶解 → 过滤 →蒸发结晶(2)玻璃棒的作用分别是:加速溶解、
引流、
使溶液均匀受热以防止晶体飞溅。3.粗盐提纯练习1 某物质经鉴定只含一种元素,则错误的是( )
A.可能是混合物 B.可能是一种单质
C.可能是化合物 D.可能是纯净物
练习2 进行过滤操作时,下列做法错误的是( )
A. 玻璃棒要靠在三层滤纸的一边
B. 漏斗下端的管口要紧靠烧杯的内壁
C. 滤纸的边缘要低于漏斗口
D. 液面不要低于滤纸边缘CD 练习3 提纯含少量泥沙的粗盐,一般经过以下操作流程:( 1 )操作 ① 中必须用到的一种仪器是 。
A .研钵 B .量筒 C .烧杯 D .试管
( 2 )操作 ④ 中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是 ( 填序号 )A D( 3 )操作 ⑤ 中除用到三脚架、洒精灯、玻璃棒、坩埚钳外,还需要用到 等仪器。 该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取 等措施。
( 4 )实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低、其可能原因是 ( 填序号 ) .
A.食盐没有全部溶解即过滤
B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿
D.器皿上沾有的精盐没全部转移到称量纸上
蒸发皿 间歇加热(或 “ 来回移动酒精灯 ” ) ABD考点三 相对原子质量和相对分子质量1. 知道相对原子质量和相对分子质量的概念(a)
2. 查询相对原子质量 (b)
3. 根据化学式计算物质的相对分子质量 (b)考点三 相对原子质量和相对分子质量1. 相对原子质量:(2)其他原子的质量与这个标准相比较,所得的比值是该种原子的相对原子质量(1)标准:一个C—12原子质量的1/12,碳原子的1/12碳原子氧原子16氧的相对原子质量 = 1.661×10-27千克2.657×10-26千克1.993×10-26千克1.661×10-27千克16=国际上有7种元素的相对原子质量采用了张青莲教授测的数据。表2-13是他所测的部分元素的相对原子质量新标准值。考点三 相对原子质量和相对分子质量2.相对原子质量计算公式:3.相对原子质量数值:相对分子质量=分子中各原子的相对原子质量的总和。4. 相对分子质量:考点三 相对原子质量和相对分子质量练习1 若作为相对原子质量标准的碳原子的质量为m千克 ,一个碘原子的质量为n千克。则碘的相对原子质量为( )。
A. n B. 12n/m C. n/12 D. 12m/n
练习2 某化合物的化学式为HnRO2n+1 ,相对分子质量为M,则R元素的化合价是 ,R的相对原子质量是 。B+(3n + 2)M - 33n-16 考点四 化学式
1.认识常见物质的化学式 (b)
2.解释化学式所表示的含义(b)
3.根据化学式计算组成物质的元素的质量比(c)
4.根据化学式计算组成物质的某元素的质量分数(c)①表示某种物质;
②表示该物质的一个分子;
③表示该物质的组成元素;
④表示每个分子里各原子个数。1.化学式所表示的含义H2SO4 考点四 化学式2.根据化学式计算组成物质的元素的质量比各元素的相对原子量与原子个数乘积之比 钙:碳:氧=(40×1):(12×1):(16×3) = 10:3:12求碳酸钙中各元素的质量比考点四 化学式3.根据化学式计算组成物质的某元素的质量分数
水中 H % =某元素的质量分数 =该元素的原子个数×该元素相对原子质量化合物的相对分子质量×100%考点四 化学式练习1(2015台州)下列有关化学符号“H2O”表示的意义,正确的是 ( )
A.水这种物质
B.水由氢原子和氧原子构成
C.一个水分子中含有一个氢分子
D.水由两个氢元素和一个氧元素组成A练习2 (2016金华)花青素(化学式C15H11O6)具有缓解眼睛疲劳,保护视力的作用,该物质主要来源于各种蔬菜和水果。下列关于花青素的说法正确的是( )
A.花青素是一种无机物
B.花青素的相对分子质量是287g
C.花青素中的C、H、O元素质量比是15:11:6
D.花青素在氧气中充分燃烧后生成二氧化碳和水 D练习3 (2016绍兴)我国科学家屠呦呦因为“发现青蒿素化学式为C15H22O5)――一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素之前最热门的抗疟药物之一。回答下列同题。
(1)一个青蒿素分子中含有 ________ 个原子。
(2)青蒿素中的氢元素与氧元素的质量比是 ________ 。
(3)14.1克青蒿素中含有碳元素的质量和多少克磺胺中含有碳元素的质量相等?
【答案(1)42(2)11:40(3)21.5】练习4 如图,某同学绘制了三条表示某金属氧化物的质量与其所含金属元素的质量的关系曲线。横坐标表示金属氧化物的质量,纵坐标表示该金属氧化物中金属元素的质量。(1)三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是 。
(2)其中绘制错误的一条曲线(不能正确表示金属氧化物与它所含金属元素的质量的关系)是 ,理由是 .金属氧化物的质量一定大于金属质量BA1.A 2.D 3.D 4.B 5.C 6.C 7.A
8.(1) 单质 ⑵ FeO
⑶ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
9. (1)引流(2)C(3)用洁净的玻璃棒蘸取少量溶液,滴在pH试纸上,显示的颜色与标准比色卡对照
10.(1)+5(2)食盐B11.(1)红 (2)32(3)mc=28.7克×(15C/C15H11O6)=28.7克×(180/287)=18克 专题14 综合训练答案
考点一 物质的分类
考点二 纯净物和混合物
考点三 相对原子质量和相对分子质量
考点四 化学式
专题14 物质的分类1.根据物质的组成对常见的物质进行分类(c)
2.指认具体物质的类别(a)考点一 物质的分类 纯净物单 质化合物金属单质非金属单质(包括稀有气体单质)混合物 (含多种成分)物质 含一种成分含一种元素含多种元素氧化物酸:碱盐金属氧化物非金属氧化物无机化合物有机化合物一般不含碳 含碳二元一氧( 溶液 、浊液 、空气 、矿石、合金 )无机物 含碳的化合物(碳的氧化物、碳酸和碳酸盐除外)考点一 物质的分类1.物质分类及依据:结晶水合物属于纯净物,如CuSO4?5H2O等考点一 物质的分类2.氧化物与含氧化合物区分:氧化物属于含氧化合物,含氧化合物不一定是氧化物。3.结晶水合物是混合物吗?练习1 【2017德州】分类是研究物质的常用方法.右图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )
A.红磷 B.干冰 C.氯酸钾 D.食盐水B练习2 下列微观模拟图中的“ ”和“ ”分别表示氢原子和氧原子,则有关说法正确的是( )
A. ①和②均为混合物
B. 只有③是单质
C. ①②④是氧化物
D. ④在一定条件下可分解成②和⑤D练习3 有下列物质:
①液氧 ②净化的空气 ③五水合硫酸铜
④五氧化二磷 ⑤石灰石 ⑥生铁 ⑦ 干冰
⑧高锰酸钾 ⑨冰水混合物 ⑩碘酒。
试分类(填编号):
混合物: , 单质: ,
氧化物: ,化合物: . ②⑤⑩⑥①④⑦⑨③④⑦⑧⑨练习4 某校实验室将药品分类后放在不同的药品柜里,已存放的部分药品如下:
该实验室新购进部分生石灰和纯碱,应将它们分别放
在( )
A. ③和① B. ④和① C. ③和④ D. ①和②C考点二 纯净物和混合物
1.区别纯净物与混合物(b)
2.说明混合物分离的主要方法(过滤、蒸发)
及操作要点(b)
3.说明粗盐提纯的过程(b)1.区别纯净物与混合物考点二 纯净物和混合物2.混合物分离主要方法之一:过滤不溶性固体和液体的分离(1)适用对象:①滤纸要紧贴漏斗内壁
②滤纸要低于漏斗边缘
③液面要低于滤纸边缘
④烧杯要紧靠玻璃棒的中下部
⑤玻璃棒的下端要紧靠三层滤纸的一侧
⑥漏斗下端尖嘴要紧靠接收器内壁(2)过滤操作的注意点:一贴二低三靠?(3)生产实例①水厂用过滤池净水②生活中也可制作简易过滤器得到过滤水③制豆腐、榨汁机、除去粗盐中的泥沙④化学工业用压滤机等过滤设备分离固体和液体的
混合物考点二 纯净物和混合物2.混合物分离主要方法之一:过滤2.混合物分离主要方法之一:蒸发除去溶液中的溶剂(1)适用对象:①加热蒸发过程中应用 不断搅拌。
②当有 但还残留少量溶液时应停止加热,利用蒸发皿的 蒸发至干,以防飞溅。 (3)主要操作事项:玻璃棒较多固体析出余热(2)仪器:考点二 纯净物和混合物沸点不同的液体混合物的分离2.混合物分离主要方法之一:蒸馏(1)适用对象(2)小石子或碎瓷片的作用:(3)具体实例:防暴沸海水制淡水分离酒精和水石油分馏分离液态空气考点二 纯净物和混合物考点二 纯净物和混合物(1)步骤:粗盐溶解 → 过滤 →蒸发结晶(2)玻璃棒的作用分别是:加速溶解、
引流、
使溶液均匀受热以防止晶体飞溅。3.粗盐提纯练习1 某物质经鉴定只含一种元素,则错误的是( )
A.可能是混合物 B.可能是一种单质
C.可能是化合物 D.可能是纯净物
练习2 进行过滤操作时,下列做法错误的是( )
A. 玻璃棒要靠在三层滤纸的一边
B. 漏斗下端的管口要紧靠烧杯的内壁
C. 滤纸的边缘要低于漏斗口
D. 液面不要低于滤纸边缘CD 练习3 提纯含少量泥沙的粗盐,一般经过以下操作流程:( 1 )操作 ① 中必须用到的一种仪器是 。
A .研钵 B .量筒 C .烧杯 D .试管
( 2 )操作 ④ 中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是 ( 填序号 )A D( 3 )操作 ⑤ 中除用到三脚架、洒精灯、玻璃棒、坩埚钳外,还需要用到 等仪器。 该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取 等措施。
( 4 )实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低、其可能原因是 ( 填序号 ) .
A.食盐没有全部溶解即过滤
B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿
D.器皿上沾有的精盐没全部转移到称量纸上
蒸发皿 间歇加热(或 “ 来回移动酒精灯 ” ) ABD考点三 相对原子质量和相对分子质量1. 知道相对原子质量和相对分子质量的概念(a)
2. 查询相对原子质量 (b)
3. 根据化学式计算物质的相对分子质量 (b)考点三 相对原子质量和相对分子质量1. 相对原子质量:(2)其他原子的质量与这个标准相比较,所得的比值是该种原子的相对原子质量(1)标准:一个C—12原子质量的1/12,碳原子的1/12碳原子氧原子16氧的相对原子质量 = 1.661×10-27千克2.657×10-26千克1.993×10-26千克1.661×10-27千克16=国际上有7种元素的相对原子质量采用了张青莲教授测的数据。表2-13是他所测的部分元素的相对原子质量新标准值。考点三 相对原子质量和相对分子质量2.相对原子质量计算公式:3.相对原子质量数值:相对分子质量=分子中各原子的相对原子质量的总和。4. 相对分子质量:考点三 相对原子质量和相对分子质量练习1 若作为相对原子质量标准的碳原子的质量为m千克 ,一个碘原子的质量为n千克。则碘的相对原子质量为( )。
A. n B. 12n/m C. n/12 D. 12m/n
练习2 某化合物的化学式为HnRO2n+1 ,相对分子质量为M,则R元素的化合价是 ,R的相对原子质量是 。B+(3n + 2)M - 33n-16 考点四 化学式
1.认识常见物质的化学式 (b)
2.解释化学式所表示的含义(b)
3.根据化学式计算组成物质的元素的质量比(c)
4.根据化学式计算组成物质的某元素的质量分数(c)①表示某种物质;
②表示该物质的一个分子;
③表示该物质的组成元素;
④表示每个分子里各原子个数。1.化学式所表示的含义H2SO4 考点四 化学式2.根据化学式计算组成物质的元素的质量比各元素的相对原子量与原子个数乘积之比 钙:碳:氧=(40×1):(12×1):(16×3) = 10:3:12求碳酸钙中各元素的质量比考点四 化学式3.根据化学式计算组成物质的某元素的质量分数
水中 H % =某元素的质量分数 =该元素的原子个数×该元素相对原子质量化合物的相对分子质量×100%考点四 化学式练习1(2015台州)下列有关化学符号“H2O”表示的意义,正确的是 ( )
A.水这种物质
B.水由氢原子和氧原子构成
C.一个水分子中含有一个氢分子
D.水由两个氢元素和一个氧元素组成A练习2 (2016金华)花青素(化学式C15H11O6)具有缓解眼睛疲劳,保护视力的作用,该物质主要来源于各种蔬菜和水果。下列关于花青素的说法正确的是( )
A.花青素是一种无机物
B.花青素的相对分子质量是287g
C.花青素中的C、H、O元素质量比是15:11:6
D.花青素在氧气中充分燃烧后生成二氧化碳和水 D练习3 (2016绍兴)我国科学家屠呦呦因为“发现青蒿素化学式为C15H22O5)――一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素之前最热门的抗疟药物之一。回答下列同题。
(1)一个青蒿素分子中含有 ________ 个原子。
(2)青蒿素中的氢元素与氧元素的质量比是 ________ 。
(3)14.1克青蒿素中含有碳元素的质量和多少克磺胺中含有碳元素的质量相等?
【答案(1)42(2)11:40(3)21.5】练习4 如图,某同学绘制了三条表示某金属氧化物的质量与其所含金属元素的质量的关系曲线。横坐标表示金属氧化物的质量,纵坐标表示该金属氧化物中金属元素的质量。(1)三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是 。
(2)其中绘制错误的一条曲线(不能正确表示金属氧化物与它所含金属元素的质量的关系)是 ,理由是 .金属氧化物的质量一定大于金属质量BA1.A 2.D 3.D 4.B 5.C 6.C 7.A
8.(1) 单质 ⑵ FeO
⑶ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
9. (1)引流(2)C(3)用洁净的玻璃棒蘸取少量溶液,滴在pH试纸上,显示的颜色与标准比色卡对照
10.(1)+5(2)食盐B11.(1)红 (2)32(3)mc=28.7克×(15C/C15H11O6)=28.7克×(180/287)=18克 专题14 综合训练答案
