高中化学沪科版高一上学期第二章2.2《海水中的氯》课件(26张)
文档属性
| 名称 | 高中化学沪科版高一上学期第二章2.2《海水中的氯》课件(26张) |

|
|
| 格式 | zip | ||
| 文件大小 | 187.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-05-28 00:00:00 | ||
图片预览








文档简介
课件26张PPT。2.2 海水中的氯用途
化学性质
学氯气的什么?决定决定比较正确、全面地认识氯气的作用、合理使用、正确使用氯气的制法1.观察氯气的颜色和状态
记录_____________________
2.试验氯气在水中的溶解性
常温下1体积水可以溶解氯气的体
积________
结论_____________________________
_______________________________
3.铁丝在氯气中的燃烧 氯气是一种黄绿色的、能溶于水的气体。实验与观察黄绿色 气体2 体积氯气的物理性质 在通常状况(25℃101kPa)下,
Cl2是一种黄绿色有强烈剌激性
气味的有毒气体,比空气重,
可溶于水 (室温时1体积水中
大约能溶解2体积氯气。
在常压下,冷却到-34.6℃
(沸点)时液化为液氯,
继续冷却到-101℃(熔点)时,
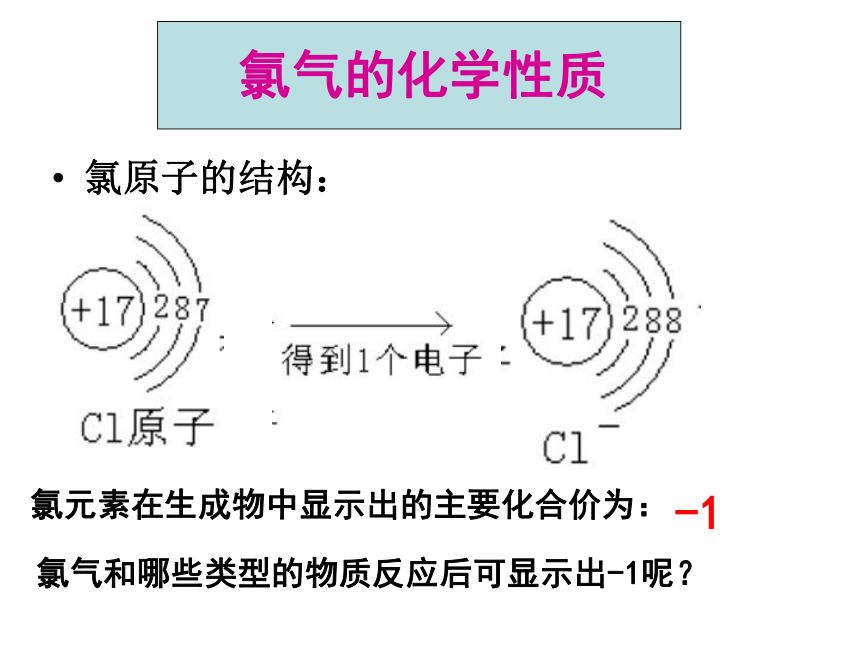
凝结为固态氯。氯气的化学性质氯原子的结构:
氯元素在生成物中显示出的主要化合价为:-1氯气和哪些类型的物质反应后可显示出-1呢?3.铁丝在氯气中的燃烧
现象 ______________________________
化学方程式 ________________________
结论 ______________________________
4.氢气与氯气的反应棕黄色的烟(氯化铁固体小颗粒分散在空气中)氯气的化学性质很活泼,与铁、铜可变价金属反应生成高价化合物4.氢气与氯气的反应
⑴氢气在氯气中燃烧
现象____________________________
____________________________
化学方程式
____________________________
⑵氢气与氯气混合后光照
现象____________________________
化学方程式
____________________________ 氢气能在氯气中安静地燃烧,产生
苍白色的火焰,瓶口有白雾爆 炸5.氯气与氢氧化钠溶液的反应
现象________________________________
实验现象说明________________________
化学方程式 _________________________
应用:写出工业上用消石灰制漂粉精的化学方程式式 ____________________________________针筒中的氯气全部溶解在氢氧化钠溶液中,
溶液仍呈无色。氯气能与碱溶液反应6.氯气与水的反应和漂白作用
氯气与干燥的色布、氯气与湿润的色布
现象 _______________________________
化学方程式(其一) ________________________
问题 使湿色布褪色的是盐酸还是次氯 酸?请设计一个简单的实验来证明。(实验室没有次氯酸)
你认为漂粉精的有效成分是什么?干燥的色布不褪色,湿润的色布褪色Cl2 + H2O HClO + HCl将色布浸在盐酸中,观察是否褪色Ca(ClO)2氯气与化合物的反应氯气的化学性质——很活泼(1)与金属化合实验现象:产生黄色火焰和大量白烟实验现象:产生大量棕色的烟,铜丝红热实验现象:产生大量棕褐色的烟,铁丝红热+1-1——生成金属氯化物2Na+Cl2 2NaCl点燃结论:在加热或点燃条件下,
氯气能跟绝大多数金属发生反应,生成金属氯化物(2)与H2等非金属化合现象:产生苍白色火焰,
瓶口有大量白雾产生。现象 :产生大量白色烟雾+1-1——非金属氯化物与磷反应氢气与氯气混合后光照:爆炸
(3)与H2O的反应 氯气溶于水所得的水溶液叫氯水,溶于水的Cl2有少量与水反应生成盐酸和次氯酸可逆反应:
在相同条件下,同时向相反方向进行的反应
为可逆反应。设问:氯水的成分是什么?颜色是什么?氯水是含Cl2、HCl、HClO三种溶质的混合溶液,
其中含有三种分子(H2O、Cl2、HClO)和
四种离子(H+、Cl-、ClO-、OH-)次氯酸的重要性质: ①HClO易溶于水,其水溶液无色
②HClO是一元弱酸,其酸性比H2CO3还弱
③ HClO很不稳定:2HClO 2HCl+O2↑
HClO只存在于稀溶液中,增大浓度、加热或光照都会加快它的分解。④ HClO是一种强氧化剂,具有很强的氧化性(比Cl2的氧化性强),能氧化而杀死水里的细菌,还能氧化而使染料和有色物质褪色,因此,常利用它的强氧化性来消毒或漂白。 问题:1.氯水的保存有什么要求?问题2:自来水厂对自来水进行消毒而通入氯气
是因为氯气有杀菌消毒漂白的能力吗?问题3:养金鱼为什么要对自来水进行曝晒?根据已学知识回答解决实际问题:久置氯水的主要成分是什么?很稀的盐酸问题4:新制的氯水滴到石蕊试纸上的
变色情况能预估吗?问题5:新制的氯水配制硝酸银溶液
会出现什么情况?(4)氯气与氢氧化钠溶液的反应
现象________________________________
实验现象说明________________________
化学方程式 _________________________
简单分析原因针筒中的氯气全部溶解在氢氧化钠溶液中,
溶液仍呈无色。氯气能与碱溶液反应应用:制消毒液目前,84消毒液的主要成分是次氯酸钠氯气的用途氯气可以用来制得聚氯乙烯、塑料、盐酸等多种含氯制品,还可以用来制取漂粉精和消毒水。 漂粉精的制取
写出工业上用氯气和消石灰制漂粉精的化学方程式问题1:这里所用的消石灰指的
是澄清石灰水还是石灰乳?问题2:漂粉精是混合物还是纯净物?
其中的关键物质是什么?漂粉精的有效成分是: Ca(ClO)2漂粉精的漂白原理:
Ca(ClO)2+2HCl CaCl2+2HClO (工业上加快)
Ca(ClO)2+2CO2+2H2O Ca(HCO3)2+2HClO反应原理:强酸制取弱酸思考 : 为什么我们要先制成漂粉精,
再将其与酸反应制成次氯酸?因次氯酸不稳定,次氯酸钙稳定,易保存,
且能与 CO2、H2O 等酸反应生成次氯酸。漂粉精在空气中长期放置也会失效:Ca(ClO)2+2CO2+2H2O Ca(HCO3)2+2HClOMnO2 + 4HCl MnCl2 + Cl2 + 2H2O氯气性质的研究
回忆工业上如何制取氯气的?
2NaCl + 2H2O 2NaOH + H2
+ Cl2
实验室制氯气原理(浓)实验室如何制取纯净的氯气?饱和食盐水浓硫酸氢氧化钠溶液漂粉精和水的消毒
问题 将氯水滴到蓝色石蕊试纸将会产生什么现象?
先变红后变白,因为氯化氢、次氯酸能电离出氢离子,具有酸的性质,使蓝色石蕊试纸先变红,又由于次氯酸能使有机色素氧化生成无色物质,故后褪色(变白)。次氯酸的性质
弱酸性 (比碳酸弱)
HClO H+ + ClO-
不稳定性
2 HClO 2 HCl + O2
强氧化性
可用来杀菌、消毒、漂白光或热问题新制氯水与久置氯水成分上有何不同?
新制氯水含:
Cl2、HClO、H2O、H+、 Cl-、ClO- 、OH-
久置氯水主要含 :
H2O、H+、 Cl-、 OH-漂粉精(物质类别)
制取
2Cl2+2Ca(OH)2 CaCl2+Ca(ClO)2+2H2O
有效成分 次氯酸钙
·漂白原理
Ca(ClO)2+2CO2+2H2O Ca(HCO3)2+2HClO
思考 为什么我们要先制成漂粉精,再将其与酸反应制成次氯酸?
因次氯酸不稳定,次氯酸钙稳定,易保存,
且能与 CO2、H2O 等酸反应生成次氯酸。水的消毒方法
氯气
臭氧
二氧化氯
物理方法
其他方法请同学自行查找
【要点梳理1】氯气的性质研究物理性质化学性质色态:黄绿色气体氯气能全部溶解于NaOH溶液中,得到无色溶
液 Cl2+2NaOH NaCl+NaClO+H2O水溶性:能溶于水(约1∶2)【要点梳理2】漂粉精和水的消毒氯气的用途漂粉精制取漂粉精的
消毒原理制聚氯乙烯、盐酸、漂粉精、医药、
氯仿、消毒水等工业 Ca(ClO)2+2HCl CaCl2+2HClO
日常生活 Ca(ClO)2+2CO2+2H2O
Ca(HCO3)2+2HClO
由于HClO、O3、ClO2都能在水中游离氧原子,具有很强的氧化性,因而具有消毒与杀菌作用。 O3 、 ClO2等是良好的消毒剂
化学性质
学氯气的什么?决定决定比较正确、全面地认识氯气的作用、合理使用、正确使用氯气的制法1.观察氯气的颜色和状态
记录_____________________
2.试验氯气在水中的溶解性
常温下1体积水可以溶解氯气的体
积________
结论_____________________________
_______________________________
3.铁丝在氯气中的燃烧 氯气是一种黄绿色的、能溶于水的气体。实验与观察黄绿色 气体2 体积氯气的物理性质 在通常状况(25℃101kPa)下,
Cl2是一种黄绿色有强烈剌激性
气味的有毒气体,比空气重,
可溶于水 (室温时1体积水中
大约能溶解2体积氯气。
在常压下,冷却到-34.6℃
(沸点)时液化为液氯,
继续冷却到-101℃(熔点)时,
凝结为固态氯。氯气的化学性质氯原子的结构:
氯元素在生成物中显示出的主要化合价为:-1氯气和哪些类型的物质反应后可显示出-1呢?3.铁丝在氯气中的燃烧
现象 ______________________________
化学方程式 ________________________
结论 ______________________________
4.氢气与氯气的反应棕黄色的烟(氯化铁固体小颗粒分散在空气中)氯气的化学性质很活泼,与铁、铜可变价金属反应生成高价化合物4.氢气与氯气的反应
⑴氢气在氯气中燃烧
现象____________________________
____________________________
化学方程式
____________________________
⑵氢气与氯气混合后光照
现象____________________________
化学方程式
____________________________ 氢气能在氯气中安静地燃烧,产生
苍白色的火焰,瓶口有白雾爆 炸5.氯气与氢氧化钠溶液的反应
现象________________________________
实验现象说明________________________
化学方程式 _________________________
应用:写出工业上用消石灰制漂粉精的化学方程式式 ____________________________________针筒中的氯气全部溶解在氢氧化钠溶液中,
溶液仍呈无色。氯气能与碱溶液反应6.氯气与水的反应和漂白作用
氯气与干燥的色布、氯气与湿润的色布
现象 _______________________________
化学方程式(其一) ________________________
问题 使湿色布褪色的是盐酸还是次氯 酸?请设计一个简单的实验来证明。(实验室没有次氯酸)
你认为漂粉精的有效成分是什么?干燥的色布不褪色,湿润的色布褪色Cl2 + H2O HClO + HCl将色布浸在盐酸中,观察是否褪色Ca(ClO)2氯气与化合物的反应氯气的化学性质——很活泼(1)与金属化合实验现象:产生黄色火焰和大量白烟实验现象:产生大量棕色的烟,铜丝红热实验现象:产生大量棕褐色的烟,铁丝红热+1-1——生成金属氯化物2Na+Cl2 2NaCl点燃结论:在加热或点燃条件下,
氯气能跟绝大多数金属发生反应,生成金属氯化物(2)与H2等非金属化合现象:产生苍白色火焰,
瓶口有大量白雾产生。现象 :产生大量白色烟雾+1-1——非金属氯化物与磷反应氢气与氯气混合后光照:爆炸
(3)与H2O的反应 氯气溶于水所得的水溶液叫氯水,溶于水的Cl2有少量与水反应生成盐酸和次氯酸可逆反应:
在相同条件下,同时向相反方向进行的反应
为可逆反应。设问:氯水的成分是什么?颜色是什么?氯水是含Cl2、HCl、HClO三种溶质的混合溶液,
其中含有三种分子(H2O、Cl2、HClO)和
四种离子(H+、Cl-、ClO-、OH-)次氯酸的重要性质: ①HClO易溶于水,其水溶液无色
②HClO是一元弱酸,其酸性比H2CO3还弱
③ HClO很不稳定:2HClO 2HCl+O2↑
HClO只存在于稀溶液中,增大浓度、加热或光照都会加快它的分解。④ HClO是一种强氧化剂,具有很强的氧化性(比Cl2的氧化性强),能氧化而杀死水里的细菌,还能氧化而使染料和有色物质褪色,因此,常利用它的强氧化性来消毒或漂白。 问题:1.氯水的保存有什么要求?问题2:自来水厂对自来水进行消毒而通入氯气
是因为氯气有杀菌消毒漂白的能力吗?问题3:养金鱼为什么要对自来水进行曝晒?根据已学知识回答解决实际问题:久置氯水的主要成分是什么?很稀的盐酸问题4:新制的氯水滴到石蕊试纸上的
变色情况能预估吗?问题5:新制的氯水配制硝酸银溶液
会出现什么情况?(4)氯气与氢氧化钠溶液的反应
现象________________________________
实验现象说明________________________
化学方程式 _________________________
简单分析原因针筒中的氯气全部溶解在氢氧化钠溶液中,
溶液仍呈无色。氯气能与碱溶液反应应用:制消毒液目前,84消毒液的主要成分是次氯酸钠氯气的用途氯气可以用来制得聚氯乙烯、塑料、盐酸等多种含氯制品,还可以用来制取漂粉精和消毒水。 漂粉精的制取
写出工业上用氯气和消石灰制漂粉精的化学方程式问题1:这里所用的消石灰指的
是澄清石灰水还是石灰乳?问题2:漂粉精是混合物还是纯净物?
其中的关键物质是什么?漂粉精的有效成分是: Ca(ClO)2漂粉精的漂白原理:
Ca(ClO)2+2HCl CaCl2+2HClO (工业上加快)
Ca(ClO)2+2CO2+2H2O Ca(HCO3)2+2HClO反应原理:强酸制取弱酸思考 : 为什么我们要先制成漂粉精,
再将其与酸反应制成次氯酸?因次氯酸不稳定,次氯酸钙稳定,易保存,
且能与 CO2、H2O 等酸反应生成次氯酸。漂粉精在空气中长期放置也会失效:Ca(ClO)2+2CO2+2H2O Ca(HCO3)2+2HClOMnO2 + 4HCl MnCl2 + Cl2 + 2H2O氯气性质的研究
回忆工业上如何制取氯气的?
2NaCl + 2H2O 2NaOH + H2
+ Cl2
实验室制氯气原理(浓)实验室如何制取纯净的氯气?饱和食盐水浓硫酸氢氧化钠溶液漂粉精和水的消毒
问题 将氯水滴到蓝色石蕊试纸将会产生什么现象?
先变红后变白,因为氯化氢、次氯酸能电离出氢离子,具有酸的性质,使蓝色石蕊试纸先变红,又由于次氯酸能使有机色素氧化生成无色物质,故后褪色(变白)。次氯酸的性质
弱酸性 (比碳酸弱)
HClO H+ + ClO-
不稳定性
2 HClO 2 HCl + O2
强氧化性
可用来杀菌、消毒、漂白光或热问题新制氯水与久置氯水成分上有何不同?
新制氯水含:
Cl2、HClO、H2O、H+、 Cl-、ClO- 、OH-
久置氯水主要含 :
H2O、H+、 Cl-、 OH-漂粉精(物质类别)
制取
2Cl2+2Ca(OH)2 CaCl2+Ca(ClO)2+2H2O
有效成分 次氯酸钙
·漂白原理
Ca(ClO)2+2CO2+2H2O Ca(HCO3)2+2HClO
思考 为什么我们要先制成漂粉精,再将其与酸反应制成次氯酸?
因次氯酸不稳定,次氯酸钙稳定,易保存,
且能与 CO2、H2O 等酸反应生成次氯酸。水的消毒方法
氯气
臭氧
二氧化氯
物理方法
其他方法请同学自行查找
【要点梳理1】氯气的性质研究物理性质化学性质色态:黄绿色气体氯气能全部溶解于NaOH溶液中,得到无色溶
液 Cl2+2NaOH NaCl+NaClO+H2O水溶性:能溶于水(约1∶2)【要点梳理2】漂粉精和水的消毒氯气的用途漂粉精制取漂粉精的
消毒原理制聚氯乙烯、盐酸、漂粉精、医药、
氯仿、消毒水等工业 Ca(ClO)2+2HCl CaCl2+2HClO
日常生活 Ca(ClO)2+2CO2+2H2O
Ca(HCO3)2+2HClO
由于HClO、O3、ClO2都能在水中游离氧原子,具有很强的氧化性,因而具有消毒与杀菌作用。 O3 、 ClO2等是良好的消毒剂
