第二节 金属的化学性质 课件(25张PPT)
文档属性
| 名称 | 第二节 金属的化学性质 课件(25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 628.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-05-30 00:00:00 | ||
图片预览








文档简介
课件25张PPT。黄金戒指以黄铜(铜、锌合金)冒充黄金进行诈骗活动。你有什么方法可以揭穿他们的骗局?
第二节 金属的化学性质铁丝在氧气中燃烧 镁条在空气中燃烧一、金属与氧气的反应铜片在加热时能与氧气反应“真金不怕火炼”说明即使在高温条件下,金也不会与氧气发生反应温故而知新【活动天地】用滤纸卷上少量铝粉,在酒精灯上点燃,迅速插入盛有氧气的集气瓶中观察有什么现象? 铝粉能在氧气中剧烈燃烧,生成白色粉末。1.常温下易与氧气反应: 以??、?为代表。
2.加热或高温时能与氧气反应:
以 、 ?为代表。
3.高温下也不能与氧气反应:以??为代表。 结 论一结论:金属的活动性Mg、Al>Fe、Cu>Au对比镁、铁、铝分别与氧气反应所需要的实验条件不同,分析一下通常有哪些因素会影响金属与氧气反应的难易和剧烈程度?影响因素:
(1)氧气的浓度 (2)反应的温度
(3)金属粉碎的程度(即金属与氧气的接触面积)
(4)金属本身的活泼性
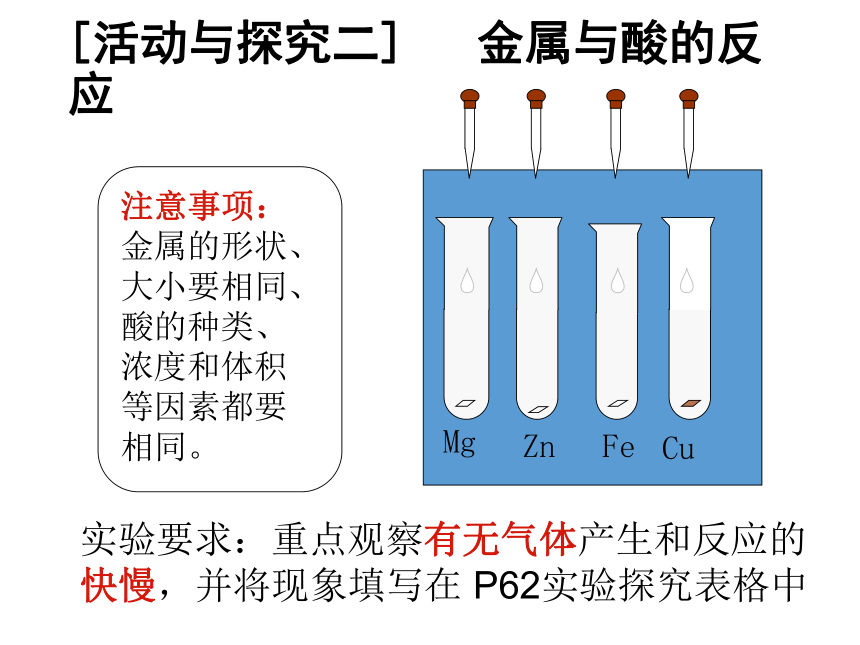
【小组讨论】 P61交流共享----------主要因素1、铝比铁活泼,但铝制品很少生锈,为什么?【自学阅读P62】 多识一点金属铝在常温下发生缓慢氧化:4Al+3O2=2Al2O3; 表面形成一层致密的氧化物薄膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性。2、为何不宜用钢刷来擦洗铝制餐具呢?若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。[活动与探究二] 金属与酸的反应 注意事项:金属的形状、大小要相同、酸的种类、浓度和体积等因素都要相同。实验要求:重点观察有无气体产生和反应的
快慢,并将现象填写在 P62实验探究表格中实验探究:金属与酸的反应2、还有哪些需要注意的问题?1、若想通过该实验比较金属本身的性质差异对于实验现象的影响情况,应控制哪些条件保持相同?实验探究9-3[活动与探究二] 金属与酸的反应 大量气泡,反应最快较多气泡,反应较快少量气泡,反应较慢,
溶液由无色变为浅绿色无现象反应快慢同
加盐酸一样【漫画展示】比较活动性:Mg>Zn > Fe > CuK Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au常见金属的活动性顺序金属活动性由强逐渐减弱
钾 钙 钠 镁 铝 锌 铁锡铅(氢)铜汞银铂金【自学阅读P63】金属活动性顺序表的意义:1.金属的位置越靠前,它的活动性就越2.排在 前面的金属能与酸反应放出 强氢氢气结 论二
2、氢前金属+盐酸(稀硫酸) 氢气+盐
1、常见金属活动性顺序【活动天地P63】金属与酸反应的特点 3、置换反应(基本反应类型之一)
①定义:一种单质与一种化合物反应生成
另一种单质 和另一种化合物的反应。
结 论二②反应通式:A+BC=AC+B注意:铁生成亚铁盐Cu + HCl —— CuCl2 + H2↑
Mg + HCl —— MgCl2 + H2↑
Al + HCl —— AlCl3 + H2↑ 铁 + 盐酸 —— 氯化铁 + 氢气×应生成氯化亚铁√√×【学以致用】 1.下列化学反应能发生吗?化学反应的基本类型两种或两种
以上一种一种两种或两种
以上一种单质,
一种化合物一种单质,
一种化合物两种化合物两种化合物交换成分【学以致用】 2.指出下列反应的基本类型
② Fe+CuSO4=Cu+FeSO4
④HCl+NaOH=NaCl+H2O【课堂小结】通过这节课你有哪些收获?还有什么疑问?
1.与氧气反应
金属越活泼,反应越容易,越剧烈。学完本课题你应该知道一、金属的化学性质:二、置换反应三、金属活动性顺序及其应用(下节课学习)判断金属能否与酸溶液发生置换反应,及反应的快慢。 A+BC=B+AC【当堂检测】1.不法分子用铜锌合金制成假元宝行骗的事件屡有发生。下列不易区别其真伪的方法是( )
A.用火烧 B.放入硫酸中
C.加盐酸 D.观察外观2.下列物质不能由金属和盐酸直接反应生成的是( )
A.MgCl2 B.CuCl2 C.FeCl2 D.ZnCl2【当堂检测】4.金属钛是航空、军工、电子等方面的必须原料。生产金属钛发生的化学反应为TiCl4+2Mg Ti+2MgCl2,该反应属于( )
A.置换反应 B.化合反应 3.下列物质能由金属和对应的酸直接反应生成的是( )
A.CuCl2 B.FeCl2 C.FeCl3 D.Fe(NO3)2【当堂检测】5. 有X、Y、Z三种金属,如果把这三种金属均投入到稀硫酸中,X、Y表面均无明显现象,Z表面有大量气泡产生。若将X、Y这两种金属放在氧气中加热,X表面无明显现象,Y表面发黑。则这三种金属活动性顺序为( )
A、X>Y> Z B 、Z>Y>X
C、Y>X>Z D、 Z>X>Y【大展身手】为研究锌和铝的金属活动性,某研究小组进行了如下探究。
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸。写出锌与盐酸反应的化学方程式 。
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是 。
(3)你认为(1)中小明的实验能否比较锌和铝的金属活动性强弱? (填“能”或“不能”),分别从设计方法和操作可行性的角度,具体说明理由 。Zn+2HCl =ZnCl2+H2↑ 因为后者有氧化铝薄膜保护层不能没有控制盐酸浓度和金属的纯度,难以控制铝片和锌粒的表面积相同。
第二节 金属的化学性质铁丝在氧气中燃烧 镁条在空气中燃烧一、金属与氧气的反应铜片在加热时能与氧气反应“真金不怕火炼”说明即使在高温条件下,金也不会与氧气发生反应温故而知新【活动天地】用滤纸卷上少量铝粉,在酒精灯上点燃,迅速插入盛有氧气的集气瓶中观察有什么现象? 铝粉能在氧气中剧烈燃烧,生成白色粉末。1.常温下易与氧气反应: 以??、?为代表。
2.加热或高温时能与氧气反应:
以 、 ?为代表。
3.高温下也不能与氧气反应:以??为代表。 结 论一结论:金属的活动性Mg、Al>Fe、Cu>Au对比镁、铁、铝分别与氧气反应所需要的实验条件不同,分析一下通常有哪些因素会影响金属与氧气反应的难易和剧烈程度?影响因素:
(1)氧气的浓度 (2)反应的温度
(3)金属粉碎的程度(即金属与氧气的接触面积)
(4)金属本身的活泼性
【小组讨论】 P61交流共享----------主要因素1、铝比铁活泼,但铝制品很少生锈,为什么?【自学阅读P62】 多识一点金属铝在常温下发生缓慢氧化:4Al+3O2=2Al2O3; 表面形成一层致密的氧化物薄膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性。2、为何不宜用钢刷来擦洗铝制餐具呢?若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。[活动与探究二] 金属与酸的反应 注意事项:金属的形状、大小要相同、酸的种类、浓度和体积等因素都要相同。实验要求:重点观察有无气体产生和反应的
快慢,并将现象填写在 P62实验探究表格中实验探究:金属与酸的反应2、还有哪些需要注意的问题?1、若想通过该实验比较金属本身的性质差异对于实验现象的影响情况,应控制哪些条件保持相同?实验探究9-3[活动与探究二] 金属与酸的反应 大量气泡,反应最快较多气泡,反应较快少量气泡,反应较慢,
溶液由无色变为浅绿色无现象反应快慢同
加盐酸一样【漫画展示】比较活动性:Mg>Zn > Fe > CuK Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au常见金属的活动性顺序金属活动性由强逐渐减弱
钾 钙 钠 镁 铝 锌 铁锡铅(氢)铜汞银铂金【自学阅读P63】金属活动性顺序表的意义:1.金属的位置越靠前,它的活动性就越2.排在 前面的金属能与酸反应放出 强氢氢气结 论二
2、氢前金属+盐酸(稀硫酸) 氢气+盐
1、常见金属活动性顺序【活动天地P63】金属与酸反应的特点 3、置换反应(基本反应类型之一)
①定义:一种单质与一种化合物反应生成
另一种单质 和另一种化合物的反应。
结 论二②反应通式:A+BC=AC+B注意:铁生成亚铁盐Cu + HCl —— CuCl2 + H2↑
Mg + HCl —— MgCl2 + H2↑
Al + HCl —— AlCl3 + H2↑ 铁 + 盐酸 —— 氯化铁 + 氢气×应生成氯化亚铁√√×【学以致用】 1.下列化学反应能发生吗?化学反应的基本类型两种或两种
以上一种一种两种或两种
以上一种单质,
一种化合物一种单质,
一种化合物两种化合物两种化合物交换成分【学以致用】 2.指出下列反应的基本类型
② Fe+CuSO4=Cu+FeSO4
④HCl+NaOH=NaCl+H2O【课堂小结】通过这节课你有哪些收获?还有什么疑问?
1.与氧气反应
金属越活泼,反应越容易,越剧烈。学完本课题你应该知道一、金属的化学性质:二、置换反应三、金属活动性顺序及其应用(下节课学习)判断金属能否与酸溶液发生置换反应,及反应的快慢。 A+BC=B+AC【当堂检测】1.不法分子用铜锌合金制成假元宝行骗的事件屡有发生。下列不易区别其真伪的方法是( )
A.用火烧 B.放入硫酸中
C.加盐酸 D.观察外观2.下列物质不能由金属和盐酸直接反应生成的是( )
A.MgCl2 B.CuCl2 C.FeCl2 D.ZnCl2【当堂检测】4.金属钛是航空、军工、电子等方面的必须原料。生产金属钛发生的化学反应为TiCl4+2Mg Ti+2MgCl2,该反应属于( )
A.置换反应 B.化合反应 3.下列物质能由金属和对应的酸直接反应生成的是( )
A.CuCl2 B.FeCl2 C.FeCl3 D.Fe(NO3)2【当堂检测】5. 有X、Y、Z三种金属,如果把这三种金属均投入到稀硫酸中,X、Y表面均无明显现象,Z表面有大量气泡产生。若将X、Y这两种金属放在氧气中加热,X表面无明显现象,Y表面发黑。则这三种金属活动性顺序为( )
A、X>Y> Z B 、Z>Y>X
C、Y>X>Z D、 Z>X>Y【大展身手】为研究锌和铝的金属活动性,某研究小组进行了如下探究。
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸。写出锌与盐酸反应的化学方程式 。
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是 。
(3)你认为(1)中小明的实验能否比较锌和铝的金属活动性强弱? (填“能”或“不能”),分别从设计方法和操作可行性的角度,具体说明理由 。Zn+2HCl =ZnCl2+H2↑ 因为后者有氧化铝薄膜保护层不能没有控制盐酸浓度和金属的纯度,难以控制铝片和锌粒的表面积相同。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
