到实验室去:氧气的实验室制取与性质 课件(17张PPT)
文档属性
| 名称 | 到实验室去:氧气的实验室制取与性质 课件(17张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-06-07 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
——氧气的实验室制取与性质
供给呼吸
供给呼吸
钢铁冶炼
实验目的:
1、掌握实验室制取氧气的原理和
实验装置。
2、初步学会用过氧化氢制取3瓶
氧气的方法,并验证氧气的性质。
我们在实验室制取氧气,需要解决哪些问题?
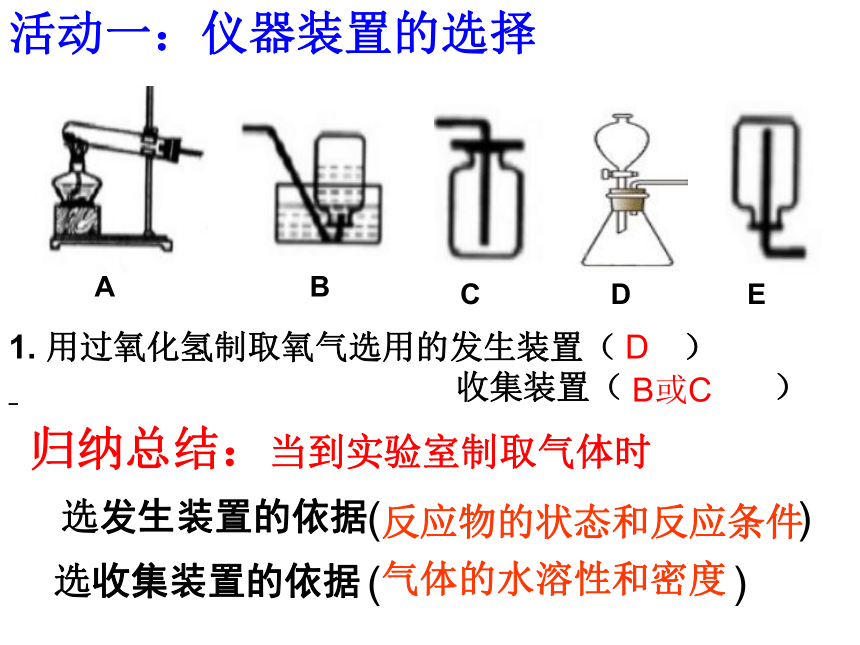
活动一:仪器装置的选择
B
C
D
E
1. 用过氧化氢制取氧气选用的发生装置( )
收集装置( )
归纳总结:当到实验室制取气体时
选发生装置的依据
选收集装置的依据
反应物的状态和反应条件
气体的水溶性和密度
(
(
)
)
A
D
B或C
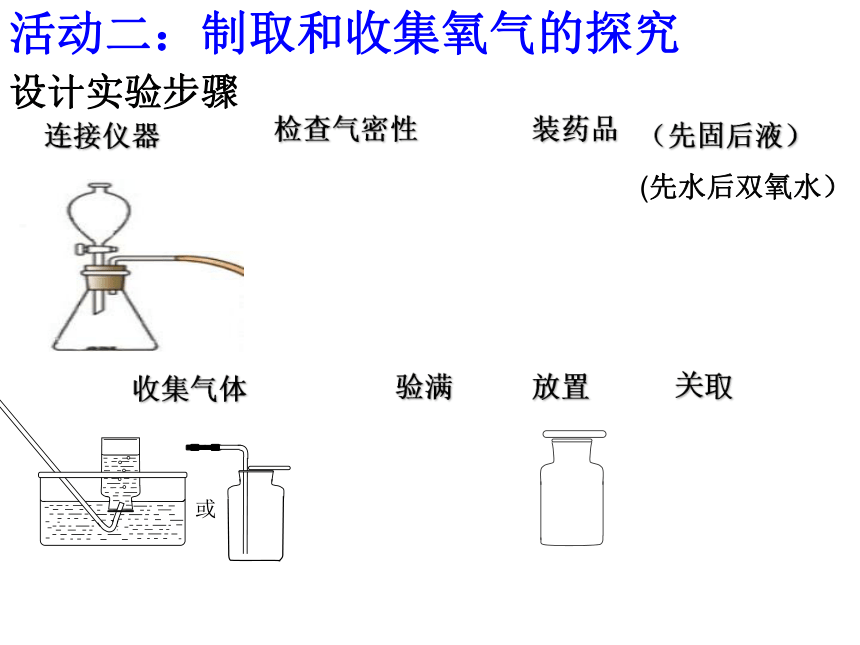
设计实验步骤
连接仪器
检查气密性
装药品
收集气体
验满
或
放置
关取
活动二:制取和收集氧气的探究
(先水后双氧水)
(先固后液)
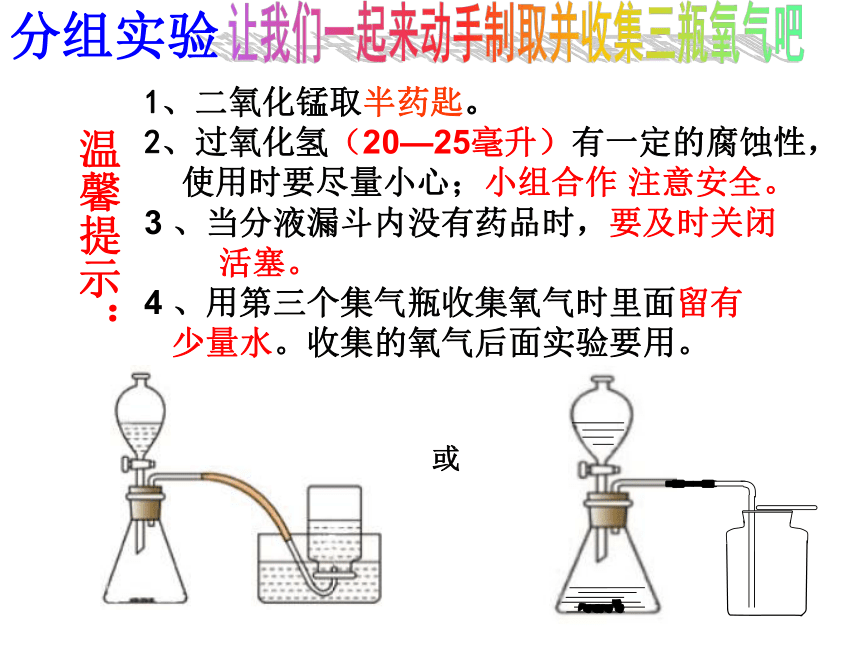
1、二氧化锰取半药匙。
2、过氧化氢(20—25毫升)有一定的腐蚀性,
使用时要尽量小心;小组合作 注意安全。
3 、当分液漏斗内没有药品时,要及时关闭
活塞。
4 、用第三个集气瓶收集氧气时里面留有
少量水。收集的氧气后面实验要用。
温馨提示:
分组实验
或
1、《木炭在氧气中燃烧》
将木炭放入氧气中时,
由瓶口向下缓慢插入
现象
反应式
活动三:氧气性质的探究
设计实验步骤: 如何检验生成物?
温馨提示:
2、《铁在氧气中燃烧》
待火柴快燃尽时,将红热铁丝从瓶口慢慢伸入集气瓶中
在瓶底放一些水或铺一层细沙
现象
反应式
温馨提示:
活动三:氧气性质的探究
设计实验步骤:
现象
反应式
在空气中发红;氧气中发白光;
放热、
生成一种使澄清石灰水变浑浊的气体
碳 + 氧气
点燃
二氧化碳
活动三:氧气性质的探究
1、《木炭在氧气中燃烧》
设计实验步骤:
现象
反应式
在氧气中剧烈燃烧,火星四射 ,放出大量热,生成黑色固体
铁 + 氧气
点燃
四氧化三铁
活动三:氧气性质的探究
2、《铁在氧气中燃烧》
设计实验步骤:
归纳总结:
氧气的化学性质( ),能与许多物质发生( )。
反思交流:
为什么木炭在纯氧气中燃烧程度比空气中燃烧要剧烈?
宏观:说明燃烧的剧烈程度跟氧气的含量有关,氧气含量越高,燃烧越剧烈。
你能否从微观角度试着解释?
分子之间欲发生反应,其首要条件是分子之间接触碰撞。在空气中,含量较多的是氮气,氧气分子含量相对较少,木炭与氧分子碰撞机会少,而在纯氧气中则大大增加了碰撞机会。
感悟、质疑、提升……
你
说
我
说
利用身边的材料(带塞子的塑料瓶、注射器、牛奶吸管、玻璃杯等)自己动手制作一套简易制氧装置。
1、用排水法收集氧气时刚冒出的气泡能马上收集吗?能说一下原因吗?
2、充满氧气的集气瓶正放在桌面上了吗?你能说一下要正方的理由吗?
3、你会判定一瓶氧气已集满了吗?验满的方法掌握了吗?
——氧气的实验室制取与性质
供给呼吸
供给呼吸
钢铁冶炼
实验目的:
1、掌握实验室制取氧气的原理和
实验装置。
2、初步学会用过氧化氢制取3瓶
氧气的方法,并验证氧气的性质。
我们在实验室制取氧气,需要解决哪些问题?
活动一:仪器装置的选择
B
C
D
E
1. 用过氧化氢制取氧气选用的发生装置( )
收集装置( )
归纳总结:当到实验室制取气体时
选发生装置的依据
选收集装置的依据
反应物的状态和反应条件
气体的水溶性和密度
(
(
)
)
A
D
B或C
设计实验步骤
连接仪器
检查气密性
装药品
收集气体
验满
或
放置
关取
活动二:制取和收集氧气的探究
(先水后双氧水)
(先固后液)
1、二氧化锰取半药匙。
2、过氧化氢(20—25毫升)有一定的腐蚀性,
使用时要尽量小心;小组合作 注意安全。
3 、当分液漏斗内没有药品时,要及时关闭
活塞。
4 、用第三个集气瓶收集氧气时里面留有
少量水。收集的氧气后面实验要用。
温馨提示:
分组实验
或
1、《木炭在氧气中燃烧》
将木炭放入氧气中时,
由瓶口向下缓慢插入
现象
反应式
活动三:氧气性质的探究
设计实验步骤: 如何检验生成物?
温馨提示:
2、《铁在氧气中燃烧》
待火柴快燃尽时,将红热铁丝从瓶口慢慢伸入集气瓶中
在瓶底放一些水或铺一层细沙
现象
反应式
温馨提示:
活动三:氧气性质的探究
设计实验步骤:
现象
反应式
在空气中发红;氧气中发白光;
放热、
生成一种使澄清石灰水变浑浊的气体
碳 + 氧气
点燃
二氧化碳
活动三:氧气性质的探究
1、《木炭在氧气中燃烧》
设计实验步骤:
现象
反应式
在氧气中剧烈燃烧,火星四射 ,放出大量热,生成黑色固体
铁 + 氧气
点燃
四氧化三铁
活动三:氧气性质的探究
2、《铁在氧气中燃烧》
设计实验步骤:
归纳总结:
氧气的化学性质( ),能与许多物质发生( )。
反思交流:
为什么木炭在纯氧气中燃烧程度比空气中燃烧要剧烈?
宏观:说明燃烧的剧烈程度跟氧气的含量有关,氧气含量越高,燃烧越剧烈。
你能否从微观角度试着解释?
分子之间欲发生反应,其首要条件是分子之间接触碰撞。在空气中,含量较多的是氮气,氧气分子含量相对较少,木炭与氧分子碰撞机会少,而在纯氧气中则大大增加了碰撞机会。
感悟、质疑、提升……
你
说
我
说
利用身边的材料(带塞子的塑料瓶、注射器、牛奶吸管、玻璃杯等)自己动手制作一套简易制氧装置。
1、用排水法收集氧气时刚冒出的气泡能马上收集吗?能说一下原因吗?
2、充满氧气的集气瓶正放在桌面上了吗?你能说一下要正方的理由吗?
3、你会判定一瓶氧气已集满了吗?验满的方法掌握了吗?
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
