理想气体状态方程(山东省枣庄市)
文档属性
| 名称 | 理想气体状态方程(山东省枣庄市) |

|
|
| 格式 | rar | ||
| 文件大小 | 44.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2009-03-26 00:00:00 | ||
图片预览






文档简介
课件15张PPT。第三节 理想气体方程知识回顾:波意耳定律一定质量的气体:在温度不变的情况下:在体积不变的情况下:在压强不变的情况下:查理定律盖-吕萨克定律 那么当气体的三个状态量:P V T 都发生变化时,其关系又是怎样?第三节 理想气体方程一、理想气体1.理想气体:为研究气体性质的方便,可以设想一种气体,能严格遵守气体实验定律称为理想气体。
(1)理想气体的宏观描述:能够严格遵守气体三个实验定律(或严格遵守)的气体叫做理想气体.
(2)理想气体的微规模型:我们把分子间不存在相互作用力(除碰撞外),并且分子是没有大小的质点的气体叫做理想气体.
(3)理想气体是从实际气体抽象出来的物理模型.
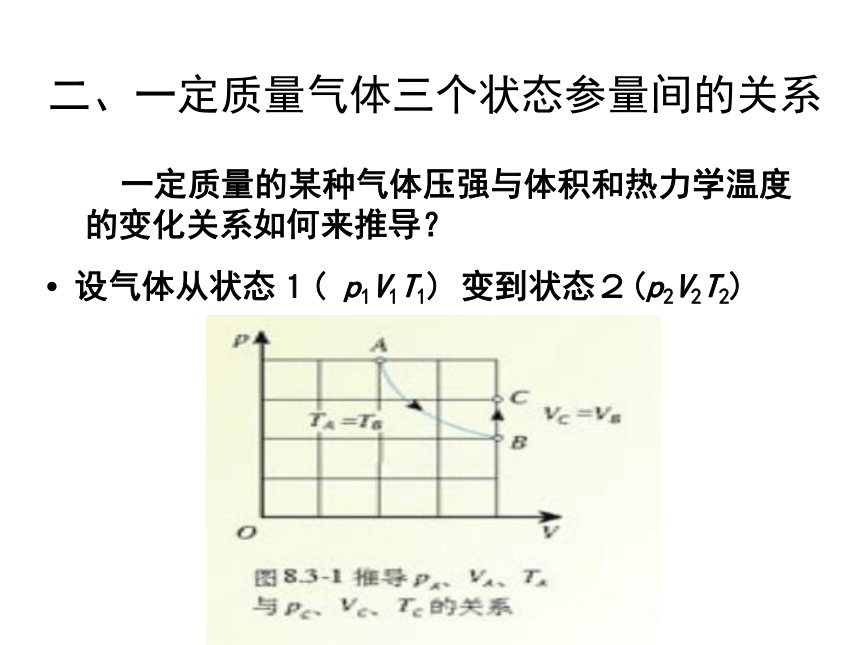
理想气体是不存在的,但在温度不太低,压强不太大的情况下,可将实际气体看做是理想气体.思考:现实中的气体能否看做理想气体二、一定质量气体三个状态参量间的关系 一定质量的某种气体压强与体积和热力学温度的变化关系如何来推导?? 设气体从状态1( p1V1T1) 变到状态2(p2V2T2)二、一定质量气体三个状态参量间的关系 有气体实验定律可知,一定质量的某种气体压强与体积和热力学温度的关系分别为:可以写成: 或上式表明,一定质量的理想气体,尽管p、V、T着三个参量都可以改变,但是 pV/T 是不变的,总等于一个常量 C.? 设气体从状态1( p1V1T1) 变到状态2(p2V2T2)则有(1)上式从气体实验定律推导而得.
(2)成立条件:气体质量一定.
(3)在温度不太低,压强不太大时,各种气体质量一定时,状态变化能较好地符合上述关系,但不满足此条件时上式与实际偏差较大.2.理想气体的状态方程 或 注意:式中的C是一个恒量,与气体的质量和种类有关.例1、内燃机汽缸里的混合气体,在吸气冲程之末,温度为50℃,压强为1.0×105Pa,体积为0.93L。在压缩冲程中,把气体的体积压缩为0.155L时,压强增大到1.2×106Pa,求这时混合气体的温度升高到多少摄氏度?思考运用理想气体状态方程解题的步骤:1、明确研究对象
2、明确研究过程,找出初末态三参量
3、列方程
4、求解1、对于理想气体,下面说法哪些是正确的:
A.理想气体是严格遵守气体实验定律的气体模型;
B.理想气体的分子没有体积;
C.理想气体分子间除了互相碰撞外,无其他相互作用;
D.实际气体在温度不太低,压强不太大的情况下,可当成理想气体.课堂练习:2、对于一个装有可以自由移动的活塞的密闭气缸内的一定质量的理想气体,在下列各状态变化中,不可能发生的是:
A.气体的温度升高,压强不变而密度也不变;
B.气体的温度降低,压强减小而密度不变;
C.气体的温度升高,压强增大,密度也增大; D.气体的温度不变,压强减小而密度也减小.
3、一气泡从30米深的海底升到水面,设水底温度是4℃,水面温度是15℃,那么气泡在水面的体积约是水底时: A.3倍 B.4倍; C.5倍 D.12倍.[分析和解答]气泡内气体可看成一定质量的理想气体.
p水=ρ水gh=1×103×10×30=3×105(Pa)=3(atm)
在水底时:p1=p0+p水=4atm, T1=4℃+273=277k.在水面时:p2=1atm, T2=15℃+273=288K.
由理想气体的状态方程:p1V1/T1=p2V2/T2,
得V2/V1=p1T2/p2T1=4×288/1×277≈4.
故正确的选项为B.4、密封的体积为2L的气体,压强为2atm,温度为27℃,加热后,压强和体积各增加20%,则它的最后温度为 .小结 实际气体在温度不太低、压强不太大时可看做理想气体.
一定质量的某种理想气体的状态方程为:或
(1)理想气体的宏观描述:能够严格遵守气体三个实验定律(或严格遵守)的气体叫做理想气体.
(2)理想气体的微规模型:我们把分子间不存在相互作用力(除碰撞外),并且分子是没有大小的质点的气体叫做理想气体.
(3)理想气体是从实际气体抽象出来的物理模型.
理想气体是不存在的,但在温度不太低,压强不太大的情况下,可将实际气体看做是理想气体.思考:现实中的气体能否看做理想气体二、一定质量气体三个状态参量间的关系 一定质量的某种气体压强与体积和热力学温度的变化关系如何来推导?? 设气体从状态1( p1V1T1) 变到状态2(p2V2T2)二、一定质量气体三个状态参量间的关系 有气体实验定律可知,一定质量的某种气体压强与体积和热力学温度的关系分别为:可以写成: 或上式表明,一定质量的理想气体,尽管p、V、T着三个参量都可以改变,但是 pV/T 是不变的,总等于一个常量 C.? 设气体从状态1( p1V1T1) 变到状态2(p2V2T2)则有(1)上式从气体实验定律推导而得.
(2)成立条件:气体质量一定.
(3)在温度不太低,压强不太大时,各种气体质量一定时,状态变化能较好地符合上述关系,但不满足此条件时上式与实际偏差较大.2.理想气体的状态方程 或 注意:式中的C是一个恒量,与气体的质量和种类有关.例1、内燃机汽缸里的混合气体,在吸气冲程之末,温度为50℃,压强为1.0×105Pa,体积为0.93L。在压缩冲程中,把气体的体积压缩为0.155L时,压强增大到1.2×106Pa,求这时混合气体的温度升高到多少摄氏度?思考运用理想气体状态方程解题的步骤:1、明确研究对象
2、明确研究过程,找出初末态三参量
3、列方程
4、求解1、对于理想气体,下面说法哪些是正确的:
A.理想气体是严格遵守气体实验定律的气体模型;
B.理想气体的分子没有体积;
C.理想气体分子间除了互相碰撞外,无其他相互作用;
D.实际气体在温度不太低,压强不太大的情况下,可当成理想气体.课堂练习:2、对于一个装有可以自由移动的活塞的密闭气缸内的一定质量的理想气体,在下列各状态变化中,不可能发生的是:
A.气体的温度升高,压强不变而密度也不变;
B.气体的温度降低,压强减小而密度不变;
C.气体的温度升高,压强增大,密度也增大; D.气体的温度不变,压强减小而密度也减小.
3、一气泡从30米深的海底升到水面,设水底温度是4℃,水面温度是15℃,那么气泡在水面的体积约是水底时: A.3倍 B.4倍; C.5倍 D.12倍.[分析和解答]气泡内气体可看成一定质量的理想气体.
p水=ρ水gh=1×103×10×30=3×105(Pa)=3(atm)
在水底时:p1=p0+p水=4atm, T1=4℃+273=277k.在水面时:p2=1atm, T2=15℃+273=288K.
由理想气体的状态方程:p1V1/T1=p2V2/T2,
得V2/V1=p1T2/p2T1=4×288/1×277≈4.
故正确的选项为B.4、密封的体积为2L的气体,压强为2atm,温度为27℃,加热后,压强和体积各增加20%,则它的最后温度为 .小结 实际气体在温度不太低、压强不太大时可看做理想气体.
一定质量的某种理想气体的状态方程为:或
