第一节 溶液的形成 课件(33张PPT)
图片预览









文档简介
课件33张PPT。 溶解和乳化是常见的物质分散现象。第三单元 溶 液第一节 溶液的形成(1)日常生活中你见过哪些溶液?食盐水食醋酒 取一只小烧杯,倒入约50mL水,加入少半匙食盐(主要是氯化钠),用玻璃棒搅拌。仔细观察发生的变化,直至食盐颗粒在水中消失。
问题:
1.实验中得到食盐水是纯净物还是混合物?
2.想一想这杯食盐水的上部、中部、下部,任一处,是否一样咸?
3.如果把上述食盐水倒入瓶子里密封起来,放置一个月,一年,……你猜测食盐会不会从水中分离出来?
混合物稳定性均一性像这样我们把食盐分散在水中形成均一,稳定的混合物我们叫做食盐的水溶液。
那我们把蔗糖也分散在水中形成的均一,稳定的混合物我们叫做蔗糖的水溶液学.科.网.
一种或几种物质分散到另一种物质里,形成均一、稳定的混合物。2.溶液的特征1.溶液的定义均一性、稳定性、混合物。 均一性:溶液形成以后,溶液任一部分的组成和性质完全相同。 稳定性:溶液在外界条件(包括温度、压强)不改变的情况下,溶液中的各组成不会发生变化。一、溶液乳浊液 由小液滴分散到液体里形成的混合物叫做乳浊液。(如:牛奶、豆浆、油水混合物 )
乳浊液不稳定,易分层 。 固体小颗粒悬浮于液体里形成的混合物叫做悬浊液(或悬浮液)。(如:泥水、面粉和水混合)悬浊液: 悬浊液和乳浊液统称浊液。
浊液的特征:不均一、不稳定。 凡是液体溶液一般都是透明的混合物。 透明的混合物,并不是说溶液为无色液体,有的溶液是有颜色的。
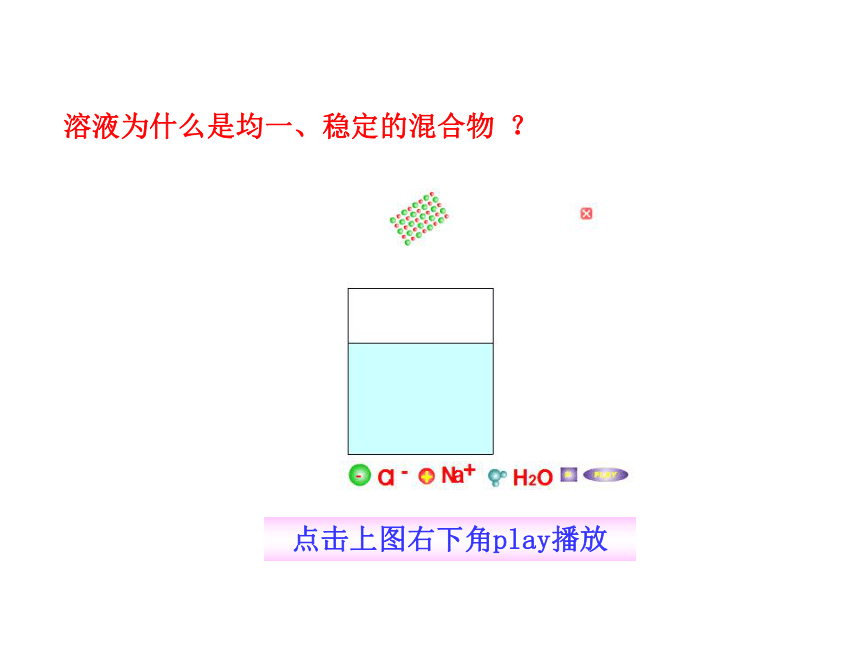
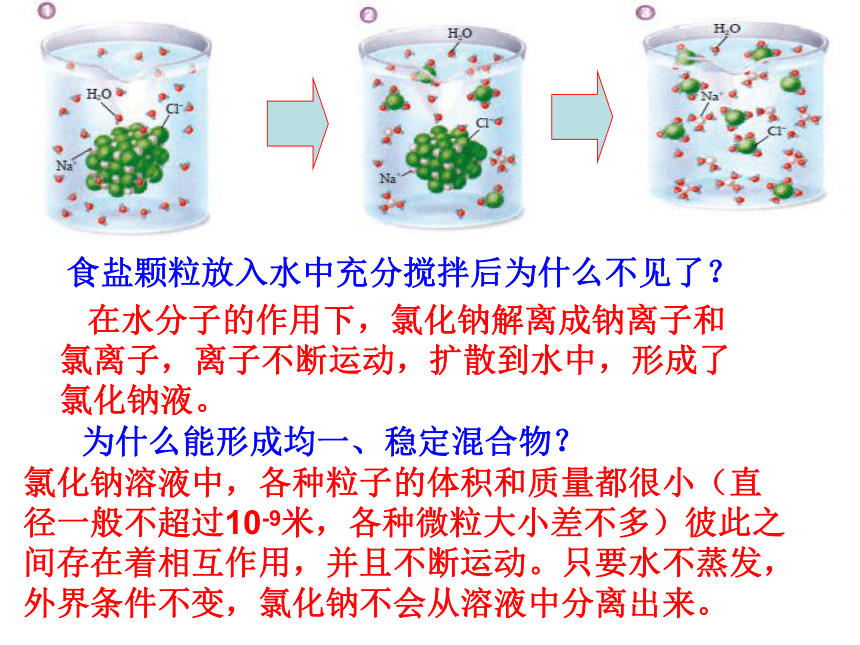
如:硫酸铜溶液为蓝色;氯化亚铁溶液为浅绿色;氯化铁溶液为黄色;高锰酸钾溶液为紫红色。但大多数的溶液为无色液体。 均一、透明、稳定的液体不一定是溶液。 注意:溶液为什么是均一、稳定的混合物 ?点击上图右下角play播放食盐颗粒放入水中充分搅拌后为什么不见了? 在水分子的作用下,氯化钠解离成钠离子和氯离子,离子不断运动,扩散到水中,形成了氯化钠液。为什么能形成均一、稳定混合物?氯化钠溶液中,各种粒子的体积和质量都很小(直径一般不超过10-9米,各种微粒大小差不多)彼此之间存在着相互作用,并且不断运动。只要水不蒸发,外界条件不变,氯化钠不会从溶液中分离出来。空气、合金也是溶液吗?分析与思考:它们具有均一性、稳定性、是混合物。因此是溶液!1.溶液是无色透明的液体。
2.冰水混合体是溶液。
3.把食盐溶液倒掉一半后,变稀了。
4.在温度不变,水不蒸发的条件下,蔗糖溶液中的蔗糖会从水中分离出来。
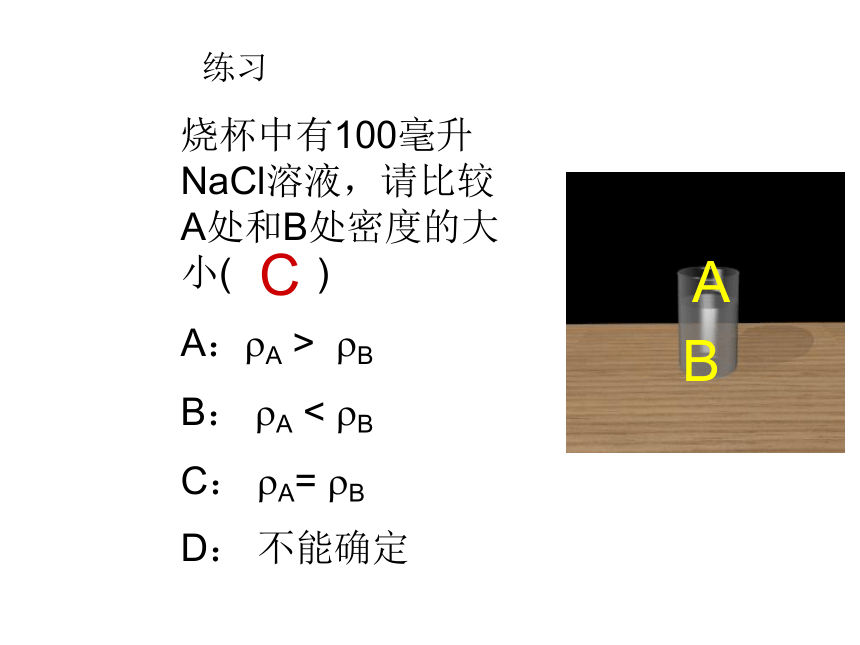
判断:练习烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B
B: ?A < ?B
C: ?A= ?B
D: 不能确定ABC练习:当水分不蒸发,温度不改变时,KNO3
溶液放置一年时间后,KNO3将( )
A:会沉降下来
B:不会分离出来
C:会浮上水面
D:不能确定B【溶剂】能溶解其他物质的物质叫做溶剂。如:水、酒精、汽油等【溶质】被溶解的物质叫做溶质。如:蔗糖、高锰酸钾、食盐NaCl溶质H2O溶剂溶液(混合物)溶液的命名:某溶质的某溶剂溶液。如氯化钠的水溶液。(或某溶质溶液,如氯化钠溶液。)3、溶液的组成溶液质量=溶质质量+溶剂质量 相同溶质在不同种溶剂里的溶解能力不同。
不同溶质在同种溶剂里的溶解能力也不同。溶液体积 < 溶质体积 + 溶剂体积 说明:
从微观上分析,溶液形成的过程是溶质的分子或离子分散到溶剂分子中的过程,因为粒子之间存在间隔,它们相互填充,所以溶液体积不等于溶质体积和溶剂体积之和。注意:
1、溶液中的溶质可以是一种或几种,而溶剂只有一种。
2、溶液不一定是液体,但初中阶段溶液一般为液态。
3、若是固体或气体与液体相互溶解成为溶液,一般习惯上把固体或气体看做溶质,液体看做溶剂。
4、当状态相同的两种物质混合形成溶液时,一般把量多的一种叫溶剂,量少的一种叫溶质。 注意:
5、其他物质与水混合形成溶液时,无论水量有多少,水都是溶剂,水是最常见的溶剂。
6、若加入的溶质没有完全溶解,那么溶质是实际溶解的那部分,未溶解的不是该溶液的溶质。
7、如果物质在溶解时发生了化学反应,生成了新物质,那么形成的溶液中溶质是反应后的生成物。
8、结晶水合物溶于水时,无水部分作溶质,结晶水作溶剂。4、水以外的溶剂酒精(碘可溶于酒精配制碘酒)汽油(可溶解油、易燃)氯仿(优良的有机溶剂、有毒)练习:指出下列溶液中溶质、溶剂各是什么?
溶质 溶剂
(1)硫酸铜溶液
(2)稀硫酸
(3)75%的医用酒精
(4)油脂溶解在汽油里
(5)白磷的二硫化碳溶液
(6)盐酸
(7) CO2的水溶液CuSO4 水H2SO4 水C2H5OH 水油脂汽油白磷二硫化碳HCl 水H2CO3 水大家在日常生活中有见过下列产品吗?魔术冰袋化学发热袋化学加热——自动加热方便面通过以上生活实例可知:
可溶的物质在溶解时,常常会使溶液的温度发生改变,这表明有些物质在溶解时会出现吸热现象,有些物质在溶解时则会出现放热现象。 二、物质溶解时溶液温度的变化
【活动与探究】NH4NO3 、NaCl 、NaOH分别溶于
水时,用温度计测量温度的变化。
实验步骤:1.将温度计插入水中插入盛水的烧杯中,观察
并记录水的温度;
2.向烧杯中分别加入NaCl 、NH4NO3、NaOH
用玻璃棒迅速搅拌,读出温度计的刻度并记
录。实验现象:实验结论:
NaCl溶于水无明显的吸热或放热现象;
NH4NO3 溶于水时吸热;
NaOH 溶于水时放热。溶 解过程扩散过程
(吸热)水合过程
(放热)扩散吸热>水合放热
(溶液温度降低)
例如:NH4NO3固体溶于水扩散吸热 =水合放热
(溶液温度不变)
例如:NaCl固体溶于水扩散吸热<水合放热
(溶液温度升高)
例如:NaOH 固体和浓硫酸
(H2SO4)溶于水1、对一杯完全溶解的糖水而言,下列叙述正确的是( )
A、 上面的比下面的甜。
B、 下面的比上面甜。
C、 中间的最甜。
D、各部分一样甜。
2、 当水分不蒸发,温度不变时,盐水放置较长时间后,盐( )
A、会沉降出来 B、不会分离出来
C、会浮上水面 D、都有可能
DB测试评价3. 下列物质属于溶液的是( )
A.石灰浆 B 生理盐水 C 菜汁 D牛奶测试评价B4、各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂不具有乳化功能的是( )
A.用汽油除去衣服上的油污
B用餐具洗洁精清洗餐具上的油污
C.用肥皂液洗衣 D.用沐浴露洗澡A5.右侧U形管中液面未发生明显变化,该物质是 ( )
A.氢氧化钠固体
B.硝酸铵晶体
C.氯化钠晶体 C若右侧U形管中液面左高右低,该物质是 ( )若右侧U形管中液面左低右高,该物质是 ( )BA5.如右图所示,向小试管中分别加入下列一定量的固体物质。观察现象溶解过程中
的能量变化溶液溶解后
温度升高浊液组成特性稳定性溶剂混合物均一性溶质溶液的形成溶解后
温度降低溶解后
温度不变
问题:
1.实验中得到食盐水是纯净物还是混合物?
2.想一想这杯食盐水的上部、中部、下部,任一处,是否一样咸?
3.如果把上述食盐水倒入瓶子里密封起来,放置一个月,一年,……你猜测食盐会不会从水中分离出来?
混合物稳定性均一性像这样我们把食盐分散在水中形成均一,稳定的混合物我们叫做食盐的水溶液。
那我们把蔗糖也分散在水中形成的均一,稳定的混合物我们叫做蔗糖的水溶液学.科.网.
一种或几种物质分散到另一种物质里,形成均一、稳定的混合物。2.溶液的特征1.溶液的定义均一性、稳定性、混合物。 均一性:溶液形成以后,溶液任一部分的组成和性质完全相同。 稳定性:溶液在外界条件(包括温度、压强)不改变的情况下,溶液中的各组成不会发生变化。一、溶液乳浊液 由小液滴分散到液体里形成的混合物叫做乳浊液。(如:牛奶、豆浆、油水混合物 )
乳浊液不稳定,易分层 。 固体小颗粒悬浮于液体里形成的混合物叫做悬浊液(或悬浮液)。(如:泥水、面粉和水混合)悬浊液: 悬浊液和乳浊液统称浊液。
浊液的特征:不均一、不稳定。 凡是液体溶液一般都是透明的混合物。 透明的混合物,并不是说溶液为无色液体,有的溶液是有颜色的。
如:硫酸铜溶液为蓝色;氯化亚铁溶液为浅绿色;氯化铁溶液为黄色;高锰酸钾溶液为紫红色。但大多数的溶液为无色液体。 均一、透明、稳定的液体不一定是溶液。 注意:溶液为什么是均一、稳定的混合物 ?点击上图右下角play播放食盐颗粒放入水中充分搅拌后为什么不见了? 在水分子的作用下,氯化钠解离成钠离子和氯离子,离子不断运动,扩散到水中,形成了氯化钠液。为什么能形成均一、稳定混合物?氯化钠溶液中,各种粒子的体积和质量都很小(直径一般不超过10-9米,各种微粒大小差不多)彼此之间存在着相互作用,并且不断运动。只要水不蒸发,外界条件不变,氯化钠不会从溶液中分离出来。空气、合金也是溶液吗?分析与思考:它们具有均一性、稳定性、是混合物。因此是溶液!1.溶液是无色透明的液体。
2.冰水混合体是溶液。
3.把食盐溶液倒掉一半后,变稀了。
4.在温度不变,水不蒸发的条件下,蔗糖溶液中的蔗糖会从水中分离出来。
判断:练习烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B
B: ?A < ?B
C: ?A= ?B
D: 不能确定ABC练习:当水分不蒸发,温度不改变时,KNO3
溶液放置一年时间后,KNO3将( )
A:会沉降下来
B:不会分离出来
C:会浮上水面
D:不能确定B【溶剂】能溶解其他物质的物质叫做溶剂。如:水、酒精、汽油等【溶质】被溶解的物质叫做溶质。如:蔗糖、高锰酸钾、食盐NaCl溶质H2O溶剂溶液(混合物)溶液的命名:某溶质的某溶剂溶液。如氯化钠的水溶液。(或某溶质溶液,如氯化钠溶液。)3、溶液的组成溶液质量=溶质质量+溶剂质量 相同溶质在不同种溶剂里的溶解能力不同。
不同溶质在同种溶剂里的溶解能力也不同。溶液体积 < 溶质体积 + 溶剂体积 说明:
从微观上分析,溶液形成的过程是溶质的分子或离子分散到溶剂分子中的过程,因为粒子之间存在间隔,它们相互填充,所以溶液体积不等于溶质体积和溶剂体积之和。注意:
1、溶液中的溶质可以是一种或几种,而溶剂只有一种。
2、溶液不一定是液体,但初中阶段溶液一般为液态。
3、若是固体或气体与液体相互溶解成为溶液,一般习惯上把固体或气体看做溶质,液体看做溶剂。
4、当状态相同的两种物质混合形成溶液时,一般把量多的一种叫溶剂,量少的一种叫溶质。 注意:
5、其他物质与水混合形成溶液时,无论水量有多少,水都是溶剂,水是最常见的溶剂。
6、若加入的溶质没有完全溶解,那么溶质是实际溶解的那部分,未溶解的不是该溶液的溶质。
7、如果物质在溶解时发生了化学反应,生成了新物质,那么形成的溶液中溶质是反应后的生成物。
8、结晶水合物溶于水时,无水部分作溶质,结晶水作溶剂。4、水以外的溶剂酒精(碘可溶于酒精配制碘酒)汽油(可溶解油、易燃)氯仿(优良的有机溶剂、有毒)练习:指出下列溶液中溶质、溶剂各是什么?
溶质 溶剂
(1)硫酸铜溶液
(2)稀硫酸
(3)75%的医用酒精
(4)油脂溶解在汽油里
(5)白磷的二硫化碳溶液
(6)盐酸
(7) CO2的水溶液CuSO4 水H2SO4 水C2H5OH 水油脂汽油白磷二硫化碳HCl 水H2CO3 水大家在日常生活中有见过下列产品吗?魔术冰袋化学发热袋化学加热——自动加热方便面通过以上生活实例可知:
可溶的物质在溶解时,常常会使溶液的温度发生改变,这表明有些物质在溶解时会出现吸热现象,有些物质在溶解时则会出现放热现象。 二、物质溶解时溶液温度的变化
【活动与探究】NH4NO3 、NaCl 、NaOH分别溶于
水时,用温度计测量温度的变化。
实验步骤:1.将温度计插入水中插入盛水的烧杯中,观察
并记录水的温度;
2.向烧杯中分别加入NaCl 、NH4NO3、NaOH
用玻璃棒迅速搅拌,读出温度计的刻度并记
录。实验现象:实验结论:
NaCl溶于水无明显的吸热或放热现象;
NH4NO3 溶于水时吸热;
NaOH 溶于水时放热。溶 解过程扩散过程
(吸热)水合过程
(放热)扩散吸热>水合放热
(溶液温度降低)
例如:NH4NO3固体溶于水扩散吸热 =水合放热
(溶液温度不变)
例如:NaCl固体溶于水扩散吸热<水合放热
(溶液温度升高)
例如:NaOH 固体和浓硫酸
(H2SO4)溶于水1、对一杯完全溶解的糖水而言,下列叙述正确的是( )
A、 上面的比下面的甜。
B、 下面的比上面甜。
C、 中间的最甜。
D、各部分一样甜。
2、 当水分不蒸发,温度不变时,盐水放置较长时间后,盐( )
A、会沉降出来 B、不会分离出来
C、会浮上水面 D、都有可能
DB测试评价3. 下列物质属于溶液的是( )
A.石灰浆 B 生理盐水 C 菜汁 D牛奶测试评价B4、各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂不具有乳化功能的是( )
A.用汽油除去衣服上的油污
B用餐具洗洁精清洗餐具上的油污
C.用肥皂液洗衣 D.用沐浴露洗澡A5.右侧U形管中液面未发生明显变化,该物质是 ( )
A.氢氧化钠固体
B.硝酸铵晶体
C.氯化钠晶体 C若右侧U形管中液面左高右低,该物质是 ( )若右侧U形管中液面左低右高,该物质是 ( )BA5.如右图所示,向小试管中分别加入下列一定量的固体物质。观察现象溶解过程中
的能量变化溶液溶解后
温度升高浊液组成特性稳定性溶剂混合物均一性溶质溶液的形成溶解后
温度降低溶解后
温度不变
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
