附录I部分酸、碱和盐的溶解性表(室温)(共17张PPT)
文档属性
| 名称 | 附录I部分酸、碱和盐的溶解性表(室温)(共17张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 85.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-06-27 16:13:52 | ||
图片预览


文档简介
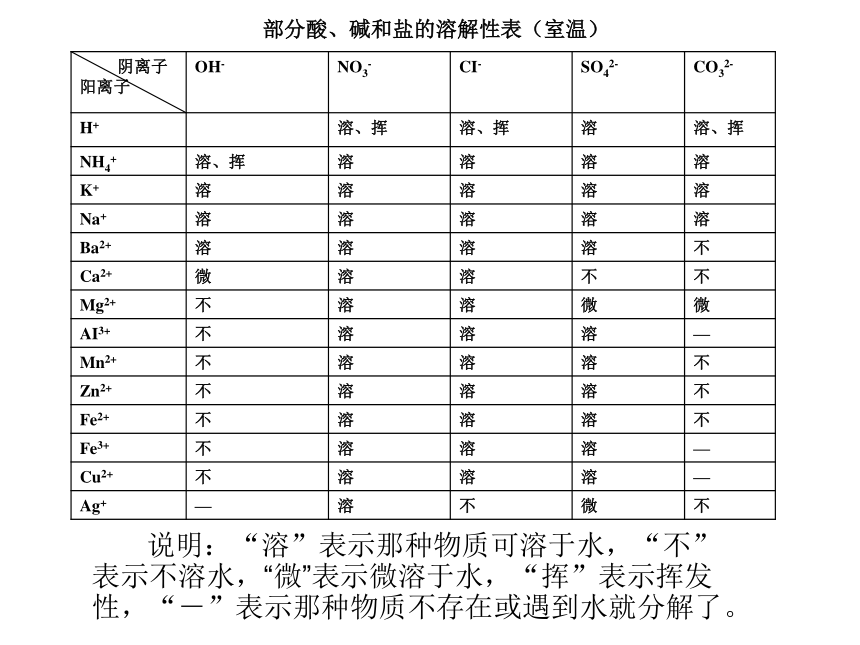
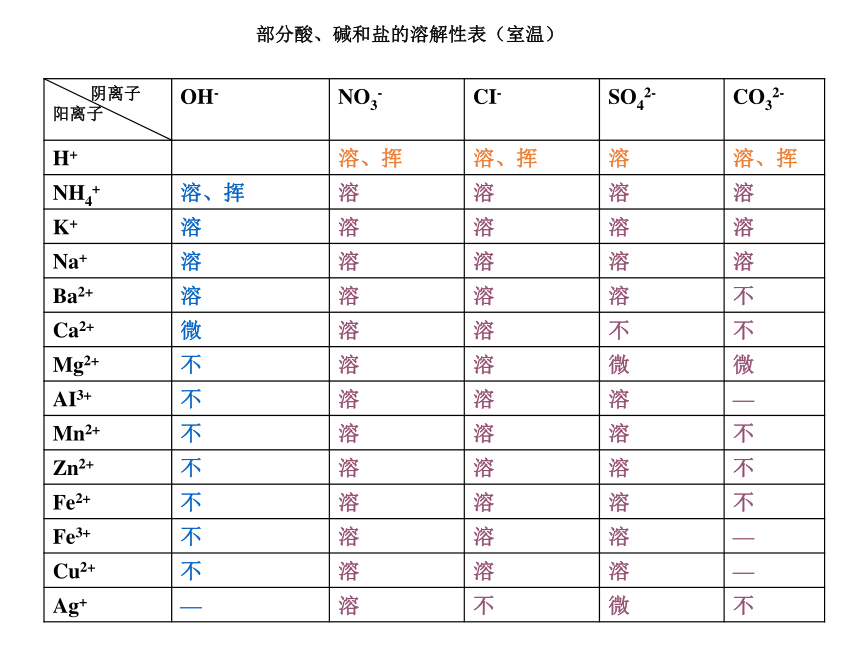
课件17张PPT。 部分酸、碱和盐的溶解性表(室温)人教版化学下册附录I 说明:“溶”表示那种物质可溶于水,“不”表示不溶水,“微”表示微溶于水,“挥”表示挥发性,“-”表示那种物质不存在或遇到水就分解了。部分酸、碱和盐的溶解性表(室温)部分酸、碱和盐的溶解性表(室温)
溶解性歌诀钾钠铵硝都溶;
盐酸盐除氯化银不溶,其它都溶;
硫酸盐除硫酸钡不溶,其它都溶;
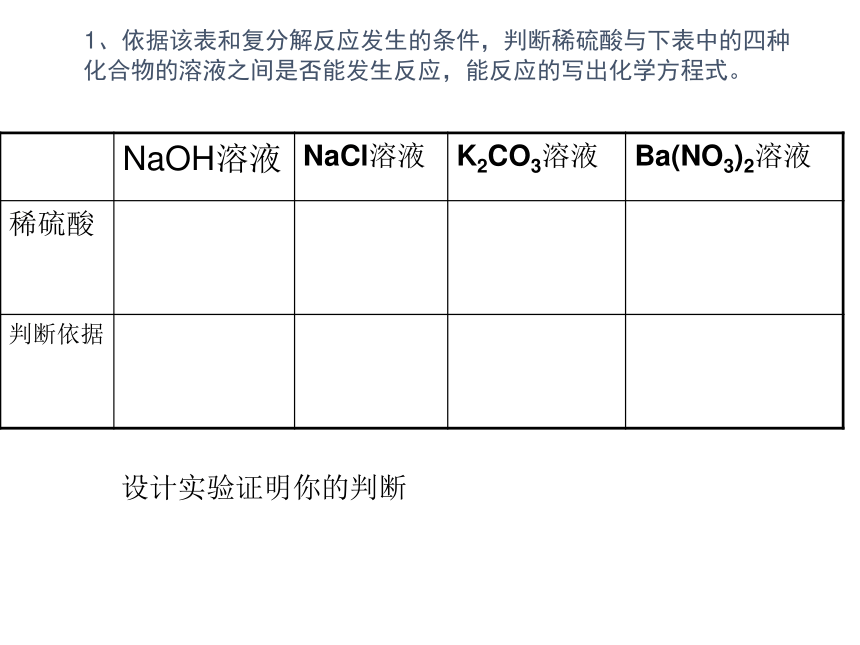
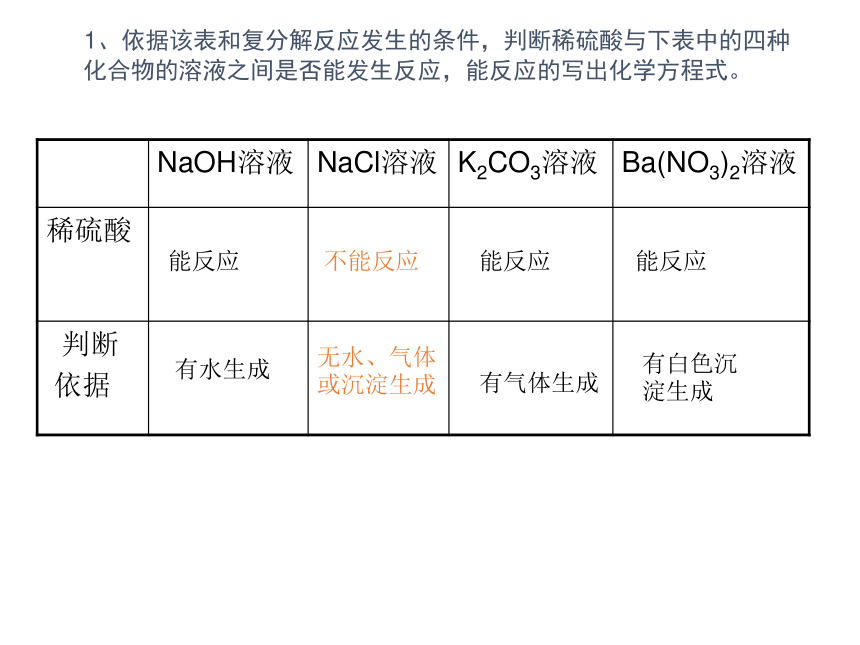
碳酸盐只有碳酸铵、碳酸钾、碳酸钠溶,碳酸镁微溶,其它都不溶。 1、依据该表和复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间是否能发生反应,能反应的写出化学方程式。设计实验证明你的判断 1、依据该表和复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间是否能发生反应,能反应的写出化学方程式。能反应有水生成能反应 能反应不能反应无水、气体或沉淀生成有气体生成有白色沉淀生成
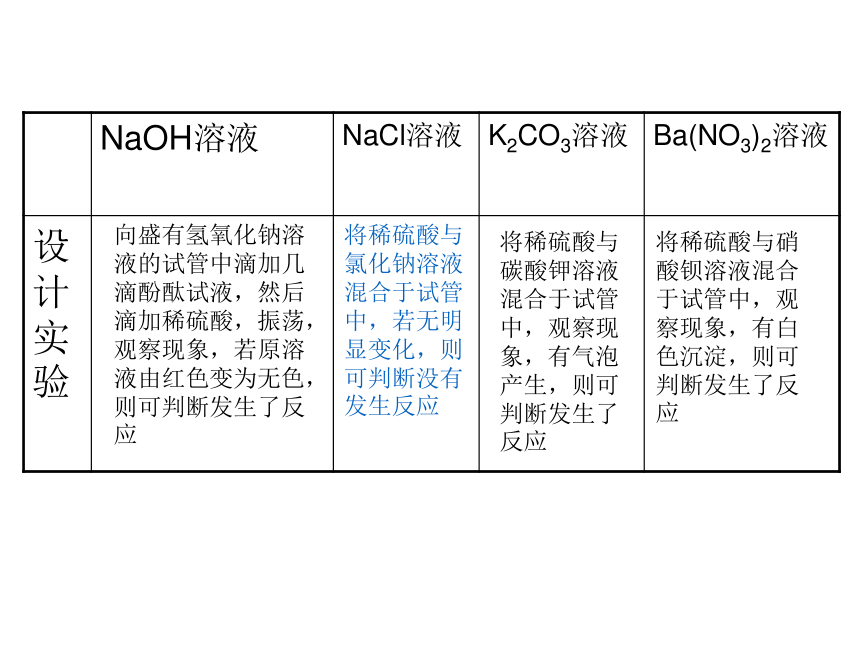
向盛有氢氧化钠溶液的试管中滴加几滴酚酞试液,然后滴加稀硫酸,振荡,观察现象,若原溶液由红色变为无色,则可判断发生了反应
将稀硫酸与氯化钠溶液混合于试管中,若无明显变化,则可判断没有发生反应将稀硫酸与碳酸钾溶液混合于试管中,观察现象,有气泡产生,则可判断发生了反应
将稀硫酸与硝酸钡溶液混合于试管中,观察现象,有白色沉淀,则可判断发生了反应
判断硝酸钡与碳酸钾能否发生复分解反应,若能试着写出化学方程式;并设计实验证明你的判断。 2、 判断下列复分解反应能否发生,若能请写出方程式,否则请说明原因。(1) Ba(OH)2 + CuSO4
(2) Ca(OH)2 + HNO3
(3) NaCl + KNO3
(4) K2CO3 + HCl 2、 判断下列复分解反应能否发生,若能请写出方程式,否则请说明原因。(1) Ba(OH)2 + CuSO4=Cu(OH)2 ↓ +BaSO4↓
(2) Ca(OH)2 + HNO3=Ca(NO3)2 + 2H2O
(3) NaCl + KNO3 无沉淀、气体、水生成
(4) K2CO3 + 2 HCl = 2KCI +H2O +CO2↑3、用水鉴别NaOH、NaCl、 CaCO3三种固体物质。 4、(2013襄阳中考)用括号内物质不能一次性区别开下列各组物质的是( )
A.CaO、CaCO3、KCl三种固体(水)
B.CaCl2、Na2CO3、K2SO4三种溶液 [Ba(OH)2溶液]
C.Cu、Fe、CuO三种固体(稀盐酸)
D.CuCl2、NaNO3、K2CO3三种溶液 [Ca(OH)2溶液]A.生石灰
B.石灰石
C.熟石灰
D. 苛性钠
5、(2014襄阳中考)要除去CaCl2溶液中的稀盐酸得到纯净的CaCl2溶液,最好的方法是加入( )
6、(2011襄阳中考)下列除杂所选择的试剂错误的是( ) A.CuSO4,NaOH,NaCl
B.NaCl, KCl,KNO3
C.NaOH, NaCl,HCl
D.MgCl2,AgNO3,NaOH7、下列各组溶液混合,能发生化学反应,并且一定能得到无色透明溶液的是( ) 8、(2015襄阳中考)下列各组溶液,不用其他试剂无法鉴别的是( )A.H2SO4 NaCl Na2CO3 CaCl2
B.HCl NaOH CuSO4 MgSO4
C.Na2CO3 K2SO4 BaCl2 HCl
D.NaNO3 HCl CaCl2 KOH 谢谢!
溶解性歌诀钾钠铵硝都溶;
盐酸盐除氯化银不溶,其它都溶;
硫酸盐除硫酸钡不溶,其它都溶;
碳酸盐只有碳酸铵、碳酸钾、碳酸钠溶,碳酸镁微溶,其它都不溶。 1、依据该表和复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间是否能发生反应,能反应的写出化学方程式。设计实验证明你的判断 1、依据该表和复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间是否能发生反应,能反应的写出化学方程式。能反应有水生成能反应 能反应不能反应无水、气体或沉淀生成有气体生成有白色沉淀生成
向盛有氢氧化钠溶液的试管中滴加几滴酚酞试液,然后滴加稀硫酸,振荡,观察现象,若原溶液由红色变为无色,则可判断发生了反应
将稀硫酸与氯化钠溶液混合于试管中,若无明显变化,则可判断没有发生反应将稀硫酸与碳酸钾溶液混合于试管中,观察现象,有气泡产生,则可判断发生了反应
将稀硫酸与硝酸钡溶液混合于试管中,观察现象,有白色沉淀,则可判断发生了反应
判断硝酸钡与碳酸钾能否发生复分解反应,若能试着写出化学方程式;并设计实验证明你的判断。 2、 判断下列复分解反应能否发生,若能请写出方程式,否则请说明原因。(1) Ba(OH)2 + CuSO4
(2) Ca(OH)2 + HNO3
(3) NaCl + KNO3
(4) K2CO3 + HCl 2、 判断下列复分解反应能否发生,若能请写出方程式,否则请说明原因。(1) Ba(OH)2 + CuSO4=Cu(OH)2 ↓ +BaSO4↓
(2) Ca(OH)2 + HNO3=Ca(NO3)2 + 2H2O
(3) NaCl + KNO3 无沉淀、气体、水生成
(4) K2CO3 + 2 HCl = 2KCI +H2O +CO2↑3、用水鉴别NaOH、NaCl、 CaCO3三种固体物质。 4、(2013襄阳中考)用括号内物质不能一次性区别开下列各组物质的是( )
A.CaO、CaCO3、KCl三种固体(水)
B.CaCl2、Na2CO3、K2SO4三种溶液 [Ba(OH)2溶液]
C.Cu、Fe、CuO三种固体(稀盐酸)
D.CuCl2、NaNO3、K2CO3三种溶液 [Ca(OH)2溶液]A.生石灰
B.石灰石
C.熟石灰
D. 苛性钠
5、(2014襄阳中考)要除去CaCl2溶液中的稀盐酸得到纯净的CaCl2溶液,最好的方法是加入( )
6、(2011襄阳中考)下列除杂所选择的试剂错误的是( ) A.CuSO4,NaOH,NaCl
B.NaCl, KCl,KNO3
C.NaOH, NaCl,HCl
D.MgCl2,AgNO3,NaOH7、下列各组溶液混合,能发生化学反应,并且一定能得到无色透明溶液的是( ) 8、(2015襄阳中考)下列各组溶液,不用其他试剂无法鉴别的是( )A.H2SO4 NaCl Na2CO3 CaCl2
B.HCl NaOH CuSO4 MgSO4
C.Na2CO3 K2SO4 BaCl2 HCl
D.NaNO3 HCl CaCl2 KOH 谢谢!
同课章节目录
