高中化学人教版选修3第三章第4节 离子晶体
文档属性
| 名称 | 高中化学人教版选修3第三章第4节 离子晶体 |

|
|
| 格式 | zip | ||
| 文件大小 | 22.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-06-30 00:00:00 | ||
图片预览







文档简介
课件24张PPT。Chemistry第四节 离子晶体第三章
晶体结构与性质 草酸合铁酸钾晶体胆矾晶体1. 定义:
2. 构成离子键的粒子:
3. 作用力:
4. 形成条件:
5. 离子键特征:
6. 离子化合物:
阴、阳离子静电作用带相反电荷离子之间的相互作用称为离子键通常由活泼金属和活泼非金属形成由离子键构成的化合物
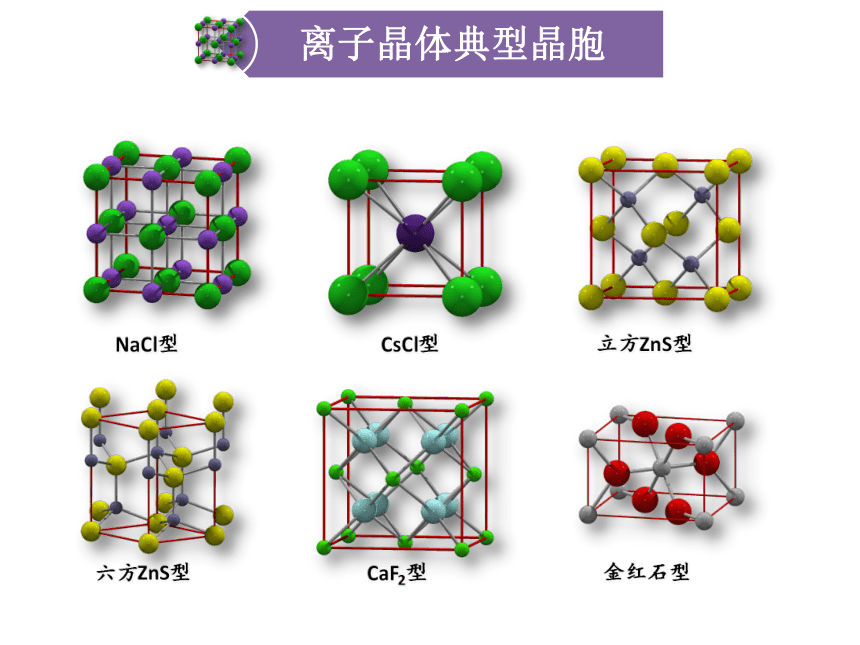
也叫离子晶体无方向性、无饱和性铁铝榴石 Fe3Al2Si3O12钙铬榴石 Ca3Cr2Si3O12NaCl型CsCl型立方ZnS型六方ZnS型CaF2型金红石型离子晶体中离子接触情况分析负负接触
正负不接触 负负接触
正负接触 正负接触
负负不接触 a=2(r+ + r-) a=2(r+ + r-) 不稳定较稳定稳定1. 粒子位置:
2. 结构基元数:
3. 正负离子配位数比:
4. Na+周围最近的Na+数:
Cl-周围最近的Cl-数:
5.负离子堆积方式:
6. 正离子所占空隙:
6:6面心立方最密堆积NaCl型4个Cl-, 4个Na+Cl-位于顶点和面心
Na+位于棱心和体心1212正八面体利用所给泡沫塑料小球搭建NaCl离子晶体的晶胞模型,画图记录你搭建NaCl的微观结构 ,总结其微观结构特征。阴离子(大球)
阳离子(小球)活动1八面体空隙添入正离子利用所给泡沫塑料小球搭建NaCl离子晶体的晶胞模型,画图记录你搭建NaCl的微观结构 ,总结其微观结构特征。活动11. 粒子位置:
2. 结构基元数:
3. 正负离子配位数比:
4. Cs+周围最近的Cs+数:
Cl-周围最近的Cl-数:
5.负离子堆积方式:
6. 正离子所占空隙:
8:8简单立方CsCl型1个Cl-, 1个Cs+Cl-位于顶点
Cs+位于体心66正方体利用所给泡沫塑料小球搭建NaCl离子晶体的晶胞模型,画图记录你搭建NaCl的微观结构 ,总结其微观结构特征。活动1活动2利用所给泡沫塑料小球搭建CsCl离子晶体的晶胞模型,画图记录你搭建CsCl的微观结构 ,总结其微观结构特征。探究1半径比与晶体结构的关系???正方体空隙正八面体空隙??0.732? r+/r- <1 正离子的配位数为8,配位多面体为立方体
0.414? r+/r- <0.732 正离子的配位数为6,配位多面体为正八面体
0.225 ? r+/r- < 0.414 由于正离子半径太小,只有选择配位多面体为正四面体,配位数为4 探究1半径比与晶体结构的关系?探究2决定晶体结构的其他因素?Ca2+F-Ca2+配位数:8
配位多面体:立方体Ca2+F-F- 配位数:4
配位多面体:正四面体 1. 粒子位置:
2. 结构基元数:
3. 正负离子配位数比:
4.负离子堆积方式:
8:4简单立方CaF2型8个F-, 4个Ca2+Ca2+位于顶点和面心
F-位于立方体内几何因素、电荷因素、键性因素
晶体结构与性质 草酸合铁酸钾晶体胆矾晶体1. 定义:
2. 构成离子键的粒子:
3. 作用力:
4. 形成条件:
5. 离子键特征:
6. 离子化合物:
阴、阳离子静电作用带相反电荷离子之间的相互作用称为离子键通常由活泼金属和活泼非金属形成由离子键构成的化合物
也叫离子晶体无方向性、无饱和性铁铝榴石 Fe3Al2Si3O12钙铬榴石 Ca3Cr2Si3O12NaCl型CsCl型立方ZnS型六方ZnS型CaF2型金红石型离子晶体中离子接触情况分析负负接触
正负不接触 负负接触
正负接触 正负接触
负负不接触 a=2(r+ + r-) a=2(r+ + r-) 不稳定较稳定稳定1. 粒子位置:
2. 结构基元数:
3. 正负离子配位数比:
4. Na+周围最近的Na+数:
Cl-周围最近的Cl-数:
5.负离子堆积方式:
6. 正离子所占空隙:
6:6面心立方最密堆积NaCl型4个Cl-, 4个Na+Cl-位于顶点和面心
Na+位于棱心和体心1212正八面体利用所给泡沫塑料小球搭建NaCl离子晶体的晶胞模型,画图记录你搭建NaCl的微观结构 ,总结其微观结构特征。阴离子(大球)
阳离子(小球)活动1八面体空隙添入正离子利用所给泡沫塑料小球搭建NaCl离子晶体的晶胞模型,画图记录你搭建NaCl的微观结构 ,总结其微观结构特征。活动11. 粒子位置:
2. 结构基元数:
3. 正负离子配位数比:
4. Cs+周围最近的Cs+数:
Cl-周围最近的Cl-数:
5.负离子堆积方式:
6. 正离子所占空隙:
8:8简单立方CsCl型1个Cl-, 1个Cs+Cl-位于顶点
Cs+位于体心66正方体利用所给泡沫塑料小球搭建NaCl离子晶体的晶胞模型,画图记录你搭建NaCl的微观结构 ,总结其微观结构特征。活动1活动2利用所给泡沫塑料小球搭建CsCl离子晶体的晶胞模型,画图记录你搭建CsCl的微观结构 ,总结其微观结构特征。探究1半径比与晶体结构的关系???正方体空隙正八面体空隙??0.732? r+/r- <1 正离子的配位数为8,配位多面体为立方体
0.414? r+/r- <0.732 正离子的配位数为6,配位多面体为正八面体
0.225 ? r+/r- < 0.414 由于正离子半径太小,只有选择配位多面体为正四面体,配位数为4 探究1半径比与晶体结构的关系?探究2决定晶体结构的其他因素?Ca2+F-Ca2+配位数:8
配位多面体:立方体Ca2+F-F- 配位数:4
配位多面体:正四面体 1. 粒子位置:
2. 结构基元数:
3. 正负离子配位数比:
4.负离子堆积方式:
8:4简单立方CaF2型8个F-, 4个Ca2+Ca2+位于顶点和面心
F-位于立方体内几何因素、电荷因素、键性因素
