浙教版科学九上 1.4 常见的碱 同步练习
文档属性
| 名称 | 浙教版科学九上 1.4 常见的碱 同步练习 |  | |
| 格式 | doc | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2018-06-29 16:16:39 | ||
图片预览



文档简介
21世纪教育网 –中小学教育资源及组卷应用平台
浙教版科学九上同步练习之1.4 常见的碱
一、单选题
1.下列不属于NaOH的俗称的是( )
A. 苛性钠 B. 烧碱 C. 纯碱 D. 火碱
2.下列潮湿的气体不能用固体氢氧化钠干燥的是( )
A. H2 B. CO2 C. CO D. O2
3.下列物质在敞口容器中久置,因发生化学变化溶液质量减小的是( )
A. 浓硫酸 B. 浓盐酸 C. 氢氧化钠溶液 D. 石灰水
4.氢氧化钠是一种常见的碱,下列有关氢氧化钠的说法正确的是( )
A. 固态氢氧化钠具有吸水性,可以用来干燥 O2、H2、CO2 等气体
B. 氢氧化钠能与酸反应,可用于治疗胃酸过多
C. 氢氧化钠与氢氧化钾在水中都能解离出 OH-,化学性质相似
D. 向露置于空气中的氢氧化钠溶液中滴加酚酞,溶液变红,说明氢氧化钠溶液没有变质
5.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
序号 实 验 现 象
A 将氢氧化钠固体放在表面皿上,放置一会儿 固体受潮,逐渐溶解
B 向盛有氢氧化钠溶液的试管中滴入无色酚酞试液 溶液变红
C 向盛有氢氧化钠溶液的试管中滴加稀盐酸 有氯化钠生成
D 向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液 产生蓝色沉淀
A. A B. B C. C D. D
6.下列实验对应的图像正确的是 ( )
A B C D
向稀硫酸中加入过量的锌,溶液中溶质质量 向pH=2的盐酸中滴加过量的氢氧化钠溶液 向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液 向pH=12的氢氧化钠溶液中加水稀释
A. A B. B C. C D. D
7.下列关于氢氧化钠和氢氧化钙的描述中错误的是( )
A. 它们的水溶液都能使石蕊溶液变红
B. 氢氧化钙的溶解度随温度升高而减小,氢氧化钠固体溶于水会放出大量的热量
C. 它们的溶液敞口放在空气中都会变质
D. 氢氧化钠可用来生产肥皂,氢氧化钙可用来杀菌消毒及改良酸性土壤
8.下列关于碱的叙述中,不正确的是( )
A. 含有氢氧根离子的化合物 B. 碱溶液能使紫色石蕊试液变蓝
C. 碱能跟酸反应生成盐和水 D. 电离出阴离子全部都是氢氧根离子的化合物是碱
9.用稀的碱性溶液或清水浸泡,可使残留在蔬菜上的农药降低毒性。如用碱性溶液浸泡蔬菜,可在水中加入适量的 ( )
A. 白酒 B. 纯碱 C. 白糖 D. 食醋
10.下列说法正确的是( )
A. pH﹥7的溶液一定是碱溶液 B. 碱溶液中阴、阳离子的数目相等
C. 碱在电离时生成的阴离子全部是OH- D. 电离时有阳离子和OH-生成的化合物叫做碱
二、填空题
11.氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是:_____________________________.测量其溶液的pH时,应该用________,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是:______________________.
(3)用熟石灰粉与草木灰(主要成分:K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.在有露水的早晨,把“黑白粉”撒在植物茎叶上,可杀灭某些害虫.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是___________________________________.
②“黑白粉”还可提供植物必需的营养素是________(填元素符号).
12.氢氧化钠溶液逐滴滴入硫酸铜、硫酸混合溶液中,生成沉淀随滴入氢氧化钠溶液的变化如图.
(1)OA 段溶液中溶质是_______________
(2)AB 段溶液中溶质是_______________
(3)BC 段溶液中溶质是_______________.
13.分析下列反应,回答有关问题.
①2KOH+CO2═K2CO3+H2O ②Ca(OH)2+CO2═CaCO3↓+H2O
(1)由上述反应可知,碱溶液与二氧化碳反应都生成________和水.
(2)根据上述规律,写出Ba(OH)2与CO2反应的化学方程式________________________.
(3)依据所学知识推测,用二氧化碳鉴别氢氧化钠和氢氧化钙两种溶液时,无明显现象的是_____________溶液.
14.结合NaOH、Ca(OH)2的相关知识,回答下列问题
(1)可用来改变良酸性土壤的碱是________;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是___________________________;
(3)除去NaOH溶液中混有的少量Ca(OH)2 , 可选用的试剂是________.
15.如图所示,向充满干燥的CO2气体的烧瓶中,第一次滴加氢氧化钠溶液,小气球发生的变化为__________,原因是___________________,反应的化学方程式为________________________;第二次再向烧瓶内溶液中滴加盐酸,小气球发生的变化为___________,其原因是(用化学方程式表示)______________________________.
16.氢氧化钙和氢氧化钠都是常用的碱.
(1)请写出氢氧化钙与下列物质反应的化学方程式:
①与盐酸反应:______________________________
②与硫酸铜溶液反应:________________________
上述反应中,属于所有的碱都有的共同化学性质是________(填编号).
(2)氢氧化钙的下列用途中,不能用氢氧化钠来代替的是________(填编号).
①中和废水中的过量硫酸②改良酸性土壤③检验二氧化碳.
三、解答题
17.甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0 g样品溶于一定量的水中得到25. 0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表:
甲 乙 丙
加入氢氧化钠溶液质量 (g) 35.0 40.0 45.0
反应得到沉淀的质量 (g) 2.5 2.9 2.9
试回答下列问题:
(1)上述实验中,________同学所用的氢氧化钠溶液一定过量。
(2)求样品中氯化镁的含量(写出计算过程,结果精确到0.1%,下同)。
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数。
18.向含CuCl2和HCl的100g混合溶液中,逐滴滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如
图所示。请据图回答
(1)在滴加NaOH溶液过程中,原溶液中________离子个数不变。(填离子符号)
(2)P点溶液中的溶质是________(填化学式)。
(3)m1的值为________
(4)M点溶液中的溶质质量分数是多少
四、实验探究题
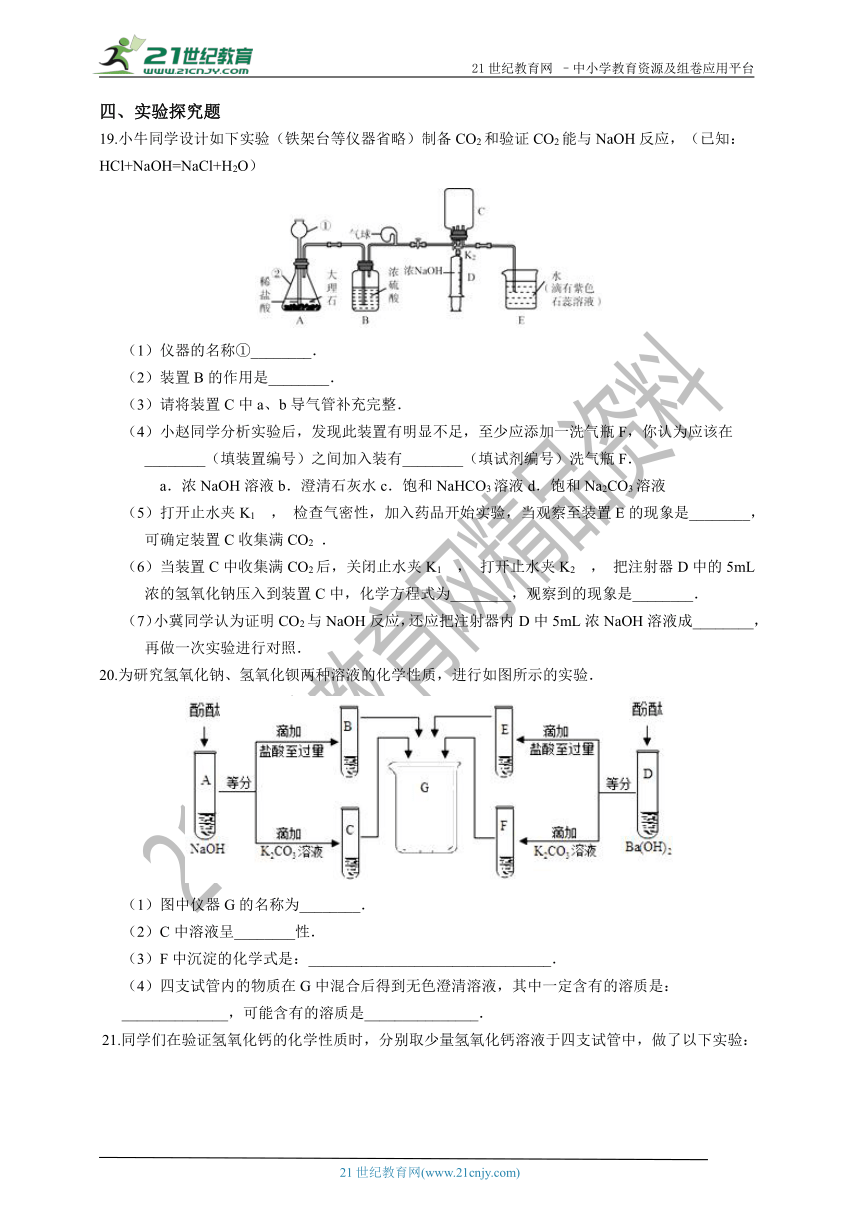
19.小牛同学设计如下实验(铁架台等仪器省略)制备CO2和验证CO2能与NaOH反应,(已知:HCl+NaOH=NaCl+H2O)
(1)仪器的名称①________.
(2)装置B的作用是________.
(3)请将装置C中a、b导气管补充完整.
(4)小赵同学分析实验后,发现此装置有明显不足,至少应添加一洗气瓶F,你认为应该在________(填装置编号)之间加入装有________(填试剂编号)洗气瓶F.
a.浓NaOH溶液b.澄清石灰水c.饱和NaHCO3溶液d.饱和Na2CO3溶液
(5)打开止水夹K1 , 检查气密性,加入药品开始实验,当观察至装置E的现象是________,可确定装置C收集满CO2 .
(6)当装置C中收集满CO2后,关闭止水夹K1 , 打开止水夹K2 , 把注射器D中的5mL浓的氢氧化钠压入到装置C中,化学方程式为________,观察到的现象是________.
(7)小冀同学认为证明CO2与NaOH反应,还应把注射器内D中5mL浓NaOH溶液成________,再做一次实验进行对照.
20.为研究氢氧化钠、氢氧化钡两种溶液的化学性质,进行如图所示的实验.
(1)图中仪器G的名称为________.
(2)C中溶液呈________性.
(3)F中沉淀的化学式是:________________________________.
(4)四支试管内的物质在G中混合后得到无色澄清溶液,其中一定含有的溶质是:______________,可能含有的溶质是_______________.
21.同学们在验证氢氧化钙的化学性质时,分别取少量氢氧化钙溶液于四支试管中,做了以下实验:
A. B. C. D.
请根据实验回答下列问题。
(1)A中观察到的现象是__________________。
(2)C中无明显现象。为证明氢氧化钙与盐酸能发生反应,于是他们向B中滴加稀盐酸,当观察到_____________时,说明两者发生了反应。
(3)实验结束后,同学们将上述四支试管中的物质倒入同一烧杯内,烧杯底部有白色固体,上层为有色溶液。为处理废液,过滤后,向有色滤液中加入稀盐酸,有气泡产生,继续加稀盐酸至溶液颜色恰好消失,此时溶液中的溶质为___________(除酚酞外)。
22.小明同学用如下实验装置探究CO2与NaOH溶液能否反应。锥形瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL)。
【查阅资料】
①通常状况下,1体积水能溶解1体积二氧化碳;
②CO2在酸性溶液中溶解性会大大降低,若向溶有CO2的水溶液中加入盐酸, 会将CO2从水中赶出,观察到溶液中有气泡。
(1)小明向A装置通入的CO2气体体积V应________200mL(填“>”、“<”或“=”)。
(2)A中的溶液是________,B中的溶液是________ , 证明氢氧化钠溶液可以与二氧化碳反应的现象是__________________。
(3)小红不用B装置,实验后他向锥形瓶A中的溶液中加入盐酸溶液发现有气泡产生,他判断该现象能证明二氧化碳和氢氧化钠溶液反应,你认为他的判断是否正确________。小丽也不用B装置,实验后她向锥形瓶A中的溶液中加入氯化钙溶液,如出现_______________ , 就能证明二氧化碳和氢氧化钠溶液反应。并写出相关化学方程式______________________________________________。
参考答案
一、单选题
1 2 3 4 5
C B D C C
6 7 8 9 10
C A A D C
二、填空题
11.(1)CaO+H2O═Ca(OH)2;用玻璃棒蘸取少量待测液滴在干燥的pH试纸上;
(2)CO2+Ca(OH)2═CaCO3↓+H2O
(3)Ca(OH)2+K2CO3=CaCO3↓+2KOH;K
12.(1)Na2SO4、CuSO4、H2SO4(2)Na2SO4、CuSO4(3)Na2SO4、NaOH
13.(1)盐(2)Ba(OH)2+CO2=BaCO3↓+H2O(3)氢氧化钠
14.(1)氢氧化钙(2)它们的溶液的阴离子均为氢氧根离子(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
15.变大;氢氧化钠吸收二氧化碳,导致瓶内压强变小;2NaOH+CO2=Na2CO3+H2O;变瘪;Na2CO3+2HCl=2NaCl+CO2↑+H2O
16.(1)Ca(OH)2+2HCl=CaCl2+2H2O;Ca(OH)2+CuSO4=CaSO4+Cu(OH)2↓;①
(2)②③
三、解答题
17.(1)丙
(2)解:设生成2.9克Mg(OH)2消耗MgCl2的质量为x,生成NaCl的质量为y,则
MgCl2+2NaOH= Mg(OH)2↓+ 2NaCl
95 58 117
x 2.9g y
95:58=x:2.9gx=4.75g
117:58=y:2.9gy=5.85g
混合物中MgCl2的质量分数为: ×100%=95.0%
(3)乙同学实验后溶液中NaCl的质量:5.0g-4.75g+5.85g=6.1g乙同学实验后溶液的质量:25.0g+40.0g-2.9g=62.1g
乙同学实验后所得溶液中氯化钠的质量分数: ×100%=9.8%
18.(1)Cl-(2)NaCl、CuCl2(3)120
(4)设HCl和NaOH溶液反应生成 NaCl的质量为x, NaOH溶液与CuCl2溶液反应生成NaCl的质量为y
HCl+ NaOH= NaCl+H2O
40 58.5
40×10% x
x = 5.85g
CuCl2+ 2NaOH = 2NaCl+ Cu(OH)2↓
117 98
y 9.8
y = 11.7g
M点溶液中的溶质质量分数= ×1 00% = 8.3%
答:M点溶液中的溶质质量分数是8.3%
四、实验探究题
19.(1)长颈漏斗(2)吸水
(3)解:如图中所示:
(4)AB;c
(5)紫色石蕊溶液变红
(6)2NaOH+CO2=Na2CO3+H2O;装置E中红色石蕊溶液会倒吸入装置C中
(7)水
20.(1)烧杯(2)碱(3)BaCO3(4)NaCl、KCl、BaCl2、酚酞;HCl
21.(1)变浑浊(2)溶液颜色由红色变为无色(3)NaCl
22.(1)>(2)NaOH;Ca(OH)2;B中不变浑浊(3)不正确;白色沉淀;CaCl2+Na2CO3=2NaCl+CaCO3↓
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
浙教版科学九上同步练习之1.4 常见的碱
一、单选题
1.下列不属于NaOH的俗称的是( )
A. 苛性钠 B. 烧碱 C. 纯碱 D. 火碱
2.下列潮湿的气体不能用固体氢氧化钠干燥的是( )
A. H2 B. CO2 C. CO D. O2
3.下列物质在敞口容器中久置,因发生化学变化溶液质量减小的是( )
A. 浓硫酸 B. 浓盐酸 C. 氢氧化钠溶液 D. 石灰水
4.氢氧化钠是一种常见的碱,下列有关氢氧化钠的说法正确的是( )
A. 固态氢氧化钠具有吸水性,可以用来干燥 O2、H2、CO2 等气体
B. 氢氧化钠能与酸反应,可用于治疗胃酸过多
C. 氢氧化钠与氢氧化钾在水中都能解离出 OH-,化学性质相似
D. 向露置于空气中的氢氧化钠溶液中滴加酚酞,溶液变红,说明氢氧化钠溶液没有变质
5.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
序号 实 验 现 象
A 将氢氧化钠固体放在表面皿上,放置一会儿 固体受潮,逐渐溶解
B 向盛有氢氧化钠溶液的试管中滴入无色酚酞试液 溶液变红
C 向盛有氢氧化钠溶液的试管中滴加稀盐酸 有氯化钠生成
D 向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液 产生蓝色沉淀
A. A B. B C. C D. D
6.下列实验对应的图像正确的是 ( )
A B C D
向稀硫酸中加入过量的锌,溶液中溶质质量 向pH=2的盐酸中滴加过量的氢氧化钠溶液 向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液 向pH=12的氢氧化钠溶液中加水稀释
A. A B. B C. C D. D
7.下列关于氢氧化钠和氢氧化钙的描述中错误的是( )
A. 它们的水溶液都能使石蕊溶液变红
B. 氢氧化钙的溶解度随温度升高而减小,氢氧化钠固体溶于水会放出大量的热量
C. 它们的溶液敞口放在空气中都会变质
D. 氢氧化钠可用来生产肥皂,氢氧化钙可用来杀菌消毒及改良酸性土壤
8.下列关于碱的叙述中,不正确的是( )
A. 含有氢氧根离子的化合物 B. 碱溶液能使紫色石蕊试液变蓝
C. 碱能跟酸反应生成盐和水 D. 电离出阴离子全部都是氢氧根离子的化合物是碱
9.用稀的碱性溶液或清水浸泡,可使残留在蔬菜上的农药降低毒性。如用碱性溶液浸泡蔬菜,可在水中加入适量的 ( )
A. 白酒 B. 纯碱 C. 白糖 D. 食醋
10.下列说法正确的是( )
A. pH﹥7的溶液一定是碱溶液 B. 碱溶液中阴、阳离子的数目相等
C. 碱在电离时生成的阴离子全部是OH- D. 电离时有阳离子和OH-生成的化合物叫做碱
二、填空题
11.氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是:_____________________________.测量其溶液的pH时,应该用________,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是:______________________.
(3)用熟石灰粉与草木灰(主要成分:K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.在有露水的早晨,把“黑白粉”撒在植物茎叶上,可杀灭某些害虫.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是___________________________________.
②“黑白粉”还可提供植物必需的营养素是________(填元素符号).
12.氢氧化钠溶液逐滴滴入硫酸铜、硫酸混合溶液中,生成沉淀随滴入氢氧化钠溶液的变化如图.
(1)OA 段溶液中溶质是_______________
(2)AB 段溶液中溶质是_______________
(3)BC 段溶液中溶质是_______________.
13.分析下列反应,回答有关问题.
①2KOH+CO2═K2CO3+H2O ②Ca(OH)2+CO2═CaCO3↓+H2O
(1)由上述反应可知,碱溶液与二氧化碳反应都生成________和水.
(2)根据上述规律,写出Ba(OH)2与CO2反应的化学方程式________________________.
(3)依据所学知识推测,用二氧化碳鉴别氢氧化钠和氢氧化钙两种溶液时,无明显现象的是_____________溶液.
14.结合NaOH、Ca(OH)2的相关知识,回答下列问题
(1)可用来改变良酸性土壤的碱是________;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是___________________________;
(3)除去NaOH溶液中混有的少量Ca(OH)2 , 可选用的试剂是________.
15.如图所示,向充满干燥的CO2气体的烧瓶中,第一次滴加氢氧化钠溶液,小气球发生的变化为__________,原因是___________________,反应的化学方程式为________________________;第二次再向烧瓶内溶液中滴加盐酸,小气球发生的变化为___________,其原因是(用化学方程式表示)______________________________.
16.氢氧化钙和氢氧化钠都是常用的碱.
(1)请写出氢氧化钙与下列物质反应的化学方程式:
①与盐酸反应:______________________________
②与硫酸铜溶液反应:________________________
上述反应中,属于所有的碱都有的共同化学性质是________(填编号).
(2)氢氧化钙的下列用途中,不能用氢氧化钠来代替的是________(填编号).
①中和废水中的过量硫酸②改良酸性土壤③检验二氧化碳.
三、解答题
17.甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0 g样品溶于一定量的水中得到25. 0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表:
甲 乙 丙
加入氢氧化钠溶液质量 (g) 35.0 40.0 45.0
反应得到沉淀的质量 (g) 2.5 2.9 2.9
试回答下列问题:
(1)上述实验中,________同学所用的氢氧化钠溶液一定过量。
(2)求样品中氯化镁的含量(写出计算过程,结果精确到0.1%,下同)。
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数。
18.向含CuCl2和HCl的100g混合溶液中,逐滴滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如
图所示。请据图回答
(1)在滴加NaOH溶液过程中,原溶液中________离子个数不变。(填离子符号)
(2)P点溶液中的溶质是________(填化学式)。
(3)m1的值为________
(4)M点溶液中的溶质质量分数是多少
四、实验探究题
19.小牛同学设计如下实验(铁架台等仪器省略)制备CO2和验证CO2能与NaOH反应,(已知:HCl+NaOH=NaCl+H2O)
(1)仪器的名称①________.
(2)装置B的作用是________.
(3)请将装置C中a、b导气管补充完整.
(4)小赵同学分析实验后,发现此装置有明显不足,至少应添加一洗气瓶F,你认为应该在________(填装置编号)之间加入装有________(填试剂编号)洗气瓶F.
a.浓NaOH溶液b.澄清石灰水c.饱和NaHCO3溶液d.饱和Na2CO3溶液
(5)打开止水夹K1 , 检查气密性,加入药品开始实验,当观察至装置E的现象是________,可确定装置C收集满CO2 .
(6)当装置C中收集满CO2后,关闭止水夹K1 , 打开止水夹K2 , 把注射器D中的5mL浓的氢氧化钠压入到装置C中,化学方程式为________,观察到的现象是________.
(7)小冀同学认为证明CO2与NaOH反应,还应把注射器内D中5mL浓NaOH溶液成________,再做一次实验进行对照.
20.为研究氢氧化钠、氢氧化钡两种溶液的化学性质,进行如图所示的实验.
(1)图中仪器G的名称为________.
(2)C中溶液呈________性.
(3)F中沉淀的化学式是:________________________________.
(4)四支试管内的物质在G中混合后得到无色澄清溶液,其中一定含有的溶质是:______________,可能含有的溶质是_______________.
21.同学们在验证氢氧化钙的化学性质时,分别取少量氢氧化钙溶液于四支试管中,做了以下实验:
A. B. C. D.
请根据实验回答下列问题。
(1)A中观察到的现象是__________________。
(2)C中无明显现象。为证明氢氧化钙与盐酸能发生反应,于是他们向B中滴加稀盐酸,当观察到_____________时,说明两者发生了反应。
(3)实验结束后,同学们将上述四支试管中的物质倒入同一烧杯内,烧杯底部有白色固体,上层为有色溶液。为处理废液,过滤后,向有色滤液中加入稀盐酸,有气泡产生,继续加稀盐酸至溶液颜色恰好消失,此时溶液中的溶质为___________(除酚酞外)。
22.小明同学用如下实验装置探究CO2与NaOH溶液能否反应。锥形瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL)。
【查阅资料】
①通常状况下,1体积水能溶解1体积二氧化碳;
②CO2在酸性溶液中溶解性会大大降低,若向溶有CO2的水溶液中加入盐酸, 会将CO2从水中赶出,观察到溶液中有气泡。
(1)小明向A装置通入的CO2气体体积V应________200mL(填“>”、“<”或“=”)。
(2)A中的溶液是________,B中的溶液是________ , 证明氢氧化钠溶液可以与二氧化碳反应的现象是__________________。
(3)小红不用B装置,实验后他向锥形瓶A中的溶液中加入盐酸溶液发现有气泡产生,他判断该现象能证明二氧化碳和氢氧化钠溶液反应,你认为他的判断是否正确________。小丽也不用B装置,实验后她向锥形瓶A中的溶液中加入氯化钙溶液,如出现_______________ , 就能证明二氧化碳和氢氧化钠溶液反应。并写出相关化学方程式______________________________________________。
参考答案
一、单选题
1 2 3 4 5
C B D C C
6 7 8 9 10
C A A D C
二、填空题
11.(1)CaO+H2O═Ca(OH)2;用玻璃棒蘸取少量待测液滴在干燥的pH试纸上;
(2)CO2+Ca(OH)2═CaCO3↓+H2O
(3)Ca(OH)2+K2CO3=CaCO3↓+2KOH;K
12.(1)Na2SO4、CuSO4、H2SO4(2)Na2SO4、CuSO4(3)Na2SO4、NaOH
13.(1)盐(2)Ba(OH)2+CO2=BaCO3↓+H2O(3)氢氧化钠
14.(1)氢氧化钙(2)它们的溶液的阴离子均为氢氧根离子(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
15.变大;氢氧化钠吸收二氧化碳,导致瓶内压强变小;2NaOH+CO2=Na2CO3+H2O;变瘪;Na2CO3+2HCl=2NaCl+CO2↑+H2O
16.(1)Ca(OH)2+2HCl=CaCl2+2H2O;Ca(OH)2+CuSO4=CaSO4+Cu(OH)2↓;①
(2)②③
三、解答题
17.(1)丙
(2)解:设生成2.9克Mg(OH)2消耗MgCl2的质量为x,生成NaCl的质量为y,则
MgCl2+2NaOH= Mg(OH)2↓+ 2NaCl
95 58 117
x 2.9g y
95:58=x:2.9gx=4.75g
117:58=y:2.9gy=5.85g
混合物中MgCl2的质量分数为: ×100%=95.0%
(3)乙同学实验后溶液中NaCl的质量:5.0g-4.75g+5.85g=6.1g乙同学实验后溶液的质量:25.0g+40.0g-2.9g=62.1g
乙同学实验后所得溶液中氯化钠的质量分数: ×100%=9.8%
18.(1)Cl-(2)NaCl、CuCl2(3)120
(4)设HCl和NaOH溶液反应生成 NaCl的质量为x, NaOH溶液与CuCl2溶液反应生成NaCl的质量为y
HCl+ NaOH= NaCl+H2O
40 58.5
40×10% x
x = 5.85g
CuCl2+ 2NaOH = 2NaCl+ Cu(OH)2↓
117 98
y 9.8
y = 11.7g
M点溶液中的溶质质量分数= ×1 00% = 8.3%
答:M点溶液中的溶质质量分数是8.3%
四、实验探究题
19.(1)长颈漏斗(2)吸水
(3)解:如图中所示:
(4)AB;c
(5)紫色石蕊溶液变红
(6)2NaOH+CO2=Na2CO3+H2O;装置E中红色石蕊溶液会倒吸入装置C中
(7)水
20.(1)烧杯(2)碱(3)BaCO3(4)NaCl、KCl、BaCl2、酚酞;HCl
21.(1)变浑浊(2)溶液颜色由红色变为无色(3)NaCl
22.(1)>(2)NaOH;Ca(OH)2;B中不变浑浊(3)不正确;白色沉淀;CaCl2+Na2CO3=2NaCl+CaCO3↓
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
