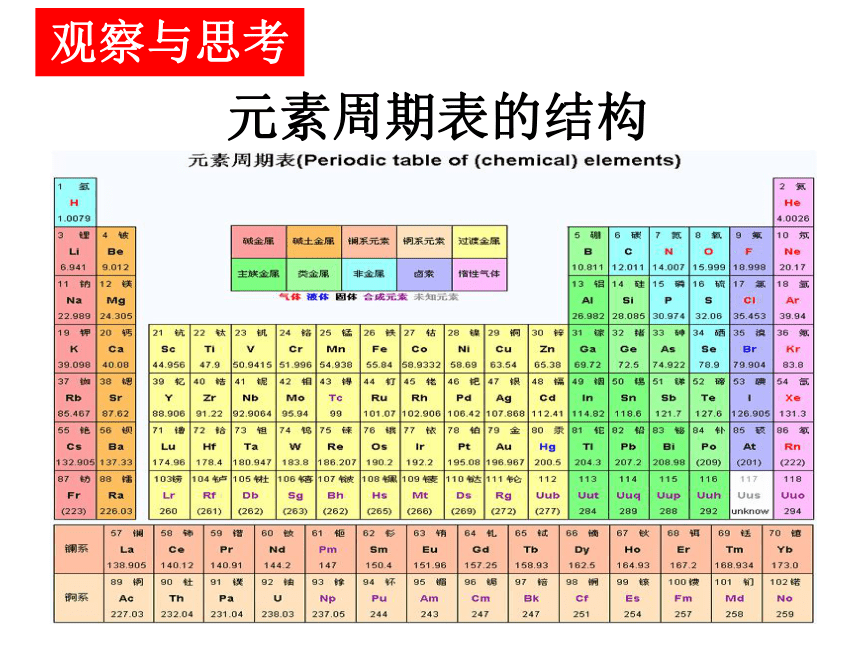
元素周期表的结构
图片预览





文档简介
课件19张PPT。德国化学家德贝莱纳:“三元素组”观点。他把当时已知的54种元素中的15种,分成5组,每组的三种元素性质相似,而且中间元素的相对原子质量等于较轻和较重的两个元素相对原子质量之和的一半。例如钙、锶、钡,性质相似,锶的相对原子质量大约是钙和钡的相对原子质量之和的一半。 现代化学的元素周期律是1869年的德米特里·伊万诺维奇·门捷列夫首创的。英国科学家莫色勒:1913年利用阴极射线撞击金属产生X射线,发现原子序数越大,X射线的频率就越高,因此他认为原子核的正电荷决定了元素的化学性质,并把元素依照核内正电荷(即质子数或原子序数)排列道尔顿提出科学原子论后,随着各种元素的相对原子质量的数据日益精确和原子价(化合价)概念的提出,就使元素相对原子质量与性质(包括化合价)之间的联系显露出来。元素周期表起源简介 德国化学家迈耶尔借鉴了德贝莱纳、纽兰兹等人的研究成果,从化合价和物理性质方面人手,去探索元素间的规律。在他的《近代化学理论》一书中,刊登了元素周期表,表中列出了28个元素,他们按相对原子质量递增的顺序排列,一共分成六族,并给出了相应的原子价是4、3、2、1、1、2。1868年,发表了第二张周期表,增加了24个元素和9个纵行,并区分了主族和副族。迈耶尔的第三张元素周期表发表于1870年,他采用了竖式周期表的形式,并且预留了一些空位给有待发现的元素,但是表中没有氢元素。可以说,迈耶尔已经发现了元素周期律后人在做法国矿物学家尚古多:“螺旋图”他将已知的62种元素按相对原子质量的大小顺序,标记在绕着圆柱体上升的螺旋线上,这样某些性质相近的元素恰好出现在同一母线上。这种排列方法很有趣,但要达到井然有序的程度还有困难英国化学家纽兰兹:把当时已知的元素按相对原子质量大小的顺序进行排列,发现无论从哪一个元素算起,每到第八个元素就和第一一个元素的性质相近。这很像音乐上的八度音循环,因此,他干脆把元素的这种周期性叫做“八音律”,并据此画出了标示元素关系的“八音律”表。显然,纽兰兹已经下意识地摸到了“真理女神"的裙角,差点就揭示元素周期律了。不过,条件限制了他做进一步的探索,因为当时相对原子质量的测定值有错误,而且他也没有考虑到还有尚未发现的元素,只是机械地按当时的相对原子质量大小将元素排列起来,所以他没能揭示出元素之间的内在规律。门捷列夫 门捷列夫对化学这一学科发展最大贡献在于发现了化学元素周期律。他根据元素周期律编制了第一个元素周期表,把已经发现的63种元素全部列入表里,从而初步完成了使元素系统化的任务。他还在表中留下空位,预言了类似硼、铝、硅的未知元素经过多年 修订补充和完善后才成为当代的周期表。常见的元素周期表为长式元素周期表。在长式元素周期表中,元素是以元素的原子序数排列,最小的排行最先。表中一横行称为一个周期,一纵列称为一个族,最后有两个系。元素周期表的结构观察与思考元素周期表中的元素排列周期族H HeLiBeBCNOFNeNaMgAlSiPSClArKCaScTiVCrMnFeCoNiCuZnGaGeAsSeBrKrRbSrYZrNbMoTcRuRhPdAgCdInSnSbTeIXeCsBaLaCePrNdPmSmEuGdTbDyHoErTmYbLuLaHfTaWReOsIrPtAuHgTlPbBiPoAtRnFrRaAcAcThPaUNpPuAmCmBkCfEsFmMdNoLrRfDbSgBhHsMtUunUuuUubⅠAⅡAⅢAⅣAⅤAⅥAⅦAⅢBⅣBⅤBⅥBⅦBⅧ ⅠBⅡB02828828
18
8
28
18
18
8
28
18
32
18
8
2短
周
期长
周
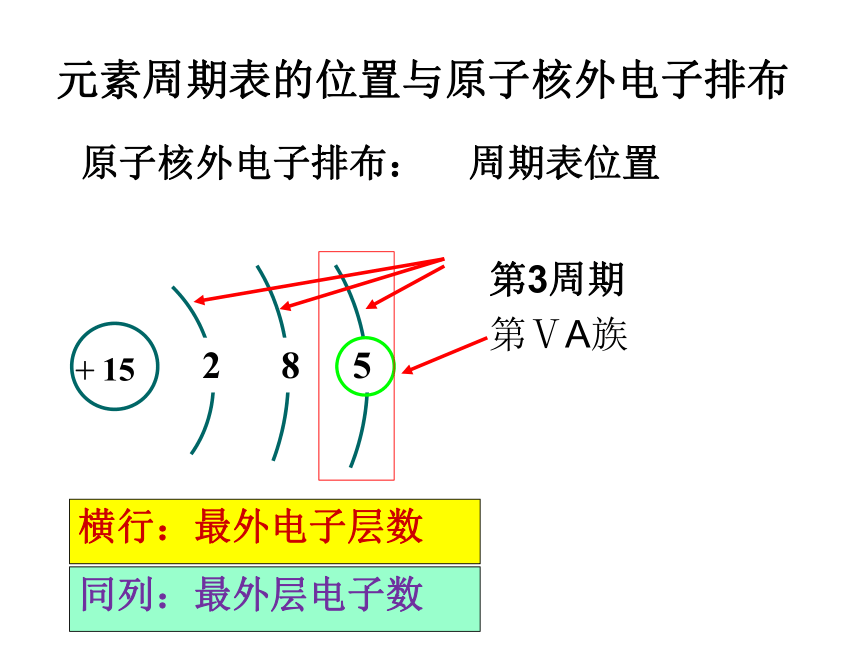
期元素周期表的位置与原子核外电子排布原子核外电子排布:周期表位置第3周期
第ⅤA族横行:最外电子层数同列:最外层电子数交流与讨论 阅读研究图1-5 周期依据: 原子核外电子层数 共有 个周期,7 各周期上的元素种数
第1周期有 种;
第2周期有 种;
第3周期有 种;
第4周期有 种;
第5周期有 种;
第6周期有 种;
第7周期有 种; 28 8 18 18 32 26 短周期 长周期 (不完全周期)横行与周期 阅读研究图1-5 同列依据: 原子最外层电子数 共有 个族, 16 表示主族, 表示副族ABAABBⅧ0同列与同族交流与讨论 共有 个列, 18同一族一定是同一列吗?同一列一定是同一族吗?元素周期表的结构B、Ⅷ族都只有长周期元素短周期元素只出现在A族元素中1.下表中的粗线是元素周期表部分边界,请ⅠA、ⅡA、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、ⅠB、ⅡB、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、ⅧB、0填入下表适当的空格中,并用粗线补元素周期表边界,将1~36个数字填入恰当的空格中,画出金属元素与非金属元素的分界线 2. (1)同一周期的X、Y两种元素,X位于ⅡA族、Y为ⅣA族,它们的原子序数分别是a和b,已知a和b的关系有:b=a+2,那么a和b还可能有什么关系?
b=a+12b=a+26指出下列元素在周期表中的位置1.根据元素序号判断元素所处周期表位置。
7N第 同期 族,16S第 同期 族;
35Br第 同期 族,26Fe第 同期 族;
2.根据元素周期表位置,判断元素名称和符号:
第 2同期 ⅣA 族的是 。第 3同期 ⅢA 族的是 。
第 4同期 ⅥA 族的是 .
第 4同期 ⅢB 族的是 .
3.与氩原子电子层结构相同的阳离子是: 。
4.与氩原子电子层结构相同的阴离子是: 。
2ⅤA3ⅥA4ⅦA4Ⅷ碳C铝Al硒Se钪ScK+/Ca2+S2-/Cl-小结主族元素:+19281原子核外电子排布:周期表位置第4周期
第ⅠA族位置与结构8第4周期
第ⅣA族+3228418试一试1、如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的7/10,则下列说法中不正确的是
A.原子半径由大到小排列顺序Z>Y>X
B.Y元素的两种同素异形体在常温下都是气体
C.最高价氧化物对应水化物的酸性W>Z
D.阴离子半径由大到小排列顺序Z>W>X>YS ClN O试一试2。如右图所示,若A、B、C为短周期元素,则A、B、C三种元素分别是
、 、 。3。如若右图所示,A、B、C为短周期元素,则A、B、C三种元素分别是 、 、 。ABCHBeMgHeFS试一试4。如右图所示,若A、B、C为短周期元素,且核电荷数之和为32,则A、B、C三种元素分别是
、 、 。SNF1。已知:A、B同周期,A为ⅡA族元素,B为ⅣA族元素,若A的核电荷数为a,则B的核电荷数可能是 。
2。已知X、Y同主族,Y是第三周期元素,X是第二周期元素,若Y的核电荷数为b,则X的核电荷数可能是 。问题解决判断正误1.最外层电子数为2的元素一定是ⅡA族元素。
2。主族元素的最外层电子数一定等于其最高正价数。
3。第3周期的元素其核外电子层数一定为3层,其原子半径一定比第2 周期的原子半径大。
4。阴离子的电子层数一定与其原子的电子层数相同,且半径比其原子半径大。
5。主族元素的阳离子的电子层数一定其原子的电子层少一层,且半径比其原子半径小。
6。核外电子排布相同的阴、阳离子,其中阳离子一定是金属元素,阴离子属于非金属元素,且两种元素一定不在同一周期,阳离子的核电荷数多于阴离子,半径小于阴离子。
×√××√√原子序数、半径大小与相对位置1。X、Y、Z为原子序数依次减小的三种元素.X与Y电子层数相同;Y和Z的最外层电子数相同.这三种元素原子的最外层电子数之和为19,原子序数之和为41,则:X是______,Y是______,Z是______.XYZ则Z、Y原子的最外层电子数为6,X的最外层电子数为7,
三原子的内层电子数之和为为22,即2、10、10,Z为O,Y为S,X为Cl习题中,Y与X,Y与Z不一定紧相邻;根据数据推断而得。
18
8
28
18
18
8
28
18
32
18
8
2短
周
期长
周
期元素周期表的位置与原子核外电子排布原子核外电子排布:周期表位置第3周期
第ⅤA族横行:最外电子层数同列:最外层电子数交流与讨论 阅读研究图1-5 周期依据: 原子核外电子层数 共有 个周期,7 各周期上的元素种数
第1周期有 种;
第2周期有 种;
第3周期有 种;
第4周期有 种;
第5周期有 种;
第6周期有 种;
第7周期有 种; 28 8 18 18 32 26 短周期 长周期 (不完全周期)横行与周期 阅读研究图1-5 同列依据: 原子最外层电子数 共有 个族, 16 表示主族, 表示副族ABAABBⅧ0同列与同族交流与讨论 共有 个列, 18同一族一定是同一列吗?同一列一定是同一族吗?元素周期表的结构B、Ⅷ族都只有长周期元素短周期元素只出现在A族元素中1.下表中的粗线是元素周期表部分边界,请ⅠA、ⅡA、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、ⅠB、ⅡB、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、ⅧB、0填入下表适当的空格中,并用粗线补元素周期表边界,将1~36个数字填入恰当的空格中,画出金属元素与非金属元素的分界线 2. (1)同一周期的X、Y两种元素,X位于ⅡA族、Y为ⅣA族,它们的原子序数分别是a和b,已知a和b的关系有:b=a+2,那么a和b还可能有什么关系?
b=a+12b=a+26指出下列元素在周期表中的位置1.根据元素序号判断元素所处周期表位置。
7N第 同期 族,16S第 同期 族;
35Br第 同期 族,26Fe第 同期 族;
2.根据元素周期表位置,判断元素名称和符号:
第 2同期 ⅣA 族的是 。第 3同期 ⅢA 族的是 。
第 4同期 ⅥA 族的是 .
第 4同期 ⅢB 族的是 .
3.与氩原子电子层结构相同的阳离子是: 。
4.与氩原子电子层结构相同的阴离子是: 。
2ⅤA3ⅥA4ⅦA4Ⅷ碳C铝Al硒Se钪ScK+/Ca2+S2-/Cl-小结主族元素:+19281原子核外电子排布:周期表位置第4周期
第ⅠA族位置与结构8第4周期
第ⅣA族+3228418试一试1、如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的7/10,则下列说法中不正确的是
A.原子半径由大到小排列顺序Z>Y>X
B.Y元素的两种同素异形体在常温下都是气体
C.最高价氧化物对应水化物的酸性W>Z
D.阴离子半径由大到小排列顺序Z>W>X>YS ClN O试一试2。如右图所示,若A、B、C为短周期元素,则A、B、C三种元素分别是
、 、 。3。如若右图所示,A、B、C为短周期元素,则A、B、C三种元素分别是 、 、 。ABCHBeMgHeFS试一试4。如右图所示,若A、B、C为短周期元素,且核电荷数之和为32,则A、B、C三种元素分别是
、 、 。SNF1。已知:A、B同周期,A为ⅡA族元素,B为ⅣA族元素,若A的核电荷数为a,则B的核电荷数可能是 。
2。已知X、Y同主族,Y是第三周期元素,X是第二周期元素,若Y的核电荷数为b,则X的核电荷数可能是 。问题解决判断正误1.最外层电子数为2的元素一定是ⅡA族元素。
2。主族元素的最外层电子数一定等于其最高正价数。
3。第3周期的元素其核外电子层数一定为3层,其原子半径一定比第2 周期的原子半径大。
4。阴离子的电子层数一定与其原子的电子层数相同,且半径比其原子半径大。
5。主族元素的阳离子的电子层数一定其原子的电子层少一层,且半径比其原子半径小。
6。核外电子排布相同的阴、阳离子,其中阳离子一定是金属元素,阴离子属于非金属元素,且两种元素一定不在同一周期,阳离子的核电荷数多于阴离子,半径小于阴离子。
×√××√√原子序数、半径大小与相对位置1。X、Y、Z为原子序数依次减小的三种元素.X与Y电子层数相同;Y和Z的最外层电子数相同.这三种元素原子的最外层电子数之和为19,原子序数之和为41,则:X是______,Y是______,Z是______.XYZ则Z、Y原子的最外层电子数为6,X的最外层电子数为7,
三原子的内层电子数之和为为22,即2、10、10,Z为O,Y为S,X为Cl习题中,Y与X,Y与Z不一定紧相邻;根据数据推断而得。
