人教版九上化学课时导学案 第三章 课题3 元素(第二课时)(含答案)
文档属性
| 名称 | 人教版九上化学课时导学案 第三章 课题3 元素(第二课时)(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-07-26 00:00:00 | ||
图片预览




文档简介
21世纪教育网 –中小学教育资源及组卷应用平台
课题3 元素(第二课时)
课时目标
1.了解元素周期表,初步学会从元素周期表中了解元素的基本信息
2.认识元素周期表的一些基本规律,了解原子结构与元素周期表的关系
课堂导学
知识点三 元素周期表简介
1.元素周期表及其结构
(1)周期表中的元素信息
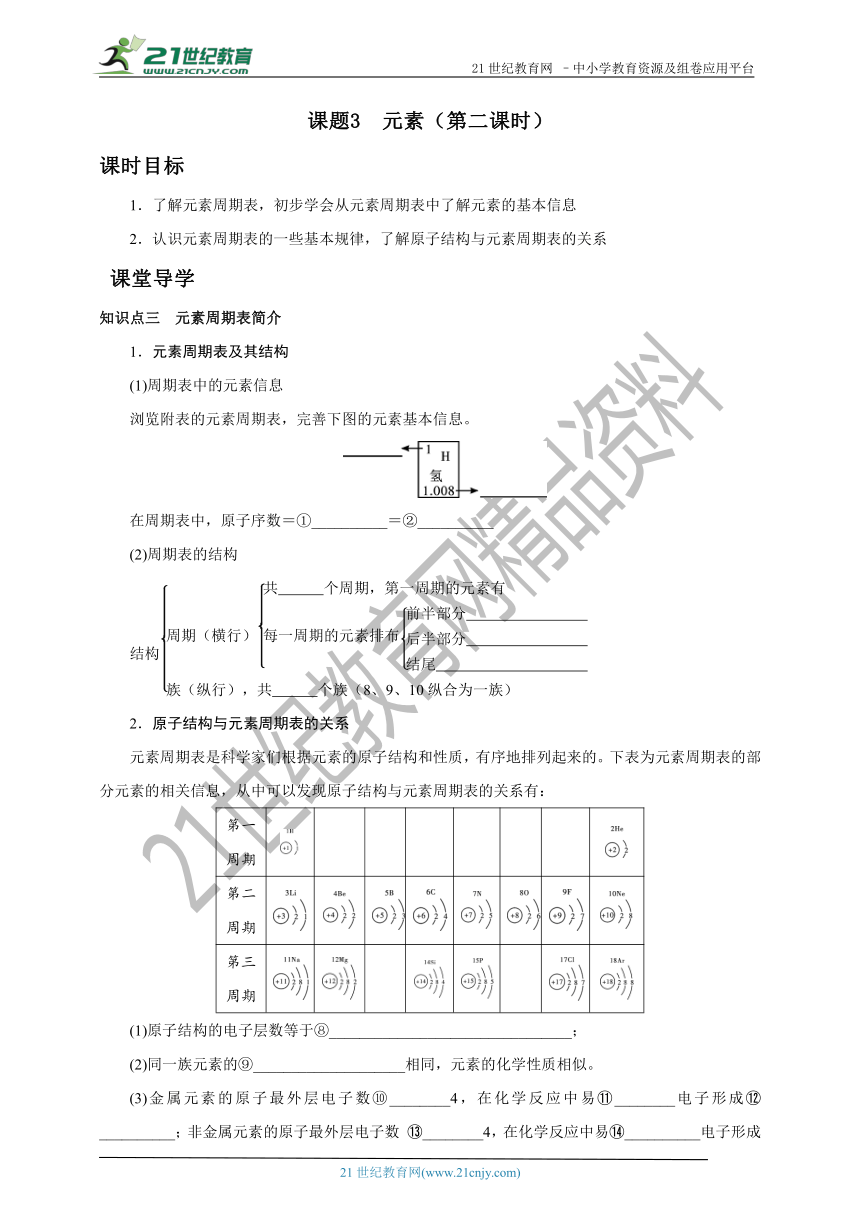
浏览附表的元素周期表,完善下图的元素基本信息。
在周期表中,原子序数=①__________=②__________
(2)周期表的结构
结构
2.原子结构与元素周期表的关系
元素周期表是科学家们根据元素的原子结构和性质,有序地排列起来的。下表为元素周期表的部分元素的相关信息,从中可以发现原子结构与元素周期表的关系有:
第一周期
第二周期
第三周期
(1)原子结构的电子层数等于⑧________________________________;
(2)同一族元素的⑨____________________相同,元素的化学性质相似。
(3)金属元素的原子最外层电子数⑩________4,在化学反应中易 ________电子形成 __________;非金属元素的原子最外层电子数 ________4,在化学反应中易 __________电子形成 ________。
典例解析
例1 元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
族周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 3 Li锂6.941 4 Be铍9.012 5 B硼10.81 6 C碳12.01 7 N氮14.01 8 O氧16.00 9 F氟19.00 10 Ne 氖20.18
3 11 Na钠22.99 12 Mg镁24.31 13 Al铝26.98 14 Si硅28.09 15 P磷30.97 16 S硫32.06 17 Cl氯35.45 18 Ar氩39.95
(1)请从上表中查出关于硼元素的一条信息:__________________。
(2)第3周期(横行)中属于金属元素的是______(填一种),其阳离子是______。
(3)画出硫元素的原子结构示意图:__________________,它位于第____周期,______族。硫元素在化学反应中易__________电子(填“得到”或“失去”)。
(4)第11号元素与第17号元素组成的物质是 ________________(写名称),构成该物质的微粒是__________(选填“分子”、“原子”或“离子”)。
(5)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是__________(填标号)。
a.C和Ne b.Be和Mg c.Al和Si d.F和Cl
(6)根据图示信息,确定1个CO分子中含有的电子总数为__________。
(7)图中元素,从左至右的排列所遵循的一条规律是______________________________。(写一条)
解析:(1)从元素周期表中可以看到原子的核电荷数,质子数,相对原子质量,算出中子数等等。(2)第三周期的金属有钠Na,镁Mg,铝Al,他们的阳离子分别是Na+,Mg2+,Al3+ 。(3)硫是13号元素,原子结构示意图为:,位于第三周期,第ⅥA族,最外层有6个电子,在反应中容易得到电子;(4)第11号元素是Na,其原子最外层电子数是1个,17号元素是氯元素,最外层电子是7个。要形成8电子稳定结构,钠原子失去一个电子,氯原子得到一个电子,形成氯化钠离子化合物。(5)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。所以在给出选项中寻找属于表格中同一竖行的就可以了。(6)1个CO分子是由2个碳原子和1个氧原子构成的,1个碳原子中有6个电子,1个氧原子中有8个电子,故1个CO分子中含有14个电子。(7)从左至右的元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。
答案:(1)硼元素的质子数为5(其他合理答案均可) (2)Na(或Mg、Al) Na+(或Mg2+、Al3+) (3) 3 ⅥA 得到 (4)氯化钠 离子 (5)bd (6)14 (7)质子数依次增加(或元素排列从金属元素到非金属元素,再到稀有气体元素)
变式训练
1. 最近科学家用钙原子轰击铕原子,合成117号元素(部分信息如图所示)。下列说法错误的是( )
A.该元素的相对原子质量为294g B.该元素的原子序数为117
C.该元素的核外电子数为117 D.钙和铕都属于金属元素
根据右图的信息判断,下列说法正确的是( )
A.硫属于金属元素
B.硫原子的核电荷数为16
C.硫原子的相对原子质量为32.07g
D.在化学反应中,硫原子容易失去电子
3.右图为元素周期表的一部分,X,Y,Z代表三种不同元素,以下判断正确的是( )
A.原子序数:ZB.核外电子数:X=Y
C.Y和Z处于同一周期
D.X,Y,Z三种元素属于金属元素
课堂小结
一、元素周期表
1.元素周期表及其结构
(1)元素周期表的元素信息 (2)元素周期表的结构
2.原子结构与元素周期表的关系
(1)原子结构的________=__________;
(2)同一族元素,________________________________________相同。
课时达标
1.人体中必需的微量元素铁、氟、锌、硒(Se)、碘等,虽然含量少,但对健康至关重要。下面提供几种微量元素的相关信息,请认真分析并回答下列问题:
(1)上述微量元素中属于非金属元素的有__________种。
(2)铁原子核外电子数为________,相对原子质量为__________。
(3)硒原子在化学反应中容易得到______个电子,形成______(选填“阴”或“阳”)离子,其离子符号为__________。
2.下表是元素周期表的一部分:
族周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 3 Li锂6.941 4 Be铍9.012 5 B硼10.81 6 C碳12.01 7 N氮14.01 8 O氧16.00 9 F氟19.00 10 Ne 氖20.18
3 11 Na钠22.99 12 Mg镁24.31 13 Al铝26.98 14 Si硅28.09 15 P磷30.97 16 S硫32.06 17 Cl氯35.45 18 Ar氩39.95
(1)发现元素周期律和元素周期表的科学家是__________________。
(2)12号元素的元素符号为________;氧元素的相对原子质量是________;14号元素属于____________元素(填“金属”或“非金属”);Ne元素的化学性质________________(填“稳定”或“不稳定”)。
(3)H和He属于不同种元素的本质区别是__________。
A.中子数不同 B.电子数不同
C.质子数不同 D.相对原子质量不同
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期,科学家相继合成了很多新的元素,他们合成了第118号元素,该元素的核电荷数为________。
课后作业
A 双基过关
右图是元素周期表中的一部分,下列有关说法中正确的是( )。
A. 锂原子的原子序数为3
B. 氢元素的相对原子质量1.008g
C. 锂元素和氢元素都属于金属元素
D. 锂元素和氢元素属于同周期元素
根据如图提供的信息,下列说法正确的是( )。
A. 钠原子最外层有11个电子
B. 钠原子在化学反应中易得到电子
C. 钠元素位于元素周期表的第3周期
D. 钠离子核外有3个电子层
3. 根据下图有关信息判断,下列说法错误的是( )。
A. 镁离子(Mg2+)核内有12个质子
B. 镁离子与硫离子的核外电子层数相等
C. 在化学反应中,硫原子容易得到2个电子
D. 镁离子与硫离子的最外层电子数相等
右图是金元素在元素周期表中的信息示意图。从图中获取的信息正确的是( )。
A. 金元素属于非金属元素
B. 一个金原子的中子数为197
C. 一个金原子的核外电子数为118
D. 一个金原子中粒子总数为276
回答下列问题:
(1)请用化学用语表示:3个钾原子_____,2个氮分子_____。
(2)右图是铝的结构示意图和在周期表中的位置图,则铝原子的核电荷数是_______,铝原子在化学反应中易______电子,形成_______(选填“阴”或“阳”)离子,其离子符号为__________。铝元素位于元素周期表的第_________周期,相对原子质量为____________。
6. 下表为元素周期表的部分元素的相关信息,利用下表回答相关问题。
(1)请画出16号元素原子结构示意图_______________,化学反应中该原子比较容易___________(选填“得到”或“失去”)电子变成离子。
(2)表示的是_______(填离子符号)。
(3)第三周期属于金属元素的有__________________(填元素符号)。
(4)上表中第二、三周期元素最外层电子数的变化规律是___________________________________________________。
(5)根据上表内容可得知原子结构与元素周期表的关系有哪些?(仅写一点)________________________________________________________________。
B能力提高
7. 将H、Li、Na、Mg、Al排成图示形式,根据各行的原子结构可以得出如下规律:
(1)纵行中,三种元素的原子在结构上的相同点是:______________________________________________,不同点是_________________________________。
(2)横行中,三种元素的原子在结构上的相同点是:__________________________________________________________________,不同点是______________________________________________________。
参考答案
课堂导练
① 原子序数 ② 相对原子质量 ③ 7 ④ 金属元素 ⑤ 非金属元素 ⑥ 稀有气体元素 ⑦16 ⑧ 周期数 ⑨ 最外层电子数 ⑩ < 失去 阳离子 > 得到 阴离子
变式训练
1.A 2.B 3.C
课堂小结
(1)核电荷数 原子序数 (2)最外层电子数
课时达标
1.(1)三 (2)26、55.8 (3)二、阴、Se2- 2.(1)门捷列夫 (2)Mg、16.00、非金属、稳定 (3)C (4)118
课后作业
A 双基过关
1. A 2. C 3. B 4. D
5. (1)3K,2N2
(2)13 失去 阳 Al3+ 三 26.98
6. (1) 得到
(2)Al3+(3)Na、Mg、Al
(4)最外层电子数从1个递增到8个
(5)电子层数等于周期数
B 能力提高
7. (1)最外层电子数都等于1 核外电子层数不同
(2)电子层数相等 最外层电子数不同
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
课题3 元素(第二课时)
课时目标
1.了解元素周期表,初步学会从元素周期表中了解元素的基本信息
2.认识元素周期表的一些基本规律,了解原子结构与元素周期表的关系
课堂导学
知识点三 元素周期表简介
1.元素周期表及其结构
(1)周期表中的元素信息
浏览附表的元素周期表,完善下图的元素基本信息。
在周期表中,原子序数=①__________=②__________
(2)周期表的结构
结构
2.原子结构与元素周期表的关系
元素周期表是科学家们根据元素的原子结构和性质,有序地排列起来的。下表为元素周期表的部分元素的相关信息,从中可以发现原子结构与元素周期表的关系有:
第一周期
第二周期
第三周期
(1)原子结构的电子层数等于⑧________________________________;
(2)同一族元素的⑨____________________相同,元素的化学性质相似。
(3)金属元素的原子最外层电子数⑩________4,在化学反应中易 ________电子形成 __________;非金属元素的原子最外层电子数 ________4,在化学反应中易 __________电子形成 ________。
典例解析
例1 元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
族周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 3 Li锂6.941 4 Be铍9.012 5 B硼10.81 6 C碳12.01 7 N氮14.01 8 O氧16.00 9 F氟19.00 10 Ne 氖20.18
3 11 Na钠22.99 12 Mg镁24.31 13 Al铝26.98 14 Si硅28.09 15 P磷30.97 16 S硫32.06 17 Cl氯35.45 18 Ar氩39.95
(1)请从上表中查出关于硼元素的一条信息:__________________。
(2)第3周期(横行)中属于金属元素的是______(填一种),其阳离子是______。
(3)画出硫元素的原子结构示意图:__________________,它位于第____周期,______族。硫元素在化学反应中易__________电子(填“得到”或“失去”)。
(4)第11号元素与第17号元素组成的物质是 ________________(写名称),构成该物质的微粒是__________(选填“分子”、“原子”或“离子”)。
(5)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是__________(填标号)。
a.C和Ne b.Be和Mg c.Al和Si d.F和Cl
(6)根据图示信息,确定1个CO分子中含有的电子总数为__________。
(7)图中元素,从左至右的排列所遵循的一条规律是______________________________。(写一条)
解析:(1)从元素周期表中可以看到原子的核电荷数,质子数,相对原子质量,算出中子数等等。(2)第三周期的金属有钠Na,镁Mg,铝Al,他们的阳离子分别是Na+,Mg2+,Al3+ 。(3)硫是13号元素,原子结构示意图为:,位于第三周期,第ⅥA族,最外层有6个电子,在反应中容易得到电子;(4)第11号元素是Na,其原子最外层电子数是1个,17号元素是氯元素,最外层电子是7个。要形成8电子稳定结构,钠原子失去一个电子,氯原子得到一个电子,形成氯化钠离子化合物。(5)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。所以在给出选项中寻找属于表格中同一竖行的就可以了。(6)1个CO分子是由2个碳原子和1个氧原子构成的,1个碳原子中有6个电子,1个氧原子中有8个电子,故1个CO分子中含有14个电子。(7)从左至右的元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。
答案:(1)硼元素的质子数为5(其他合理答案均可) (2)Na(或Mg、Al) Na+(或Mg2+、Al3+) (3) 3 ⅥA 得到 (4)氯化钠 离子 (5)bd (6)14 (7)质子数依次增加(或元素排列从金属元素到非金属元素,再到稀有气体元素)
变式训练
1. 最近科学家用钙原子轰击铕原子,合成117号元素(部分信息如图所示)。下列说法错误的是( )
A.该元素的相对原子质量为294g B.该元素的原子序数为117
C.该元素的核外电子数为117 D.钙和铕都属于金属元素
根据右图的信息判断,下列说法正确的是( )
A.硫属于金属元素
B.硫原子的核电荷数为16
C.硫原子的相对原子质量为32.07g
D.在化学反应中,硫原子容易失去电子
3.右图为元素周期表的一部分,X,Y,Z代表三种不同元素,以下判断正确的是( )
A.原子序数:Z
C.Y和Z处于同一周期
D.X,Y,Z三种元素属于金属元素
课堂小结
一、元素周期表
1.元素周期表及其结构
(1)元素周期表的元素信息 (2)元素周期表的结构
2.原子结构与元素周期表的关系
(1)原子结构的________=__________;
(2)同一族元素,________________________________________相同。
课时达标
1.人体中必需的微量元素铁、氟、锌、硒(Se)、碘等,虽然含量少,但对健康至关重要。下面提供几种微量元素的相关信息,请认真分析并回答下列问题:
(1)上述微量元素中属于非金属元素的有__________种。
(2)铁原子核外电子数为________,相对原子质量为__________。
(3)硒原子在化学反应中容易得到______个电子,形成______(选填“阴”或“阳”)离子,其离子符号为__________。
2.下表是元素周期表的一部分:
族周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 3 Li锂6.941 4 Be铍9.012 5 B硼10.81 6 C碳12.01 7 N氮14.01 8 O氧16.00 9 F氟19.00 10 Ne 氖20.18
3 11 Na钠22.99 12 Mg镁24.31 13 Al铝26.98 14 Si硅28.09 15 P磷30.97 16 S硫32.06 17 Cl氯35.45 18 Ar氩39.95
(1)发现元素周期律和元素周期表的科学家是__________________。
(2)12号元素的元素符号为________;氧元素的相对原子质量是________;14号元素属于____________元素(填“金属”或“非金属”);Ne元素的化学性质________________(填“稳定”或“不稳定”)。
(3)H和He属于不同种元素的本质区别是__________。
A.中子数不同 B.电子数不同
C.质子数不同 D.相对原子质量不同
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期,科学家相继合成了很多新的元素,他们合成了第118号元素,该元素的核电荷数为________。
课后作业
A 双基过关
右图是元素周期表中的一部分,下列有关说法中正确的是( )。
A. 锂原子的原子序数为3
B. 氢元素的相对原子质量1.008g
C. 锂元素和氢元素都属于金属元素
D. 锂元素和氢元素属于同周期元素
根据如图提供的信息,下列说法正确的是( )。
A. 钠原子最外层有11个电子
B. 钠原子在化学反应中易得到电子
C. 钠元素位于元素周期表的第3周期
D. 钠离子核外有3个电子层
3. 根据下图有关信息判断,下列说法错误的是( )。
A. 镁离子(Mg2+)核内有12个质子
B. 镁离子与硫离子的核外电子层数相等
C. 在化学反应中,硫原子容易得到2个电子
D. 镁离子与硫离子的最外层电子数相等
右图是金元素在元素周期表中的信息示意图。从图中获取的信息正确的是( )。
A. 金元素属于非金属元素
B. 一个金原子的中子数为197
C. 一个金原子的核外电子数为118
D. 一个金原子中粒子总数为276
回答下列问题:
(1)请用化学用语表示:3个钾原子_____,2个氮分子_____。
(2)右图是铝的结构示意图和在周期表中的位置图,则铝原子的核电荷数是_______,铝原子在化学反应中易______电子,形成_______(选填“阴”或“阳”)离子,其离子符号为__________。铝元素位于元素周期表的第_________周期,相对原子质量为____________。
6. 下表为元素周期表的部分元素的相关信息,利用下表回答相关问题。
(1)请画出16号元素原子结构示意图_______________,化学反应中该原子比较容易___________(选填“得到”或“失去”)电子变成离子。
(2)表示的是_______(填离子符号)。
(3)第三周期属于金属元素的有__________________(填元素符号)。
(4)上表中第二、三周期元素最外层电子数的变化规律是___________________________________________________。
(5)根据上表内容可得知原子结构与元素周期表的关系有哪些?(仅写一点)________________________________________________________________。
B能力提高
7. 将H、Li、Na、Mg、Al排成图示形式,根据各行的原子结构可以得出如下规律:
(1)纵行中,三种元素的原子在结构上的相同点是:______________________________________________,不同点是_________________________________。
(2)横行中,三种元素的原子在结构上的相同点是:__________________________________________________________________,不同点是______________________________________________________。
参考答案
课堂导练
① 原子序数 ② 相对原子质量 ③ 7 ④ 金属元素 ⑤ 非金属元素 ⑥ 稀有气体元素 ⑦16 ⑧ 周期数 ⑨ 最外层电子数 ⑩ < 失去 阳离子 > 得到 阴离子
变式训练
1.A 2.B 3.C
课堂小结
(1)核电荷数 原子序数 (2)最外层电子数
课时达标
1.(1)三 (2)26、55.8 (3)二、阴、Se2- 2.(1)门捷列夫 (2)Mg、16.00、非金属、稳定 (3)C (4)118
课后作业
A 双基过关
1. A 2. C 3. B 4. D
5. (1)3K,2N2
(2)13 失去 阳 Al3+ 三 26.98
6. (1) 得到
(2)Al3+(3)Na、Mg、Al
(4)最外层电子数从1个递增到8个
(5)电子层数等于周期数
B 能力提高
7. (1)最外层电子数都等于1 核外电子层数不同
(2)电子层数相等 最外层电子数不同
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
