高一上学期人教版必修一第二章第一节第二课时胶体及其性质(共23张PPT)
文档属性
| 名称 | 高一上学期人教版必修一第二章第一节第二课时胶体及其性质(共23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 999.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-05 00:00:00 | ||
图片预览








文档简介
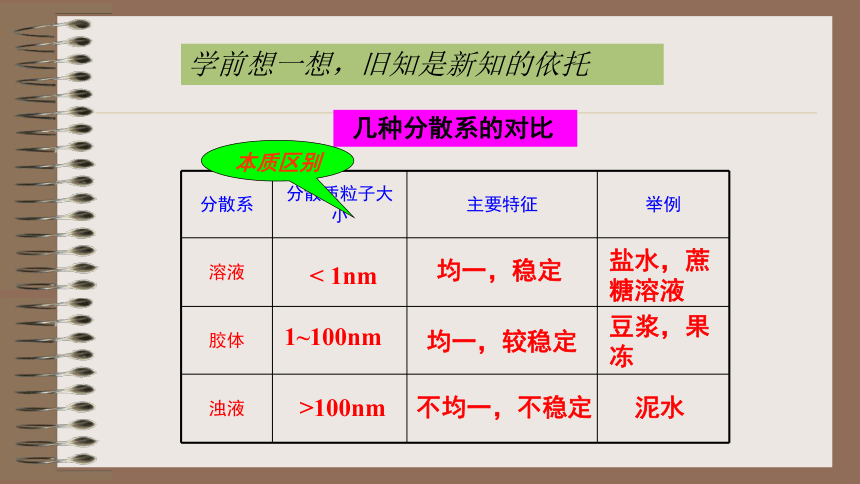
课件23张PPT。第一节 物质的分类第二章 化学物质及其变化第二课时 胶体及其性质 几种分散系的对比本质区别学前想一想,旧知是新知的依托1~100nm< 1nm>100nm均一,稳定均一,较稳定不均一,不稳定盐水,蔗糖溶液豆浆,果冻泥水1.丁达尔效应 利用丁达尔效应是区分胶体与溶液的一种常用物理方法。由于胶体粒子对光线散射形成的光亮的通路丁达尔效应:一、胶体的性质2.布朗运动1827年,英国植物学家布朗把花粉悬浮在水中,用显微镜观察,发现花粉的小颗粒在做不停地、无秩序地运动,这种现象就叫做布朗运动。胶体粒子也做布朗运动。布朗运动的产生,与粒子所处的体系中的分散及分子对粒子无休止的随机撞击有关,并不是粒子本身固有的性质。布朗运动使胶粒难以沉降,这是胶体稳定的一个因素3.电泳在外加电场的作用下胶体微粒在分散剂里做定向移动的现象。 因为胶体的微粒是带电的粒子,所以在电场的作用下发生定向移动,产生了电泳现象。电泳现象:产生电泳现象的原因:正电荷的:金属氢氧化物(Fe(OH)3胶体)、金属氧化物等。
负电荷的:金属硫化物、非金属氧化物、硅酸,土壤。
中性的分子胶体:淀粉、蛋白质(蛋清)等。 (1).为什么胶体微粒带有电荷? 胶体微粒表面积大,吸附力强,吸附阴离子的带上负
电荷,吸附阳离子的带上正电荷。(注:整个胶体呈电中性)(2).哪些胶体带正电荷?哪些带负电荷? (3).胶体处于介稳性的原因次因:布朗运动能克服重力作用,胶粒不易沉积。
主因:同种胶粒带同种电荷,相互排斥而不容易聚集;4.胶体的聚沉 ③加热:消除胶粒所带电荷,并使其凝聚沉降的方法:①加电解质溶液:如卤水点豆腐(卤水主要成分为MgCI2) ②加带相反电荷的胶粒:如煮鸡蛋(蛋清是胶体)如不同品牌墨水混用(带相反电荷)二、胶体的应用?: 1、使用静电除尘器除去空气或工厂废气中的飘尘物;血清电泳用于诊断疾病(电泳)。
2、土壤的保肥作用(土壤是胶体带负电)。
3、明矾的净水作用。(胶体能够使水中的悬浮的固体颗粒 凝聚而沉降下来,具有凝聚作用,因此,氢氧化铁胶体可以用来净水。日常生活中我们常用来净水的是KAl(SO4)2·12H2O(十二水硫酸铝钾),俗称明矾,溶于水可形成Al(OH)3胶体, Al(OH)3具有很好的凝聚作用,是一种良好的净水剂。所有可溶性铝盐都可以作净水剂)
4、江河人海口处形成三角洲(原理是海水中电解 使江河泥沙所形成胶体发生聚沉)。
5、豆腐的制作原理,FeCl3溶液用于伤口止血,不同品牌的墨水不能混用(胶体的聚沉)考点一:溶液、胶体、浊液三种分散系的比较。释疑解难扫除认知障碍探规寻律掌握类题解法知识先导:三种分散系的性质对比 1.溶液、胶体和浊液这三种分散系的根本区别是 ( )
A.是否为大量分子或离子的集合体
B.分散质微粒的大小
C.能否透过滤纸
D.是否均一、稳定、透明
B 练习巩固2. 下列分散系属于胶体的是( )
①肥皂水 ②豆浆 ③食盐水
④蔗糖水 ⑤泥水 ⑥淀粉溶液
A. 只有② B. ①②③
C. ①②⑥ D. ①②③④⑥
C 练习巩固考点二: 胶体的性质及应用
释疑解难扫除认知障碍探规寻律掌握类题解法知识先导:胶体的性质及应用知识先导:胶体的性质及应用1.判断正误(正确的打“√”,错误的打“×”号)。
(1)溶液是纯净物,浊液是混合物 ( )
(2)烟、雾、云都是气溶胶 ( )
(3)溶液和胶体的本质区别是能否产生丁达尔效应 ( )
(4)FeCl3溶液呈电中性,Fe(OH)3胶体带正电 ( )
(5)江河入海口处易形成三角洲,这与胶体的性质有关
( )
针对训练,当堂强化所学×××√√2.我们常用“往伤口上撒盐”来比喻某些人趁人之危的行为,其实从化学的角度说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人.那么,这种做法的化学原理是( ) A.胶体的电泳 B.胶体的聚沉 C.血液中发生复分解反应 D.血液的氧化还原反应 针对训练,当堂强化所学B 针对训练,当堂强化所学3.从下列选项中选择适当的字母填入下列横线上: A.过滤 B.聚沉 C.凝胶 D.布朗运动 E.电泳? F.丁达尔效应 (1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫______; (2)光束通过Fe(OH)3胶体,可看到光亮的通路,这种现象叫______; (3)Fe(OH)3胶体中加入硅酸胶体(胶体粒子带负电),胶体变得浑浊,这是发生了______; (4)鉴别Fe(OH)3胶体和盐酸的方法是______. EFFB再见
负电荷的:金属硫化物、非金属氧化物、硅酸,土壤。
中性的分子胶体:淀粉、蛋白质(蛋清)等。 (1).为什么胶体微粒带有电荷? 胶体微粒表面积大,吸附力强,吸附阴离子的带上负
电荷,吸附阳离子的带上正电荷。(注:整个胶体呈电中性)(2).哪些胶体带正电荷?哪些带负电荷? (3).胶体处于介稳性的原因次因:布朗运动能克服重力作用,胶粒不易沉积。
主因:同种胶粒带同种电荷,相互排斥而不容易聚集;4.胶体的聚沉 ③加热:消除胶粒所带电荷,并使其凝聚沉降的方法:①加电解质溶液:如卤水点豆腐(卤水主要成分为MgCI2) ②加带相反电荷的胶粒:如煮鸡蛋(蛋清是胶体)如不同品牌墨水混用(带相反电荷)二、胶体的应用?: 1、使用静电除尘器除去空气或工厂废气中的飘尘物;血清电泳用于诊断疾病(电泳)。
2、土壤的保肥作用(土壤是胶体带负电)。
3、明矾的净水作用。(胶体能够使水中的悬浮的固体颗粒 凝聚而沉降下来,具有凝聚作用,因此,氢氧化铁胶体可以用来净水。日常生活中我们常用来净水的是KAl(SO4)2·12H2O(十二水硫酸铝钾),俗称明矾,溶于水可形成Al(OH)3胶体, Al(OH)3具有很好的凝聚作用,是一种良好的净水剂。所有可溶性铝盐都可以作净水剂)
4、江河人海口处形成三角洲(原理是海水中电解 使江河泥沙所形成胶体发生聚沉)。
5、豆腐的制作原理,FeCl3溶液用于伤口止血,不同品牌的墨水不能混用(胶体的聚沉)考点一:溶液、胶体、浊液三种分散系的比较。释疑解难扫除认知障碍探规寻律掌握类题解法知识先导:三种分散系的性质对比 1.溶液、胶体和浊液这三种分散系的根本区别是 ( )
A.是否为大量分子或离子的集合体
B.分散质微粒的大小
C.能否透过滤纸
D.是否均一、稳定、透明
B 练习巩固2. 下列分散系属于胶体的是( )
①肥皂水 ②豆浆 ③食盐水
④蔗糖水 ⑤泥水 ⑥淀粉溶液
A. 只有② B. ①②③
C. ①②⑥ D. ①②③④⑥
C 练习巩固考点二: 胶体的性质及应用
释疑解难扫除认知障碍探规寻律掌握类题解法知识先导:胶体的性质及应用知识先导:胶体的性质及应用1.判断正误(正确的打“√”,错误的打“×”号)。
(1)溶液是纯净物,浊液是混合物 ( )
(2)烟、雾、云都是气溶胶 ( )
(3)溶液和胶体的本质区别是能否产生丁达尔效应 ( )
(4)FeCl3溶液呈电中性,Fe(OH)3胶体带正电 ( )
(5)江河入海口处易形成三角洲,这与胶体的性质有关
( )
针对训练,当堂强化所学×××√√2.我们常用“往伤口上撒盐”来比喻某些人趁人之危的行为,其实从化学的角度说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人.那么,这种做法的化学原理是( ) A.胶体的电泳 B.胶体的聚沉 C.血液中发生复分解反应 D.血液的氧化还原反应 针对训练,当堂强化所学B 针对训练,当堂强化所学3.从下列选项中选择适当的字母填入下列横线上: A.过滤 B.聚沉 C.凝胶 D.布朗运动 E.电泳? F.丁达尔效应 (1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫______; (2)光束通过Fe(OH)3胶体,可看到光亮的通路,这种现象叫______; (3)Fe(OH)3胶体中加入硅酸胶体(胶体粒子带负电),胶体变得浑浊,这是发生了______; (4)鉴别Fe(OH)3胶体和盐酸的方法是______. EFFB再见
