兴义四中九年级化学上册同步练习3.2原子的结构
文档属性
| 名称 | 兴义四中九年级化学上册同步练习3.2原子的结构 |  | |
| 格式 | zip | ||
| 文件大小 | 242.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-05 11:05:58 | ||
图片预览



文档简介
一、单项选择题
1.下列关于离子的说法,正确的是(?? )
A.离子都是带电的原子
B.离子是构成物质的最小微粒
C.在化学变化中离子不能再分
D.有些物质直接由离子构成,有些物质却是由原子直接构成的
【答案】D
2.已知1个C-12原子的质量为akg,则实际质量为b kg的另一种原子的相对原子质量为( )
A.12b/a kg B.12b/a C.12a/b D.12a/b kg
【答案】B
3.某原子的结构示意图为 ,有关它的说法正确的是( )
A.最外层电子数是8 B.质子数为12
C.该元素的原子化学性质稳定 D.该元素属于非金属元素
【答案】B
4.在原子里,质子数等于 ( )
A.中子数 B.核外电子总数 C.最外层电子数 D.电子层数
【答案】B
5.下列哪种微粒第三电子层上的电子数最多(?? )
A. B. C. D.
【答案】C
6.知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c对应的是( )
A.原子、原子核、核外电子 B.原子核、原子、核外电子
C.原子、核外电子、原子核 D.核外电子、原子核、原子
【答案】A
7.某元素原子结构示意图为 ,根据元素原子结构示意图,不能直接获得的信息是( )
A.核电荷数 B.原子质量 C.电子层数 D.最外层电子数
【答案】B
8.下列叙述中不正确的是( )
A.钠原子失去电子后变成钠离子 B.氯离子失去电子后变成氯原子
C.原子的质量主要集中在原子核上 D.化学变化中分子不能再分
【答案】D
9.下列各组分子中,核外电子总数相等的一组是(?? )
A.CO和NO B.和 C.和 D.和
【答案】B
10.下列关于相对原子质量的说法不正确的是 (??? )
A.相对原子质量单位为1
B.相对原子质量是一个比值
C.相对原子质量就是原子的实际质量
D.相对原子质量代表各类原子实际质量的相对大小
【答案】C
11.某元素的原子最外层电子数为2,则该元素为(?? )
A.一定是金属元素 B.一定是非金属元素
C.一定是稀的气体元素 D.可能是稀有气体元素
【答案】D
12.碳的原子量是( )
A.12克 B.12
C.1.993×10﹣26千克 D.克
【答案】B
13.美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通讯,其要发射卫星的数目恰好与铱元素(Ir)的原子核外电子数目相等。下列关于铱元素的各种说法中正确的是 ( )
A. 铱原子的质子数为70 B. 铱原子的相对原子量质量为77
C. 铱原子的核电荷数为77 D. 铱元素为非金属元素
【答案】C
14.下列各组数字代表了元素的核电荷数,其中能组成AB2型离子化合物的一组是( )
A.11和7 ??? B.12和17 C.8和12 ? D.11和16
【答案】B
15.用微粒结构示意图表示微粒,通过改变x的值,可表示多少种不同的微粒(?? )
A.4种 B.5种 C.6种 D.8种
【答案】D
二、填空题
16.相对原子质量:国际上以一种碳原子质量的 作为标准,其他原子的质量跟它相比较所得到的 ,就是该原子的相对原子质量.相对原子质量近似等于 和 之和。
【答案】1/12 比 质子数 中子数
17.1996年科学家在宇宙深处发现了离子和分子。请回答:
(1)1个离子中含有____个质子,_ _个电子。
(2)构成H3分子的原子的结构示意图是__________(填序号)。
(3)H3属于_______(填混合物或单质或化合物)
【答案】(1)3 2 (2)C (3)单质
18.在下列示意图表示的粒子中,属于原子的有 (填序号,下同),属于阴离子的有 ,属于阳离子的为 。
【答案】②⑤⑥ ③ ①④
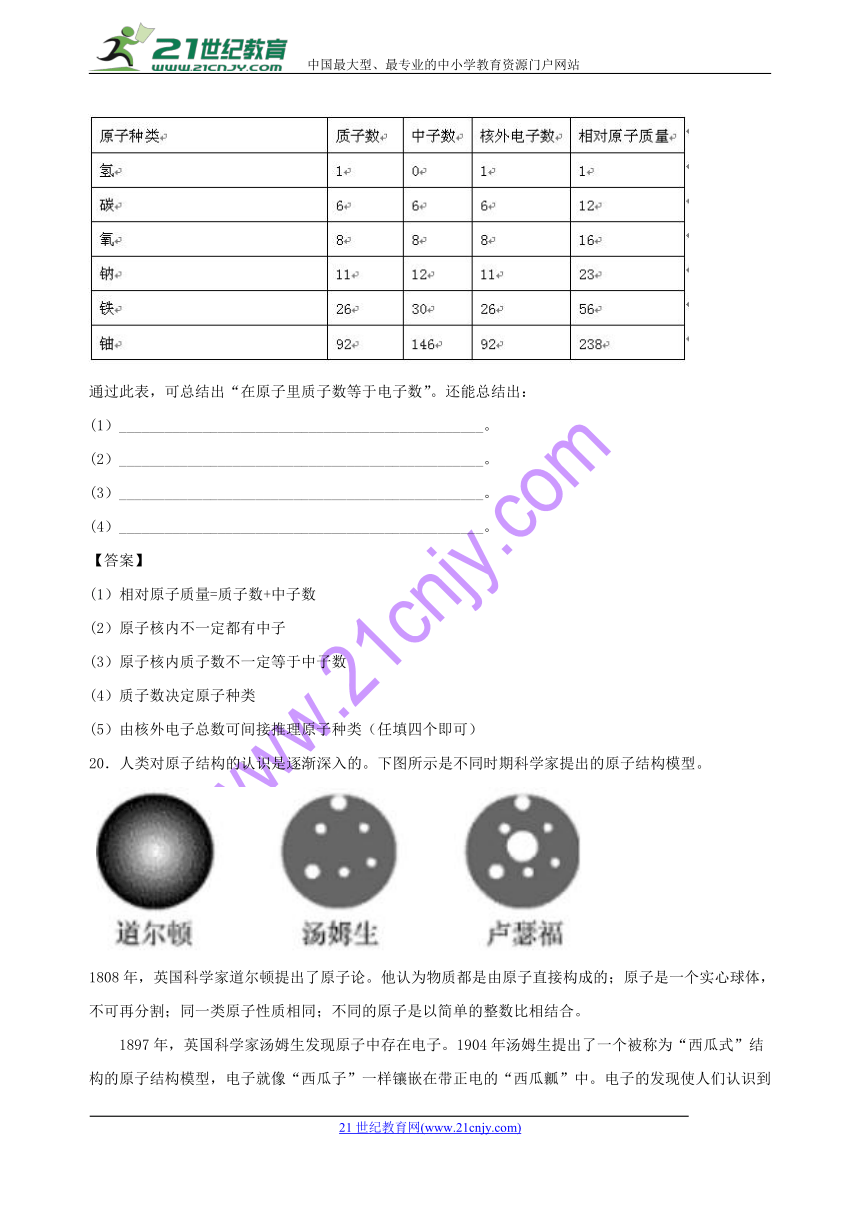
19.已知每个电子的质量约为每个质子(或中子)质量的1/1 836,所以在科学上计算原子的质量时只计算质子和中子的质量,电子质量忽略不计,下表是部分原子的构成指数:
通过此表,可总结出“在原子里质子数等于电子数”。还能总结出:
(1)________________________________________________。
(2)________________________________________________。
(3)________________________________________________。
(4)________________________________________________。
【答案】
(1)相对原子质量=质子数+中子数
(2)原子核内不一定都有中子
(3)原子核内质子数不一定等于中子数
(4)质子数决定原子种类
(5)由核外电子总数可间接推理原子种类(任填四个即可)
20.人类对原子结构的认识是逐渐深入的。下图所示是不同时期科学家提出的原子结构模型。
1808年,英国科学家道尔顿提出了原子论。他认为物质都是由原子直接构成的;原子是一个实心球体,不可再分割;同一类原子性质相同;不同的原子是以简单的整数比相结合。
1897年,英国科学家汤姆生发现原子中存在电子。1904年汤姆生提出了一个被称为“西瓜式”结构的原子结构模型,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中。电子的发现使人们认识到原子是由更小的粒子构成的。
1911年英国科学家卢瑟福做了一个实验:用一束质量比电子大很多的带正电的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,还有极少数的α粒子被反弹了回来。据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成。
……
根据以上材料,请回答:
(1)道尔顿提出了原子论,汤姆生发现了原子中的电子,这在当时是件很了不起的事,但由于受到那时科学技术水平的限制,他们的理论中存在一些缺陷甚至错误,按照目前初中阶段你学的原子结构的理论,你认为道尔顿的原子论存在的缺陷是
;汤姆生原子结构模型的缺陷是
。
(2)根据卢瑟福的实验所产生的现象,不能够获得的结论是 。
A.原子核体积很小 B.原子核质量较大
C.原子核带有正电 D.核外电子带有负电
(3)通过人类认识原子结构的历史,你对科学的发展有哪些感想?
。
【答案】(1)物质都是由原子直接构成的;原子是一个实心球体;不可分割;没有发现带正电荷的原子核 (2)D (3)科学是不断发展的;科学发展的道路是曲折而漫长的;任何一种科学理论都有它的局限性
21.某原子结构示意图和在周期表中的信息如下图。则该元素的质子数为 ,元素的相对原子质量为 ,它在化合物中的化合价为 。
【答案】11 23.0 +1
22.稀有气体元素的原子最外层电子数一般是 个(氦原子是 个),形成相对稳定结构;金属元素的原子最外层电子数一般少于 个,在化学反应中易 ;非金属元素的原子最外层电子数则一般多于 个,在化学反应中易 电子,均趋向于达到相对稳定结构。
【答案】8 2 4 失去电子 4 得到电子
23.有A、B、C、D四种原子,已知它们的核电荷数依次增大且为四个连续的数。B和D的原子核里质子数和中子数相等, A和C的原子核里质子数比中子数少1,已知B原子核外有10个电子。
(1)根据以上事实填写下表:
(2)分析表中的数据,你发现了哪些规律?
①
②
【答案】
(2)①质子数=核电荷数=核外电子数 ②质子数不一定等于中子数
24.已知每个电子的质量约为每个质子(或中子)质量的1/1836。表4-1是关于原子的一些信息。据此表,可总结出“在原子里质子数等于电子数”,你还能总结出哪些信息:
⑴???????????????????????????????????????????????????????????? ;
⑵???????????????????????????????????????????????????????????? ;
⑶?????? ??????????????????????????????????????????????????????;
⑷???????????????????????????????????????????????????????????? 。
【答案】⑴电子的质量很小,原子的质量主要集中在原子核上
⑵原子核内不一定有中子
⑶数值上,原子的相对原子质量等于质子数和中子数之和
⑷中子数不一定等于质子数(其他合理答案均可)
25.铁是由 构成;碳由 构成;水由 构成;二氧化碳分子由 构成;3个氧分子由 构成;氩气由 构成.
【答案】铁原子 碳原子 水分子 碳原子和氧原子 6个氧原子 氩原子
26.1911年,一位科学家用一束平行的高速运动的α粒子(带2个单位正电荷的氦原子核)轰击金箔时,出现了三种实验现象:
(1)有一小部分α粒子改变了原来的运动路径,原因是α粒子途经金原子核附近时,受到了斥力而稍微改变了运动方向;
(2)大多数α粒子不改变原来的运动方向,顺利地穿过了金箔,原因是???????????
????????????????????????????????????????????????????????????????????????? ;
(3)极少数α粒子轰击金箔时被弹了回来,原因是 ?? 。
【答案】⑵原子内存在很大的间隙,a粒子没有受到阻碍顺利穿过
⑶原子内有一个很小的原子核,a粒子正好撞在原子核上被反弹回来
27.氮元素的原子结构示意图为
(1)“+7”表示 及
(2)弧线表示 。
(3)弧线上的数字表示 。
【答案】(1)原子核带正电荷 核电荷数(或质子数) (2)电子层 (3)该电子层上的电子数
28.原子的构成:①原子由居于 和 构成的,原子核由 和 构成的。②在原子中,核电荷数= =
【答案】①原子中心的带正电荷的原子核 核外带负电荷的电子 质子 中子 ②质子数 核外电子数
1.下列关于离子的说法,正确的是(?? )
A.离子都是带电的原子
B.离子是构成物质的最小微粒
C.在化学变化中离子不能再分
D.有些物质直接由离子构成,有些物质却是由原子直接构成的
【答案】D
2.已知1个C-12原子的质量为akg,则实际质量为b kg的另一种原子的相对原子质量为( )
A.12b/a kg B.12b/a C.12a/b D.12a/b kg
【答案】B
3.某原子的结构示意图为 ,有关它的说法正确的是( )
A.最外层电子数是8 B.质子数为12
C.该元素的原子化学性质稳定 D.该元素属于非金属元素
【答案】B
4.在原子里,质子数等于 ( )
A.中子数 B.核外电子总数 C.最外层电子数 D.电子层数
【答案】B
5.下列哪种微粒第三电子层上的电子数最多(?? )
A. B. C. D.
【答案】C
6.知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c对应的是( )
A.原子、原子核、核外电子 B.原子核、原子、核外电子
C.原子、核外电子、原子核 D.核外电子、原子核、原子
【答案】A
7.某元素原子结构示意图为 ,根据元素原子结构示意图,不能直接获得的信息是( )
A.核电荷数 B.原子质量 C.电子层数 D.最外层电子数
【答案】B
8.下列叙述中不正确的是( )
A.钠原子失去电子后变成钠离子 B.氯离子失去电子后变成氯原子
C.原子的质量主要集中在原子核上 D.化学变化中分子不能再分
【答案】D
9.下列各组分子中,核外电子总数相等的一组是(?? )
A.CO和NO B.和 C.和 D.和
【答案】B
10.下列关于相对原子质量的说法不正确的是 (??? )
A.相对原子质量单位为1
B.相对原子质量是一个比值
C.相对原子质量就是原子的实际质量
D.相对原子质量代表各类原子实际质量的相对大小
【答案】C
11.某元素的原子最外层电子数为2,则该元素为(?? )
A.一定是金属元素 B.一定是非金属元素
C.一定是稀的气体元素 D.可能是稀有气体元素
【答案】D
12.碳的原子量是( )
A.12克 B.12
C.1.993×10﹣26千克 D.克
【答案】B
13.美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通讯,其要发射卫星的数目恰好与铱元素(Ir)的原子核外电子数目相等。下列关于铱元素的各种说法中正确的是 ( )
A. 铱原子的质子数为70 B. 铱原子的相对原子量质量为77
C. 铱原子的核电荷数为77 D. 铱元素为非金属元素
【答案】C
14.下列各组数字代表了元素的核电荷数,其中能组成AB2型离子化合物的一组是( )
A.11和7 ??? B.12和17 C.8和12 ? D.11和16
【答案】B
15.用微粒结构示意图表示微粒,通过改变x的值,可表示多少种不同的微粒(?? )
A.4种 B.5种 C.6种 D.8种
【答案】D
二、填空题
16.相对原子质量:国际上以一种碳原子质量的 作为标准,其他原子的质量跟它相比较所得到的 ,就是该原子的相对原子质量.相对原子质量近似等于 和 之和。
【答案】1/12 比 质子数 中子数
17.1996年科学家在宇宙深处发现了离子和分子。请回答:
(1)1个离子中含有____个质子,_ _个电子。
(2)构成H3分子的原子的结构示意图是__________(填序号)。
(3)H3属于_______(填混合物或单质或化合物)
【答案】(1)3 2 (2)C (3)单质
18.在下列示意图表示的粒子中,属于原子的有 (填序号,下同),属于阴离子的有 ,属于阳离子的为 。
【答案】②⑤⑥ ③ ①④
19.已知每个电子的质量约为每个质子(或中子)质量的1/1 836,所以在科学上计算原子的质量时只计算质子和中子的质量,电子质量忽略不计,下表是部分原子的构成指数:
通过此表,可总结出“在原子里质子数等于电子数”。还能总结出:
(1)________________________________________________。
(2)________________________________________________。
(3)________________________________________________。
(4)________________________________________________。
【答案】
(1)相对原子质量=质子数+中子数
(2)原子核内不一定都有中子
(3)原子核内质子数不一定等于中子数
(4)质子数决定原子种类
(5)由核外电子总数可间接推理原子种类(任填四个即可)
20.人类对原子结构的认识是逐渐深入的。下图所示是不同时期科学家提出的原子结构模型。
1808年,英国科学家道尔顿提出了原子论。他认为物质都是由原子直接构成的;原子是一个实心球体,不可再分割;同一类原子性质相同;不同的原子是以简单的整数比相结合。
1897年,英国科学家汤姆生发现原子中存在电子。1904年汤姆生提出了一个被称为“西瓜式”结构的原子结构模型,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中。电子的发现使人们认识到原子是由更小的粒子构成的。
1911年英国科学家卢瑟福做了一个实验:用一束质量比电子大很多的带正电的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,还有极少数的α粒子被反弹了回来。据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成。
……
根据以上材料,请回答:
(1)道尔顿提出了原子论,汤姆生发现了原子中的电子,这在当时是件很了不起的事,但由于受到那时科学技术水平的限制,他们的理论中存在一些缺陷甚至错误,按照目前初中阶段你学的原子结构的理论,你认为道尔顿的原子论存在的缺陷是
;汤姆生原子结构模型的缺陷是
。
(2)根据卢瑟福的实验所产生的现象,不能够获得的结论是 。
A.原子核体积很小 B.原子核质量较大
C.原子核带有正电 D.核外电子带有负电
(3)通过人类认识原子结构的历史,你对科学的发展有哪些感想?
。
【答案】(1)物质都是由原子直接构成的;原子是一个实心球体;不可分割;没有发现带正电荷的原子核 (2)D (3)科学是不断发展的;科学发展的道路是曲折而漫长的;任何一种科学理论都有它的局限性
21.某原子结构示意图和在周期表中的信息如下图。则该元素的质子数为 ,元素的相对原子质量为 ,它在化合物中的化合价为 。
【答案】11 23.0 +1
22.稀有气体元素的原子最外层电子数一般是 个(氦原子是 个),形成相对稳定结构;金属元素的原子最外层电子数一般少于 个,在化学反应中易 ;非金属元素的原子最外层电子数则一般多于 个,在化学反应中易 电子,均趋向于达到相对稳定结构。
【答案】8 2 4 失去电子 4 得到电子
23.有A、B、C、D四种原子,已知它们的核电荷数依次增大且为四个连续的数。B和D的原子核里质子数和中子数相等, A和C的原子核里质子数比中子数少1,已知B原子核外有10个电子。
(1)根据以上事实填写下表:
(2)分析表中的数据,你发现了哪些规律?
①
②
【答案】
(2)①质子数=核电荷数=核外电子数 ②质子数不一定等于中子数
24.已知每个电子的质量约为每个质子(或中子)质量的1/1836。表4-1是关于原子的一些信息。据此表,可总结出“在原子里质子数等于电子数”,你还能总结出哪些信息:
⑴???????????????????????????????????????????????????????????? ;
⑵???????????????????????????????????????????????????????????? ;
⑶?????? ??????????????????????????????????????????????????????;
⑷???????????????????????????????????????????????????????????? 。
【答案】⑴电子的质量很小,原子的质量主要集中在原子核上
⑵原子核内不一定有中子
⑶数值上,原子的相对原子质量等于质子数和中子数之和
⑷中子数不一定等于质子数(其他合理答案均可)
25.铁是由 构成;碳由 构成;水由 构成;二氧化碳分子由 构成;3个氧分子由 构成;氩气由 构成.
【答案】铁原子 碳原子 水分子 碳原子和氧原子 6个氧原子 氩原子
26.1911年,一位科学家用一束平行的高速运动的α粒子(带2个单位正电荷的氦原子核)轰击金箔时,出现了三种实验现象:
(1)有一小部分α粒子改变了原来的运动路径,原因是α粒子途经金原子核附近时,受到了斥力而稍微改变了运动方向;
(2)大多数α粒子不改变原来的运动方向,顺利地穿过了金箔,原因是???????????
????????????????????????????????????????????????????????????????????????? ;
(3)极少数α粒子轰击金箔时被弹了回来,原因是 ?? 。
【答案】⑵原子内存在很大的间隙,a粒子没有受到阻碍顺利穿过
⑶原子内有一个很小的原子核,a粒子正好撞在原子核上被反弹回来
27.氮元素的原子结构示意图为
(1)“+7”表示 及
(2)弧线表示 。
(3)弧线上的数字表示 。
【答案】(1)原子核带正电荷 核电荷数(或质子数) (2)电子层 (3)该电子层上的电子数
28.原子的构成:①原子由居于 和 构成的,原子核由 和 构成的。②在原子中,核电荷数= =
【答案】①原子中心的带正电荷的原子核 核外带负电荷的电子 质子 中子 ②质子数 核外电子数
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
