1.1.1 原子核外电子的排布.pptx
图片预览






文档简介
课件26张PPT。第1课时 原子核外电子的排布专题1 第一单元 原子核外电子排布与元素周期律学习目标定位
1.知道核外电子能量高低与分层排布的关系。
2.能够根据核外电子排布规律写出常见简单原子的原子结构示意图。内容索引新知导学 —— 新知探究 点点落实达标检测 —— 当堂检测 巩固反馈新知导学1.原子的构成
(1)原子是由 和 构成的。
(2)在多电子原子里,电子的能量 。
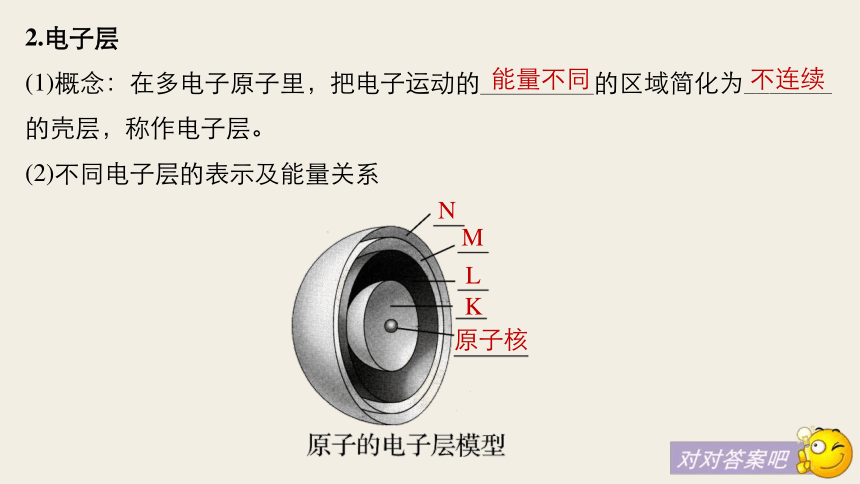
(3)在离核近的区域运动的电子的能量 ,在离核远的区域运动的电子的能量 。原子核核外电子一、原子结构不同较低较高2.电子层
(1)概念:在多电子原子里,把电子运动的 的区域简化为_______
的壳层,称作电子层。
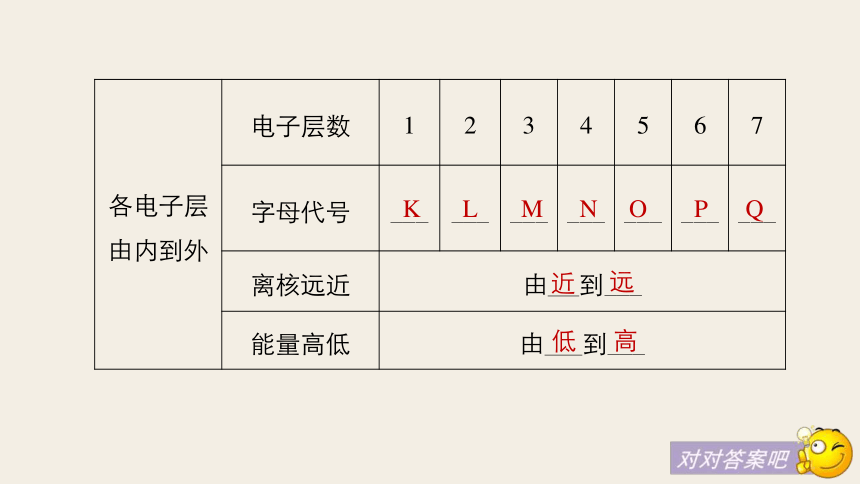
(2)不同电子层的表示及能量关系能量不同不连续NMLK原子核KLMNOPQ近远低高3.电子层的表示方法
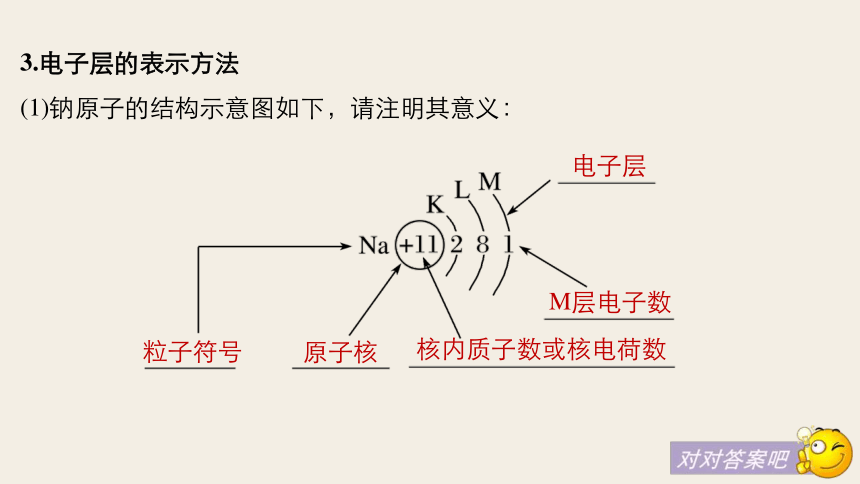
(1)钠原子的结构示意图如下,请注明其意义:电子层粒子符号M层电子数原子核核内质子数或核电荷数(2)原子结构示意图中,核内质子数等于核外电子数,而离子结构示意图中,二者则不相等。如:
Na+ ;Cl- 。
阳离子:核外电子数 核电荷数。
阴离子:核外电子数 核电荷数。小于大于1.下面关于多电子原子的核外电子的运动规律的叙述正确的是
①核外电子是分层运动的 ②所有电子在同一区域里运动 ③能量高的电子在离核近的区域内运动 ④能量低的电子在离核近的区域内运动
A.①④ B.②③ C.①③ D.②④√答案解析解析 原子核外电子是分层运动的,能量越低离核越近,能量越高离核越远。2.排布在下列各电子层上的一个电子,所具有的能量最低的是
A.K层 B.L层
C.M层 D.N层√答案1.完成下列表格:12二、原子核外电子的排布规律628128728828812.观察分析上表,元素原子核外电子排布的规律特点:(1)_________
。(2) 。(3) 。(4) 等。原子核外电子分层排布K层最多容纳电子数为2L层最多排8个电子最外层电子数不超过8个 原子核外电子的排布规律
(1)能量规律:根据电子能量由 到 ,依次在由 向 的电子层上排布。
(2)数量规律:每层最多容纳 个电子,最外层电子数目不超过 个,次外层电子数目不超过18个,倒数第三层电子数目不超过 个。低高内外2n2832特别提醒 核外电子排布的规律是互相联系的,不能孤立地理解。如钙原子由于受最外层电子数不超过8个的限制。其原子结构示意图
为 ,而不是 。3.下列关于原子结构的叙述中正确的是
A.所有的原子核都由质子和中子构成
B.原子的最外层电子数不超过8个
C.稀有气体原子的最外层电子数均为8个
D.原子的次外层电子数都是8个√答案解析解析 A项, 不含有中子;
C项,He最外层电子数为2个;
D项,第2周期元素原子的次外层电子数为2个。4.在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与(n-1)层相同,当它作为原子的次外层时,其电子数比(n+1)层最多能多10个,则此电子层是
A.K层 B.L层 C.M层 D.N层√答案解析解析 n作为最外层时,最多只能容纳8个电子,所以(n-1)层应为8个电子,为L层,则n应为M层;若n为次外层,则(n+1)为最外层,则次外层电子数最多为10+8=18,则进一步证明n为M层。达标检测1.同种元素的原子和离子具有相同的
A.质子数 B.电子数
C.电子层数 D.最外层电子数解析 由原子变成离子时核外电子(特别是最外层电子)发生变化,导致电子数、最外层电子数发生变化,电子层数也可能变化,但原子核中的质子数不变。12345√答案解析解析 电子能量越低,运动区域离核越近,A错;
电子的分层排布即是电子的分层运动,B正确;
稀有气体元素中He原子最外层只有2个电子,C错;
M层为最外层时,最多只能排8个电子,D错。2.下列叙述正确的是
A.电子的能量越低,运动区域离核越远
B.核外电子的分层排布即是核外电子的分层运动
C.稀有气体元素原子的最外层都排有8个电子
D.当M层是最外层时,最多可排布18个电子√12345答案解析3.已知A的原子序数是x,B2-与A3+具有相同的电子层结构,则B元素的原子序数为
A.x+5 B.x-5
C.x+1 D.x-1解析 设B的原子序数为y,则x-3=y+2,y=x-5,B项正确。√12345答案解析4.根据下列叙述,写出元素名称并画出原子结构示意图。12345答案解析硅硼钠氧解析 L层有8个电子,则M层有4个电子,故A为硅12345。当次外层为K层时,B元素原子最外层电子数则为3,是硼;当次外层为L层时,B元素原子最外层电子数为1.5×8=12,违背了排布规律,故不可能。C元素原子的质子数为10+1=11,故为钠。当次外层为K层时,D为氧;当次外层为L层时,最外层则有24个电子,故不可能。5.已知元素X和Y的核电荷数均小于18,最外层电子数分别为n和m-5,次外层分别有(n+2)个和m个电子,据此推断元素X和Y,其名称为X_____,Y____。解析 元素X和Y的核电荷数均小于18,元素X次外层有(n+2)个电子,此层为L层,n+2=8,n=6,元素X为硫;元素Y最外层电子数为m-5,m大于5,而次外层有m个电子,则m等于8,元素Y为铝。12345答案解析硫铝本课结束
1.知道核外电子能量高低与分层排布的关系。
2.能够根据核外电子排布规律写出常见简单原子的原子结构示意图。内容索引新知导学 —— 新知探究 点点落实达标检测 —— 当堂检测 巩固反馈新知导学1.原子的构成
(1)原子是由 和 构成的。
(2)在多电子原子里,电子的能量 。
(3)在离核近的区域运动的电子的能量 ,在离核远的区域运动的电子的能量 。原子核核外电子一、原子结构不同较低较高2.电子层
(1)概念:在多电子原子里,把电子运动的 的区域简化为_______
的壳层,称作电子层。
(2)不同电子层的表示及能量关系能量不同不连续NMLK原子核KLMNOPQ近远低高3.电子层的表示方法
(1)钠原子的结构示意图如下,请注明其意义:电子层粒子符号M层电子数原子核核内质子数或核电荷数(2)原子结构示意图中,核内质子数等于核外电子数,而离子结构示意图中,二者则不相等。如:
Na+ ;Cl- 。
阳离子:核外电子数 核电荷数。
阴离子:核外电子数 核电荷数。小于大于1.下面关于多电子原子的核外电子的运动规律的叙述正确的是
①核外电子是分层运动的 ②所有电子在同一区域里运动 ③能量高的电子在离核近的区域内运动 ④能量低的电子在离核近的区域内运动
A.①④ B.②③ C.①③ D.②④√答案解析解析 原子核外电子是分层运动的,能量越低离核越近,能量越高离核越远。2.排布在下列各电子层上的一个电子,所具有的能量最低的是
A.K层 B.L层
C.M层 D.N层√答案1.完成下列表格:12二、原子核外电子的排布规律628128728828812.观察分析上表,元素原子核外电子排布的规律特点:(1)_________
。(2) 。(3) 。(4) 等。原子核外电子分层排布K层最多容纳电子数为2L层最多排8个电子最外层电子数不超过8个 原子核外电子的排布规律
(1)能量规律:根据电子能量由 到 ,依次在由 向 的电子层上排布。
(2)数量规律:每层最多容纳 个电子,最外层电子数目不超过 个,次外层电子数目不超过18个,倒数第三层电子数目不超过 个。低高内外2n2832特别提醒 核外电子排布的规律是互相联系的,不能孤立地理解。如钙原子由于受最外层电子数不超过8个的限制。其原子结构示意图
为 ,而不是 。3.下列关于原子结构的叙述中正确的是
A.所有的原子核都由质子和中子构成
B.原子的最外层电子数不超过8个
C.稀有气体原子的最外层电子数均为8个
D.原子的次外层电子数都是8个√答案解析解析 A项, 不含有中子;
C项,He最外层电子数为2个;
D项,第2周期元素原子的次外层电子数为2个。4.在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与(n-1)层相同,当它作为原子的次外层时,其电子数比(n+1)层最多能多10个,则此电子层是
A.K层 B.L层 C.M层 D.N层√答案解析解析 n作为最外层时,最多只能容纳8个电子,所以(n-1)层应为8个电子,为L层,则n应为M层;若n为次外层,则(n+1)为最外层,则次外层电子数最多为10+8=18,则进一步证明n为M层。达标检测1.同种元素的原子和离子具有相同的
A.质子数 B.电子数
C.电子层数 D.最外层电子数解析 由原子变成离子时核外电子(特别是最外层电子)发生变化,导致电子数、最外层电子数发生变化,电子层数也可能变化,但原子核中的质子数不变。12345√答案解析解析 电子能量越低,运动区域离核越近,A错;
电子的分层排布即是电子的分层运动,B正确;
稀有气体元素中He原子最外层只有2个电子,C错;
M层为最外层时,最多只能排8个电子,D错。2.下列叙述正确的是
A.电子的能量越低,运动区域离核越远
B.核外电子的分层排布即是核外电子的分层运动
C.稀有气体元素原子的最外层都排有8个电子
D.当M层是最外层时,最多可排布18个电子√12345答案解析3.已知A的原子序数是x,B2-与A3+具有相同的电子层结构,则B元素的原子序数为
A.x+5 B.x-5
C.x+1 D.x-1解析 设B的原子序数为y,则x-3=y+2,y=x-5,B项正确。√12345答案解析4.根据下列叙述,写出元素名称并画出原子结构示意图。12345答案解析硅硼钠氧解析 L层有8个电子,则M层有4个电子,故A为硅12345。当次外层为K层时,B元素原子最外层电子数则为3,是硼;当次外层为L层时,B元素原子最外层电子数为1.5×8=12,违背了排布规律,故不可能。C元素原子的质子数为10+1=11,故为钠。当次外层为K层时,D为氧;当次外层为L层时,最外层则有24个电子,故不可能。5.已知元素X和Y的核电荷数均小于18,最外层电子数分别为n和m-5,次外层分别有(n+2)个和m个电子,据此推断元素X和Y,其名称为X_____,Y____。解析 元素X和Y的核电荷数均小于18,元素X次外层有(n+2)个电子,此层为L层,n+2=8,n=6,元素X为硫;元素Y最外层电子数为m-5,m大于5,而次外层有m个电子,则m等于8,元素Y为铝。12345答案解析硫铝本课结束
