高中化学苏教版必修1课件专题三:第2单元第铁盐、亚铁盐性质和应用 (共33张ppt)
文档属性
| 名称 | 高中化学苏教版必修1课件专题三:第2单元第铁盐、亚铁盐性质和应用 (共33张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-10 00:00:00 | ||
图片预览











文档简介
课件33张PPT。铁盐、亚铁盐性质和应用
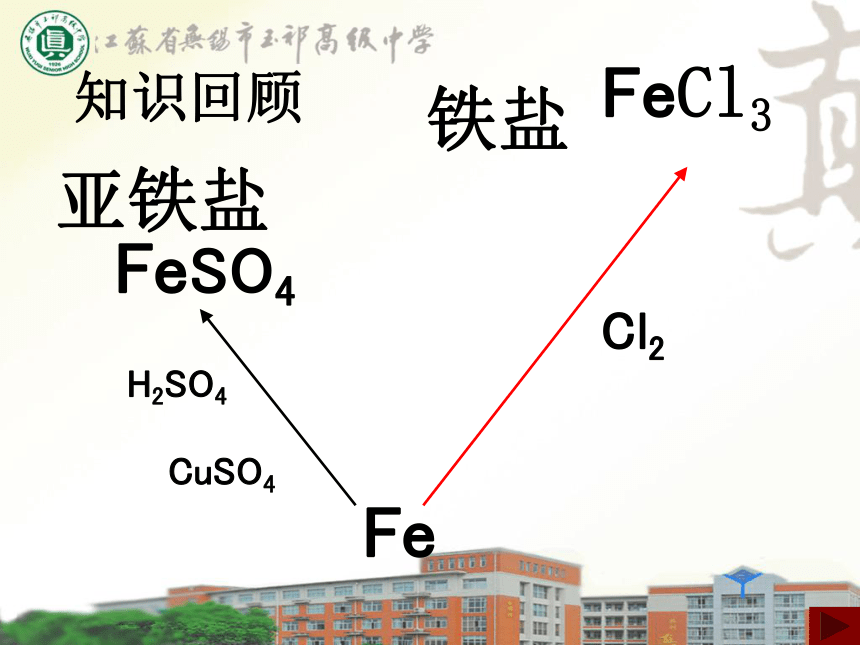
FeFeSO4FeCl3H2SO4CuSO4Cl2亚铁盐铁盐知识回顾
外观一、鉴别铁盐、亚铁盐氯化铁晶体硫酸铁硫酸亚铁晶体(绿矾)硫酸亚铁溶液氯化亚铁铁盐棕黄色
亚铁盐蓝绿色1 观察法 碘水氯化铁溶液
疑似 2试剂法:
(1) NaOH溶液实验1:
向0.1mol.l-1FeCl3溶液和0.1mol.l-1 FeCl2溶液中分别加NaOH溶液(实验视频)
Fe3+ + 3OH-=Fe(OH)3↓ (红褐色)
Fe2+ + 2OH- = Fe(OH)2↓ (白色)
实验2 :向接近无色的FeCl3、FeCl2溶液中滴入NaOH溶液 均无明显现象
(2)KSCN 硫氰化钾实验3
在试管里注入接近无色的FeCl3、FeCl2溶液,再逐滴滴入KSCN溶液。观察发生的现象Fe3+ + 3SCN- = Fe(SCN)3
硫氰化铁血红色Fe2+ 无明显现象Fe2+ 怎么检验?Fe(OH)2露置于空气中久置的FeSO4溶液这种颜色变化与空气中那种气体有关?通过颜色变化,你感觉到亚铁离子转化成了什么离子?Fe2+ 的检验: 亚铁离子先加入硫氰化钾无明显现象,再转化成铁离子,溶液变血红色。
二、 Fe2+、Fe3+ 相互转化探究: Fe2+转化为Fe3+ 的条件1 Fe2+转化为Fe3+FeFe2+Fe3+H+Cu2+Cl2O2 强
氧
化
剂弱
氧
化
剂强氧化剂?实验4 :将加入KSCN 的FeCl2溶液分成两份,分别滴入氯水、过氧化氢溶液能将亚铁离子氧化成铁离子的强氧化剂有: 氧气、氯气、过氧化氢、硝酸、高锰酸钾等。思考:氧化剂和KSCN哪一个先加?现象:溶液均变成血红色Fe2+ Fe3+ + Cl2 + 2Cl-
22=Fe3+ Fe2+还原剂2 Fe3+转化为Fe2+金属单质是非常好的还原剂集成电路板的制作:
人们将一块很大的Cu板上画好电路图,然后用例如蜡之类的东西封好需保留的部份,再放到FeCl3溶液中浸泡,使多余部分溶解掉。
这个工艺很像印刷书本,所以叫印刷电路。你知道吗?实验5 FeCl3 浓溶液刻蚀铜片实验6 向实验3血红色Fe(SCN)3溶液中加入铁粉思考:
FeCl3 与铜、铁反应,试写出化学方程式
Fe+2FeCl3=
Cu+2FeCl3=3FeCl2
2FeCl2+CuCl2
上述离子反应:
Fe+2Fe3+= 3Fe2+
Cu+2Fe3+= 2Fe2+ +Cu2+ 三、铁盐、亚铁盐的用途铁盐部分用途:1 刻蚀五金
2 净化水质 Na2FeO4 Fe3+ +3H2O=Fe(OH)3(胶体)+3H+高铁酸钠亚铁盐主要用途:1、水处理:污水混凝剂以及去除磷酸盐
2、还原剂:去除污水、水泥中的铬酸盐
3、药用 :治疗贫血
不同价态的铁元素之间的相互转化在生产生活中和科学研究中有着广泛的应用。例如: 工业上用FeCl3溶液腐蚀铜板蚀刻电路板后的所得废液中常含有较多Fe2+、Cu2+和少量Fe3+,思考如何用废液来获得纯铜、FeCl3溶液以循环利用? 【学以致用:联系生产】废液FeCl3溶液FeCl2Fe Cu FeCl2【学以致用:联系科研】FeSO4溶液中滴加硫氰化钾(KSCN)溶液,发现出现浅红色,试分析原因。实验室该如何保存FeSO4溶液?【学以致用:联系生活】铁参与叶绿素的形成,缺绿的叶片往往缺铁 铁在生物固氮中起重要作用。【学以致用:联系生活】练一练1、能与Fe3+反应且能证明Fe3+具有氧化性的物质是:
①KSCN②Fe③FeCl2④NaOH( )
A.④ B. ① C. ③ D. ②2、某溶液中加入KSCN溶液无明显现象,再滴加氯水,溶液立即变为红色,说明原溶液中一定含有( )
A.Fe3+ B. Fe2+ C. Cu2+ D. Zn2+
BD若先加入氯水,再加入KSCN溶液,溶液立即变为红色,能否说明原溶液中一定含有Fe2+ ?4如何除去杂质,提纯下列各物质足量铁粉足量Cl2或氯水足量铁粉
FeFeSO4FeCl3H2SO4CuSO4Cl2亚铁盐铁盐知识回顾
外观一、鉴别铁盐、亚铁盐氯化铁晶体硫酸铁硫酸亚铁晶体(绿矾)硫酸亚铁溶液氯化亚铁铁盐棕黄色
亚铁盐蓝绿色1 观察法 碘水氯化铁溶液
疑似 2试剂法:
(1) NaOH溶液实验1:
向0.1mol.l-1FeCl3溶液和0.1mol.l-1 FeCl2溶液中分别加NaOH溶液(实验视频)
Fe3+ + 3OH-=Fe(OH)3↓ (红褐色)
Fe2+ + 2OH- = Fe(OH)2↓ (白色)
实验2 :向接近无色的FeCl3、FeCl2溶液中滴入NaOH溶液 均无明显现象
(2)KSCN 硫氰化钾实验3
在试管里注入接近无色的FeCl3、FeCl2溶液,再逐滴滴入KSCN溶液。观察发生的现象Fe3+ + 3SCN- = Fe(SCN)3
硫氰化铁血红色Fe2+ 无明显现象Fe2+ 怎么检验?Fe(OH)2露置于空气中久置的FeSO4溶液这种颜色变化与空气中那种气体有关?通过颜色变化,你感觉到亚铁离子转化成了什么离子?Fe2+ 的检验: 亚铁离子先加入硫氰化钾无明显现象,再转化成铁离子,溶液变血红色。
二、 Fe2+、Fe3+ 相互转化探究: Fe2+转化为Fe3+ 的条件1 Fe2+转化为Fe3+FeFe2+Fe3+H+Cu2+Cl2O2 强
氧
化
剂弱
氧
化
剂强氧化剂?实验4 :将加入KSCN 的FeCl2溶液分成两份,分别滴入氯水、过氧化氢溶液能将亚铁离子氧化成铁离子的强氧化剂有: 氧气、氯气、过氧化氢、硝酸、高锰酸钾等。思考:氧化剂和KSCN哪一个先加?现象:溶液均变成血红色Fe2+ Fe3+ + Cl2 + 2Cl-
22=Fe3+ Fe2+还原剂2 Fe3+转化为Fe2+金属单质是非常好的还原剂集成电路板的制作:
人们将一块很大的Cu板上画好电路图,然后用例如蜡之类的东西封好需保留的部份,再放到FeCl3溶液中浸泡,使多余部分溶解掉。
这个工艺很像印刷书本,所以叫印刷电路。你知道吗?实验5 FeCl3 浓溶液刻蚀铜片实验6 向实验3血红色Fe(SCN)3溶液中加入铁粉思考:
FeCl3 与铜、铁反应,试写出化学方程式
Fe+2FeCl3=
Cu+2FeCl3=3FeCl2
2FeCl2+CuCl2
上述离子反应:
Fe+2Fe3+= 3Fe2+
Cu+2Fe3+= 2Fe2+ +Cu2+ 三、铁盐、亚铁盐的用途铁盐部分用途:1 刻蚀五金
2 净化水质 Na2FeO4 Fe3+ +3H2O=Fe(OH)3(胶体)+3H+高铁酸钠亚铁盐主要用途:1、水处理:污水混凝剂以及去除磷酸盐
2、还原剂:去除污水、水泥中的铬酸盐
3、药用 :治疗贫血
不同价态的铁元素之间的相互转化在生产生活中和科学研究中有着广泛的应用。例如: 工业上用FeCl3溶液腐蚀铜板蚀刻电路板后的所得废液中常含有较多Fe2+、Cu2+和少量Fe3+,思考如何用废液来获得纯铜、FeCl3溶液以循环利用? 【学以致用:联系生产】废液FeCl3溶液FeCl2Fe Cu FeCl2【学以致用:联系科研】FeSO4溶液中滴加硫氰化钾(KSCN)溶液,发现出现浅红色,试分析原因。实验室该如何保存FeSO4溶液?【学以致用:联系生活】铁参与叶绿素的形成,缺绿的叶片往往缺铁 铁在生物固氮中起重要作用。【学以致用:联系生活】练一练1、能与Fe3+反应且能证明Fe3+具有氧化性的物质是:
①KSCN②Fe③FeCl2④NaOH( )
A.④ B. ① C. ③ D. ②2、某溶液中加入KSCN溶液无明显现象,再滴加氯水,溶液立即变为红色,说明原溶液中一定含有( )
A.Fe3+ B. Fe2+ C. Cu2+ D. Zn2+
BD若先加入氯水,再加入KSCN溶液,溶液立即变为红色,能否说明原溶液中一定含有Fe2+ ?4如何除去杂质,提纯下列各物质足量铁粉足量Cl2或氯水足量铁粉
