高中化学人教版必修一 第一章第二节 化学计量在实验中的应用
文档属性
| 名称 | 高中化学人教版必修一 第一章第二节 化学计量在实验中的应用 |
|
|
| 格式 | zip | ||
| 文件大小 | 662.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-20 00:00:00 | ||
图片预览





文档简介
课件22张PPT。第二节 化学计量在实验中的应用【结论】 (1) 1mol不同的粒子都含有相同数目的粒子数;
(2) 1mol不同粒子或物质的质量一般是不相同的;
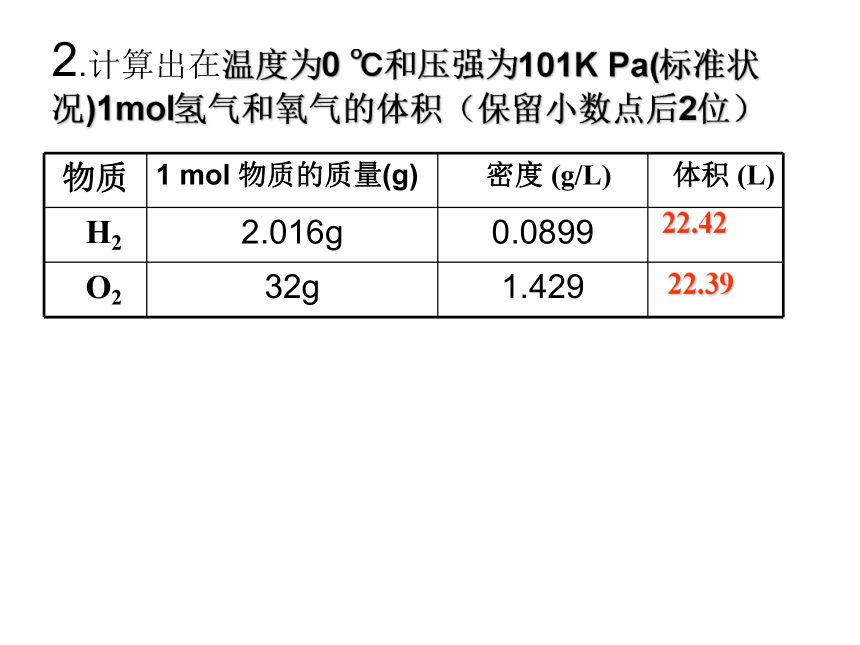
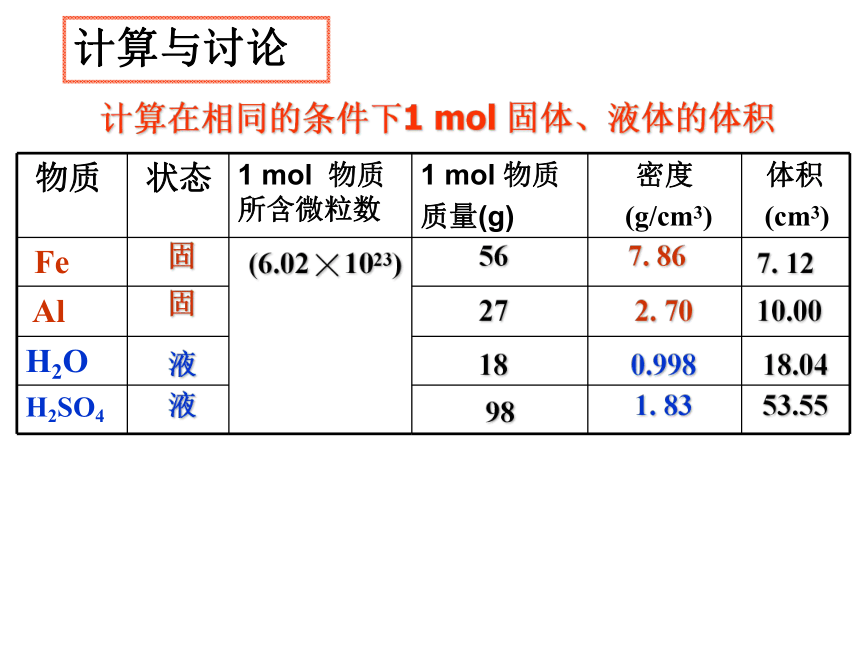
(3)【问题】:那么1mol不同的物质的所占的体积是相同还是不同呢?0.2g1.6g0.1mol0.05mol2︰1361.8g40.2g321.6g(1) H2和O2体积之比?(2)2︰1【科学探究】P13页H2和O2物质的量之比 2︰1 H2和O2体积之比 2︰1 相同温度和压强下,1molH2和 1molO2的体积是 。相等的2.计算出在温度为0 ℃和压强为101K Pa(标准状况)1mol氢气和氧气的体积(保留小数点后2位)22.4222.39计算与讨论计算在相同的条件下1 mol 固体、液体的体积固固液液56 2718987. 862. 701. 837. 1210.0018.0453.55(6.02 ╳ 1023)0.998【结论】 1mol不同的物质的所占的体积1:在相同条件下,1mol不同固体或液体物质的体积是不相同。
2:在相同条件下,1mol 不同气态物质所占的体积是相同的
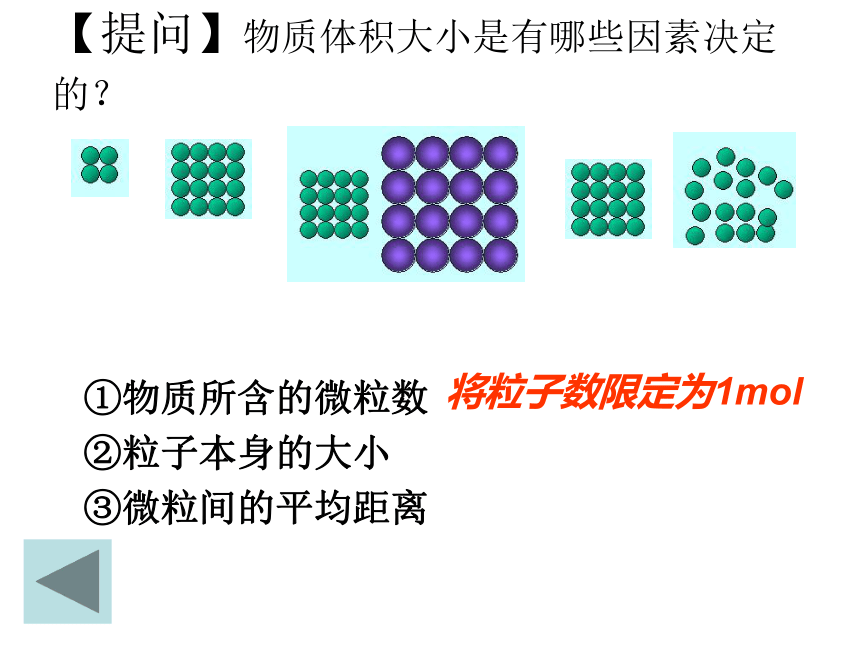
【提问】物质体积大小是有哪些因素决定的?
①物质所含的微粒数
②粒子本身的大小
③微粒间的平均距离
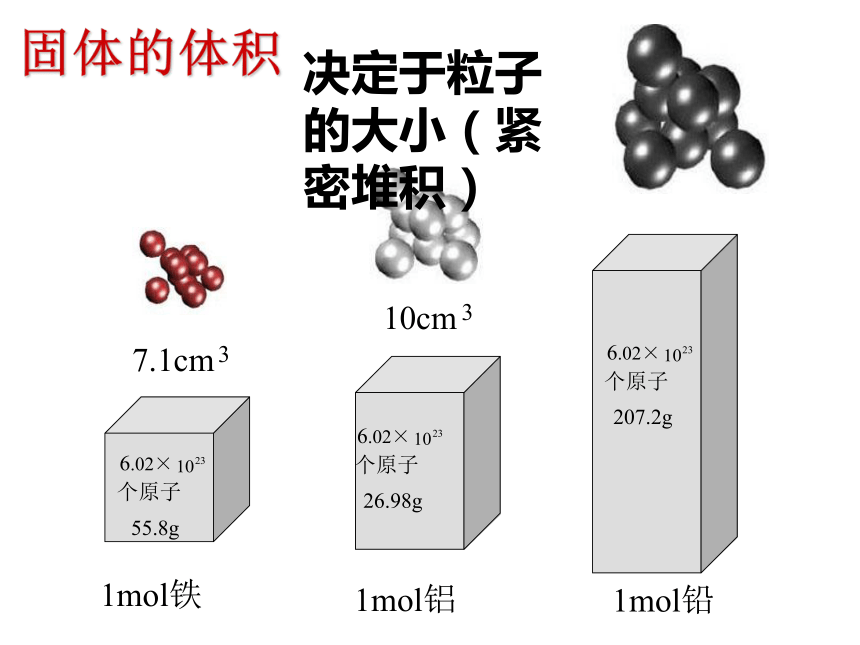
将粒子数限定为1mol固体的体积决定于粒子的大小(紧密堆积)液体体积1mol硫酸决定于粒子的大小(紧密堆积) 【问题1】在相同的条件下,当粒子数相同时,决定固体或液体体积大小的主要因素是什么?【小结】粒子的____,
由于不同粒子的大小一般是不同的,所以在相同的条件下,当粒子数相同时,固体或液体的体积不同。(无规律)
大小决定于粒子间的距离的大小气
体
的
体
积 【问题2】在相同的条件下,当粒子数相同时,决定气体体积大小的主要因素是什么?【小结】主要因素是_____
由于在相同的条件下,粒子间的距离可以看成是是相等的,所以当粒子数相等的时候,气体的体积相同。(有规律)
【思考】粒子间的距离取决于__和__
(1)温度越高,体积越__
(2)压强越大,体积越__
粒子间的距离温度压强大小【结论】若温度和压强相同,任何气体粒子间的距离 ,因此,粒子数相同的任何气体具有的体积 ____ 。相等相等阿伏加德罗定律:相同温度和压强条件下,具有相同的体积的任何气体都含有相同数目的粒子数。0℃,101kPa(标准状况)1 mol二:气体摩尔体积1:概念:
单位物质的量的气体所占有的体积。
2:符号 Vm
3:单位:L/mol
4:在标准状况下,气体摩尔体积约为22.4L/mol
5:影响气体摩尔体积大小的因素:
粒子间的距离(即与 温度和压强有关)【实战演练】辨析下列说法是否正确?① 任何条件下,气体摩尔体积都均为22.4L/mol
【错误】没有指明是标准状况下
②1molCO2所占的体积约为22.4L
【错误】没有指明物质所处于的温度和压强
③标况下,1mol任何物质的体积约是22.4L
【错误】没有指明是气态物质
④在标况下,1mol水的体积约为22.4L
【错误】水在标况下为液态
6、标准状况下气体体积(V)、物质的量(n)、气体摩尔体积(V m)三者间的关系?VV mn=V=n ×V m(例1)0.5 mol H2 在标况下占有的体积约是多少?
(例2)求标况下,6.72 L CO2气体的物质的量约是多少?(例3)求标况下0.2molCO2和0.8molH2 的体积之和为多少?
【试一试】1.下列物质的体积为22.4L的是( )
A.标准状况下1mol H2O
B.17g 氨气
C.标准状况下 44g CO2
D .0℃、200kPa下的 2g 氢气 C【试一试】 2、用13.0gZn与足量的盐酸反应,求可得标准状况下氢气的体积?(Zn-65)÷M质量(m) 物质的量(n) 分子数(N)
M ×
体积(V)
(标况) Vm ÷ 7、物质的质量(m)、物质的量(n)、分子数(N)、标况下气体体积(V) 四者之间的换算关系×NANA ÷×Vm
【实战演练】
1:2molO3与3molO2的质量____(填相等、不相等或无法判定);分子数之比____;含有的氧原子数之比为_____;在标况下气体的体积比为____。
2:下列数量的各物质:(1)0.5molNH3 (2)标准状况下22.4L氦气,(3)4oC时9ml水(4)0.2mol磷酸钠(Na3PO4),所含原子个数由大到小的排列顺序是 _____________________。
相等 2:3 1:1 2:3 (1)>(4)>(3)>(2)
(2) 1mol不同粒子或物质的质量一般是不相同的;
(3)【问题】:那么1mol不同的物质的所占的体积是相同还是不同呢?0.2g1.6g0.1mol0.05mol2︰1361.8g40.2g321.6g(1) H2和O2体积之比?(2)2︰1【科学探究】P13页H2和O2物质的量之比 2︰1 H2和O2体积之比 2︰1 相同温度和压强下,1molH2和 1molO2的体积是 。相等的2.计算出在温度为0 ℃和压强为101K Pa(标准状况)1mol氢气和氧气的体积(保留小数点后2位)22.4222.39计算与讨论计算在相同的条件下1 mol 固体、液体的体积固固液液56 2718987. 862. 701. 837. 1210.0018.0453.55(6.02 ╳ 1023)0.998【结论】 1mol不同的物质的所占的体积1:在相同条件下,1mol不同固体或液体物质的体积是不相同。
2:在相同条件下,1mol 不同气态物质所占的体积是相同的
【提问】物质体积大小是有哪些因素决定的?
①物质所含的微粒数
②粒子本身的大小
③微粒间的平均距离
将粒子数限定为1mol固体的体积决定于粒子的大小(紧密堆积)液体体积1mol硫酸决定于粒子的大小(紧密堆积) 【问题1】在相同的条件下,当粒子数相同时,决定固体或液体体积大小的主要因素是什么?【小结】粒子的____,
由于不同粒子的大小一般是不同的,所以在相同的条件下,当粒子数相同时,固体或液体的体积不同。(无规律)
大小决定于粒子间的距离的大小气
体
的
体
积 【问题2】在相同的条件下,当粒子数相同时,决定气体体积大小的主要因素是什么?【小结】主要因素是_____
由于在相同的条件下,粒子间的距离可以看成是是相等的,所以当粒子数相等的时候,气体的体积相同。(有规律)
【思考】粒子间的距离取决于__和__
(1)温度越高,体积越__
(2)压强越大,体积越__
粒子间的距离温度压强大小【结论】若温度和压强相同,任何气体粒子间的距离 ,因此,粒子数相同的任何气体具有的体积 ____ 。相等相等阿伏加德罗定律:相同温度和压强条件下,具有相同的体积的任何气体都含有相同数目的粒子数。0℃,101kPa(标准状况)1 mol二:气体摩尔体积1:概念:
单位物质的量的气体所占有的体积。
2:符号 Vm
3:单位:L/mol
4:在标准状况下,气体摩尔体积约为22.4L/mol
5:影响气体摩尔体积大小的因素:
粒子间的距离(即与 温度和压强有关)【实战演练】辨析下列说法是否正确?① 任何条件下,气体摩尔体积都均为22.4L/mol
【错误】没有指明是标准状况下
②1molCO2所占的体积约为22.4L
【错误】没有指明物质所处于的温度和压强
③标况下,1mol任何物质的体积约是22.4L
【错误】没有指明是气态物质
④在标况下,1mol水的体积约为22.4L
【错误】水在标况下为液态
6、标准状况下气体体积(V)、物质的量(n)、气体摩尔体积(V m)三者间的关系?VV mn=V=n ×V m(例1)0.5 mol H2 在标况下占有的体积约是多少?
(例2)求标况下,6.72 L CO2气体的物质的量约是多少?(例3)求标况下0.2molCO2和0.8molH2 的体积之和为多少?
【试一试】1.下列物质的体积为22.4L的是( )
A.标准状况下1mol H2O
B.17g 氨气
C.标准状况下 44g CO2
D .0℃、200kPa下的 2g 氢气 C【试一试】 2、用13.0gZn与足量的盐酸反应,求可得标准状况下氢气的体积?(Zn-65)÷M质量(m) 物质的量(n) 分子数(N)
M ×
体积(V)
(标况) Vm ÷ 7、物质的质量(m)、物质的量(n)、分子数(N)、标况下气体体积(V) 四者之间的换算关系×NANA ÷×Vm
【实战演练】
1:2molO3与3molO2的质量____(填相等、不相等或无法判定);分子数之比____;含有的氧原子数之比为_____;在标况下气体的体积比为____。
2:下列数量的各物质:(1)0.5molNH3 (2)标准状况下22.4L氦气,(3)4oC时9ml水(4)0.2mol磷酸钠(Na3PO4),所含原子个数由大到小的排列顺序是 _____________________。
相等 2:3 1:1 2:3 (1)>(4)>(3)>(2)
