浙教版九年级科学上册 2.5 物质的转化 同步练习
文档属性
| 名称 | 浙教版九年级科学上册 2.5 物质的转化 同步练习 |

|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2018-08-17 00:00:00 | ||
图片预览


文档简介
21世纪教育网 –中小学教育资源及组卷应用平台
浙教版九年级科学上册 2.5 物质的转化 同步练习
一、单选题
1.如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( )
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
2.下列物质中含少量杂质(括号内为杂质),除去杂质所用试剂均适量,其它操作或反应条件已略去,其中利用甲、乙两试剂都能除去的选项是( )
A.①② B.③④ C.②④ D.①③
3.下图是无色溶液X发生化学反应时的颜色变化,无色溶液X是( )
A.稀盐酸 B.稀硫酸 C.澄清石灰水 D.硫酸钠溶液
4.某班甲、乙两组同学分别做常见酸和碱与指示剂反应的实验,使用的试剂有稀盐酸、稀硫酸、氢氧化钠溶液和酚酞试液。实验后废液分别集中到各组的一个废液缸中。研究小组对两个组的废液进行检测,结果如下表。下列说法正确的是( )
A.甲组废液中一定含有稀盐酸或稀硫酸
B.乙组废液中一定含有氢氧化钠、氯化钠、硫酸钠
C.甲组废液可直接排放,乙组处理后再排放
D.如将两组的废液合并在一起,如溶液呈无色,混合液可直接排放。
5.右图是某同学的学习笔记,其中“→”表示物质之间能转化,“—”表示物质之间能发生化学反应。关于该图,下列说法中不正确的是 ( )
A.反应⑤不一定属于复分解反应
B.该图中的所有反应一定不涉及置换反应
C.反应①是一个放热反应
D.反应②的转化中必须有盐类物质参加
6.甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是( )
A. 若丙、丁为盐和水,则甲、乙一定是酸、碱
B. 若丙为气体,则甲、乙中一定有单质
C. 若丁为水,则该反应一定是复分解反应
D. 若只有甲、丁是单质,则该反应一定是置换反应
7.下列转化不能通过一步反应实现的是( )
①SiO2→Na2SiO3 ②SiO2→H2SiO3 ③CuSO4→Cu(NO3)2 ④CuO→Cu(OH)2 ⑤Fe(OH)2→Fe(OH)3
A.①②③ B.②④ C.③④⑤ D.②③④
8.右图中有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有a、AgNO3溶液 b、MgSO4溶液 c、BaCl2溶液 d、H2SO4溶液 e、Fe f、Cu(NO3)2溶液则图中①表示的物质的编号是( )
A. b B. f C. a D. c
9.下列物质的变化中,只有加酸才能一步实现的是( )
A.CaCO3→CO2 B.Fe2O3→FeCl3 C.Zn→ZnSO4 D. KOH→KCl
10.铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象。下列说法中错误的是( )
A .a处产生白色物质 B.b处生成蓝色沉淀
C .c处发生复分解反应 D .d处产生气泡
二、填空题
11.某不纯的 K2CO3 样品中可能含有的杂质是 Na2CO3、KNO3、CuSO4 和 Ba(NO3)2 几种物质中的一种或几种,进行以下实验:
①取一定量该样品放入烧杯中并加入足量水搅拌后,样品全部溶解且得到无色溶液;
②向无色溶液中加入过量的 CaCl2 溶液充分反应,出现白色沉淀,将白色沉淀经过滤、洗涤、干燥、称量。根据上述实验现象回答:
(1)样品所含杂质肯定没有________;
(2)若所取的样品为 13.8 克,得到白色沉淀 9 克,则样品中杂质的可能组成:________。
12.有A、B、C、D四种物质的稀溶液,它们分别是Na2CO3、BaCl2、AgNO3、HCl中的某一种溶液。如图为常温下上述溶液两两混合的实验现象,其中“↓”表示产生沉淀,“↑”表示产生气体,“─”表示无明显现象,试回答:
(1)试判断A物质是________。
(2)请写出D与C反应的化学方程式_________________________。
13.如图是一些常见物质间互相转化的关系图(部分反应条件已省略)。A、B均为无色气体,X为固体,Y为能使澄清石灰水变浑浊的无色气体,E、F为常见金属,试推断:
(1)乙、戊物质的化学式分别为________。
(2)写出下列转化的化学方程式(丙+X→F+Y):________。
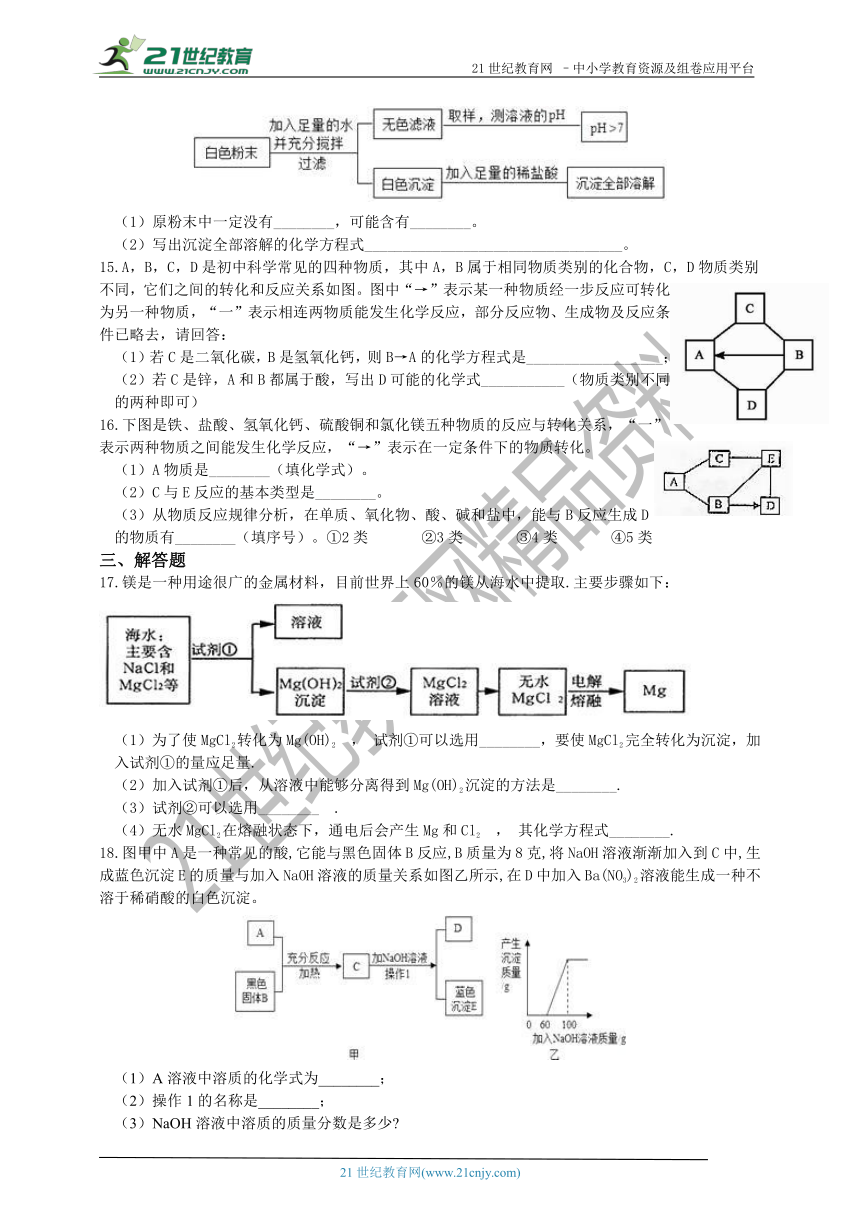
14.已知某固体粉末是KOH、FeCl3、BaCl2、Na2CO3、K2SO4之一或几种,为探究其组成,探究小组同还查阅资料得知KCl、BaCl2溶液呈中性,BaSO4不溶于酸。经思考设计如下实验,请分析实验过程,回答下列问题:
(1)原粉末中一定没有________,可能含有________。
(2)写出沉淀全部溶解的化学方程式__________________________________。
15.A,B,C,D是初中科学常见的四种物质,其中A,B属于相同物质类别的化合物,C,D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“一”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去,请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是__________________;
(2)若C是锌,A和B都属于酸,写出D可能的化学式___________(物质类别不同的两种即可)
16.下图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)A物质是________(填化学式)。
(2)C与E反应的基本类型是________。
(3)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有________(填序号)。①2类 ②3类 ③4类 ④5类
三、解答题
17.镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取.主要步骤如下:
(1)为了使MgCl2转化为Mg(OH)2 , 试剂①可以选用________,要使MgCl2完全转化为沉淀,加入试剂①的量应足量.
(2)加入试剂①后,从溶液中能够分离得到Mg(OH)2沉淀的方法是________.
(3)试剂②可以选用________ .
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2 , 其化学方程式________.
18.图甲中A是一种常见的酸,它能与黑色固体B反应,B质量为8克,将NaOH溶液渐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示,在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)A溶液中溶质的化学式为________;
(2)操作1的名称是________;
(3)NaOH溶液中溶质的质量分数是多少
(4)C溶液中加入NaOH溶液至恰好完全反应时,所得溶液溶质的质量是多少
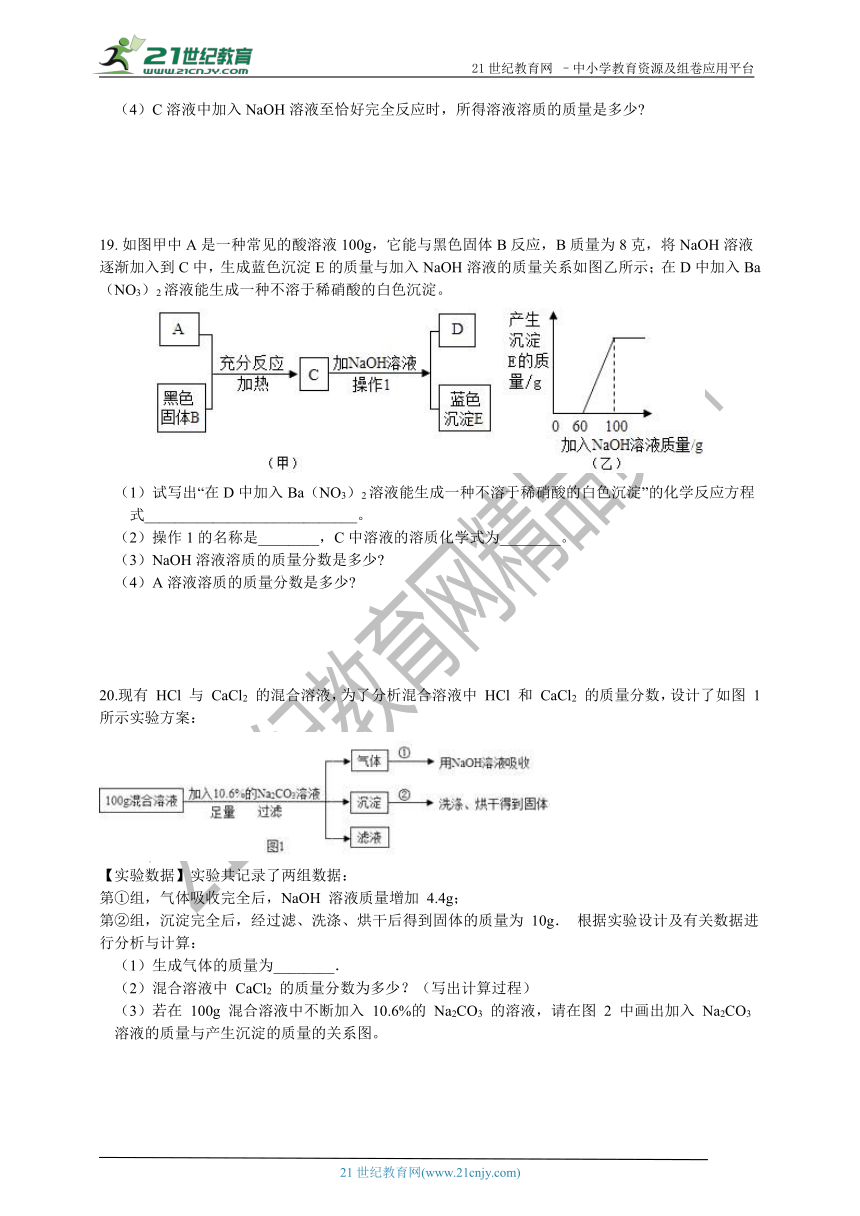
19. 如图甲中A是一种常见的酸溶液100g,它能与黑色固体B反应,B质量为8克,将NaOH溶液逐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示;在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)试写出“在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀”的化学反应方程式____________________________。
(2)操作1的名称是________,C中溶液的溶质化学式为________。
(3)NaOH溶液溶质的质量分数是多少
(4)A溶液溶质的质量分数是多少
20.现有 HCl 与 CaCl2 的混合溶液,为了分析混合溶液中 HCl 和 CaCl2 的质量分数,设计了如图 1 所示实验方案:
【实验数据】实验共记录了两组数据:
第①组,气体吸收完全后,NaOH 溶液质量增加 4.4g;
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为 10g. 根据实验设计及有关数据进行分析与计算:
(1)生成气体的质量为________.
(2)混合溶液中 CaCl2 的质量分数为多少?(写出计算过程)
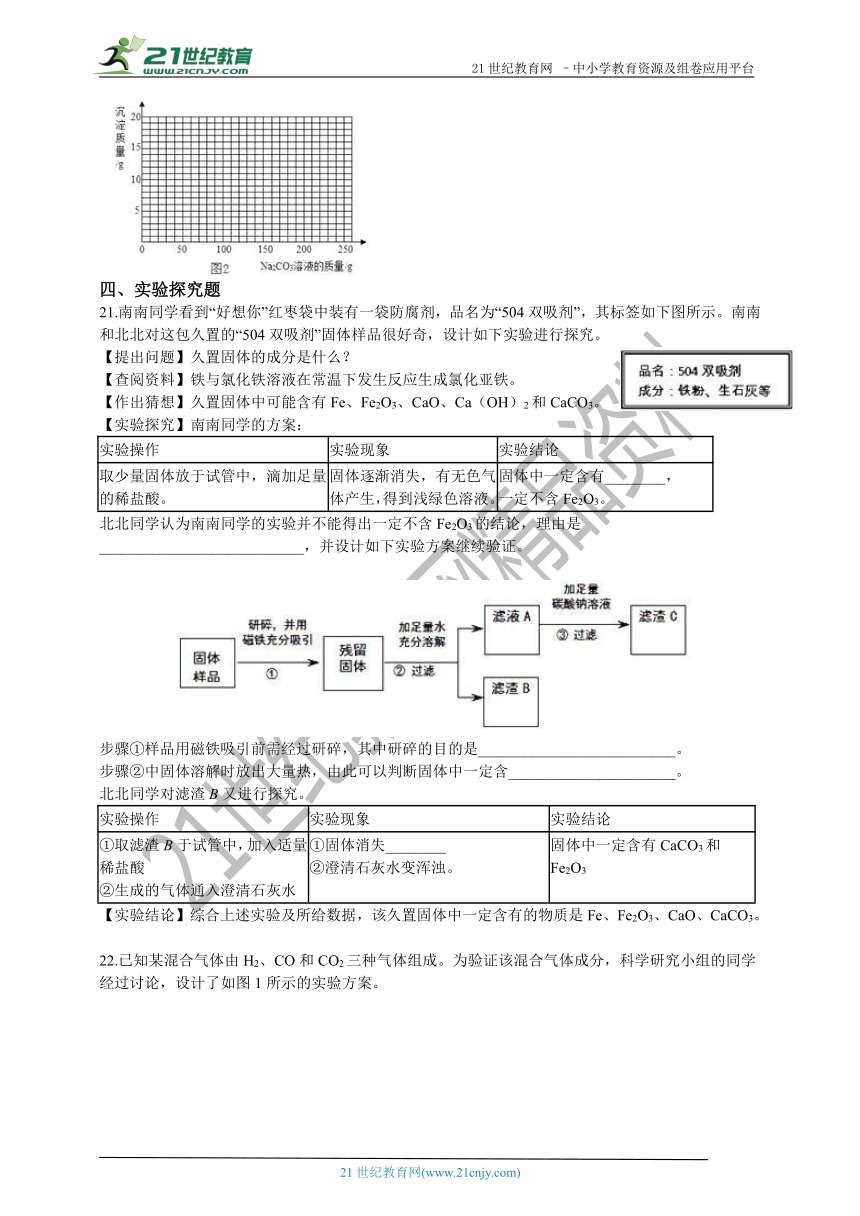
(3)若在 100g 混合溶液中不断加入 10.6%的 Na2CO3 的溶液,请在图 2 中画出加入 Na2CO3
溶液的质量与产生沉淀的质量的关系图。
四、实验探究题
21.南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如下图所示。南南和北北对这包久置的“504双吸剂”固体样品很好奇,设计如下实验进行探究。
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
【实验探究】南南同学的方案:
实验操作 实验现象 实验结论
取少量固体放于试管中,滴加足量的稀盐酸。 固体逐渐消失,有无色气体产生,得到浅绿色溶液。 固体中一定含有________,
一定不含Fe2O3。
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是___________________________,并设计如下实验方案继续验证。
步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是__________________________。
步骤②中固体溶解时放出大量热,由此可以判断固体中一定含______________________。
北北同学对滤渣B又进行探究。
实验操作 实验现象 实验结论
①取滤渣B于试管中,加入适量
稀盐酸
②生成的气体通入澄清石灰水 ①固体消失________
②澄清石灰水变浑浊。 固体中一定含有CaCO3和Fe2O3
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3。
22.已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图1所示的实验方案。(查阅资料可知:CuO+H2Cu+H2O;CuO+COCu+CO2 )
根据方案回答下列问题:
(1)装置C在实验中的作用是_________________________________。
(2)若证明混合气体中一定存在CO,那么依据的现象是__________________________ 。
(3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论是否可靠?若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见。___________。
(4)图1方案中B装置可用来吸收CO2但没有现象。为证明CO2和NaOH能发生反应,小丁又设计了图2所示的方案。则图2方案中所加试剂X应该是 。
23.现有一份二氧化锰样品(含有杂质炭),为测定该样品中二氧化锰的质量分数,兴趣小组设计了如下实验方案:在一定量的样品中通入某气体a,使杂质炭在加热条件下反应生成CO2 , 通过吸收气体来进行测定分析。
(1)在使用图甲装置前应先检查气密性,操作是:先用夹子夹紧橡皮管,再往仪器①中加入足量水,使长颈漏斗下端内出现一段高于锥形瓶中的液面的液柱,当观察到的现象为________________时,说明气密性良好。
(2)甲装置制取a气体的化学方程式为__________________________________。
(3)兴趣小组同学认为在装置②与③之间接入丙装置更加合理,若没有丙接入,则不能确定________,从而使测量值很可能偏小。
24.“管道疏通剂”为什么能很好地解决家用下水管道堵塞问题。带着疑问,小科买来“妙管家”和“花仙子”两个品牌的“管道疏通剂”。说明书中均标明主要成分是氢氧化钠固体和铝粉。
【实验一】他将理发店收集的毛发及饭粒的混合物放入锥形瓶中,向瓶中加入20g疏通剂和100mL水。反应时瓶内物上下翻动明显、有大量气体产生、放热,反应后发现饭粒成粥状,毛发小部分消失,用玻璃棒挤压,头发容易压断变成碎屑。
【实验启示】气体能起物理松动效果;“毛发部分消失易断裂”说明疏通剂具有________性;实验中产生的气体仅是水蒸气吗?小科查资料明白气体中还含有氢气:铝与氢氧化钠溶液反应时放出大量的热,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
【提出问题】疏通剂在使用时遇到明火,氢气会被点燃吗?
【实验二】小科取两只250 mL锥形瓶,分别加入“妙管家”和“花仙子”50g、水150mL 。过程中用燃着的木条点燃产生的气体,“妙管家”产生的气体可以被点燃,而“花仙子”产生的气体未被点燃。
【实验猜想】“花仙子”产生的气体未被点燃的原因?
猜想一:________导致了“花仙子”产生的气体中氢气的量较少;
猜想二:反应中有大量的热产生,导致产生的气体中混有大量的水蒸气。
【实验设计】能否让“花仙子”产生的气体被点燃?
热的水蒸气遇冷会________(填物态变化名称),小科依据猜想二设计了用浓硫酸和冷的蒸馏水来处理水蒸气的两种实验方案;实验前,为安全考虑,小科请老师对方案进行审查。若你是指导老师,你会选择方案________来完成实验。通过实验,小科认为,管道疏通剂疏通效果好,但存在着安全隐患,应要有更好的产品替代。
参考答案
一、单选题
1 2 3 4 5 6 7 8 9 10
B C B B D D B A B A
二、填空题
11.(1)CuSO4 和 Ba(NO3)2 (2)KNO3 或 Na2CO3、KNO3
12.(1)BaCl2 (2)Na2CO3+2AgNO3=Ag2CO3↓+2NaNO3
13.(1)Fe3O4、FeSO4(2)2CuO+C△2Cu+CO2↑
14.(1)FeCl3和K2SO4;KOH(2)BaCO3+2HCl=BaCl2+H2O+CO2↑
15.(1)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(2)Na2CO3 , CuO,NaOH
16.(1)Fe(2)复分解反应(3)③
三、解答题
17.(1)NaOH(2)过滤(3)HCl(4)MgCl2 Mg+Cl2↑
18.(1)H2SO4(2)过滤
(3)解:设由CuO生成的CuSO4的质量为X
CuO+H2SO4= CuSO4+H2O
80 160
8g X
X =16 g
设与CuSO4反应的NaOH的质量为y,同时生成Na2SO4的质量为a
CuSO4+ 2NaOH=Cu(OH)2↓+ Na2SO4
160 80 142
16 g y a
y =8 g
所用氢氧化钠溶液质量分数=
a=14.2 g
(4)设与H2SO4反应的NaOH的质量为b
H2SO4+ 2NaOH= Na2SO4+ 2H2O
80 142
60×20% b
b=21.3 g
所得溶液中溶质的质量为21.3+14.2=35.5g
19.(1)Na2SO4+ Ba(NO3)2=BaSO4↓+2NaNO3 (2)过滤;CuSO4和H2SO4
(3)解:黑色固体为CuO,质量为8g
CuO+ H2SO4= CuSO4+H2O
80 160
8g x
CuSO4+ 2NaOH=Cu(OH)2↓+Na2SO4
160 80
16g y
Y=8g
NaOH%=8/(100-60)=20%
(4)解:
H2SO4+ 2NaOH=Na2SO4+2H2O
98 80
A 60g×20%
A=14.7g
CuO + H2SO4 = CuSO4 + H2O
80 98
8g B
B=9.8g
原有硫酸质量为14.7g+9.8g=24.5g,H2SO4%=24.5/100=24.5%
20.(1)4.4g
(2)
CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl
111 106 100
x y×10% 10g
p%=11.1/100=11.1%
y=100g
(3)解:如图所示:
Na2CO3+2HCl= NaCl+H2O CO2↑
106 44
Z×10.6% 4.4g
z=100g
四、实验探究题
21.Fe;氧化铁和盐酸反应生成氯化铁,氯化铁和铁反应生成氯化亚铁也是浅绿色的;增大接触面积,使反应充分;CaO;有气泡产生,溶液变黄色
22.(1)二氧化碳是否除尽(2)C中不变浑浊D中固体黑色变红色F 中变浑浊(3)不可靠,应在CD之间加一个干燥装置(如:浓硫酸)(4)BaCl2 和 NaOH
23.(1)长颈漏斗下端内的液面在一段时间内不再下降(2)2H2O2=2H2O+O2↑(3)二氧化碳气体是否已被氢氧化钠溶液完全(全部)吸收
24.腐蚀;铝(氢氧化钠)的含量少;液化;二
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)浙教版九年级科学上册 2.5 物质的转化 同步练习
一、单选题
1.如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是(?? )
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气??
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管???
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
2.下列物质中含少量杂质(括号内为杂质),除去杂质所用试剂均适量,其它操作或反应条件已略去,其中利用甲、乙两试剂都能除去的选项是(?? )
A.①②?????B.③④?????C.②④??????D.①③
3.下图是无色溶液X发生化学反应时的颜色变化,无色溶液X是(??????? )
A.稀盐酸???B.稀硫酸????C.澄清石灰水???D.硫酸钠溶液
4.某班甲、乙两组同学分别做常见酸和碱与指示剂反应的实验,使用的试剂有稀盐酸、稀硫酸、氢氧化钠溶液和酚酞试液。实验后废液分别集中到各组的一个废液缸中。研究小组对两个组的废液进行检测,结果如下表。下列说法正确的是(?? )
A.甲组废液中一定含有稀盐酸或稀硫酸
B.乙组废液中一定含有氢氧化钠、氯化钠、硫酸钠 C.甲组废液可直接排放,乙组处理后再排放 D.如将两组的废液合并在一起,如溶液呈无色,混合液可直接排放。
5.右图是某同学的学习笔记,其中“→”表示物质之间能转化,“—”表示物质之间能发生化学反应。关于该图,下列说法中不正确的是 (? )
A.反应⑤不一定属于复分解反应??
B.该图中的所有反应一定不涉及置换反应
C.反应①是一个放热反应?? ??
D.反应②的转化中必须有盐类物质参加
6.甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是(? ?)
A.?若丙、丁为盐和水,则甲、乙一定是酸、碱??????????
B.?若丙为气体,则甲、乙中一定有单质
C.?若丁为水,则该反应一定是复分解反应???????????????
D.?若只有甲、丁是单质,则该反应一定是置换反应
7.下列转化不能通过一步反应实现的是(?? ) ①SiO2→Na2SiO3?? ②SiO2→H2SiO3?? ③CuSO4→Cu(NO3)2 ④CuO→Cu(OH)2?? ⑤Fe(OH)2→Fe(OH)3
A.①②③?????B.②④?????C.③④⑤?????D.②③④
8.右图中有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有a、AgNO3溶液?b、MgSO4溶液?? c、BaCl2溶液??d、H2SO4溶液? e、Fe?? f、Cu(NO3)2溶液则图中①表示的物质的编号是(?? )
A.?b?????B.?f?????C.?a?????D.?c
9.下列物质的变化中,只有加酸才能一步实现的是(??? )
A.CaCO3→CO2????B.Fe2O3→FeCl3????C.Zn→ZnSO4????D.?KOH→KCl
10.铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象。下列说法中错误的是( ???)
A .a处产生白色物质?????? B.b处生成蓝色沉淀??????
C .c处发生复分解反应??????D .d处产生气泡
二、填空题
11.某不纯的 K2CO3 样品中可能含有的杂质是 Na2CO3、KNO3、CuSO4 和 Ba(NO3)2 几种物质中的一种或几种,进行以下实验: ①取一定量该样品放入烧杯中并加入足量水搅拌后,样品全部溶解且得到无色溶液; ②向无色溶液中加入过量的 CaCl2 溶液充分反应,出现白色沉淀,将白色沉淀经过滤、洗涤、干燥、称量。根据上述实验现象回答:
(1)样品所含杂质肯定没有________;
(2)若所取的样品为 13.8 克,得到白色沉淀 9 克,则样品中杂质的可能组成:________。
12.有A、B、C、D四种物质的稀溶液,它们分别是Na2CO3、BaCl2、AgNO3、HCl中的某一种溶液。如图为常温下上述溶液两两混合的实验现象,其中“↓”表示产生沉淀,“↑”表示产生气体,“─”表示无明显现象,试回答:
(1)试判断A物质是________。
(2)请写出D与C反应的化学方程式_________________________。
13.如图是一些常见物质间互相转化的关系图(部分反应条件已省略)。A、B均为无色气体,X为固体,Y为能使澄清石灰水变浑浊的无色气体,E、F为常见金属,试推断:
(1)乙、戊物质的化学式分别为________。
(2)写出下列转化的化学方程式(丙+X→F+Y):________。
14.已知某固体粉末是KOH、FeCl3、BaCl2、Na2CO3、K2SO4之一或几种,为探究其组成,探究小组同还查阅资料得知KCl、BaCl2溶液呈中性,BaSO4不溶于酸。经思考设计如下实验,请分析实验过程,回答下列问题:
(1)原粉末中一定没有________,可能含有________。
(2)写出沉淀全部溶解的化学方程式__________________________________。
15.A,B,C,D是初中科学常见的四种物质,其中A,B属于相同物质类别的化合物,C,D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“一”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去,请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是__________________;
(2)若C是锌,A和B都属于酸,写出D可能的化学式___________(物质类别不同的两种即可)
16.下图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)A物质是________(填化学式)。
(2)C与E反应的基本类型是________。
(3)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有________(填序号)。①2类 ???②3类??? ③4类??? ④5类
三、解答题
17.镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取.主要步骤如下:
(1)为了使MgCl2转化为Mg(OH)2 , 试剂①可以选用________,要使MgCl2完全转化为沉淀,加入试剂①的量应足量.
(2)加入试剂①后,从溶液中能够分离得到Mg(OH)2沉淀的方法是________.
(3)试剂②可以选用________?.
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2 , 其化学方程式________.
18.图甲中A是一种常见的酸,它能与黑色固体B反应,B质量为8克,将NaOH溶液渐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示,在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)A溶液中溶质的化学式为________;
(2)操作1的名称是________;
(3)NaOH溶液中溶质的质量分数是多少?
(4)C溶液中加入NaOH溶液至恰好完全反应时,所得溶液溶质的质量是多少?
如图甲中A是一种常见的酸溶液100g,它能与黑色固体B反应,B质量为8克,将NaOH溶液逐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示;在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)试写出“在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀”的化学反应方程式____________________________。
(2)操作1的名称是________,C中溶液的溶质化学式为________。
(3)NaOH溶液溶质的质量分数是多少?
(4)A溶液溶质的质量分数是多少?
20.现有 HCl 与 CaCl2 的混合溶液,为了分析混合溶液中 HCl 和 CaCl2 的质量分数,设计了如图 1 所示实验方案: 【实验数据】实验共记录了两组数据: 第①组,气体吸收完全后,NaOH 溶液质量增加 4.4g; 第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为 10g. 根据实验设计及有关数据进行分析与计算:
(1)生成气体的质量为________.
(2)混合溶液中 CaCl2 的质量分数为多少?(写出计算过程)
(3)若在 100g 混合溶液中不断加入 10.6%的 Na2CO3 的溶液,请在图 2 中画出加入 Na2CO3 溶液的质量与产生沉淀的质量的关系图。
四、实验探究题
21.南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如下图所示。南南和北北对这包久置的“504双吸剂”固体样品很好奇,设计如下实验进行探究。 【提出问题】久置固体的成分是什么? 【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。 【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。 【实验探究】南南同学的方案:
实验操作
实验现象
实验结论
取少量固体放于试管中,滴加足量的稀盐酸。
固体逐渐消失,有无色气体产生,得到浅绿色溶液。
固体中一定含有________, 一定不含Fe2O3。
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是___________________________,并设计如下实验方案继续验证。
步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是__________________________。 步骤②中固体溶解时放出大量热,由此可以判断固体中一定含______________________。 北北同学对滤渣B又进行探究。
实验操作
实验现象
实验结论
①取滤渣B于试管中,加入适量 稀盐酸 ②生成的气体通入澄清石灰水
①固体消失________ ②澄清石灰水变浑浊。
固体中一定含有CaCO3和Fe2O3
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3。
22.已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图1所示的实验方案。(查阅资料可知:CuO+H2Cu+H2O;CuO+COCu+CO2 ) 根据方案回答下列问题:
(1)装置C在实验中的作用是_________________________________。
(2)若证明混合气体中一定存在CO,那么依据的现象是__________________________?。
(3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论是否可靠?若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见。___________。
(4)图1方案中B装置可用来吸收CO2但没有现象。为证明CO2和NaOH能发生反应,小丁又设计了图2所示的方案。则图2方案中所加试剂X应该是?????????????? ?。
23.现有一份二氧化锰样品(含有杂质炭),为测定该样品中二氧化锰的质量分数,兴趣小组设计了如下实验方案:在一定量的样品中通入某气体a,使杂质炭在加热条件下反应生成CO2 , 通过吸收气体来进行测定分析。
(1)在使用图甲装置前应先检查气密性,操作是:先用夹子夹紧橡皮管,再往仪器①中加入足量水,使长颈漏斗下端内出现一段高于锥形瓶中的液面的液柱,当观察到的现象为________________时,说明气密性良好。
(2)甲装置制取a气体的化学方程式为__________________________________。
(3)兴趣小组同学认为在装置②与③之间接入丙装置更加合理,若没有丙接入,则不能确定________,从而使测量值很可能偏小。
24.“管道疏通剂”为什么能很好地解决家用下水管道堵塞问题。带着疑问,小科买来“妙管家”和“花仙子”两个品牌的“管道疏通剂”。说明书中均标明主要成分是氢氧化钠固体和铝粉。 【实验一】他将理发店收集的毛发及饭粒的混合物放入锥形瓶中,向瓶中加入20g疏通剂和100mL水。反应时瓶内物上下翻动明显、有大量气体产生、放热,反应后发现饭粒成粥状,毛发小部分消失,用玻璃棒挤压,头发容易压断变成碎屑。 【实验启示】气体能起物理松动效果;“毛发部分消失易断裂”说明疏通剂具有________性;实验中产生的气体仅是水蒸气吗?小科查资料明白气体中还含有氢气:铝与氢氧化钠溶液反应时放出大量的热,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。 【提出问题】疏通剂在使用时遇到明火,氢气会被点燃吗? 【实验二】小科取两只250 mL锥形瓶,分别加入“妙管家”和“花仙子”50g、水150mL 。过程中用燃着的木条点燃产生的气体,“妙管家”产生的气体可以被点燃,而“花仙子”产生的气体未被点燃。 【实验猜想】“花仙子”产生的气体未被点燃的原因? 猜想一:________导致了“花仙子”产生的气体中氢气的量较少; 猜想二:反应中有大量的热产生,导致产生的气体中混有大量的水蒸气。 【实验设计】能否让“花仙子”产生的气体被点燃? 热的水蒸气遇冷会________(填物态变化名称),小科依据猜想二设计了用浓硫酸和冷的蒸馏水来处理水蒸气的两种实验方案;实验前,为安全考虑,小科请老师对方案进行审查。若你是指导老师,你会选择方案________来完成实验。通过实验,小科认为,管道疏通剂疏通效果好,但存在着安全隐患,应要有更好的产品替代。
参考答案
一、单选题
1
2
3
4
5
6
7
8
9
10
B
C
B
B
D
D
B
A
B
A
二、填空题
11.(1)CuSO4 和 Ba(NO3)2 (2)KNO3 或 Na2CO3、KNO3
12.(1)BaCl2 (2)Na2CO3+2AgNO3=Ag2CO3↓+2NaNO3
13.(1)Fe3O4、FeSO4(2)2CuO+C△2Cu+CO2↑
14.(1)FeCl3和K2SO4;KOH(2)BaCO3+2HCl=BaCl2+H2O+CO2↑
15.(1)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(2)Na2CO3 , CuO,NaOH
16.(1)Fe(2)复分解反应(3)③
三、解答题
17.(1)NaOH(2)过滤(3)HCl(4)MgCl2 Mg+Cl2↑
18.(1)H2SO4(2)过滤 (3)解:设由CuO生成的CuSO4的质量为X
CuO+H2SO4=
CuSO4+H2O
80
160
8g
X
X =16 g 设与CuSO4反应的NaOH的质量为y,同时生成Na2SO4的质量为a
CuSO4+
2NaOH=Cu(OH)2↓+
Na2SO4
160
80
142
16 g
y
a
y =8 g 所用氢氧化钠溶液质量分数= a=14.2 g (4)设与H2SO4反应的NaOH的质量为b
H2SO4+
2NaOH=
Na2SO4+ 2H2O
80
142
60×20%
b
b=21.3 g 所得溶液中溶质的质量为21.3+14.2=35.5g
19.(1)Na2SO4+ Ba(NO3)2=BaSO4↓+2NaNO3 (2)过滤;CuSO4和H2SO4 (3)解:黑色固体为CuO,质量为8g
CuO+ H2SO4=
CuSO4+H2O
80
160
8g
x
CuSO4+
2NaOH=Cu(OH)2↓+Na2SO4
160
80
16g
y
Y=8g NaOH%=8/(100-60)=20% (4)解:
H2SO4+
2NaOH=Na2SO4+2H2O
98
80
A
60g×20%
A=14.7g
CuO +
H2SO4 = CuSO4 + H2O
80
98
8g
B
??? B=9.8g 原有硫酸质量为14.7g+9.8g=24.5g,H2SO4%=24.5/100=24.5%
20.(1)4.4g (2)
CaCl2 +
Na2CO3 =
CaCO3↓+ 2NaCl
111
106
100
x
y×10%
10g
p%=11.1/100=11.1% y=100g (3)解:如图所示:
Na2CO3+2HCl= NaCl+H2O
CO2↑
106
44
Z×10.6%
4.4g
z=100g
四、实验探究题
21.Fe;氧化铁和盐酸反应生成氯化铁,氯化铁和铁反应生成氯化亚铁也是浅绿色的;增大接触面积,使反应充分;CaO;有气泡产生,溶液变黄色
22.(1)二氧化碳是否除尽(2)C中不变浑浊D中固体黑色变红色F 中变浑浊(3)不可靠,应在CD之间加一个干燥装置(如:浓硫酸)(4)BaCl2? 和 NaOH
23.(1)长颈漏斗下端内的液面在一段时间内不再下降(2)2H2O2=2H2O+O2↑(3)二氧化碳气体是否已被氢氧化钠溶液完全(全部)吸收
24.腐蚀;铝(氢氧化钠)的含量少;液化;二
浙教版九年级科学上册 2.5 物质的转化 同步练习
一、单选题
1.如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( )
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
2.下列物质中含少量杂质(括号内为杂质),除去杂质所用试剂均适量,其它操作或反应条件已略去,其中利用甲、乙两试剂都能除去的选项是( )
A.①② B.③④ C.②④ D.①③
3.下图是无色溶液X发生化学反应时的颜色变化,无色溶液X是( )
A.稀盐酸 B.稀硫酸 C.澄清石灰水 D.硫酸钠溶液
4.某班甲、乙两组同学分别做常见酸和碱与指示剂反应的实验,使用的试剂有稀盐酸、稀硫酸、氢氧化钠溶液和酚酞试液。实验后废液分别集中到各组的一个废液缸中。研究小组对两个组的废液进行检测,结果如下表。下列说法正确的是( )
A.甲组废液中一定含有稀盐酸或稀硫酸
B.乙组废液中一定含有氢氧化钠、氯化钠、硫酸钠
C.甲组废液可直接排放,乙组处理后再排放
D.如将两组的废液合并在一起,如溶液呈无色,混合液可直接排放。
5.右图是某同学的学习笔记,其中“→”表示物质之间能转化,“—”表示物质之间能发生化学反应。关于该图,下列说法中不正确的是 ( )
A.反应⑤不一定属于复分解反应
B.该图中的所有反应一定不涉及置换反应
C.反应①是一个放热反应
D.反应②的转化中必须有盐类物质参加
6.甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是( )
A. 若丙、丁为盐和水,则甲、乙一定是酸、碱
B. 若丙为气体,则甲、乙中一定有单质
C. 若丁为水,则该反应一定是复分解反应
D. 若只有甲、丁是单质,则该反应一定是置换反应
7.下列转化不能通过一步反应实现的是( )
①SiO2→Na2SiO3 ②SiO2→H2SiO3 ③CuSO4→Cu(NO3)2 ④CuO→Cu(OH)2 ⑤Fe(OH)2→Fe(OH)3
A.①②③ B.②④ C.③④⑤ D.②③④
8.右图中有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有a、AgNO3溶液 b、MgSO4溶液 c、BaCl2溶液 d、H2SO4溶液 e、Fe f、Cu(NO3)2溶液则图中①表示的物质的编号是( )
A. b B. f C. a D. c
9.下列物质的变化中,只有加酸才能一步实现的是( )
A.CaCO3→CO2 B.Fe2O3→FeCl3 C.Zn→ZnSO4 D. KOH→KCl
10.铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象。下列说法中错误的是( )
A .a处产生白色物质 B.b处生成蓝色沉淀
C .c处发生复分解反应 D .d处产生气泡
二、填空题
11.某不纯的 K2CO3 样品中可能含有的杂质是 Na2CO3、KNO3、CuSO4 和 Ba(NO3)2 几种物质中的一种或几种,进行以下实验:
①取一定量该样品放入烧杯中并加入足量水搅拌后,样品全部溶解且得到无色溶液;
②向无色溶液中加入过量的 CaCl2 溶液充分反应,出现白色沉淀,将白色沉淀经过滤、洗涤、干燥、称量。根据上述实验现象回答:
(1)样品所含杂质肯定没有________;
(2)若所取的样品为 13.8 克,得到白色沉淀 9 克,则样品中杂质的可能组成:________。
12.有A、B、C、D四种物质的稀溶液,它们分别是Na2CO3、BaCl2、AgNO3、HCl中的某一种溶液。如图为常温下上述溶液两两混合的实验现象,其中“↓”表示产生沉淀,“↑”表示产生气体,“─”表示无明显现象,试回答:
(1)试判断A物质是________。
(2)请写出D与C反应的化学方程式_________________________。
13.如图是一些常见物质间互相转化的关系图(部分反应条件已省略)。A、B均为无色气体,X为固体,Y为能使澄清石灰水变浑浊的无色气体,E、F为常见金属,试推断:
(1)乙、戊物质的化学式分别为________。
(2)写出下列转化的化学方程式(丙+X→F+Y):________。
14.已知某固体粉末是KOH、FeCl3、BaCl2、Na2CO3、K2SO4之一或几种,为探究其组成,探究小组同还查阅资料得知KCl、BaCl2溶液呈中性,BaSO4不溶于酸。经思考设计如下实验,请分析实验过程,回答下列问题:
(1)原粉末中一定没有________,可能含有________。
(2)写出沉淀全部溶解的化学方程式__________________________________。
15.A,B,C,D是初中科学常见的四种物质,其中A,B属于相同物质类别的化合物,C,D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“一”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去,请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是__________________;
(2)若C是锌,A和B都属于酸,写出D可能的化学式___________(物质类别不同的两种即可)
16.下图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)A物质是________(填化学式)。
(2)C与E反应的基本类型是________。
(3)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有________(填序号)。①2类 ②3类 ③4类 ④5类
三、解答题
17.镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取.主要步骤如下:
(1)为了使MgCl2转化为Mg(OH)2 , 试剂①可以选用________,要使MgCl2完全转化为沉淀,加入试剂①的量应足量.
(2)加入试剂①后,从溶液中能够分离得到Mg(OH)2沉淀的方法是________.
(3)试剂②可以选用________ .
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2 , 其化学方程式________.
18.图甲中A是一种常见的酸,它能与黑色固体B反应,B质量为8克,将NaOH溶液渐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示,在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)A溶液中溶质的化学式为________;
(2)操作1的名称是________;
(3)NaOH溶液中溶质的质量分数是多少
(4)C溶液中加入NaOH溶液至恰好完全反应时,所得溶液溶质的质量是多少
19. 如图甲中A是一种常见的酸溶液100g,它能与黑色固体B反应,B质量为8克,将NaOH溶液逐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示;在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)试写出“在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀”的化学反应方程式____________________________。
(2)操作1的名称是________,C中溶液的溶质化学式为________。
(3)NaOH溶液溶质的质量分数是多少
(4)A溶液溶质的质量分数是多少
20.现有 HCl 与 CaCl2 的混合溶液,为了分析混合溶液中 HCl 和 CaCl2 的质量分数,设计了如图 1 所示实验方案:
【实验数据】实验共记录了两组数据:
第①组,气体吸收完全后,NaOH 溶液质量增加 4.4g;
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为 10g. 根据实验设计及有关数据进行分析与计算:
(1)生成气体的质量为________.
(2)混合溶液中 CaCl2 的质量分数为多少?(写出计算过程)
(3)若在 100g 混合溶液中不断加入 10.6%的 Na2CO3 的溶液,请在图 2 中画出加入 Na2CO3
溶液的质量与产生沉淀的质量的关系图。
四、实验探究题
21.南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如下图所示。南南和北北对这包久置的“504双吸剂”固体样品很好奇,设计如下实验进行探究。
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
【实验探究】南南同学的方案:
实验操作 实验现象 实验结论
取少量固体放于试管中,滴加足量的稀盐酸。 固体逐渐消失,有无色气体产生,得到浅绿色溶液。 固体中一定含有________,
一定不含Fe2O3。
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是___________________________,并设计如下实验方案继续验证。
步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是__________________________。
步骤②中固体溶解时放出大量热,由此可以判断固体中一定含______________________。
北北同学对滤渣B又进行探究。
实验操作 实验现象 实验结论
①取滤渣B于试管中,加入适量
稀盐酸
②生成的气体通入澄清石灰水 ①固体消失________
②澄清石灰水变浑浊。 固体中一定含有CaCO3和Fe2O3
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3。
22.已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图1所示的实验方案。(查阅资料可知:CuO+H2Cu+H2O;CuO+COCu+CO2 )
根据方案回答下列问题:
(1)装置C在实验中的作用是_________________________________。
(2)若证明混合气体中一定存在CO,那么依据的现象是__________________________ 。
(3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论是否可靠?若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见。___________。
(4)图1方案中B装置可用来吸收CO2但没有现象。为证明CO2和NaOH能发生反应,小丁又设计了图2所示的方案。则图2方案中所加试剂X应该是 。
23.现有一份二氧化锰样品(含有杂质炭),为测定该样品中二氧化锰的质量分数,兴趣小组设计了如下实验方案:在一定量的样品中通入某气体a,使杂质炭在加热条件下反应生成CO2 , 通过吸收气体来进行测定分析。
(1)在使用图甲装置前应先检查气密性,操作是:先用夹子夹紧橡皮管,再往仪器①中加入足量水,使长颈漏斗下端内出现一段高于锥形瓶中的液面的液柱,当观察到的现象为________________时,说明气密性良好。
(2)甲装置制取a气体的化学方程式为__________________________________。
(3)兴趣小组同学认为在装置②与③之间接入丙装置更加合理,若没有丙接入,则不能确定________,从而使测量值很可能偏小。
24.“管道疏通剂”为什么能很好地解决家用下水管道堵塞问题。带着疑问,小科买来“妙管家”和“花仙子”两个品牌的“管道疏通剂”。说明书中均标明主要成分是氢氧化钠固体和铝粉。
【实验一】他将理发店收集的毛发及饭粒的混合物放入锥形瓶中,向瓶中加入20g疏通剂和100mL水。反应时瓶内物上下翻动明显、有大量气体产生、放热,反应后发现饭粒成粥状,毛发小部分消失,用玻璃棒挤压,头发容易压断变成碎屑。
【实验启示】气体能起物理松动效果;“毛发部分消失易断裂”说明疏通剂具有________性;实验中产生的气体仅是水蒸气吗?小科查资料明白气体中还含有氢气:铝与氢氧化钠溶液反应时放出大量的热,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
【提出问题】疏通剂在使用时遇到明火,氢气会被点燃吗?
【实验二】小科取两只250 mL锥形瓶,分别加入“妙管家”和“花仙子”50g、水150mL 。过程中用燃着的木条点燃产生的气体,“妙管家”产生的气体可以被点燃,而“花仙子”产生的气体未被点燃。
【实验猜想】“花仙子”产生的气体未被点燃的原因?
猜想一:________导致了“花仙子”产生的气体中氢气的量较少;
猜想二:反应中有大量的热产生,导致产生的气体中混有大量的水蒸气。
【实验设计】能否让“花仙子”产生的气体被点燃?
热的水蒸气遇冷会________(填物态变化名称),小科依据猜想二设计了用浓硫酸和冷的蒸馏水来处理水蒸气的两种实验方案;实验前,为安全考虑,小科请老师对方案进行审查。若你是指导老师,你会选择方案________来完成实验。通过实验,小科认为,管道疏通剂疏通效果好,但存在着安全隐患,应要有更好的产品替代。
参考答案
一、单选题
1 2 3 4 5 6 7 8 9 10
B C B B D D B A B A
二、填空题
11.(1)CuSO4 和 Ba(NO3)2 (2)KNO3 或 Na2CO3、KNO3
12.(1)BaCl2 (2)Na2CO3+2AgNO3=Ag2CO3↓+2NaNO3
13.(1)Fe3O4、FeSO4(2)2CuO+C△2Cu+CO2↑
14.(1)FeCl3和K2SO4;KOH(2)BaCO3+2HCl=BaCl2+H2O+CO2↑
15.(1)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(2)Na2CO3 , CuO,NaOH
16.(1)Fe(2)复分解反应(3)③
三、解答题
17.(1)NaOH(2)过滤(3)HCl(4)MgCl2 Mg+Cl2↑
18.(1)H2SO4(2)过滤
(3)解:设由CuO生成的CuSO4的质量为X
CuO+H2SO4= CuSO4+H2O
80 160
8g X
X =16 g
设与CuSO4反应的NaOH的质量为y,同时生成Na2SO4的质量为a
CuSO4+ 2NaOH=Cu(OH)2↓+ Na2SO4
160 80 142
16 g y a
y =8 g
所用氢氧化钠溶液质量分数=
a=14.2 g
(4)设与H2SO4反应的NaOH的质量为b
H2SO4+ 2NaOH= Na2SO4+ 2H2O
80 142
60×20% b
b=21.3 g
所得溶液中溶质的质量为21.3+14.2=35.5g
19.(1)Na2SO4+ Ba(NO3)2=BaSO4↓+2NaNO3 (2)过滤;CuSO4和H2SO4
(3)解:黑色固体为CuO,质量为8g
CuO+ H2SO4= CuSO4+H2O
80 160
8g x
CuSO4+ 2NaOH=Cu(OH)2↓+Na2SO4
160 80
16g y
Y=8g
NaOH%=8/(100-60)=20%
(4)解:
H2SO4+ 2NaOH=Na2SO4+2H2O
98 80
A 60g×20%
A=14.7g
CuO + H2SO4 = CuSO4 + H2O
80 98
8g B
B=9.8g
原有硫酸质量为14.7g+9.8g=24.5g,H2SO4%=24.5/100=24.5%
20.(1)4.4g
(2)
CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl
111 106 100
x y×10% 10g
p%=11.1/100=11.1%
y=100g
(3)解:如图所示:
Na2CO3+2HCl= NaCl+H2O CO2↑
106 44
Z×10.6% 4.4g
z=100g
四、实验探究题
21.Fe;氧化铁和盐酸反应生成氯化铁,氯化铁和铁反应生成氯化亚铁也是浅绿色的;增大接触面积,使反应充分;CaO;有气泡产生,溶液变黄色
22.(1)二氧化碳是否除尽(2)C中不变浑浊D中固体黑色变红色F 中变浑浊(3)不可靠,应在CD之间加一个干燥装置(如:浓硫酸)(4)BaCl2 和 NaOH
23.(1)长颈漏斗下端内的液面在一段时间内不再下降(2)2H2O2=2H2O+O2↑(3)二氧化碳气体是否已被氢氧化钠溶液完全(全部)吸收
24.腐蚀;铝(氢氧化钠)的含量少;液化;二
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)浙教版九年级科学上册 2.5 物质的转化 同步练习
一、单选题
1.如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是(?? )
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气??
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管???
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
2.下列物质中含少量杂质(括号内为杂质),除去杂质所用试剂均适量,其它操作或反应条件已略去,其中利用甲、乙两试剂都能除去的选项是(?? )
A.①②?????B.③④?????C.②④??????D.①③
3.下图是无色溶液X发生化学反应时的颜色变化,无色溶液X是(??????? )
A.稀盐酸???B.稀硫酸????C.澄清石灰水???D.硫酸钠溶液
4.某班甲、乙两组同学分别做常见酸和碱与指示剂反应的实验,使用的试剂有稀盐酸、稀硫酸、氢氧化钠溶液和酚酞试液。实验后废液分别集中到各组的一个废液缸中。研究小组对两个组的废液进行检测,结果如下表。下列说法正确的是(?? )
A.甲组废液中一定含有稀盐酸或稀硫酸
B.乙组废液中一定含有氢氧化钠、氯化钠、硫酸钠 C.甲组废液可直接排放,乙组处理后再排放 D.如将两组的废液合并在一起,如溶液呈无色,混合液可直接排放。
5.右图是某同学的学习笔记,其中“→”表示物质之间能转化,“—”表示物质之间能发生化学反应。关于该图,下列说法中不正确的是 (? )
A.反应⑤不一定属于复分解反应??
B.该图中的所有反应一定不涉及置换反应
C.反应①是一个放热反应?? ??
D.反应②的转化中必须有盐类物质参加
6.甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是(? ?)
A.?若丙、丁为盐和水,则甲、乙一定是酸、碱??????????
B.?若丙为气体,则甲、乙中一定有单质
C.?若丁为水,则该反应一定是复分解反应???????????????
D.?若只有甲、丁是单质,则该反应一定是置换反应
7.下列转化不能通过一步反应实现的是(?? ) ①SiO2→Na2SiO3?? ②SiO2→H2SiO3?? ③CuSO4→Cu(NO3)2 ④CuO→Cu(OH)2?? ⑤Fe(OH)2→Fe(OH)3
A.①②③?????B.②④?????C.③④⑤?????D.②③④
8.右图中有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有a、AgNO3溶液?b、MgSO4溶液?? c、BaCl2溶液??d、H2SO4溶液? e、Fe?? f、Cu(NO3)2溶液则图中①表示的物质的编号是(?? )
A.?b?????B.?f?????C.?a?????D.?c
9.下列物质的变化中,只有加酸才能一步实现的是(??? )
A.CaCO3→CO2????B.Fe2O3→FeCl3????C.Zn→ZnSO4????D.?KOH→KCl
10.铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象。下列说法中错误的是( ???)
A .a处产生白色物质?????? B.b处生成蓝色沉淀??????
C .c处发生复分解反应??????D .d处产生气泡
二、填空题
11.某不纯的 K2CO3 样品中可能含有的杂质是 Na2CO3、KNO3、CuSO4 和 Ba(NO3)2 几种物质中的一种或几种,进行以下实验: ①取一定量该样品放入烧杯中并加入足量水搅拌后,样品全部溶解且得到无色溶液; ②向无色溶液中加入过量的 CaCl2 溶液充分反应,出现白色沉淀,将白色沉淀经过滤、洗涤、干燥、称量。根据上述实验现象回答:
(1)样品所含杂质肯定没有________;
(2)若所取的样品为 13.8 克,得到白色沉淀 9 克,则样品中杂质的可能组成:________。
12.有A、B、C、D四种物质的稀溶液,它们分别是Na2CO3、BaCl2、AgNO3、HCl中的某一种溶液。如图为常温下上述溶液两两混合的实验现象,其中“↓”表示产生沉淀,“↑”表示产生气体,“─”表示无明显现象,试回答:
(1)试判断A物质是________。
(2)请写出D与C反应的化学方程式_________________________。
13.如图是一些常见物质间互相转化的关系图(部分反应条件已省略)。A、B均为无色气体,X为固体,Y为能使澄清石灰水变浑浊的无色气体,E、F为常见金属,试推断:
(1)乙、戊物质的化学式分别为________。
(2)写出下列转化的化学方程式(丙+X→F+Y):________。
14.已知某固体粉末是KOH、FeCl3、BaCl2、Na2CO3、K2SO4之一或几种,为探究其组成,探究小组同还查阅资料得知KCl、BaCl2溶液呈中性,BaSO4不溶于酸。经思考设计如下实验,请分析实验过程,回答下列问题:
(1)原粉末中一定没有________,可能含有________。
(2)写出沉淀全部溶解的化学方程式__________________________________。
15.A,B,C,D是初中科学常见的四种物质,其中A,B属于相同物质类别的化合物,C,D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“一”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去,请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是__________________;
(2)若C是锌,A和B都属于酸,写出D可能的化学式___________(物质类别不同的两种即可)
16.下图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)A物质是________(填化学式)。
(2)C与E反应的基本类型是________。
(3)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有________(填序号)。①2类 ???②3类??? ③4类??? ④5类
三、解答题
17.镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取.主要步骤如下:
(1)为了使MgCl2转化为Mg(OH)2 , 试剂①可以选用________,要使MgCl2完全转化为沉淀,加入试剂①的量应足量.
(2)加入试剂①后,从溶液中能够分离得到Mg(OH)2沉淀的方法是________.
(3)试剂②可以选用________?.
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2 , 其化学方程式________.
18.图甲中A是一种常见的酸,它能与黑色固体B反应,B质量为8克,将NaOH溶液渐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示,在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)A溶液中溶质的化学式为________;
(2)操作1的名称是________;
(3)NaOH溶液中溶质的质量分数是多少?
(4)C溶液中加入NaOH溶液至恰好完全反应时,所得溶液溶质的质量是多少?
如图甲中A是一种常见的酸溶液100g,它能与黑色固体B反应,B质量为8克,将NaOH溶液逐渐加入到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示;在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
(1)试写出“在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀”的化学反应方程式____________________________。
(2)操作1的名称是________,C中溶液的溶质化学式为________。
(3)NaOH溶液溶质的质量分数是多少?
(4)A溶液溶质的质量分数是多少?
20.现有 HCl 与 CaCl2 的混合溶液,为了分析混合溶液中 HCl 和 CaCl2 的质量分数,设计了如图 1 所示实验方案: 【实验数据】实验共记录了两组数据: 第①组,气体吸收完全后,NaOH 溶液质量增加 4.4g; 第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为 10g. 根据实验设计及有关数据进行分析与计算:
(1)生成气体的质量为________.
(2)混合溶液中 CaCl2 的质量分数为多少?(写出计算过程)
(3)若在 100g 混合溶液中不断加入 10.6%的 Na2CO3 的溶液,请在图 2 中画出加入 Na2CO3 溶液的质量与产生沉淀的质量的关系图。
四、实验探究题
21.南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如下图所示。南南和北北对这包久置的“504双吸剂”固体样品很好奇,设计如下实验进行探究。 【提出问题】久置固体的成分是什么? 【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。 【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。 【实验探究】南南同学的方案:
实验操作
实验现象
实验结论
取少量固体放于试管中,滴加足量的稀盐酸。
固体逐渐消失,有无色气体产生,得到浅绿色溶液。
固体中一定含有________, 一定不含Fe2O3。
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是___________________________,并设计如下实验方案继续验证。
步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是__________________________。 步骤②中固体溶解时放出大量热,由此可以判断固体中一定含______________________。 北北同学对滤渣B又进行探究。
实验操作
实验现象
实验结论
①取滤渣B于试管中,加入适量 稀盐酸 ②生成的气体通入澄清石灰水
①固体消失________ ②澄清石灰水变浑浊。
固体中一定含有CaCO3和Fe2O3
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3。
22.已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图1所示的实验方案。(查阅资料可知:CuO+H2Cu+H2O;CuO+COCu+CO2 ) 根据方案回答下列问题:
(1)装置C在实验中的作用是_________________________________。
(2)若证明混合气体中一定存在CO,那么依据的现象是__________________________?。
(3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论是否可靠?若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见。___________。
(4)图1方案中B装置可用来吸收CO2但没有现象。为证明CO2和NaOH能发生反应,小丁又设计了图2所示的方案。则图2方案中所加试剂X应该是?????????????? ?。
23.现有一份二氧化锰样品(含有杂质炭),为测定该样品中二氧化锰的质量分数,兴趣小组设计了如下实验方案:在一定量的样品中通入某气体a,使杂质炭在加热条件下反应生成CO2 , 通过吸收气体来进行测定分析。
(1)在使用图甲装置前应先检查气密性,操作是:先用夹子夹紧橡皮管,再往仪器①中加入足量水,使长颈漏斗下端内出现一段高于锥形瓶中的液面的液柱,当观察到的现象为________________时,说明气密性良好。
(2)甲装置制取a气体的化学方程式为__________________________________。
(3)兴趣小组同学认为在装置②与③之间接入丙装置更加合理,若没有丙接入,则不能确定________,从而使测量值很可能偏小。
24.“管道疏通剂”为什么能很好地解决家用下水管道堵塞问题。带着疑问,小科买来“妙管家”和“花仙子”两个品牌的“管道疏通剂”。说明书中均标明主要成分是氢氧化钠固体和铝粉。 【实验一】他将理发店收集的毛发及饭粒的混合物放入锥形瓶中,向瓶中加入20g疏通剂和100mL水。反应时瓶内物上下翻动明显、有大量气体产生、放热,反应后发现饭粒成粥状,毛发小部分消失,用玻璃棒挤压,头发容易压断变成碎屑。 【实验启示】气体能起物理松动效果;“毛发部分消失易断裂”说明疏通剂具有________性;实验中产生的气体仅是水蒸气吗?小科查资料明白气体中还含有氢气:铝与氢氧化钠溶液反应时放出大量的热,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。 【提出问题】疏通剂在使用时遇到明火,氢气会被点燃吗? 【实验二】小科取两只250 mL锥形瓶,分别加入“妙管家”和“花仙子”50g、水150mL 。过程中用燃着的木条点燃产生的气体,“妙管家”产生的气体可以被点燃,而“花仙子”产生的气体未被点燃。 【实验猜想】“花仙子”产生的气体未被点燃的原因? 猜想一:________导致了“花仙子”产生的气体中氢气的量较少; 猜想二:反应中有大量的热产生,导致产生的气体中混有大量的水蒸气。 【实验设计】能否让“花仙子”产生的气体被点燃? 热的水蒸气遇冷会________(填物态变化名称),小科依据猜想二设计了用浓硫酸和冷的蒸馏水来处理水蒸气的两种实验方案;实验前,为安全考虑,小科请老师对方案进行审查。若你是指导老师,你会选择方案________来完成实验。通过实验,小科认为,管道疏通剂疏通效果好,但存在着安全隐患,应要有更好的产品替代。
参考答案
一、单选题
1
2
3
4
5
6
7
8
9
10
B
C
B
B
D
D
B
A
B
A
二、填空题
11.(1)CuSO4 和 Ba(NO3)2 (2)KNO3 或 Na2CO3、KNO3
12.(1)BaCl2 (2)Na2CO3+2AgNO3=Ag2CO3↓+2NaNO3
13.(1)Fe3O4、FeSO4(2)2CuO+C△2Cu+CO2↑
14.(1)FeCl3和K2SO4;KOH(2)BaCO3+2HCl=BaCl2+H2O+CO2↑
15.(1)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(2)Na2CO3 , CuO,NaOH
16.(1)Fe(2)复分解反应(3)③
三、解答题
17.(1)NaOH(2)过滤(3)HCl(4)MgCl2 Mg+Cl2↑
18.(1)H2SO4(2)过滤 (3)解:设由CuO生成的CuSO4的质量为X
CuO+H2SO4=
CuSO4+H2O
80
160
8g
X
X =16 g 设与CuSO4反应的NaOH的质量为y,同时生成Na2SO4的质量为a
CuSO4+
2NaOH=Cu(OH)2↓+
Na2SO4
160
80
142
16 g
y
a
y =8 g 所用氢氧化钠溶液质量分数= a=14.2 g (4)设与H2SO4反应的NaOH的质量为b
H2SO4+
2NaOH=
Na2SO4+ 2H2O
80
142
60×20%
b
b=21.3 g 所得溶液中溶质的质量为21.3+14.2=35.5g
19.(1)Na2SO4+ Ba(NO3)2=BaSO4↓+2NaNO3 (2)过滤;CuSO4和H2SO4 (3)解:黑色固体为CuO,质量为8g
CuO+ H2SO4=
CuSO4+H2O
80
160
8g
x
CuSO4+
2NaOH=Cu(OH)2↓+Na2SO4
160
80
16g
y
Y=8g NaOH%=8/(100-60)=20% (4)解:
H2SO4+
2NaOH=Na2SO4+2H2O
98
80
A
60g×20%
A=14.7g
CuO +
H2SO4 = CuSO4 + H2O
80
98
8g
B
??? B=9.8g 原有硫酸质量为14.7g+9.8g=24.5g,H2SO4%=24.5/100=24.5%
20.(1)4.4g (2)
CaCl2 +
Na2CO3 =
CaCO3↓+ 2NaCl
111
106
100
x
y×10%
10g
p%=11.1/100=11.1% y=100g (3)解:如图所示:
Na2CO3+2HCl= NaCl+H2O
CO2↑
106
44
Z×10.6%
4.4g
z=100g
四、实验探究题
21.Fe;氧化铁和盐酸反应生成氯化铁,氯化铁和铁反应生成氯化亚铁也是浅绿色的;增大接触面积,使反应充分;CaO;有气泡产生,溶液变黄色
22.(1)二氧化碳是否除尽(2)C中不变浑浊D中固体黑色变红色F 中变浑浊(3)不可靠,应在CD之间加一个干燥装置(如:浓硫酸)(4)BaCl2? 和 NaOH
23.(1)长颈漏斗下端内的液面在一段时间内不再下降(2)2H2O2=2H2O+O2↑(3)二氧化碳气体是否已被氢氧化钠溶液完全(全部)吸收
24.腐蚀;铝(氢氧化钠)的含量少;液化;二
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
