第1节构成物质的基本微粒——原子(原子的构成19张PPT)
文档属性
| 名称 | 第1节构成物质的基本微粒——原子(原子的构成19张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 36.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-20 00:00:00 | ||
图片预览





文档简介
课件19张PPT。道尔顿1803年创立了“原子论”。原子像一个实心球3.1 构成物质的基本微粒
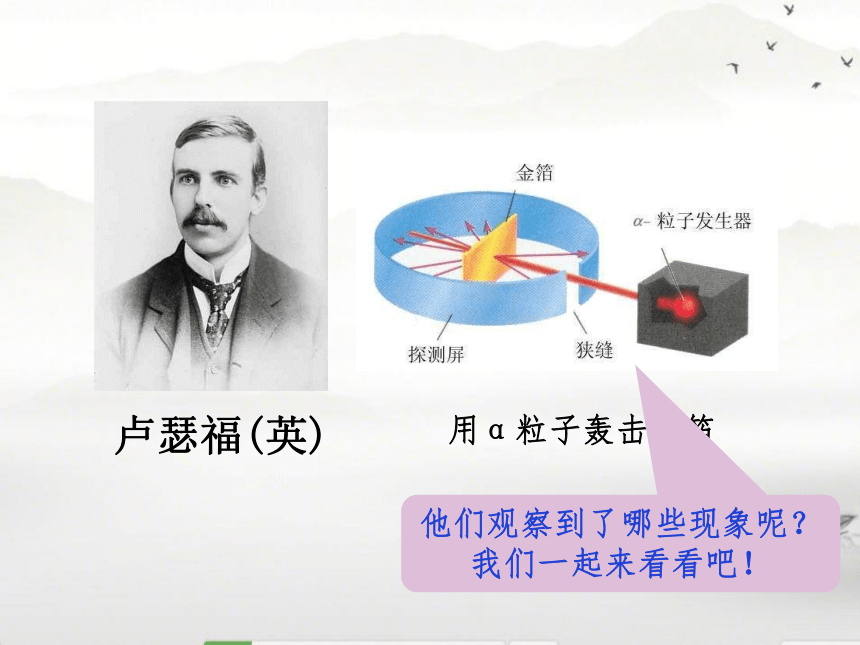
——原子原子是构成物质的最小微粒吗?原子能不能再分?它的内部结构如何呢?汤姆生(英)“葡萄干蛋糕模型”1897年,汤姆生确定所有原子都含有带负电荷的电子。卢瑟福(英)用α粒子轰击金箔他们观察到了哪些现象呢?
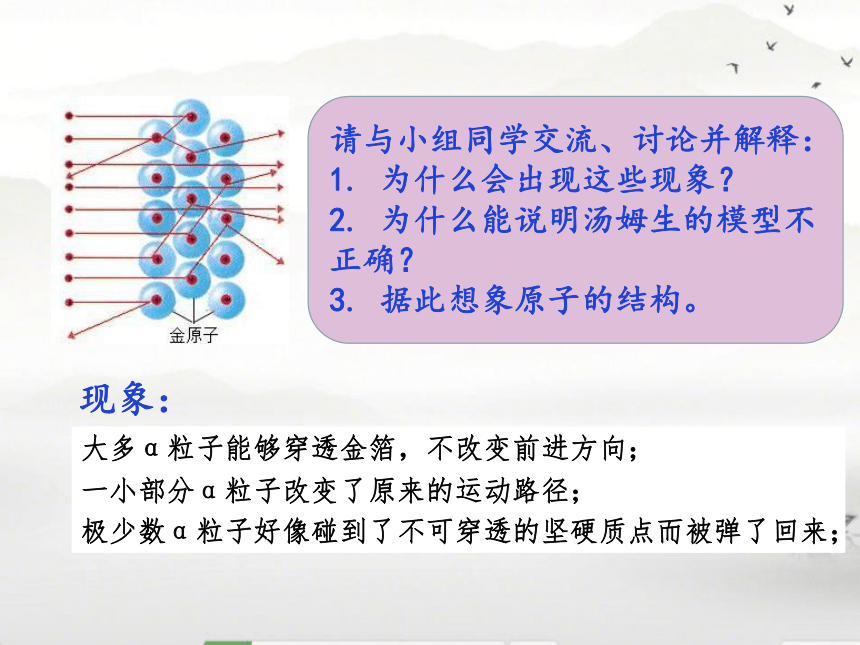
我们一起来看看吧!请与小组同学交流、讨论并解释:
1. 为什么会出现这些现象?
2. 为什么能说明汤姆生的模型不正确?
3. 据此想象原子的结构。现象:大多α粒子能够穿透金箔,不改变前进方向;一小部分α粒子改变了原来的运动路径;极少数α粒子好像碰到了不可穿透的坚硬质点而被弹了回来;“有核原子模型”卢瑟福(英) 原子像一个微型太阳系,带正电的原子核像太阳,带负电的核外电子像绕着太阳转的行星,在核外空间作高速运动。 原子的结构:原子原子核核外电子显电中性,为什么?电量大小相等,
但电性相反。 原子核的半径大约是原子半径的十万分之一,在原子中的所占体积极小。
但原子核几乎集中了原子的全部质量,电子的质量相对要小得多。“有核原子模型”原子原子核卢瑟福(英)原子核内有什么呢?有质子卢瑟福(英)但他又遇到了新问题? 1920年,卢瑟福预言:原子核中有不带电荷的中性粒子。 除氢原子外,其它原子的质量明显大于核中质子的总质量。查德威克 查德威克因发现中子,获得1935年诺贝尔物理学奖。让我们一起来补充原子的构成原子原子核核外电子原子的结构:质子中子实验证明:有一种氢原子的核内只有1个质子,没有中子,核外有1个电子;
有一种碳原子的核内有6个质子,6个中子,核外有6个电子。又知:1个质子带1个单位正电荷,1个电子带1个单位负电荷。质子数=核电荷数=核外电子数通过今天的学习,你有何收获?道尔顿原子结构的探究历程汤姆生卢瑟福... ...想要认识原子更深层次的奥秘,
打开优酷,搜索“BBC之原子”。
——原子原子是构成物质的最小微粒吗?原子能不能再分?它的内部结构如何呢?汤姆生(英)“葡萄干蛋糕模型”1897年,汤姆生确定所有原子都含有带负电荷的电子。卢瑟福(英)用α粒子轰击金箔他们观察到了哪些现象呢?
我们一起来看看吧!请与小组同学交流、讨论并解释:
1. 为什么会出现这些现象?
2. 为什么能说明汤姆生的模型不正确?
3. 据此想象原子的结构。现象:大多α粒子能够穿透金箔,不改变前进方向;一小部分α粒子改变了原来的运动路径;极少数α粒子好像碰到了不可穿透的坚硬质点而被弹了回来;“有核原子模型”卢瑟福(英) 原子像一个微型太阳系,带正电的原子核像太阳,带负电的核外电子像绕着太阳转的行星,在核外空间作高速运动。 原子的结构:原子原子核核外电子显电中性,为什么?电量大小相等,
但电性相反。 原子核的半径大约是原子半径的十万分之一,在原子中的所占体积极小。
但原子核几乎集中了原子的全部质量,电子的质量相对要小得多。“有核原子模型”原子原子核卢瑟福(英)原子核内有什么呢?有质子卢瑟福(英)但他又遇到了新问题? 1920年,卢瑟福预言:原子核中有不带电荷的中性粒子。 除氢原子外,其它原子的质量明显大于核中质子的总质量。查德威克 查德威克因发现中子,获得1935年诺贝尔物理学奖。让我们一起来补充原子的构成原子原子核核外电子原子的结构:质子中子实验证明:有一种氢原子的核内只有1个质子,没有中子,核外有1个电子;
有一种碳原子的核内有6个质子,6个中子,核外有6个电子。又知:1个质子带1个单位正电荷,1个电子带1个单位负电荷。质子数=核电荷数=核外电子数通过今天的学习,你有何收获?道尔顿原子结构的探究历程汤姆生卢瑟福... ...想要认识原子更深层次的奥秘,
打开优酷,搜索“BBC之原子”。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
