第2节 化学反应中的质量关系 课件(33张PPT)
文档属性
| 名称 | 第2节 化学反应中的质量关系 课件(33张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 10.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-20 16:01:52 | ||
图片预览







文档简介
课件33张PPT。化学反应中的质量关系真伪高低蜡烛的燃烧 实验中将两支燃着的蜡烛罩上大烧杯,一会儿后, ▲ 。(填高或低)的蜡烛先熄灭。质变量变?反应前
物质总质量反应后
物质总质量><=真伪硫酸铜溶液和氢氧化钠溶液反应前后质量的测定活动探究一1、取两只50ml小烧杯,分别向当中加入大约10ml的硫酸铜溶液和氢氧化钠溶液;
2、将两只小烧杯一起放在电子秤上称量,记录数据;1、取两只50ml小烧杯,分别向当中加入大约
10ml的硫酸铜溶液和氢氧化钠溶液;
2、将两只小烧杯一起放在电子秤上称量,记录
数据;
3、把两只烧杯内的溶液混合,观察现象,再将
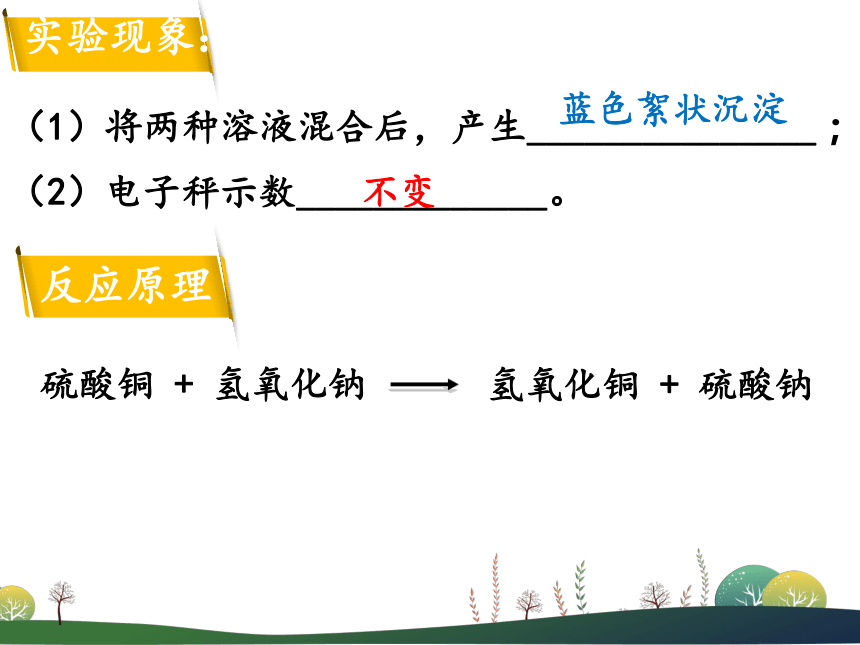
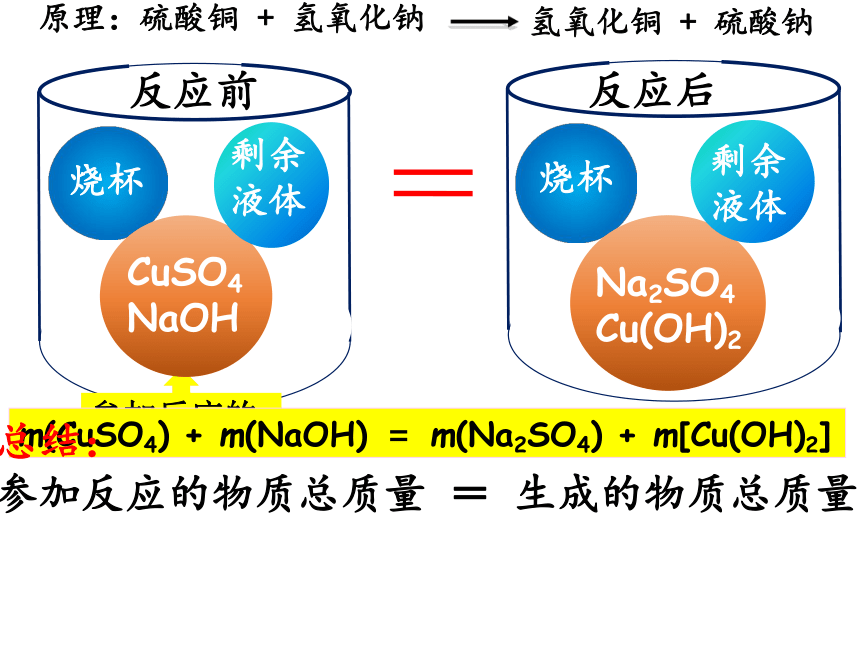
两只小烧杯一起放在电子秤上称量,记录数据。(1)将两种溶液混合后,产生_______________;蓝色絮状沉淀(2)电子秤示数_____________。不变反应原理参加反应的m(CuSO4) + m(NaOH) = m(Na2SO4) + m[Cu(OH)2]总结:
参加反应的物质总质量 = 生成的物质总质量碳酸钠与稀盐酸反应前后质量的测定活动探究二【实验步骤】
1、取两只50ml烧杯,分别向当中加入1~2平勺的碳酸钠粉末,15ml的稀盐酸;
2、将两只小烧杯一起放在电子秤上称量,
记录数据;
3、把稀盐酸倒入装有碳酸钠粉末的烧杯中,观察现象,再将两只小烧杯一起放在电子秤上称量,记录数据。(1)将稀盐酸倒入装有碳酸钠粉末的烧杯中,
有__________ 产生;【实验现象】(2)电子秤示数_____________。气泡变小【反应原理】反应后测得的质量为什么减小了?二氧化碳反应后测得的质量为什么减小了? 请你用所学过的知识,结合我所提供的仪器。设计一套测定盐酸与碳酸钠反应前后质量变化的理想装置。【改进方案】1、取出纱布袋,装入一勺碳酸钠粉末,并绕好线,收口;
2、向塑料瓶中倒入稀盐酸,到达黑色线即可;
3、按图所示,将纱布袋装入
塑料瓶中,并将线放在瓶外,
拧紧盖子。称量,记录数据;
4、上下摇动塑料瓶,观察现象,
称量,记录数据。电子秤示数______________。【改进方案】不变=总结:
参加反应的物质总质量=生成的物质总质量反应后物质的总质量反应前物质的总质量 m(锥形瓶) m(锥形瓶) m(P) m(O2) m(其它) m(P2O5) m(其它)参加反应m(P)+参加反应m(O2) m(P2O5)总结:
参加反应的物质总质量=生成的物质的总质量2018.01.01你能解释吗?为什么镁带燃烧后,
质量变大了? 在定量研究化学反应时,若有气体参加反应或有气体生成,要在密闭容器内进行测定。参加化学反应的各物质的质量总和生成的各物质的质量总和问题1:
10g的冰变成10g的水,符合质量守恒定律吗?问题2:
铁丝生锈,质量增加了,符合质量守恒定律吗?问题3:判断正误
6g红磷在50g空气中充分燃烧,生成56g五氧化二磷。 其实,
今天我们已经追寻了科学家的足迹,
体验了一回质量守恒定律的发现之旅。
历史上的巨人1673年,波义耳开始对化学反应进行定量研究 1777年,拉瓦锡进行大量的实验后,发现质量守恒定律 第五章说过程 教学流程质量守恒定律的发现史通电分解成重新组合水分子氧原子氢原子氧分子氢分子 质量守恒 究其本质 原子的种类
个数
质量
不变 反应前后
物质的总质量
保持不变解释 质量守恒 究其本质 在一切化学反应中,反应前后:原子数目种类质量元素种类质量各物质的质量总和不变分子的种类物质的种类天道酬勤 其实,人生又何尝不是如此,汗水和收获总是“守恒”的。付出与回报总是“平衡”的。结束语
物质总质量反应后
物质总质量><=真伪硫酸铜溶液和氢氧化钠溶液反应前后质量的测定活动探究一1、取两只50ml小烧杯,分别向当中加入大约10ml的硫酸铜溶液和氢氧化钠溶液;
2、将两只小烧杯一起放在电子秤上称量,记录数据;1、取两只50ml小烧杯,分别向当中加入大约
10ml的硫酸铜溶液和氢氧化钠溶液;
2、将两只小烧杯一起放在电子秤上称量,记录
数据;
3、把两只烧杯内的溶液混合,观察现象,再将
两只小烧杯一起放在电子秤上称量,记录数据。(1)将两种溶液混合后,产生_______________;蓝色絮状沉淀(2)电子秤示数_____________。不变反应原理参加反应的m(CuSO4) + m(NaOH) = m(Na2SO4) + m[Cu(OH)2]总结:
参加反应的物质总质量 = 生成的物质总质量碳酸钠与稀盐酸反应前后质量的测定活动探究二【实验步骤】
1、取两只50ml烧杯,分别向当中加入1~2平勺的碳酸钠粉末,15ml的稀盐酸;
2、将两只小烧杯一起放在电子秤上称量,
记录数据;
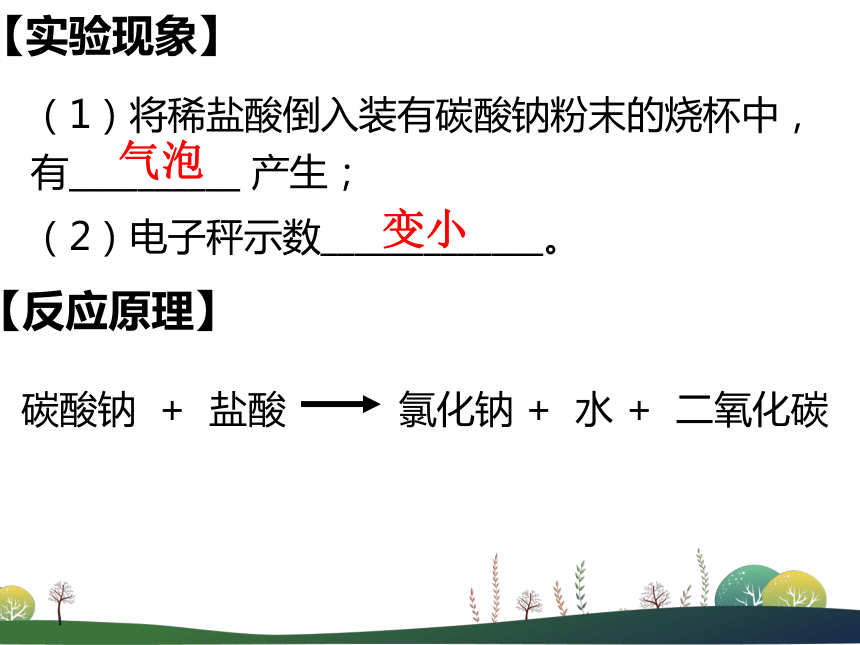
3、把稀盐酸倒入装有碳酸钠粉末的烧杯中,观察现象,再将两只小烧杯一起放在电子秤上称量,记录数据。(1)将稀盐酸倒入装有碳酸钠粉末的烧杯中,
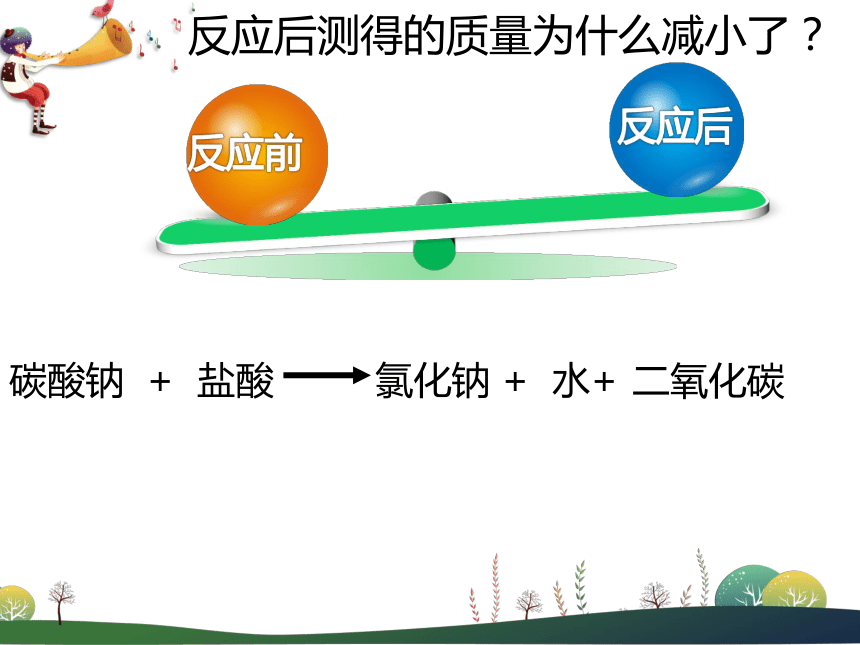
有__________ 产生;【实验现象】(2)电子秤示数_____________。气泡变小【反应原理】反应后测得的质量为什么减小了?二氧化碳反应后测得的质量为什么减小了? 请你用所学过的知识,结合我所提供的仪器。设计一套测定盐酸与碳酸钠反应前后质量变化的理想装置。【改进方案】1、取出纱布袋,装入一勺碳酸钠粉末,并绕好线,收口;
2、向塑料瓶中倒入稀盐酸,到达黑色线即可;
3、按图所示,将纱布袋装入
塑料瓶中,并将线放在瓶外,
拧紧盖子。称量,记录数据;
4、上下摇动塑料瓶,观察现象,
称量,记录数据。电子秤示数______________。【改进方案】不变=总结:
参加反应的物质总质量=生成的物质总质量反应后物质的总质量反应前物质的总质量 m(锥形瓶) m(锥形瓶) m(P) m(O2) m(其它) m(P2O5) m(其它)参加反应m(P)+参加反应m(O2) m(P2O5)总结:
参加反应的物质总质量=生成的物质的总质量2018.01.01你能解释吗?为什么镁带燃烧后,
质量变大了? 在定量研究化学反应时,若有气体参加反应或有气体生成,要在密闭容器内进行测定。参加化学反应的各物质的质量总和生成的各物质的质量总和问题1:
10g的冰变成10g的水,符合质量守恒定律吗?问题2:
铁丝生锈,质量增加了,符合质量守恒定律吗?问题3:判断正误
6g红磷在50g空气中充分燃烧,生成56g五氧化二磷。 其实,
今天我们已经追寻了科学家的足迹,
体验了一回质量守恒定律的发现之旅。
历史上的巨人1673年,波义耳开始对化学反应进行定量研究 1777年,拉瓦锡进行大量的实验后,发现质量守恒定律 第五章说过程 教学流程质量守恒定律的发现史通电分解成重新组合水分子氧原子氢原子氧分子氢分子 质量守恒 究其本质 原子的种类
个数
质量
不变 反应前后
物质的总质量
保持不变解释 质量守恒 究其本质 在一切化学反应中,反应前后:原子数目种类质量元素种类质量各物质的质量总和不变分子的种类物质的种类天道酬勤 其实,人生又何尝不是如此,汗水和收获总是“守恒”的。付出与回报总是“平衡”的。结束语
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
