人教版高中化学必修1 4.2富集在海水中的元素-氯 (1)
文档属性
| 名称 | 人教版高中化学必修1 4.2富集在海水中的元素-氯 (1) |

|
|
| 格式 | zip | ||
| 文件大小 | 577.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-26 00:00:00 | ||
图片预览







文档简介
课件21张PPT。 非金属及其化合物第二节 富集在海水中的元素
----氯资料卡片 大海有几十种化学元素,大部分以盐的形式存在,氯是最重要的成盐元素,海水中含盐约3%。地球总面积5.1亿平方公里
海洋总面积3.6亿平方公里
占地球表面积的71%
相当于38个中国的面积
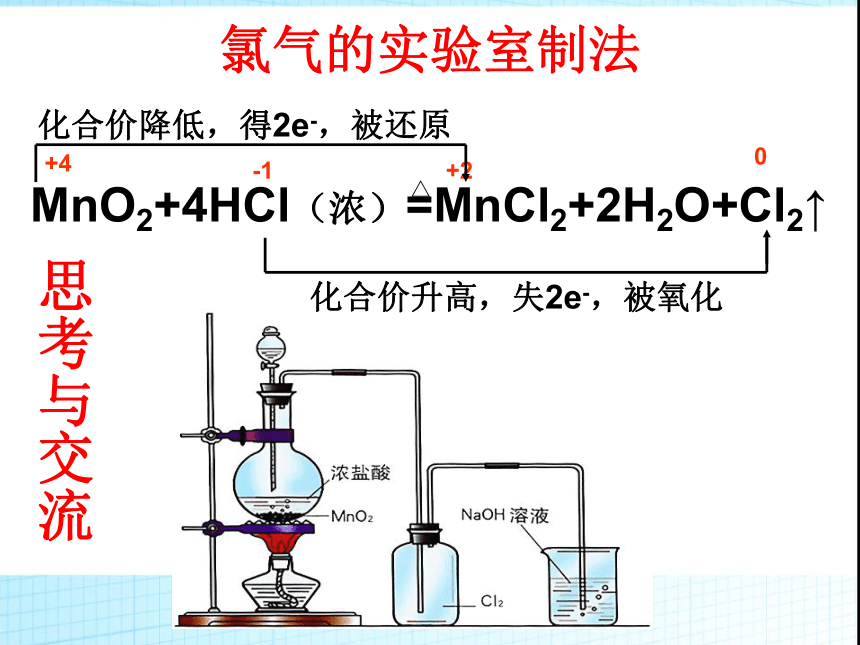
若将海洋中的盐全提取出来,铺在地球的陆地上,可使陆地平均升高150m。氯气的实验室制法化合价升高,失2e-,被氧化化合价降低,得2e-,被还原思考与交流一、氯气(Cl2)(一)物理性质
黄绿色,有强烈刺激性气味的有毒气体,
低温和加压条件下可转变为液态和固态,密
度比空气大,能溶于水(1:2)。
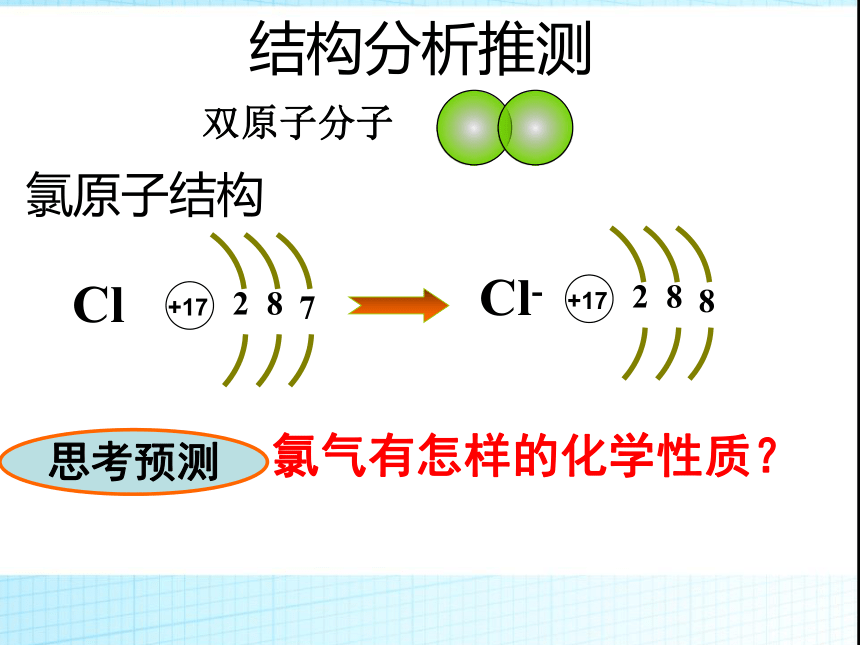
氯原子结构结构分析推测Cl 氯气有怎样的化学性质?思考预测双原子分子1、与金属单质反应(二)氯气的化学性质(1)氯气与铜的反应(产生棕色的烟,溶于水溶液呈蓝绿色)(2)氯气与铁的反应(产生棕黄色的烟,溶于水溶液呈黄色) 常温下干燥的氯气或液氯不能与铁发生反应,所以工业上常把干燥的液氯储存在钢瓶中注:变价金属与氯气反应都被氧化成高价态的氯化物(3)氯气与钠的反应(钠剧烈燃烧,发出黄色火焰,产生大量白色的烟)2、与非金属单质反应(氯气跟氢气的反应)现象:氢气在氯气安静的燃烧,发出苍白色的火焰,产生白雾。什么叫燃烧可燃物是否一定有氧气才能燃烧呢?
燃烧的本质是什么?任何发光发热的剧烈的化学反应叫做燃烧。
思考与交流Cl2 + H2O = HCl + HClO(次氯酸)3、与水反应离子式:
Cl2 + H2O = H++ Cl- + HClO实验4-4实验4-5现象结论与解释现象结论与解释有色纸条褪色有色纸条不褪色氯水有漂白作用干燥的氯气无漂白作用次氯酸的性质(2)不稳定(只存在于水溶液中),易分解(1)强的氧化性,具杀菌消毒、漂白作用(3)弱酸性 (比H2CO3弱)与指示剂有何变化?液氯与氯水,新制氯水与久置氯水的区别?纯净物混合物分子:离子:Cl2 ,HClO,H2OH+,Cl-,ClO-,OH-分子:H2O离子:
H+,Cl-, OH-新制氧化性有酸性,强氧化性,漂白性久置只有Cl2只有酸性★ 久置氯水相当于稀盐酸
实验室中使用的氯水只能现配现用,并盛放在棕色试剂瓶中氯水中含有多种成分,向氯水中加入以下各种物质匀会出现明显现象和反应。请指出起作用的微粒。(1)加入石灰石颗粒有气泡放出
(2)加入红色鲜花瓣,褪色
(3)加入硝酸银溶液产生白色沉淀
(4)加入石蕊试液先变红,后褪色练 习4、氯气与碱溶液反应Cl2+2NaOH=NaCl+NaClO+H2O次氯酸钠2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 氯化钙+ 次氯酸钙 漂白粉的主要成分:漂白粉的有效成分:次氯酸钙 漂白粉的漂白原理思
考 Ca(ClO)2 + 2HCl = CaCl2 + 2 HClO怎样保存漂白粉?密封,保存于阴凉干燥处。酸性:HClO_______H2CO3<产生白色沉淀产生白色沉淀产生白色沉淀产生白色沉淀无现象沉淀不溶解沉淀不溶解沉淀不溶解沉淀溶解无现象Cl-+Ag+=AgCl↓Cl-+Ag+=AgCl↓Cl-+Ag+=AgCl↓CO32-+2Ag+=Ag2CO3↓
Ag2CO3+2H+=2Ag++
H2O+CO2 ↑
二.氯离子( Cl- )的检验实验4-6步骤:
1.滴入少量稀HNO3使其酸化
2.滴加AgNO3溶液
现象:有白色沉淀生成
结论:溶液中存在Cl-
注意:
①用稀HNO3酸化,主要是排除CO32-的干扰。
②不能用稀盐酸酸化,因为盐酸会引入Cl-。1、下列对Cl2的性质叙述不正确的是( )
A.有刺激性气味
B.溶于水但不与水反应
C.与氢气反应
D.与碱反应
B练 习2、在久置的氯水中放入几片鲜花花瓣,发现花瓣并不褪色,其主要原因是( )
A.久置氯水中Cl2全部挥发了
B.久置氯水中Cl2未与水反应生成HClO
C.Cl2与水反应生成HClO在长期放置的过程中已全部分解了
D.氯水中的HClO不能氧化鲜花中的有机色素C
----氯资料卡片 大海有几十种化学元素,大部分以盐的形式存在,氯是最重要的成盐元素,海水中含盐约3%。地球总面积5.1亿平方公里
海洋总面积3.6亿平方公里
占地球表面积的71%
相当于38个中国的面积
若将海洋中的盐全提取出来,铺在地球的陆地上,可使陆地平均升高150m。氯气的实验室制法化合价升高,失2e-,被氧化化合价降低,得2e-,被还原思考与交流一、氯气(Cl2)(一)物理性质
黄绿色,有强烈刺激性气味的有毒气体,
低温和加压条件下可转变为液态和固态,密
度比空气大,能溶于水(1:2)。
氯原子结构结构分析推测Cl 氯气有怎样的化学性质?思考预测双原子分子1、与金属单质反应(二)氯气的化学性质(1)氯气与铜的反应(产生棕色的烟,溶于水溶液呈蓝绿色)(2)氯气与铁的反应(产生棕黄色的烟,溶于水溶液呈黄色) 常温下干燥的氯气或液氯不能与铁发生反应,所以工业上常把干燥的液氯储存在钢瓶中注:变价金属与氯气反应都被氧化成高价态的氯化物(3)氯气与钠的反应(钠剧烈燃烧,发出黄色火焰,产生大量白色的烟)2、与非金属单质反应(氯气跟氢气的反应)现象:氢气在氯气安静的燃烧,发出苍白色的火焰,产生白雾。什么叫燃烧可燃物是否一定有氧气才能燃烧呢?
燃烧的本质是什么?任何发光发热的剧烈的化学反应叫做燃烧。
思考与交流Cl2 + H2O = HCl + HClO(次氯酸)3、与水反应离子式:
Cl2 + H2O = H++ Cl- + HClO实验4-4实验4-5现象结论与解释现象结论与解释有色纸条褪色有色纸条不褪色氯水有漂白作用干燥的氯气无漂白作用次氯酸的性质(2)不稳定(只存在于水溶液中),易分解(1)强的氧化性,具杀菌消毒、漂白作用(3)弱酸性 (比H2CO3弱)与指示剂有何变化?液氯与氯水,新制氯水与久置氯水的区别?纯净物混合物分子:离子:Cl2 ,HClO,H2OH+,Cl-,ClO-,OH-分子:H2O离子:
H+,Cl-, OH-新制氧化性有酸性,强氧化性,漂白性久置只有Cl2只有酸性★ 久置氯水相当于稀盐酸
实验室中使用的氯水只能现配现用,并盛放在棕色试剂瓶中氯水中含有多种成分,向氯水中加入以下各种物质匀会出现明显现象和反应。请指出起作用的微粒。(1)加入石灰石颗粒有气泡放出
(2)加入红色鲜花瓣,褪色
(3)加入硝酸银溶液产生白色沉淀
(4)加入石蕊试液先变红,后褪色练 习4、氯气与碱溶液反应Cl2+2NaOH=NaCl+NaClO+H2O次氯酸钠2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 氯化钙+ 次氯酸钙 漂白粉的主要成分:漂白粉的有效成分:次氯酸钙 漂白粉的漂白原理思
考 Ca(ClO)2 + 2HCl = CaCl2 + 2 HClO怎样保存漂白粉?密封,保存于阴凉干燥处。酸性:HClO_______H2CO3<产生白色沉淀产生白色沉淀产生白色沉淀产生白色沉淀无现象沉淀不溶解沉淀不溶解沉淀不溶解沉淀溶解无现象Cl-+Ag+=AgCl↓Cl-+Ag+=AgCl↓Cl-+Ag+=AgCl↓CO32-+2Ag+=Ag2CO3↓
Ag2CO3+2H+=2Ag++
H2O+CO2 ↑
二.氯离子( Cl- )的检验实验4-6步骤:
1.滴入少量稀HNO3使其酸化
2.滴加AgNO3溶液
现象:有白色沉淀生成
结论:溶液中存在Cl-
注意:
①用稀HNO3酸化,主要是排除CO32-的干扰。
②不能用稀盐酸酸化,因为盐酸会引入Cl-。1、下列对Cl2的性质叙述不正确的是( )
A.有刺激性气味
B.溶于水但不与水反应
C.与氢气反应
D.与碱反应
B练 习2、在久置的氯水中放入几片鲜花花瓣,发现花瓣并不褪色,其主要原因是( )
A.久置氯水中Cl2全部挥发了
B.久置氯水中Cl2未与水反应生成HClO
C.Cl2与水反应生成HClO在长期放置的过程中已全部分解了
D.氯水中的HClO不能氧化鲜花中的有机色素C
