2018-2019学年新高一开学第一周 化学 周测 Word版含答案
文档属性
| 名称 | 2018-2019学年新高一开学第一周 化学 周测 Word版含答案 |
|
|
| 格式 | zip | ||
| 文件大小 | 121.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-08-27 00:00:00 | ||
图片预览



文档简介
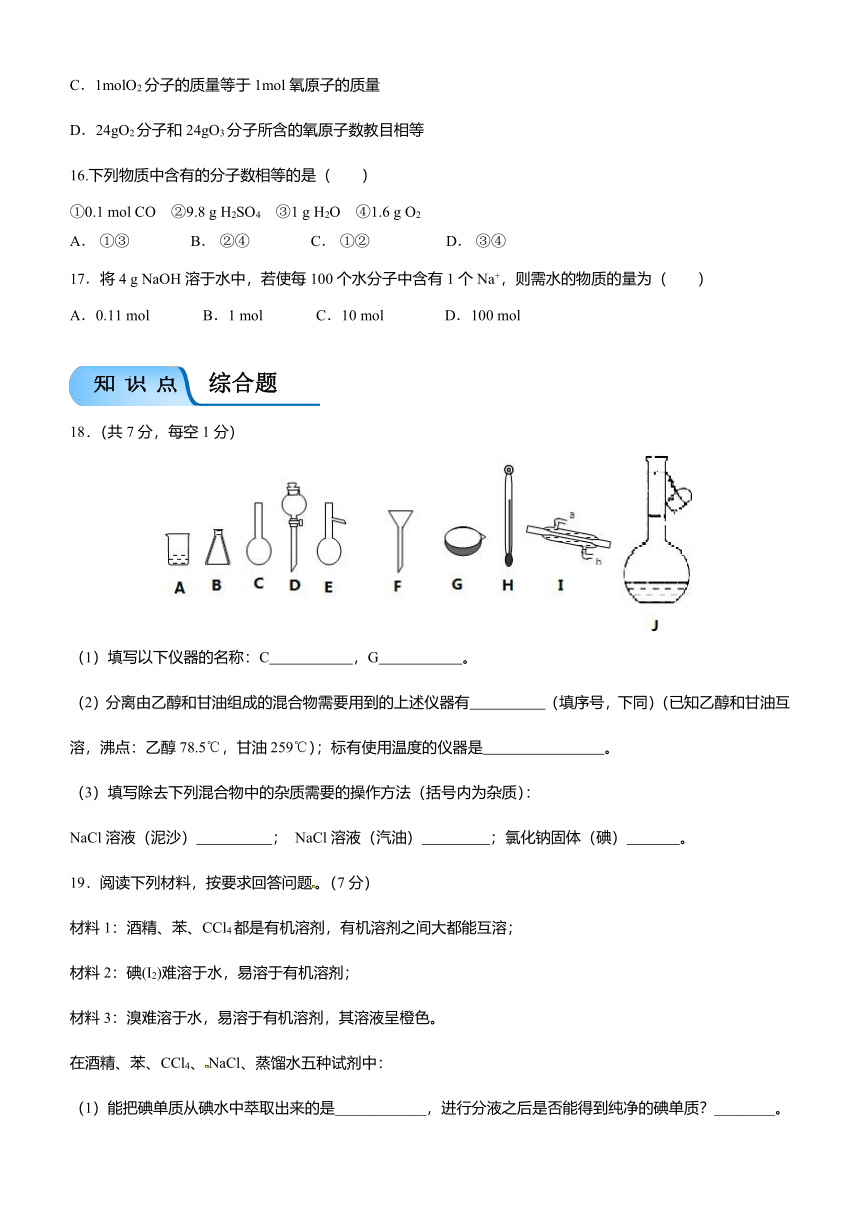
1.正确的实验操作是实验成功的重要因素,下列实验操作正确的是( )
A.①② B.②③ C.①④ D.③④
2.已知金属钾投入水中会发生剧烈反应,并有氢气生成。运输金属钾的包装箱应贴有的图标是( )
A.易燃液体 B.遇湿易燃物品
C. 氧化剂 D.腐蚀品
3.下列仪器常用于物质分离的是( )
①漏斗 ②试管 ③蒸馏烧瓶 ④托盘天平 ⑤分液漏斗 ⑥研钵
A.②④⑤ B.①③④ C.②③⑥ D.①③⑤
4.实验室中,下列行为不符合安全要求的是( )
A.稀释浓硫酸时,将浓硫酸缓慢注入水中并搅拌
B.实验结束后将废液倒入指定容器中
C.金属钠着火时,立即用水扑灭
D.在通风橱内制备有毒气体
5.下列混合物的分离方法不可行的是( )
A.互溶的液态混合物可用分液方法分离
B.互不相溶的液态混合物可用分液方法分离
C.沸点不同的液态混合物可用蒸馏方法分离
D.可溶于水的固体与难溶于水的固体形成的混合物可用溶解、过滤蒸发的方法分离
6.下列有关化学实验的操作中,一般情况下不能相互接触的是( )
A.过滤操作中,玻璃棒与三层滤纸
B.过滤操作中,漏斗下端管口与烧杯内壁
C.分液操作中,分液漏斗下端管口与烧杯内壁
D.用胶头滴管向试管滴加液体时,滴管尖端与试管内壁
7.苯是一种不溶于水且密度小于水的有机物,可以用它来提取碘水中的碘,量取100mL碘的饱和水溶液,倒入分液漏斗中,然后再注入4mL苯,用力振荡后静置,实验现象为( )
A.液体分层,上层为苯层,紫红色 B.液体分层,上层为水层,紫红色
C.液体分层,下层为苯层,紫红色 D.液体分层,上层为水层,无色
8.我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和精人甑,蒸令气上……其清如水,球极浓烈,盖酒露也。”这里所用的“法”悬指( )
A.萃取 B.过滤 C.蒸馏 D.干馏
9.下列实验操作错误的是( )
A.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片
D.碘在酒精的溶解度很大,而且酒精和水互溶,故可用酒精萃取碘水中的碘
10.能够用来鉴别BaCl2?、NaCl?、Na2CO3三种物质的试剂是( )
A.AgNO3溶液 B.稀硫酸 C.稀盐酸 D.稀硝酸
11.检验某未知溶液中是否含有SO下列操作最合理的是( )
A.加入硝酸酸化的Ba(NO3)2溶液
B.先加硝酸酸化,再加Ba(NO3)2溶液
C.加入盐酸酸化的BaCl2溶液
D.先用盐酸酸化,若无沉淀,再加BaCl2溶液
12.下列对于“摩尔”的说法和理解正确的是( )
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
C.国际上规定,0.012 kg碳原子所含有的碳原子数目为1 mol
D.摩尔是物质的量的单位,简称摩,符号为mol
13.ngSO2中含有m个O原子,则阿伏加德罗常数NA的数值可表示为( )
A.64m/n B.32m/n C.n/32m D.n/64m
14.下列说法不正确的是( )
A.磷酸(H3PO4)的摩尔质量与NA个磷酸分子的质量(单位:g)在数值上相等
B.6.02×1023个氮气分子和6.02×1023个氢气分子的质量比等于14∶1
C.32 g氧气所含的原子数目为2×6.02×1023个
D.0.5×6.02×1023个一氧化碳分子比0.5×6.02×1023个二氧化碳分子质量少16 g
15.下列说法正确的是( )
A.28g氮气含有的原子数为NA
B.4g金属钙的物质的量为1mol
C.1molO2分子的质量等于1mol氧原子的质量
D.24gO2分子和24gO3分子所含的氧原子数教目相等
16.下列物质中含有的分子数相等的是( )
①0.1 mol CO ②9.8 g H2SO4 ③1 g H2O ④1.6 g O2
A.?①③ B.?②④ C.?①② D.?③④
17.将4 g NaOH溶于水中,若使每100个水分子中含有1个Na+,则需水的物质的量为( )
A.0.11 mol B.1 mol C.10 mol D.100 mol
18.(共7分,每空1分)
(1)填写以下仪器的名称:C ,G 。
(2)分离由乙醇和甘油组成的混合物需要用到的上述仪器有 (填序号,下同)(已知乙醇和甘油互溶,沸点:乙醇78.5℃,甘油259℃);标有使用温度的仪器是 。
(3)填写除去下列混合物中的杂质需要的操作方法(括号内为杂质):
NaCl溶液(泥沙) ; NaCl溶液(汽油) ;氯化钠固体(碘) 。
19.阅读下列材料,按要求回答问题。(7分)
材料1:酒精、苯、CCl4都是有机溶剂,有机溶剂之间大都能互溶;
材料2:碘(I2)难溶于水,易溶于有机溶剂;
材料3:溴难溶于水,易溶于有机溶剂,其溶液呈橙色。
在酒精、苯、CCl4、NaCl、蒸馏水五种试剂中:
(1)能把碘单质从碘水中萃取出来的是____________,进行分液之后是否能得到纯净的碘单质?________。
(2)能把溴从溴水中萃取出来,并在分液时使溴从分液漏斗下端流出的是________;萃取时,液体接近无色的是________层,有色层是________层。
(3)CCl4能把碘酒中的碘萃取出来吗?为什么?________________________。
20.(共8分,每空1分)
(1)写出下列仪器的名称:a. b. c. 。
(2)仪器a~e中,使用前必须检查是否漏水的有 。(填序号)
(3)若利用上图装置分离四氯化碳和酒精的混合物,还缺少的仪器是 ,将仪器补充完整后进行实验,温度计水银球的位置在 处。冷凝水由 (填f或g)口通入 口流出。
21.(共18分,每空2分)
(1)在 mol Al2(SO4)3中含0.3NA个SO,其中含Al3+ mol。
(2)含有相同原子个数的SO2和SO3,其物质的量之比为 ,其中所含氧原子个数比为 。
(3)49gH2SO4中含__________mol原子,含__________个质子。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_________,R的相对原子质量为_____ ___;含R的质量为1.6 g的Na2R,其物质的量为_________。
1.【答案】C
【解析】①闻气体气味要将少量气体扇入鼻孔,故①正确;②通过洗气瓶干燥气体,气体要“长进短出”,故②错误;③稀释浓硫酸要将浓硫酸加入水中,故③错误;④向酒精灯中添加酒精要使用漏斗,故④正确。故选C。
2.【答案】B
【解析】试题分析:钾是活泼的固态金属,其有很强的还原性,投入水中会发生剧烈反应,有氢气生成,并放出大量的热,故钾和氢气均可能燃烧,甚至会发生爆炸,所以,钾属于遇湿易燃物品,运输金属钾的包装箱应贴有的图标是B,本题选B。
3.【答案】D
【解析】①普通漏斗常用于过滤,可用来分离固液混合物;②试管常用于物质的制备、发生装置;③蒸馏烧瓶常用于分离沸点不同的液体混合物;④托盘天平常用于称量固体的质量;⑤分液漏斗常用于分离互不相溶的液体混合物;⑥研钵常用于固体药品的研磨,不能用来分离。所以用来分离的仪器有①③⑤。故选C。
4.【答案】C
【解析】浓硫酸密度比水大,溶于水放热,稀释浓硫酸时,将浓硫酸缓慢注入水中并搅拌,故A符合安全要求;为防止污染,实验结束后将废液倒入指定容器中,故B符合安全要求;钠与水反应放出氢气,金属钠着火时,不能用水扑灭,要用沙子盖灭,故C不符合安全要求;为防止中毒,在通风橱内制备有毒气体,故D符合安全要求。
5. 【答案】A
6.【答案】D
【解析】为防止液体迸溅,故在过滤时玻璃棒应与三层滤纸接触、漏斗下端管口应与烧杯内壁接触,A、B项正确;分液时,分液漏斗的下端管口应与烧杯内壁接触,C项正确;若胶头滴管的尖端与试管内壁接触,当滴管放回原试剂瓶时,容易污染原试剂,D项错误。
7.【答案】A
【解析】苯的密度比水小,且不溶于水,故液体会分层,上层苯层,碘在苯中的溶解度大于水中,苯层中会出现紫色,故选A。
8.【答案】C
【解析】从浓酒中分离出乙醇,利用酒精与水的沸点不同,用蒸馏的方法将其分离提纯,这种方法是蒸馏,故C正确。
9.【答案】D
10.【答案】B
11.【答案】D
12.【答案】D
【解析】A.摩尔是物质的量的单位,A错误;B.物质的量可以把物质的宏观数量与微观粒子的数量联系起来,B错误;C.国际上规定,0.012kg12C所含有的碳原子数目为1mol,C错误;D.摩尔是物质的量的单位,简称摩,符号为mol,D正确,答案选D。
13.【答案】B
【解析】ngSO2的物质的量为ng÷64g/mol=n/64mol,n/64molSO2含有的氧原子的物质的量为n/64mol×2= n/32mol,根据N=nNA可知:NA=m÷n/32mol=32m/nmol-1,故答案为B。
14.【答案】D
15.【答案】D
【解析】A.氮气分子式为N2,28g氮气含有原子的物质的量为28×2/28mol=2mol,故错误;B.根据n= m/M,4g钙的物质的量为4/40mol=0.1mol,故错误;C、氧气是由氧气分子组成,根据n=m/M,1mol氧气的质量为32g,1mol氧原子的质量为16g,两者不相等,故错误;D、氧气含有氧原子的物质的量为24×2/32 mol =1.5mol,臭氧含有氧原子的物质的量为24×3/48mol=1.5mol,故正确。
16.【答案】C
【解析】根据题目所给出的数据,统一以各物质的物质的量进行比较:①0.1 mol CO ②0.1 mol H2SO4 ③0.056mol H2O ④0.05 mol O2,故相等的为①②,答案选C。
17.【答案】C
【解析】n(NaOH)=4g×40g/mol =0.1 mol,每100个水分子中含有1个Na+,即N(NaOH)∶N(H2O) =1∶100,因为N(NaOH)=n(NaOH)·NA,N(H2O)=n(H2O)·NA,所以n(H2O)=100n(NaOH)=10 mol。答案选C。
18.【答案】(1)圆底烧瓶、蒸发皿;(2)B、E、H、I ;J;(3)过滤,分液,升华。
【解析】(1)常见仪器的A为烧杯,B为锥形瓶,C为圆底烧瓶,D为分液漏斗,E为蒸馏烧瓶,F为长颈漏斗,G为蒸发皿,H为温度计,I为冷凝管,J为容量瓶;(2)乙醇和甘油两种互溶的液体,分离采用蒸馏的方法,用到仪器有带铁圈的铁架台、石棉网、酒精灯、蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶,因此需要上述仪器有B、E、H、I,标有使用温度的是一般是量取液体体积的仪器,如容量瓶、量筒等,因此选J;(3)泥沙和氯化钠溶液属于可溶和不可溶的,因此采用过滤除杂,汽油和氯化钠是两种互不相溶的液体,采用分液的方法分离,碘单质易升华,采取加热升华方法除去碘单质。
19.【答案】(1)苯与四氯化碳 否(2)四氯化碳 上 下(3)不能,因为四氯化碳与酒精互溶
【解析】(1)能把碘单质从碘水中萃取出来的是 苯和CCl4,进行分液之后是否已经得到纯净的碘单质?分液后得不到碘单质,得到的是碘和有机溶剂的混合物,故答案为:苯与四氯化碳;否;(2)四氯化碳的密度大于水的密度,所以四氯化碳在下方,水在上方;萃取时,上层液体是水,溴被萃取到下方四氯化碳中,所以上层无色,下层橙色,故答案为:CCl4;无;橙;(3)四氯化碳和乙醇互溶,不符合萃取剂的选择标准,故不能,故答案为:不能,四氯化碳与酒精混溶。
20.【答案】(1)蒸馏烧瓶,冷凝管,500mL容量瓶;(2)c;(3)酒精灯,蒸馏烧瓶支管口处g f
【解析】(1)是蒸馏烧瓶,冷凝管,500mL容量瓶;(2)需要使用前检查漏水的是500mL容量瓶;(3)装置I是蒸馏装置,利用其沸点不同,得到分离目的,缺少的仪器是酒精灯,因为要测馏分的沸点,因此温度计水银球的位置应在支管口处,为了达到更好的冷凝效果,通冷凝水时从下口进入上口出水,即由g口通入f口流出。
21.【答案】(1) 0.1 0.2 (2) 4:3 ; 8:9 (3)3.5 25NA (5)62 g·mol-1 16 0.1 mol
【解析】(1)N(SO)=0.3NA,则n(SO)=0.3NA÷NA/mol=0.3mol,根据物质电离方程式:Al2(SO4)3= 2Al3+ +3SO可知:n[Al2(SO4)3]=1/3 n(SO)=1/3×0.3mol=0.1mol;根据物质电离方程式可知n(Al3+)=2 /3n(SO)= 2/3×0.3mol=0.2mol,(2)在1个SO2分子中含有3个原子,在1个SO3中含有4个原子,则若SO2和SO3含有相同原子个数,其物质的量之比为1/3∶1/4=4∶3;在1个SO2分子中含有2个氧原子,在1个SO3分子中含有3个氧原子,则其中所含氧原子个数比为(4×2)∶(3×3) =8∶9;。(3)49gH2SO4的物质的量为=0.5mol,含原子0.5mol×7=3.5mol,含质子0.5mol×(16+8×4+1×2)=25mol,数目为25NA,故答案为:3.5;25NA;(4)1?mol?Na2R中含2?mol?Na+,题目中有Na+?0.4?mol,则有0.2?mol?Na2R。运用公式M=m/n得M(Na2R)=12.4g/0.2mol=62 g·mol-1。然后,根据摩尔质量以g·mol-1为单位时,在数值上与物质的相对原子质量或相对分子质量相等,得:Mr(Na2R)=62,求得Mr(R)=62-2×23=16。根据n=m/M得n(R)=0.1 mol,则n(Na2R)=0.1?mol。
