2018-2019学年化学鲁科版选修1同步主题综合测评2 能源与材料(含主题3、4)
文档属性
| 名称 | 2018-2019学年化学鲁科版选修1同步主题综合测评2 能源与材料(含主题3、4) |
|
|
| 格式 | zip | ||
| 文件大小 | 283.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-09-09 00:00:00 | ||
图片预览





文档简介
主题综合测评(二) 能源与材料(含主题3、4)
(时间90分钟,满分100分)
一、选择题(本题包括16小题,每小题3分,共48分)
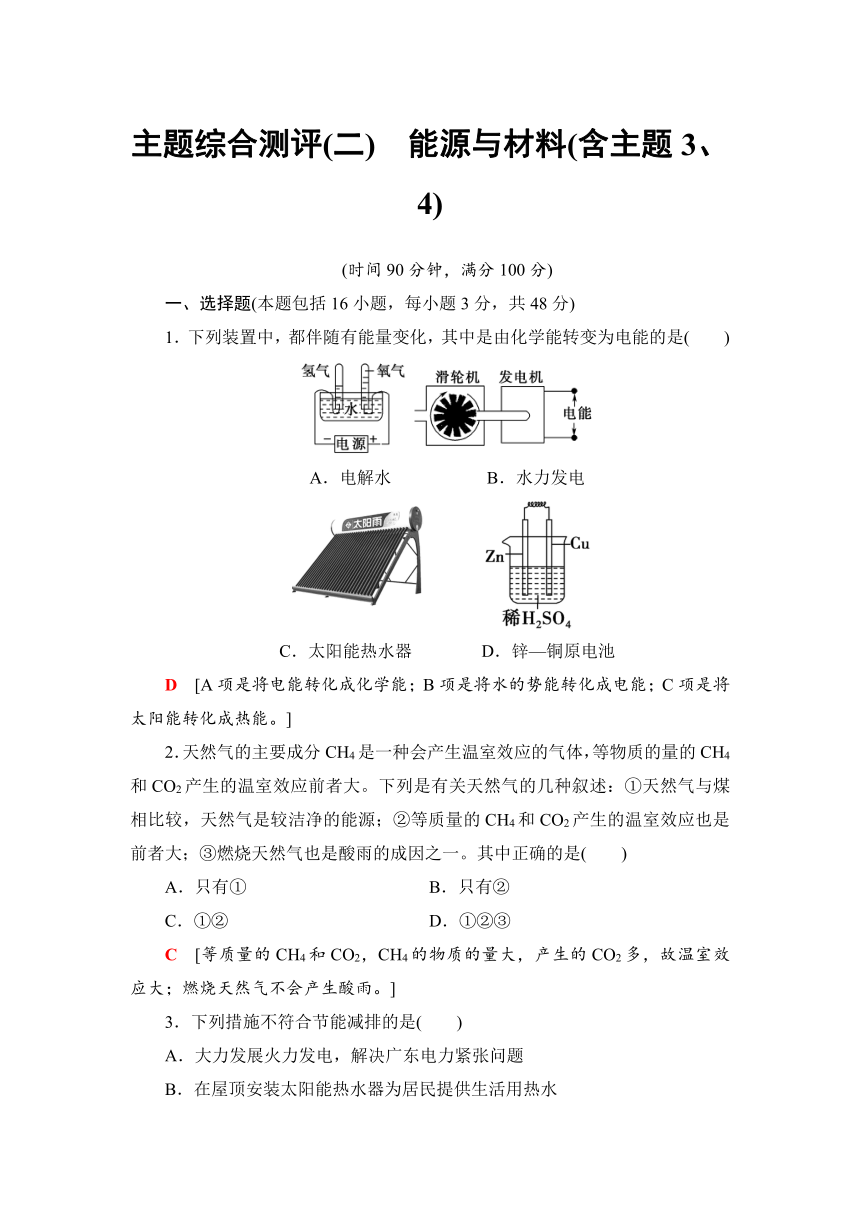
1.下列装置中,都伴随有能量变化,其中是由化学能转变为电能的是( )
A.电解水 B.水力发电
C.太阳能热水器 D.锌—铜原电池
D [A项是将电能转化成化学能;B项是将水的势能转化成电能;C项是将太阳能转化成热能。]
2.天然气的主要成分CH4是一种会产生温室效应的气体,等物质的量的CH4和CO2产生的温室效应前者大。下列是有关天然气的几种叙述:①天然气与煤相比较,天然气是较洁净的能源;②等质量的CH4和CO2产生的温室效应也是前者大;③燃烧天然气也是酸雨的成因之一。其中正确的是( )
A.只有① B.只有②
C.①② D.①②③
C [等质量的CH4和CO2,CH4的物质的量大,产生的CO2多,故温室效应大;燃烧天然气不会产生酸雨。]
3.下列措施不符合节能减排的是( )
A.大力发展火力发电,解决广东电力紧张问题
B.在屋顶安装太阳能热水器为居民提供生活用热水
C.用石灰对燃烧后形成的烟气脱硫,并回收石膏
D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
A [大力发展火力发电,会大量增加燃煤消耗,加重环境污染。]
4.汽油是多种烃类的混合物。在汽车的发动机中,汽油汽化后与进入汽缸的空气按一定比例混合,在引擎的电火花点燃下燃烧,产生大量热能,但进入汽缸的空气过少或过多都将在汽车尾气中产生有害的大气污染物。目前正在研究和开发的一种催化式排气净化器,是以Pt—Rh及CuO—Cr2O3做主体催化剂,它可将80%以上的有害尾气转化成无毒气体。但汽油中为增强其抗震性而添加的Pb(C2H5)4会使这种转化明显降低。汽缸中空气进量过少或过多时,产生的主要有害气体依次是( )
A.气态烃和NO、NO2等
B.CO、气态烃和NO、NO2等
C.CO和CO2
D.气态烃和CO2
B [空气过少,碳不完全燃烧产生CO;空气过多,N元素被氧化为氮氧化物。]
5.下列烷烃含量越高,汽油品质越好的是( )
A.CH3(CH2)6CH3
B.CH3CH(CH3)CH2CH2CH3
C.(CH3)2CHCH2C(CH3)3
D.CH3(CH2)14CH3
C [汽油所含分子支链多的链烃、芳香烃、环烷烃的比例越高,它的抗爆震性越好;所含直链烃分子越多,抗爆震性越差。]
6.甲醇燃料电池被广泛应用于电动汽车的动力来源,下列说法不正确的是( )
A.负极通入甲醇
B.正极通入氧气或空气
C.无污染物质生成
D.甲醇燃料电池的能量利用率比甲醇燃烧的能量利用率小
D [甲醇燃料电池的能量利用率比甲醇燃烧的能量利用率大。]
7.下列关于煤、石油和天然气的说法正确的是( )
A.煤的干馏是将煤在空气中加强热使之分解的过程
B.煤的气化是将其通过物理变化转化为气态的过程
C.天然气除了作燃料之外,还可用于合成氨和生产甲醇
D.石油分馏可获得乙酸、苯及其衍生物
C [煤的干馏是在隔绝空气的条件下加强热分解的过程,A项错误;煤的气化是碳与水蒸气发生化学反应,生成水煤气的过程,B项错误;石油分馏可得到石油气、汽油、煤油、柴油和重油等,D项错误。]
8.下列叙述正确的是( )
①原电池是把化学能转化成电能的一种装置
②原电池的正极发生氧化反应,负极发生还原反应
③不能自发进行的氧化还原反应,通过原电池的装置均可以实现
④碳棒不能用来作原电池的电极
⑤反应Cu+2Ag+===2Ag+Cu2+,能以原电池的形式来实现
A.①⑤ B.①④⑤
C.②③④ D.②⑤
A [原电池中化学能转化为电能,①正确;原电池中负极上发生氧化反应,正极上发生还原反应,②不正确;原电池中发生的反应必须是能自发进行的氧化还原反应,③不正确;碳棒是常用的电极材料,可用来作原电池的电极,④不正确;反应Cu+2Ag+===2Ag+Cu2+能自发发生,能以原电池反应来实现,⑤正确。]
9.在洗衣粉中加入蛋白酶,可以提高对血渍、奶渍等蛋白质污物的去污能力,下列原料制成的纺织品不能用加酶洗衣粉洗涤的是( )
①羊毛衫 ②棉制品 ③腈纶制品 ④真丝制品
A.①② B.②③
C.③④ D.①④
D [“加酶洗衣粉”中的酶是一种碱性蛋白酶的生物催化剂,能“消化”蛋白质,而羊毛衫和真丝制品的主要化学成分就是蛋白质,酶对它们也有作用。所以羊毛衫和真丝制品不能用加酶洗衣粉洗涤。]
10.激光技术利用了宝石中的( )
A.金刚石 B.珍珠
C.金刚砂 D.红宝石
D [宝石除了用来加工工艺品和首饰外,在其他方面也应用广泛,其中用于激光技术的是红宝石。]
11.下列说法中错误的是( )
A.珍珠遇到酸或碱时会发生化学变化,因此要注意对珍珠饰品的保养
B.红宝石含有微量的Cr元素;蓝宝石中含有微量的Fe元素和Ti元素
C.将孔雀石燃烧可得CuO固体
D.HCl溶于水,共价键被破坏,Na2O2溶于水仅破坏了共价键
D [珍珠遇酸或碱会发生化学变化;红宝石中含Cr元素,蓝宝石含有微量的Fe元素和Ti元素;孔雀石燃烧的主要反应为Cu2(OH)2CO32CuO+CO2↑+H2O;HCl溶于水,共价键被破坏,Na2O2溶于水后,不仅共价键被破坏,离子键也被破坏。]
12.根据普通玻璃、普通水泥和普通陶瓷的生产过程,总结出硅酸盐工业的一般特点是( )
①原料一定是含硅元素的物质 ②生成物是硅酸盐
③反应条件是高温 ④发生复杂的物理、化学反应
A.只有①② B.只有①②③
C.只有①③④ D.①②③④
D [水泥和陶瓷的生产原料均用黏土,而玻璃用SiO2,均含Si元素;反应条件均为高温;反应产物均为硅酸盐产品;变化过程均为复杂的物理、化学变化。答案为D。]
13.下列叙述不正确的是( )
A.从石灰窑、玻璃熔炉出来的气体的主要成分相同
B.用石灰抹墙和用水泥砌墙过程的硬化原理相同
C.玻璃、陶瓷、水泥容器均不能贮存氢氟酸
D.熔融烧碱不能用瓷坩埚,也不能用刚玉坩埚
B [A中气体主要成分均是CO2,C中的物质均能和氢氟酸反应,D中瓷坩埚成分中有SiO2,刚玉的成分是Al2O3均能和NaOH反应。]
14.为了防止钢铁锈蚀,下列防护方法中正确的是( )
A.在精密机床的铁床上安装铜螺钉
B.在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中
C.在海轮舷上用铁丝系住锌板浸在海水里
D.在地下输油的铸铁管上接直流电源的正极
C [金属防护方法中被保护金属作原电池的正极,或作电解池的阴极即接电源负极,均可达到防护的目的。]
15. “神舟七号”回收伞(如图)不同于普通的航空伞,它是采用强度高、重量轻、缓冲性好的特制涤纶材料制成的,伞撑开的面积有1 200平方米。下列关于涤纶材料的说法中不正确的是( )
A.涤纶属于高分子材料
B. “神舟七号”回收伞用的这种涤纶材料耐高温
C.涤纶属于合成橡胶
D.合成涤纶的反应属于聚合反应
C [涤纶属于合成纤维,不属于合成橡胶。]
16.下列说法中,正确的是( )
A.利用衣料纤维的热塑性对服装熨烫定型
B.将铜块焊接在轮船水面下的船体上,以达轮船防腐目的
C.保存水玻璃溶液时应将其密闭放在磨口玻璃塞的细口瓶内
D.在自行车圈、车把等处镀铬的主要目的是起美观作用
A [铜与铁在电解质溶液中接触时,形成原电池,铁将被腐蚀,不但不能保护船体,而且腐蚀更快了;水玻璃有黏性,可导致玻璃塞与瓶颈粘连,无法打开;镀铬的主要目的是防止内部铁受到腐蚀,同时起美观作用。]
二、非选择题(本题包括6小题,共52分)
17.(8分)下图是某衣服的标签,根据标签回答:
(1)该布料为______________(填“纯棉”“混纺”或“纯涤纶”)。
(2)该布料的洗涤方式为
______________________________________________________________。
(3)该衣服的熨烫方式为
______________________________________________________________。
(4)注意问题:①晾干方式
______________________________________________________________,
②能否漂白________________。
【解析】 (1)纯棉与化纤混合纺织而成的布料属于混纺。
(2)该布料洗涤时,水温不超过30 ℃(由标签信息推知)。
(3)由标签信息可知该布料熨烫方式为蒸汽熨烫。
(4)注意问题可由标签信息获得。
【答案】 (1)混纺 (2)30 ℃水洗,不宜拧干 (3)蒸汽低温轻烫 (4)低温晾干 不能
18.(5分)用短线把下列正确关系连接起来。
纺织纤维 种类 种类
(1)羊毛
(2)棉、麻 ①动物纤维
(3)丝 a.化学纤维 ②植物纤维
(4)锦纶 b.天然纤维 ③人造纤维
(5)涤纶 ④合成纤维
(6)黏胶纤维
【答案】 (1)b① (2)b② (3)b① (4)a④ (5)a④ (6)a③
19.(10分)汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物有:CmHn(烃)、SO2、NOx、CO和C等,请回答下列有关问题。
(1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为______________________________________________________________
______________________________________________________________,
汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由________能转化为________能,最终转化为机械能。
(2)通过车用燃油的精炼加工处理,可减少汽车尾气中的________________(填化学式)排放。
(3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下NOx与CO反应的化学方程式______________________________________________________________
______________________________________________________________。
(4)控制城市空气污染源的方法可以有________。
A.开发新能源 B.使用电动车
C.植树造林 D.戴上呼吸面具
【解析】 (1)CmHn完全燃烧生成CO2和H2O,并放出热量。
(2)化石燃料汽油中含有一定量的硫,在加工过程中可脱去,以减少汽车尾气中的SO2。
(3)NOx与CO反应生成N2和CO2。
(4)开发新能源和使用电动车可以从源头上减少污染气体的排放,而植树造林和戴上呼吸面具不能减少污染气体的排放,只能减小其危害程度。
【答案】 (1)4CmHn+(4m+n)O24mCO2+2nH2O 化学 热
(2)SO2
(3)2NOx+2xCON2+2xCO2
(4)AB
20.(8分)现在城市使用的燃料大多是煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,由煤炭与水(蒸气)反应制得,故又称水煤气。
(1)试写出制取煤气的主要化学方程式:______________________________________________________________。
(2)已知在常温下,1 mol丙烷(C3H8)完全燃烧放出2 220.0 kJ热量;1 mol CO完全燃烧放出282.57 kJ热量;1 mol H2完全燃烧放出285.8 kJ热量。试比较:
①相同质量的丙烷和氢气燃烧,产生热量的比值为________。
②相同条件下,相同体积的丙烷和CO完全燃烧产生热量的比值为________。
(3)氢气是未来的理想能源,除产生的热量大之外,还具有的优点是
______________________________________________________________
______________________________________________________________。
【解析】 (1)制取水煤气的主要化学方程式为:C+H2O(g)CO+H2。
(2)①设丙烷和H2的质量都为x,则燃烧时产生的热量的比值为C3H8∶H2=(×2 220.0)∶(×285.8)≈1∶2.83。
②相同条件下,相同体积的丙烷和CO物质的量相同,完全燃烧时放出的热量比值为2 220.0∶282.57≈8∶1。
(3)氢气是未来的理想能源,其优点有三:一是产生的热量多,二是来源广泛,三是产物无污染。
【答案】 (1)C+H2O(g)CO+H2
(2)①1∶2.83 ②8∶1
(3)来源广泛、产物无污染
21.(12分)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为_____________________________________。
(2)B中Sn极的电极反应式为______________________________________。
Sn极附近溶液的pH________(填“增大”“减小”或“不变”)。
(3)C中被腐蚀的金属是________,总反应方程式为__________________
______________________________________________________________。
比较A、B、C中Fe被腐蚀的速率,由快到慢的顺序是
________________________。
【解析】 A中直接发生置换反应,B、C都是形成原电池的装置,B中Fe做负极,Sn极上发生还原反应:2H++2e-===H2↑,C中Zn做负极被腐蚀,Fe做正极被保护。
【答案】 (1)Fe+2H+===Fe2++H2↑
(2)2H++2e-===H2↑ 增大
(3)Zn Zn+H2SO4===ZnSO4+H2↑ B、A、C
22.(9分)上海世博实现了环保世博、生态世博的目标,如日本馆的超轻“膜结构”,能发电,会呼吸;澳大利亚馆外表覆盖着比不锈钢更便宜耐用的“耐候钢”。
(1)上海世博会中国馆“东方之冠”的主体结构是用国产Q460钢制成的。下列有关Q460钢的性质中,属于化学性质的是________。
A.强度高 B.能导电
C.耐腐蚀 D.抗震性好
(2)“耐候钢”看起来有些锈迹斑斑,再仔细一瞧却是光滑如新,这得益于“耐候钢”在大气中具有优良的抗腐蚀性能。请你列举两种防止铁制品被腐蚀的方法______________________________________________________________
______________________________________________________________
______________________________________________________________。
(3)石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是________(填化学式);有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种________(填“橡胶”“纤维”或“塑料”)。
(4)日本馆的超轻“膜结构”,这层膜白天能透过阳光,利用太阳能发电,从而实现了将________转化为______________________________________________________________。
【解析】 (1)钢铁耐腐蚀,属于它的化学性质。
(2)可对铁制品表面进行处理生成一层致密的氧化膜、刷油漆、电镀或采用外加电流的阴极保护法等。
(3)石英玻璃的主要成分为SiO2,有机玻璃是一种塑料材料。
(4)利用太阳能发电,是将太阳能转化成电能。
【答案】 (1)C (2)对铁器表面进行处理生成一层致密的氧化膜、刷油漆、电镀、外加电流的阴极保护法(合理即可) (3)SiO2 塑料 (4)太阳能 电能
(时间90分钟,满分100分)
一、选择题(本题包括16小题,每小题3分,共48分)
1.下列装置中,都伴随有能量变化,其中是由化学能转变为电能的是( )
A.电解水 B.水力发电
C.太阳能热水器 D.锌—铜原电池
D [A项是将电能转化成化学能;B项是将水的势能转化成电能;C项是将太阳能转化成热能。]
2.天然气的主要成分CH4是一种会产生温室效应的气体,等物质的量的CH4和CO2产生的温室效应前者大。下列是有关天然气的几种叙述:①天然气与煤相比较,天然气是较洁净的能源;②等质量的CH4和CO2产生的温室效应也是前者大;③燃烧天然气也是酸雨的成因之一。其中正确的是( )
A.只有① B.只有②
C.①② D.①②③
C [等质量的CH4和CO2,CH4的物质的量大,产生的CO2多,故温室效应大;燃烧天然气不会产生酸雨。]
3.下列措施不符合节能减排的是( )
A.大力发展火力发电,解决广东电力紧张问题
B.在屋顶安装太阳能热水器为居民提供生活用热水
C.用石灰对燃烧后形成的烟气脱硫,并回收石膏
D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
A [大力发展火力发电,会大量增加燃煤消耗,加重环境污染。]
4.汽油是多种烃类的混合物。在汽车的发动机中,汽油汽化后与进入汽缸的空气按一定比例混合,在引擎的电火花点燃下燃烧,产生大量热能,但进入汽缸的空气过少或过多都将在汽车尾气中产生有害的大气污染物。目前正在研究和开发的一种催化式排气净化器,是以Pt—Rh及CuO—Cr2O3做主体催化剂,它可将80%以上的有害尾气转化成无毒气体。但汽油中为增强其抗震性而添加的Pb(C2H5)4会使这种转化明显降低。汽缸中空气进量过少或过多时,产生的主要有害气体依次是( )
A.气态烃和NO、NO2等
B.CO、气态烃和NO、NO2等
C.CO和CO2
D.气态烃和CO2
B [空气过少,碳不完全燃烧产生CO;空气过多,N元素被氧化为氮氧化物。]
5.下列烷烃含量越高,汽油品质越好的是( )
A.CH3(CH2)6CH3
B.CH3CH(CH3)CH2CH2CH3
C.(CH3)2CHCH2C(CH3)3
D.CH3(CH2)14CH3
C [汽油所含分子支链多的链烃、芳香烃、环烷烃的比例越高,它的抗爆震性越好;所含直链烃分子越多,抗爆震性越差。]
6.甲醇燃料电池被广泛应用于电动汽车的动力来源,下列说法不正确的是( )
A.负极通入甲醇
B.正极通入氧气或空气
C.无污染物质生成
D.甲醇燃料电池的能量利用率比甲醇燃烧的能量利用率小
D [甲醇燃料电池的能量利用率比甲醇燃烧的能量利用率大。]
7.下列关于煤、石油和天然气的说法正确的是( )
A.煤的干馏是将煤在空气中加强热使之分解的过程
B.煤的气化是将其通过物理变化转化为气态的过程
C.天然气除了作燃料之外,还可用于合成氨和生产甲醇
D.石油分馏可获得乙酸、苯及其衍生物
C [煤的干馏是在隔绝空气的条件下加强热分解的过程,A项错误;煤的气化是碳与水蒸气发生化学反应,生成水煤气的过程,B项错误;石油分馏可得到石油气、汽油、煤油、柴油和重油等,D项错误。]
8.下列叙述正确的是( )
①原电池是把化学能转化成电能的一种装置
②原电池的正极发生氧化反应,负极发生还原反应
③不能自发进行的氧化还原反应,通过原电池的装置均可以实现
④碳棒不能用来作原电池的电极
⑤反应Cu+2Ag+===2Ag+Cu2+,能以原电池的形式来实现
A.①⑤ B.①④⑤
C.②③④ D.②⑤
A [原电池中化学能转化为电能,①正确;原电池中负极上发生氧化反应,正极上发生还原反应,②不正确;原电池中发生的反应必须是能自发进行的氧化还原反应,③不正确;碳棒是常用的电极材料,可用来作原电池的电极,④不正确;反应Cu+2Ag+===2Ag+Cu2+能自发发生,能以原电池反应来实现,⑤正确。]
9.在洗衣粉中加入蛋白酶,可以提高对血渍、奶渍等蛋白质污物的去污能力,下列原料制成的纺织品不能用加酶洗衣粉洗涤的是( )
①羊毛衫 ②棉制品 ③腈纶制品 ④真丝制品
A.①② B.②③
C.③④ D.①④
D [“加酶洗衣粉”中的酶是一种碱性蛋白酶的生物催化剂,能“消化”蛋白质,而羊毛衫和真丝制品的主要化学成分就是蛋白质,酶对它们也有作用。所以羊毛衫和真丝制品不能用加酶洗衣粉洗涤。]
10.激光技术利用了宝石中的( )
A.金刚石 B.珍珠
C.金刚砂 D.红宝石
D [宝石除了用来加工工艺品和首饰外,在其他方面也应用广泛,其中用于激光技术的是红宝石。]
11.下列说法中错误的是( )
A.珍珠遇到酸或碱时会发生化学变化,因此要注意对珍珠饰品的保养
B.红宝石含有微量的Cr元素;蓝宝石中含有微量的Fe元素和Ti元素
C.将孔雀石燃烧可得CuO固体
D.HCl溶于水,共价键被破坏,Na2O2溶于水仅破坏了共价键
D [珍珠遇酸或碱会发生化学变化;红宝石中含Cr元素,蓝宝石含有微量的Fe元素和Ti元素;孔雀石燃烧的主要反应为Cu2(OH)2CO32CuO+CO2↑+H2O;HCl溶于水,共价键被破坏,Na2O2溶于水后,不仅共价键被破坏,离子键也被破坏。]
12.根据普通玻璃、普通水泥和普通陶瓷的生产过程,总结出硅酸盐工业的一般特点是( )
①原料一定是含硅元素的物质 ②生成物是硅酸盐
③反应条件是高温 ④发生复杂的物理、化学反应
A.只有①② B.只有①②③
C.只有①③④ D.①②③④
D [水泥和陶瓷的生产原料均用黏土,而玻璃用SiO2,均含Si元素;反应条件均为高温;反应产物均为硅酸盐产品;变化过程均为复杂的物理、化学变化。答案为D。]
13.下列叙述不正确的是( )
A.从石灰窑、玻璃熔炉出来的气体的主要成分相同
B.用石灰抹墙和用水泥砌墙过程的硬化原理相同
C.玻璃、陶瓷、水泥容器均不能贮存氢氟酸
D.熔融烧碱不能用瓷坩埚,也不能用刚玉坩埚
B [A中气体主要成分均是CO2,C中的物质均能和氢氟酸反应,D中瓷坩埚成分中有SiO2,刚玉的成分是Al2O3均能和NaOH反应。]
14.为了防止钢铁锈蚀,下列防护方法中正确的是( )
A.在精密机床的铁床上安装铜螺钉
B.在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中
C.在海轮舷上用铁丝系住锌板浸在海水里
D.在地下输油的铸铁管上接直流电源的正极
C [金属防护方法中被保护金属作原电池的正极,或作电解池的阴极即接电源负极,均可达到防护的目的。]
15. “神舟七号”回收伞(如图)不同于普通的航空伞,它是采用强度高、重量轻、缓冲性好的特制涤纶材料制成的,伞撑开的面积有1 200平方米。下列关于涤纶材料的说法中不正确的是( )
A.涤纶属于高分子材料
B. “神舟七号”回收伞用的这种涤纶材料耐高温
C.涤纶属于合成橡胶
D.合成涤纶的反应属于聚合反应
C [涤纶属于合成纤维,不属于合成橡胶。]
16.下列说法中,正确的是( )
A.利用衣料纤维的热塑性对服装熨烫定型
B.将铜块焊接在轮船水面下的船体上,以达轮船防腐目的
C.保存水玻璃溶液时应将其密闭放在磨口玻璃塞的细口瓶内
D.在自行车圈、车把等处镀铬的主要目的是起美观作用
A [铜与铁在电解质溶液中接触时,形成原电池,铁将被腐蚀,不但不能保护船体,而且腐蚀更快了;水玻璃有黏性,可导致玻璃塞与瓶颈粘连,无法打开;镀铬的主要目的是防止内部铁受到腐蚀,同时起美观作用。]
二、非选择题(本题包括6小题,共52分)
17.(8分)下图是某衣服的标签,根据标签回答:
(1)该布料为______________(填“纯棉”“混纺”或“纯涤纶”)。
(2)该布料的洗涤方式为
______________________________________________________________。
(3)该衣服的熨烫方式为
______________________________________________________________。
(4)注意问题:①晾干方式
______________________________________________________________,
②能否漂白________________。
【解析】 (1)纯棉与化纤混合纺织而成的布料属于混纺。
(2)该布料洗涤时,水温不超过30 ℃(由标签信息推知)。
(3)由标签信息可知该布料熨烫方式为蒸汽熨烫。
(4)注意问题可由标签信息获得。
【答案】 (1)混纺 (2)30 ℃水洗,不宜拧干 (3)蒸汽低温轻烫 (4)低温晾干 不能
18.(5分)用短线把下列正确关系连接起来。
纺织纤维 种类 种类
(1)羊毛
(2)棉、麻 ①动物纤维
(3)丝 a.化学纤维 ②植物纤维
(4)锦纶 b.天然纤维 ③人造纤维
(5)涤纶 ④合成纤维
(6)黏胶纤维
【答案】 (1)b① (2)b② (3)b① (4)a④ (5)a④ (6)a③
19.(10分)汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物有:CmHn(烃)、SO2、NOx、CO和C等,请回答下列有关问题。
(1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为______________________________________________________________
______________________________________________________________,
汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由________能转化为________能,最终转化为机械能。
(2)通过车用燃油的精炼加工处理,可减少汽车尾气中的________________(填化学式)排放。
(3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下NOx与CO反应的化学方程式______________________________________________________________
______________________________________________________________。
(4)控制城市空气污染源的方法可以有________。
A.开发新能源 B.使用电动车
C.植树造林 D.戴上呼吸面具
【解析】 (1)CmHn完全燃烧生成CO2和H2O,并放出热量。
(2)化石燃料汽油中含有一定量的硫,在加工过程中可脱去,以减少汽车尾气中的SO2。
(3)NOx与CO反应生成N2和CO2。
(4)开发新能源和使用电动车可以从源头上减少污染气体的排放,而植树造林和戴上呼吸面具不能减少污染气体的排放,只能减小其危害程度。
【答案】 (1)4CmHn+(4m+n)O24mCO2+2nH2O 化学 热
(2)SO2
(3)2NOx+2xCON2+2xCO2
(4)AB
20.(8分)现在城市使用的燃料大多是煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,由煤炭与水(蒸气)反应制得,故又称水煤气。
(1)试写出制取煤气的主要化学方程式:______________________________________________________________。
(2)已知在常温下,1 mol丙烷(C3H8)完全燃烧放出2 220.0 kJ热量;1 mol CO完全燃烧放出282.57 kJ热量;1 mol H2完全燃烧放出285.8 kJ热量。试比较:
①相同质量的丙烷和氢气燃烧,产生热量的比值为________。
②相同条件下,相同体积的丙烷和CO完全燃烧产生热量的比值为________。
(3)氢气是未来的理想能源,除产生的热量大之外,还具有的优点是
______________________________________________________________
______________________________________________________________。
【解析】 (1)制取水煤气的主要化学方程式为:C+H2O(g)CO+H2。
(2)①设丙烷和H2的质量都为x,则燃烧时产生的热量的比值为C3H8∶H2=(×2 220.0)∶(×285.8)≈1∶2.83。
②相同条件下,相同体积的丙烷和CO物质的量相同,完全燃烧时放出的热量比值为2 220.0∶282.57≈8∶1。
(3)氢气是未来的理想能源,其优点有三:一是产生的热量多,二是来源广泛,三是产物无污染。
【答案】 (1)C+H2O(g)CO+H2
(2)①1∶2.83 ②8∶1
(3)来源广泛、产物无污染
21.(12分)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为_____________________________________。
(2)B中Sn极的电极反应式为______________________________________。
Sn极附近溶液的pH________(填“增大”“减小”或“不变”)。
(3)C中被腐蚀的金属是________,总反应方程式为__________________
______________________________________________________________。
比较A、B、C中Fe被腐蚀的速率,由快到慢的顺序是
________________________。
【解析】 A中直接发生置换反应,B、C都是形成原电池的装置,B中Fe做负极,Sn极上发生还原反应:2H++2e-===H2↑,C中Zn做负极被腐蚀,Fe做正极被保护。
【答案】 (1)Fe+2H+===Fe2++H2↑
(2)2H++2e-===H2↑ 增大
(3)Zn Zn+H2SO4===ZnSO4+H2↑ B、A、C
22.(9分)上海世博实现了环保世博、生态世博的目标,如日本馆的超轻“膜结构”,能发电,会呼吸;澳大利亚馆外表覆盖着比不锈钢更便宜耐用的“耐候钢”。
(1)上海世博会中国馆“东方之冠”的主体结构是用国产Q460钢制成的。下列有关Q460钢的性质中,属于化学性质的是________。
A.强度高 B.能导电
C.耐腐蚀 D.抗震性好
(2)“耐候钢”看起来有些锈迹斑斑,再仔细一瞧却是光滑如新,这得益于“耐候钢”在大气中具有优良的抗腐蚀性能。请你列举两种防止铁制品被腐蚀的方法______________________________________________________________
______________________________________________________________
______________________________________________________________。
(3)石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是________(填化学式);有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种________(填“橡胶”“纤维”或“塑料”)。
(4)日本馆的超轻“膜结构”,这层膜白天能透过阳光,利用太阳能发电,从而实现了将________转化为______________________________________________________________。
【解析】 (1)钢铁耐腐蚀,属于它的化学性质。
(2)可对铁制品表面进行处理生成一层致密的氧化膜、刷油漆、电镀或采用外加电流的阴极保护法等。
(3)石英玻璃的主要成分为SiO2,有机玻璃是一种塑料材料。
(4)利用太阳能发电,是将太阳能转化成电能。
【答案】 (1)C (2)对铁器表面进行处理生成一层致密的氧化膜、刷油漆、电镀、外加电流的阴极保护法(合理即可) (3)SiO2 塑料 (4)太阳能 电能
