第二节 铁的冶炼 合金(第一课时)[上学期]
文档属性
| 名称 | 第二节 铁的冶炼 合金(第一课时)[上学期] |
|
|
| 格式 | rar | ||
| 文件大小 | 11.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-12-23 00:00:00 | ||
图片预览

文档简介
第二节 铁的冶炼 合金(第一课时)
【学习目标】
知识与技能:1、学会用实验的方法将氧化铁中的铁还原出来;
2、了解工业炼铁的原理、设备、原料。
3、认识金属材料在生产生活和社会发展中的重要作用。
过程与方法:1、通过对工业上铁的冶炼原理的探讨与研究,学会运用知识于实际生活的能力;
2、提高分析和解决实际问题的能力及创新思维能力。
情感、态度与价值观:1、通过对钢铁知识的介绍,培养爱国主义情感;
2、通过对冶铁原理的分析,养成安全操作意识和良好的环保意识。
【学习重点】铁的冶炼原理。
【学习难点】工业炼铁的化学原理。
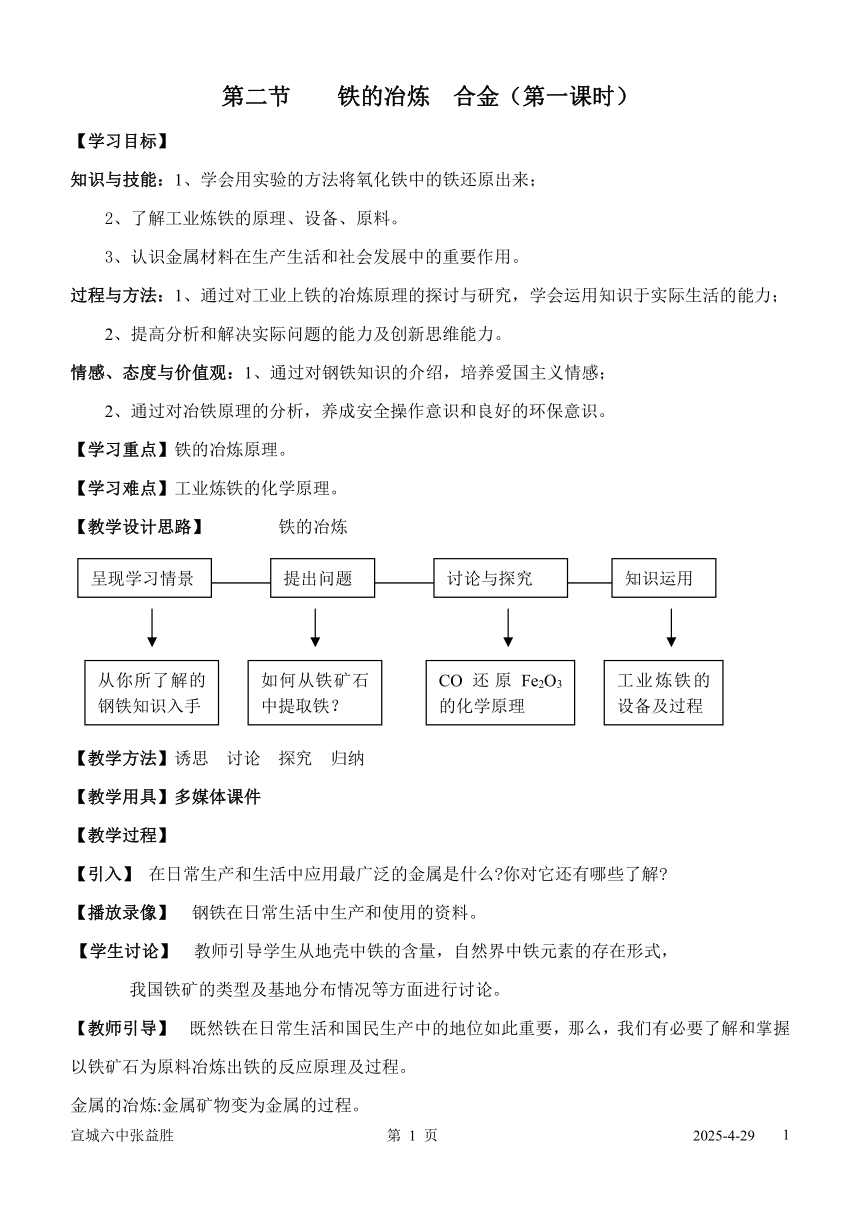
【教学设计思路】 铁的冶炼
【教学方法】诱思 讨论 探究 归纳
【教学用具】多媒体课件
【教学过程】
【引入】 在日常生产和生活中应用最广泛的金属是什么 你对它还有哪些了解
【播放录像】 钢铁在日常生活中生产和使用的资料。
【学生讨论】 教师引导学生从地壳中铁的含量,自然界中铁元素的存在形式,
我国铁矿的类型及基地分布情况等方面进行讨论。
【教师引导】 既然铁在日常生活和国民生产中的地位如此重要,那么,我们有必要了解和掌握以铁矿石为原料冶炼出铁的反应原理及过程。
金属的冶炼:金属矿物变为金属的过程。
【交流与讨论】Fe2O3和Fe的组成上均含有Fe元素,不同之处在于Fe少了O元素,要使Fe2O3转变成Fe ,可从哪些方面入手?
【教师引导】 (1)可在 一定条件下,使Fe2O3直接失氧,转变成铁;
(2)可加入某类物质,让其与Fe2O3中的O元素结合,主动夺取Fe2O3中的“O”元素,使Fe2O3转变成金属Fe。
金属铁的冶炼,是把它们的矿物跟易得氧的物质一起加热反应,以夺氧的方式还原铁的氧化物。通常使用的还原剂是CO。
【动画演示】 CO还原Fe2O3过程及注意事项.
【实验现象】1、红棕色的固体逐渐变成黑色,且能被磁铁吸引; 2、澄清的石灰水变浑浊。
【化学反应】3CO+Fe2O3===2Fe+3CO2 CO2+Ca(OH)2===CaCO3↓+H2O
【学生阅读】 教师引导学生阅读P119页 “观察与思考”中CO与Fe2O3的反应——工业炼铁的反应原理。并思考下列问题:
(1)澄清石灰水的作用是什么?实验中会出现什么现象? (2)尾气如何处理?
(3)实验中为什么要先通一段时间CO,再加热Fe2O3?
(4)实验结束前应如何操作 (5)如何验证实验中产生了铁?
【学生总结】实验步骤:
(1)检查装置的气密性;(2)装入药品并固定;(3)向玻璃管内通入一氧化碳气体;
(4)给氧化铁加热;(5)停止加热;(6)待试管冷却后停止通一氧化碳。
【注意事项】
(1)实验中先通一段时间CO,再加热Fe2O3的目的:排出装置内的空气,以免加热时CO与空气混合,可能会发生爆炸。
(2)实验完毕后继续通一氧化碳的目的防止水倒吸(不撤离CO装置);防止生成的铁重新被氧化(撤离CO装置)。
(3)尾气的成分中含有CO,必须加以处理,方法有: a、用气球收集; b、点燃。
【引入】这是实验室炼铁的过程,那么工业上是如何炼铁的呢 让我们一起走进炼铁厂去看看。参观的过程中请大家注意以下几个小问题,如果有答案的话请举手回答,我们看哪一位同学最先找到问题的答案。
【动画演示】工业高炉炼铁过程。
【播放录像】工业高炉炼铁录像。
【问题】(1)工业炼铁的主要设备是什么?(2)工业炼铁的原料是什么?各原料的作用是什么?
(3)工业炼铁的原理是什么?还原剂是什么?
【学生总结】 1、工业炼铁的主要设备是:高炉。 2、工业炼铁的原料:
(1)铁矿石:提供铁元素;(2)焦炭:a、提供热源、维持炉温;b、制还原剂
(3)石灰石:制造炉渣;(4)空气:提供氧气
2、工业炼铁的原理:3CO+Fe2O3===2Fe+3CO2
在高温条件下,用还原剂一氧化碳从铁的氧化物中将铁还原出来。
【引入】我们已经学习了工业炼铁的原理,那么工业上是如何冶炼其他的金属的呢
【指导阅读】P120“拓展视野”
(1)许多金属的冶炼,是把它们的矿物跟焦炭或氢气、一氧化碳等物质一起加热反应。(如锰、锌、铁、镍、铅等)
(2)有些金属很难从其矿物中提取出来,需用电解的方法。(如铝等)
【图片展示】各种合金在生产中的应用。
【阅读讨论】1、什么是合金? 2、了解课文中提及的几种合金的用途?
3、你还知道哪些合金及其用途? 4、合金的使用对于人类有何意义?
【师生归纳】合金概念:是由一种金属跟其他金属(或非金属)熔合形成的有金属特性的物质。
【播放录像】铝合金、铜合金、不锈钢和形状记忆合金在生产中的应用。
【问题】武得合金与其各组分金属熔点的高低,你能得出什么结论?
【结论】多数合金的熔点低于组成它的成分金属。
【展示】一些常见金属的特性和用途。
【课后探究】 1、你家都有哪些铁制品?你是如何防锈的?
2、调查你家或附近都有哪些合金制品?它们 有什么优良性能?
3、实验室有Cu—Zn合金与Cu—Ag各一份,你能鉴别它们吗?
呈现学习情景
提出问题
讨论与探究
知识运用
从你所了解的钢铁知识入手
如何从铁矿石中提取铁?
CO还原Fe2O3的化学原理
工业炼铁的设备及过程
高温
PAGE
1
宣城六中张益胜 第 1 页 2006-12-22
【学习目标】
知识与技能:1、学会用实验的方法将氧化铁中的铁还原出来;
2、了解工业炼铁的原理、设备、原料。
3、认识金属材料在生产生活和社会发展中的重要作用。
过程与方法:1、通过对工业上铁的冶炼原理的探讨与研究,学会运用知识于实际生活的能力;
2、提高分析和解决实际问题的能力及创新思维能力。
情感、态度与价值观:1、通过对钢铁知识的介绍,培养爱国主义情感;
2、通过对冶铁原理的分析,养成安全操作意识和良好的环保意识。
【学习重点】铁的冶炼原理。
【学习难点】工业炼铁的化学原理。
【教学设计思路】 铁的冶炼
【教学方法】诱思 讨论 探究 归纳
【教学用具】多媒体课件
【教学过程】
【引入】 在日常生产和生活中应用最广泛的金属是什么 你对它还有哪些了解
【播放录像】 钢铁在日常生活中生产和使用的资料。
【学生讨论】 教师引导学生从地壳中铁的含量,自然界中铁元素的存在形式,
我国铁矿的类型及基地分布情况等方面进行讨论。
【教师引导】 既然铁在日常生活和国民生产中的地位如此重要,那么,我们有必要了解和掌握以铁矿石为原料冶炼出铁的反应原理及过程。
金属的冶炼:金属矿物变为金属的过程。
【交流与讨论】Fe2O3和Fe的组成上均含有Fe元素,不同之处在于Fe少了O元素,要使Fe2O3转变成Fe ,可从哪些方面入手?
【教师引导】 (1)可在 一定条件下,使Fe2O3直接失氧,转变成铁;
(2)可加入某类物质,让其与Fe2O3中的O元素结合,主动夺取Fe2O3中的“O”元素,使Fe2O3转变成金属Fe。
金属铁的冶炼,是把它们的矿物跟易得氧的物质一起加热反应,以夺氧的方式还原铁的氧化物。通常使用的还原剂是CO。
【动画演示】 CO还原Fe2O3过程及注意事项.
【实验现象】1、红棕色的固体逐渐变成黑色,且能被磁铁吸引; 2、澄清的石灰水变浑浊。
【化学反应】3CO+Fe2O3===2Fe+3CO2 CO2+Ca(OH)2===CaCO3↓+H2O
【学生阅读】 教师引导学生阅读P119页 “观察与思考”中CO与Fe2O3的反应——工业炼铁的反应原理。并思考下列问题:
(1)澄清石灰水的作用是什么?实验中会出现什么现象? (2)尾气如何处理?
(3)实验中为什么要先通一段时间CO,再加热Fe2O3?
(4)实验结束前应如何操作 (5)如何验证实验中产生了铁?
【学生总结】实验步骤:
(1)检查装置的气密性;(2)装入药品并固定;(3)向玻璃管内通入一氧化碳气体;
(4)给氧化铁加热;(5)停止加热;(6)待试管冷却后停止通一氧化碳。
【注意事项】
(1)实验中先通一段时间CO,再加热Fe2O3的目的:排出装置内的空气,以免加热时CO与空气混合,可能会发生爆炸。
(2)实验完毕后继续通一氧化碳的目的防止水倒吸(不撤离CO装置);防止生成的铁重新被氧化(撤离CO装置)。
(3)尾气的成分中含有CO,必须加以处理,方法有: a、用气球收集; b、点燃。
【引入】这是实验室炼铁的过程,那么工业上是如何炼铁的呢 让我们一起走进炼铁厂去看看。参观的过程中请大家注意以下几个小问题,如果有答案的话请举手回答,我们看哪一位同学最先找到问题的答案。
【动画演示】工业高炉炼铁过程。
【播放录像】工业高炉炼铁录像。
【问题】(1)工业炼铁的主要设备是什么?(2)工业炼铁的原料是什么?各原料的作用是什么?
(3)工业炼铁的原理是什么?还原剂是什么?
【学生总结】 1、工业炼铁的主要设备是:高炉。 2、工业炼铁的原料:
(1)铁矿石:提供铁元素;(2)焦炭:a、提供热源、维持炉温;b、制还原剂
(3)石灰石:制造炉渣;(4)空气:提供氧气
2、工业炼铁的原理:3CO+Fe2O3===2Fe+3CO2
在高温条件下,用还原剂一氧化碳从铁的氧化物中将铁还原出来。
【引入】我们已经学习了工业炼铁的原理,那么工业上是如何冶炼其他的金属的呢
【指导阅读】P120“拓展视野”
(1)许多金属的冶炼,是把它们的矿物跟焦炭或氢气、一氧化碳等物质一起加热反应。(如锰、锌、铁、镍、铅等)
(2)有些金属很难从其矿物中提取出来,需用电解的方法。(如铝等)
【图片展示】各种合金在生产中的应用。
【阅读讨论】1、什么是合金? 2、了解课文中提及的几种合金的用途?
3、你还知道哪些合金及其用途? 4、合金的使用对于人类有何意义?
【师生归纳】合金概念:是由一种金属跟其他金属(或非金属)熔合形成的有金属特性的物质。
【播放录像】铝合金、铜合金、不锈钢和形状记忆合金在生产中的应用。
【问题】武得合金与其各组分金属熔点的高低,你能得出什么结论?
【结论】多数合金的熔点低于组成它的成分金属。
【展示】一些常见金属的特性和用途。
【课后探究】 1、你家都有哪些铁制品?你是如何防锈的?
2、调查你家或附近都有哪些合金制品?它们 有什么优良性能?
3、实验室有Cu—Zn合金与Cu—Ag各一份,你能鉴别它们吗?
呈现学习情景
提出问题
讨论与探究
知识运用
从你所了解的钢铁知识入手
如何从铁矿石中提取铁?
CO还原Fe2O3的化学原理
工业炼铁的设备及过程
高温
PAGE
1
宣城六中张益胜 第 1 页 2006-12-22
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
