金属的防护和回收[上学期]
图片预览


文档简介
课题 金属的防护和回收
(执教:裴锐 单位:淮阴中学 指导:肖红梅)
一、知识提要
1、实验探究钢铁锈蚀的条件
2、防止金属锈蚀的简单方法
3、废金属对环境的污染,回收金属的重要性。
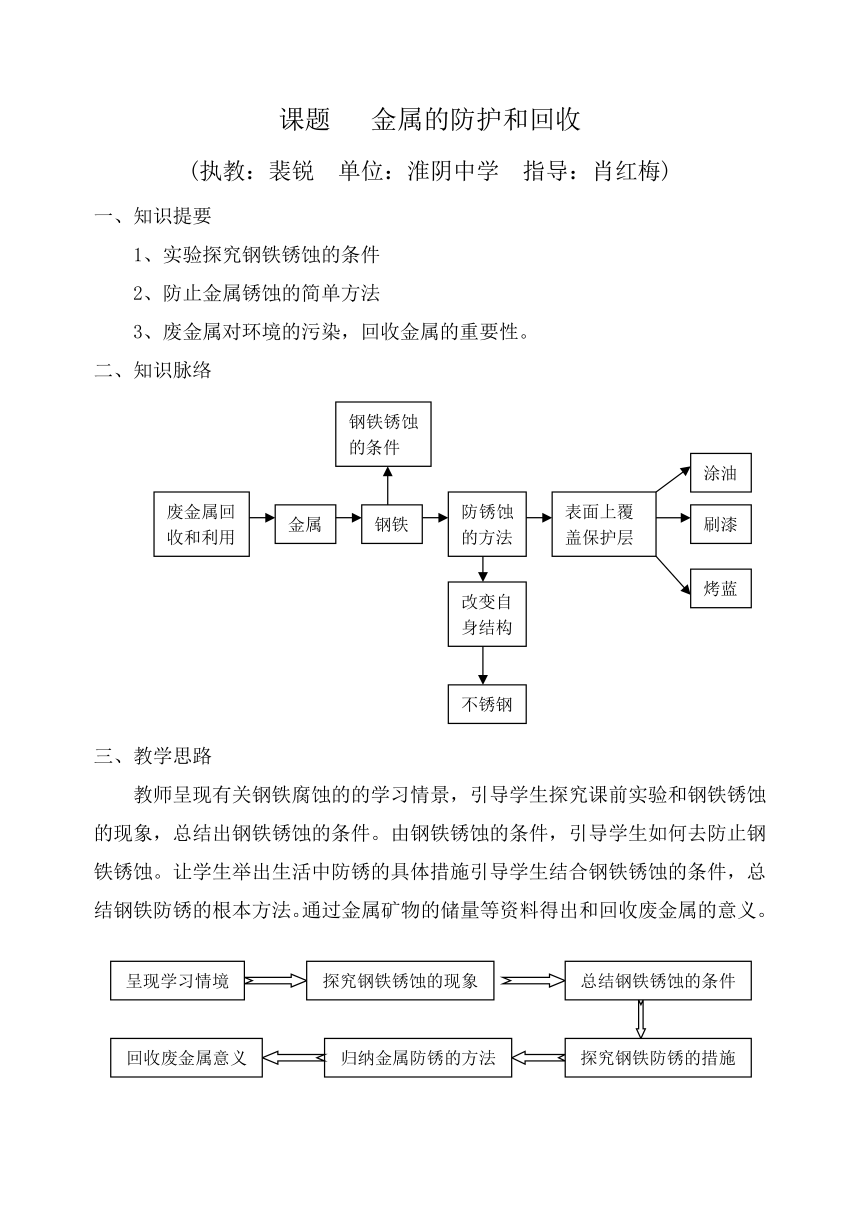
二、知识脉络
三、教学思路
教师呈现有关钢铁腐蚀的的学习情景,引导学生探究课前实验和钢铁锈蚀的现象,总结出钢铁锈蚀的条件。由钢铁锈蚀的条件,引导学生如何去防止钢铁锈蚀。让学生举出生活中防锈的具体措施引导学生结合钢铁锈蚀的条件,总结钢铁防锈的根本方法。通过金属矿物的储量等资料得出和回收废金属的意义。
四、组块设计
组块1 钢铁的锈蚀条件
教师活动 学生活动 提示或建议
【创设情境】 同学们,在日常生活中大家经常见到金属锈蚀的现象。据报道:在英国,每90秒就有1吨钢铁因为锈蚀而废弃,金属锈蚀使英国每年损失约50亿英镑,这个数字比英国政府每年用于中等教育的总和还多。全世界每年由于锈蚀而报废的金属约占世界金属全年产量的20%-40%其中钢铁的锈蚀占金属锈蚀的一半。( 教师用电脑展示上面报道和一些金属锈蚀的图片)【适时发问】读了这则报道你有哪些感想?【及时追问】 既然防止金属锈蚀的意义如此重大,那么我们如何才能防止金属的锈蚀呢?钢铁锈蚀的条件是什么呢?防锈的方法和具体措施有哪些呢?【指导阅读】 教材P136页的活动与探究【友情提示】1、实验中铁钉所处的环境?【及时追问】实验结果如何呢?【拓展提高】通过实验,分析铁打所处环境与结果的比较,说明铁制品生锈的条件是?【板 书】一、铁生锈的条件:同时存在水、氧气,有且酸与盐等物质的存在能使铁在潮湿的空气中生锈速度加快。【讲 解】 铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。铁锈是棕红色固体,主要成分是Fe2O3·xH2O。铁锈是一种疏松多孔的物质。具有吸水性,它能让水分和空气中的氧气穿过它的空隙,不断向里层渗透,继续跟铁反应,直至铁被完全锈蚀。故铁锈反而能加速里层铁的生锈。 【观察与思考】学生观察电脑投影的材料【交流与讨论】 1、金属锈蚀造成的损失太大了。 2、防止金属的锈蚀太重要了。【汇报与交流】活动与探究的内容(要求学生提前一周做,并记录实验的现象和结论)【归纳小结】 试管①:铁钉所处的介质是酸、水、氧气。试管②:铁钉所处的介质是氯化钠、水、氧气。试管③:铁钉所处的介质是水、氧气。试管④:铁钉所处的介质是水(迅速冷却的沸水中氧气极少)试管⑤:铁钉所处的介质是氧气(生石灰或无水氯化钙是干燥剂,除去试管中的水)【归纳小结】试管④⑤没有生锈,而试管②③中铁钉生锈的速度明显快于试管①。【归纳总结】在水、氧气同时存在的环境中(即潮湿的空气中);并且酸与氯化钠等物质的存在能使铁钉在潮湿的空气中生锈速度加快。【归纳记录】(1)颜色状态:棕红色固体,或者称红色固体。(2)主要成份:铁锈是混合物,主要成分是Fe2O3·xH2O(3)结构特点:疏松多孔,铁锈能加速里层铁的生锈。 师生课前要共同准备相关素材和图片教师提出问题,要留给学生充足的时间交流讨论,使学生在互相交流中互相学习,然后汇报结果,培养学生互帮互助的合作精神,并能够清楚地表达自己的观点,激发学生学习的主动性,并使不同层次的学生都在交流中有收获。注意引导学生对比分析问题
评注:
通过创设情境导入金属的锈蚀比较自然,易于激发学生的学习兴趣,增强了学生的责任感和使命感。从学生熟悉的身边现象入手探究铁钉的锈蚀,引导他们发现问题,分析问题,获得知识和方法。
组块2 防止钢铁锈蚀的方法
教师活动 学生活动 提示或建议
【创设情境】小明在参观博物馆时发现铁制品的文物一般都在我国西北地区干旱地区发掘出来,而雨水充足,古代就很发达的江南地区却很少发掘出铁制文物。你能帮他找到答案吗?【适时发问】 你知道日常生活中有哪些防止钢铁锈蚀的具体措施吗?【及时追问】你能从这些防锈的具体措施中分析出防止锈蚀的基本原理吗?【板 书】 二、防止钢铁锈蚀的方法1、加保护层(具体措施:涂油、刷漆、烤蓝、烤搪瓷、电镀也叫做克罗米等)2、改变金属的结构(具体措施:制成不锈钢)【拓展提高】铝的 “自我保护” 【交流与讨论】学生分小组讨论【汇报与交流】 并不是江南地区不用铁器,而是江南地区雨水充足,埋藏在地下的铁制文物都基本上锈蚀了。【交流与讨论】 (1)用完铁制品后及时擦洗干净,置于干燥的环境。(2)在铁制品表面涂一层油,如机械零件等。(3)在铁制品表面涂上一层油漆,如家用电器、自行车车架、钢窗等。(4)在铁制品表面进行烤蓝、煮黑等处理(在其表面形成一层致密的四氧化三铁薄膜),如锯条、链条等。(5)在铁制品表面镀上一层其他金属,如镀锌、锡、铬等,如自行车车把,钢圈等。(6)制成不锈钢。【交流与讨论】学生分小组讨论【汇报与交流】1、保持钢铁表面的洁净、干燥。最好不与水和氧气接触。2、改善自身的抗腐蚀的能力。【归纳记录】学生纪录,完成笔记。【交流与讨论】学生阅读后分小组讨论汇报结果 可以提示学生从自己的自行车上发现问题注意提醒和要求语言的严密性
评注:
通过学生已有的生活经验入手,引导他们发现问题,分析和解决问题,拉近化学与学生的距离,使学生感受到身边处处有化学,感悟到化学学科的价值和化学学习的意义和方法。
组块3废金属的回收和利用
教师活动 学生活动 提示或建议
【创设情境】资料一:据估计一些矿物可供开采的年限资料二:随着社会进步,人们的生活水平的提高,在日常生活中出现了大量金属废弃物,如废弃的汽车以及电脑、电视机,金属的易拉罐等。资料三:据计算回收一个铝制饮料罐比造一个新饮料罐要便宜20%,1t废钢铁回炉冶炼可炼成近1t钢,跟用铁矿石冶炼比,能节约11t煤和铁矿石,减少污染空气的悬浮微粒11kg。【问题讨论】1、地球上金属矿物的储量是否很丰富?2、废金属的来源?3、废金属能否随意丢弃?应该怎样处理?4、回收废金属的意义?【板 书】三、废金属回收利用1、来源 2、回收的意义 【阅读思考】学生看老师提供的三份资料并阅读课本。【交流与讨论】学生阅读后分小组讨论汇报结果【汇报与交流】 1、金属资源不可再生,随着经济的不断发展,金属资源呈日益短缺之势,故保护金属资源人人有责。2、废金属是指冶金工业、金属加工业及家庭丢弃的金属碎块、碎屑,锈蚀和报废的金属物品等。3、废金属不能随意丢弃,否则不仅造成资源浪费,还会污染环境,所以必须回收和经处理后,重新利用。4、节约矿物资源,节约能源,保护环境,给带来巨大的经济效益。 让学生充分讨论材料并结合课本培养学生自主学习的能力
评注:
现代高素质的社会公民的标志之一,是具有较强的资源观和环保的理念。通过本部分知识的学习,力求促进学生树立科学的资源观和环保理念。
五、参考资料
金属的防腐
根据腐蚀机理和不同环境,金属主要有以下几种防腐方法:
(1)改变金属的成分,提高材料本身的抗腐能力。如在冶炼金属时加入一些合金元素(如镍、铬、硅、锰、钛、钨、钼、钒、稀土等),铁与这些元素结合,可增强抗蚀性能,不锈钢就是如此。此外,利用热处理或渗铬、渗铝、渗氮等来改变金属的内部结构,或使金属产生一层抗蚀性能很强的表面。
(2)用耐腐蚀材料覆盖金属表面。可以用辗压、浸镀、喷镀、电镀和化学镀等方法在金属器件的表面覆盖耐腐蚀的金属层。这种金属覆盖层分为两类:一类是阳极保护层,它用的金属材料电位比主体金属要低,如在铁上镀锌、镉等。另一类是阴极保护层,其电位比主体金属高,比被保护的金属更耐腐蚀,如在钢铁上镀镍,在熟铁上镀锡等;也可以用非金属材料覆盖金属表面,非金属覆盖材料有涂料、塑料、硬橡胶、搪瓷、沥青等;还可以用磷化、发蓝、氧化等方法处理金属表面,然后用浸油或刷漆等方法将转化层的微小孔隙封闭。
(3)电化学保护。电化学保护有阴极保护和阳极保护两种。阴极保护即用电极电位较低的金属与被保护金属接触,使被保护金属表面成阴极而不被腐蚀。阳极保护即用外加电流使被保护的金属表面产生阳极极化,电位变正,达到钝化状态而不被腐蚀。
(4)改善腐蚀环境。即在介质中加入某些缓蚀剂,以改善腐蚀介质的腐蚀作用。例如,用亚硫酸钠除去水中溶解的氧,可防止锅炉腐蚀。常用的缓蚀剂还有重铬酸钾、硅酸钠、尿素、苯甲酸钠、石油、磺酸类、酯类、羧酸和羧酸皂等。
除采用各种防腐措施外,在金属材料的保管中应做到:选择远离有害气体和粉尘的场地或库房;保持库房干燥,妥善码垛和密封;保护金属材料的防护层或包装不受损坏,保持清洁等。
六、相关链接
1.期刊:中学化学《新课程典型案例》赵宁等
上海教育出版社教材及教师指导用书
2.网站:
中学化学教育资源网
课件中心网
废金属回
收和利用
表面上覆
盖保护层
防锈蚀的方法
金属
钢铁
呈现学习情境
探究钢铁锈蚀的现象
总结钢铁锈蚀的条件
探究钢铁防锈的措施
归纳金属防锈的方法
回收废金属意义
钢铁锈蚀的条件
改变自
身结构
涂油
刷漆
烤蓝
不锈钢
(执教:裴锐 单位:淮阴中学 指导:肖红梅)
一、知识提要
1、实验探究钢铁锈蚀的条件
2、防止金属锈蚀的简单方法
3、废金属对环境的污染,回收金属的重要性。
二、知识脉络
三、教学思路
教师呈现有关钢铁腐蚀的的学习情景,引导学生探究课前实验和钢铁锈蚀的现象,总结出钢铁锈蚀的条件。由钢铁锈蚀的条件,引导学生如何去防止钢铁锈蚀。让学生举出生活中防锈的具体措施引导学生结合钢铁锈蚀的条件,总结钢铁防锈的根本方法。通过金属矿物的储量等资料得出和回收废金属的意义。
四、组块设计
组块1 钢铁的锈蚀条件
教师活动 学生活动 提示或建议
【创设情境】 同学们,在日常生活中大家经常见到金属锈蚀的现象。据报道:在英国,每90秒就有1吨钢铁因为锈蚀而废弃,金属锈蚀使英国每年损失约50亿英镑,这个数字比英国政府每年用于中等教育的总和还多。全世界每年由于锈蚀而报废的金属约占世界金属全年产量的20%-40%其中钢铁的锈蚀占金属锈蚀的一半。( 教师用电脑展示上面报道和一些金属锈蚀的图片)【适时发问】读了这则报道你有哪些感想?【及时追问】 既然防止金属锈蚀的意义如此重大,那么我们如何才能防止金属的锈蚀呢?钢铁锈蚀的条件是什么呢?防锈的方法和具体措施有哪些呢?【指导阅读】 教材P136页的活动与探究【友情提示】1、实验中铁钉所处的环境?【及时追问】实验结果如何呢?【拓展提高】通过实验,分析铁打所处环境与结果的比较,说明铁制品生锈的条件是?【板 书】一、铁生锈的条件:同时存在水、氧气,有且酸与盐等物质的存在能使铁在潮湿的空气中生锈速度加快。【讲 解】 铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。铁锈是棕红色固体,主要成分是Fe2O3·xH2O。铁锈是一种疏松多孔的物质。具有吸水性,它能让水分和空气中的氧气穿过它的空隙,不断向里层渗透,继续跟铁反应,直至铁被完全锈蚀。故铁锈反而能加速里层铁的生锈。 【观察与思考】学生观察电脑投影的材料【交流与讨论】 1、金属锈蚀造成的损失太大了。 2、防止金属的锈蚀太重要了。【汇报与交流】活动与探究的内容(要求学生提前一周做,并记录实验的现象和结论)【归纳小结】 试管①:铁钉所处的介质是酸、水、氧气。试管②:铁钉所处的介质是氯化钠、水、氧气。试管③:铁钉所处的介质是水、氧气。试管④:铁钉所处的介质是水(迅速冷却的沸水中氧气极少)试管⑤:铁钉所处的介质是氧气(生石灰或无水氯化钙是干燥剂,除去试管中的水)【归纳小结】试管④⑤没有生锈,而试管②③中铁钉生锈的速度明显快于试管①。【归纳总结】在水、氧气同时存在的环境中(即潮湿的空气中);并且酸与氯化钠等物质的存在能使铁钉在潮湿的空气中生锈速度加快。【归纳记录】(1)颜色状态:棕红色固体,或者称红色固体。(2)主要成份:铁锈是混合物,主要成分是Fe2O3·xH2O(3)结构特点:疏松多孔,铁锈能加速里层铁的生锈。 师生课前要共同准备相关素材和图片教师提出问题,要留给学生充足的时间交流讨论,使学生在互相交流中互相学习,然后汇报结果,培养学生互帮互助的合作精神,并能够清楚地表达自己的观点,激发学生学习的主动性,并使不同层次的学生都在交流中有收获。注意引导学生对比分析问题
评注:
通过创设情境导入金属的锈蚀比较自然,易于激发学生的学习兴趣,增强了学生的责任感和使命感。从学生熟悉的身边现象入手探究铁钉的锈蚀,引导他们发现问题,分析问题,获得知识和方法。
组块2 防止钢铁锈蚀的方法
教师活动 学生活动 提示或建议
【创设情境】小明在参观博物馆时发现铁制品的文物一般都在我国西北地区干旱地区发掘出来,而雨水充足,古代就很发达的江南地区却很少发掘出铁制文物。你能帮他找到答案吗?【适时发问】 你知道日常生活中有哪些防止钢铁锈蚀的具体措施吗?【及时追问】你能从这些防锈的具体措施中分析出防止锈蚀的基本原理吗?【板 书】 二、防止钢铁锈蚀的方法1、加保护层(具体措施:涂油、刷漆、烤蓝、烤搪瓷、电镀也叫做克罗米等)2、改变金属的结构(具体措施:制成不锈钢)【拓展提高】铝的 “自我保护” 【交流与讨论】学生分小组讨论【汇报与交流】 并不是江南地区不用铁器,而是江南地区雨水充足,埋藏在地下的铁制文物都基本上锈蚀了。【交流与讨论】 (1)用完铁制品后及时擦洗干净,置于干燥的环境。(2)在铁制品表面涂一层油,如机械零件等。(3)在铁制品表面涂上一层油漆,如家用电器、自行车车架、钢窗等。(4)在铁制品表面进行烤蓝、煮黑等处理(在其表面形成一层致密的四氧化三铁薄膜),如锯条、链条等。(5)在铁制品表面镀上一层其他金属,如镀锌、锡、铬等,如自行车车把,钢圈等。(6)制成不锈钢。【交流与讨论】学生分小组讨论【汇报与交流】1、保持钢铁表面的洁净、干燥。最好不与水和氧气接触。2、改善自身的抗腐蚀的能力。【归纳记录】学生纪录,完成笔记。【交流与讨论】学生阅读后分小组讨论汇报结果 可以提示学生从自己的自行车上发现问题注意提醒和要求语言的严密性
评注:
通过学生已有的生活经验入手,引导他们发现问题,分析和解决问题,拉近化学与学生的距离,使学生感受到身边处处有化学,感悟到化学学科的价值和化学学习的意义和方法。
组块3废金属的回收和利用
教师活动 学生活动 提示或建议
【创设情境】资料一:据估计一些矿物可供开采的年限资料二:随着社会进步,人们的生活水平的提高,在日常生活中出现了大量金属废弃物,如废弃的汽车以及电脑、电视机,金属的易拉罐等。资料三:据计算回收一个铝制饮料罐比造一个新饮料罐要便宜20%,1t废钢铁回炉冶炼可炼成近1t钢,跟用铁矿石冶炼比,能节约11t煤和铁矿石,减少污染空气的悬浮微粒11kg。【问题讨论】1、地球上金属矿物的储量是否很丰富?2、废金属的来源?3、废金属能否随意丢弃?应该怎样处理?4、回收废金属的意义?【板 书】三、废金属回收利用1、来源 2、回收的意义 【阅读思考】学生看老师提供的三份资料并阅读课本。【交流与讨论】学生阅读后分小组讨论汇报结果【汇报与交流】 1、金属资源不可再生,随着经济的不断发展,金属资源呈日益短缺之势,故保护金属资源人人有责。2、废金属是指冶金工业、金属加工业及家庭丢弃的金属碎块、碎屑,锈蚀和报废的金属物品等。3、废金属不能随意丢弃,否则不仅造成资源浪费,还会污染环境,所以必须回收和经处理后,重新利用。4、节约矿物资源,节约能源,保护环境,给带来巨大的经济效益。 让学生充分讨论材料并结合课本培养学生自主学习的能力
评注:
现代高素质的社会公民的标志之一,是具有较强的资源观和环保的理念。通过本部分知识的学习,力求促进学生树立科学的资源观和环保理念。
五、参考资料
金属的防腐
根据腐蚀机理和不同环境,金属主要有以下几种防腐方法:
(1)改变金属的成分,提高材料本身的抗腐能力。如在冶炼金属时加入一些合金元素(如镍、铬、硅、锰、钛、钨、钼、钒、稀土等),铁与这些元素结合,可增强抗蚀性能,不锈钢就是如此。此外,利用热处理或渗铬、渗铝、渗氮等来改变金属的内部结构,或使金属产生一层抗蚀性能很强的表面。
(2)用耐腐蚀材料覆盖金属表面。可以用辗压、浸镀、喷镀、电镀和化学镀等方法在金属器件的表面覆盖耐腐蚀的金属层。这种金属覆盖层分为两类:一类是阳极保护层,它用的金属材料电位比主体金属要低,如在铁上镀锌、镉等。另一类是阴极保护层,其电位比主体金属高,比被保护的金属更耐腐蚀,如在钢铁上镀镍,在熟铁上镀锡等;也可以用非金属材料覆盖金属表面,非金属覆盖材料有涂料、塑料、硬橡胶、搪瓷、沥青等;还可以用磷化、发蓝、氧化等方法处理金属表面,然后用浸油或刷漆等方法将转化层的微小孔隙封闭。
(3)电化学保护。电化学保护有阴极保护和阳极保护两种。阴极保护即用电极电位较低的金属与被保护金属接触,使被保护金属表面成阴极而不被腐蚀。阳极保护即用外加电流使被保护的金属表面产生阳极极化,电位变正,达到钝化状态而不被腐蚀。
(4)改善腐蚀环境。即在介质中加入某些缓蚀剂,以改善腐蚀介质的腐蚀作用。例如,用亚硫酸钠除去水中溶解的氧,可防止锅炉腐蚀。常用的缓蚀剂还有重铬酸钾、硅酸钠、尿素、苯甲酸钠、石油、磺酸类、酯类、羧酸和羧酸皂等。
除采用各种防腐措施外,在金属材料的保管中应做到:选择远离有害气体和粉尘的场地或库房;保持库房干燥,妥善码垛和密封;保护金属材料的防护层或包装不受损坏,保持清洁等。
六、相关链接
1.期刊:中学化学《新课程典型案例》赵宁等
上海教育出版社教材及教师指导用书
2.网站:
中学化学教育资源网
课件中心网
废金属回
收和利用
表面上覆
盖保护层
防锈蚀的方法
金属
钢铁
呈现学习情境
探究钢铁锈蚀的现象
总结钢铁锈蚀的条件
探究钢铁防锈的措施
归纳金属防锈的方法
回收废金属意义
钢铁锈蚀的条件
改变自
身结构
涂油
刷漆
烤蓝
不锈钢
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
