课题 金属的防护和回收[上学期]
图片预览

文档简介
课题 金属的防护和回收
执教者:付明义 单 位:河南省光山县槐店中学 指导者:李竞峰
一、知识提要
1、钢铁的锈蚀条件
2、防止金属锈蚀的简单方法
3、废弃金属对环境的污染、回收金属的重要性
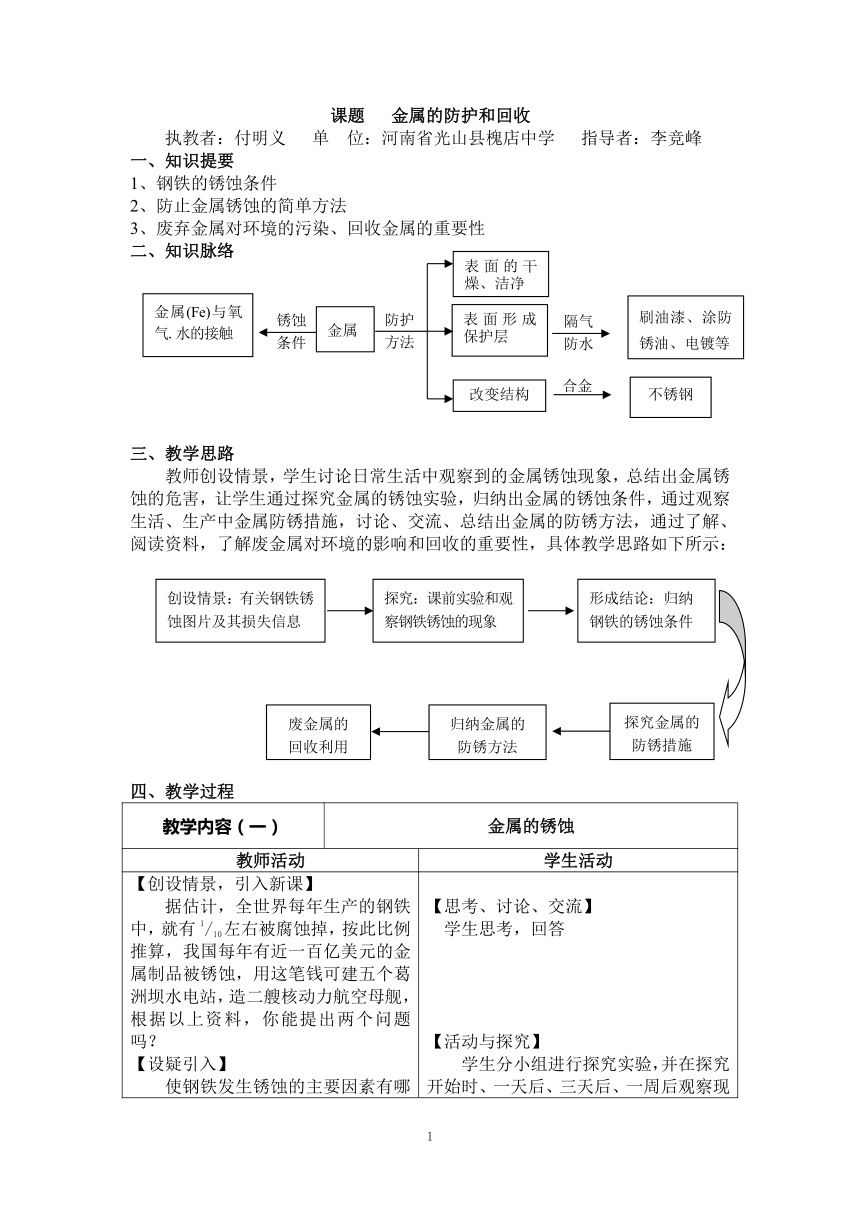
二、知识脉络
三、教学思路
教师创设情景,学生讨论日常生活中观察到的金属锈蚀现象,总结出金属锈蚀的危害,让学生通过探究金属的锈蚀实验,归纳出金属的锈蚀条件,通过观察生活、生产中金属防锈措施,讨论、交流、总结出金属的防锈方法,通过了解、阅读资料,了解废金属对环境的影响和回收的重要性,具体教学思路如下所示:
四、教学过程
教学内容(一) 金属的锈蚀
教师活动 学生活动
【创设情景,引入新课】据估计,全世界每年生产的钢铁中,就有1/10左右被腐蚀掉,按此比例推算,我国每年有近一百亿美元的金属制品被锈蚀,用这笔钱可建五个葛洲坝水电站,造二艘核动力航空母舰,根据以上资料,你能提出两个问题吗?【设疑引入】使钢铁发生锈蚀的主要因素有哪些?(课前一周时间前,指导学生按照教材第126页设计实验方案,指导学生对钢铁生绣的条件进行探究。)教师对学生的实验进行点评【问题引导】根据所做的实验,同学们能分析、总结出使铁钉生锈的主要因素有哪些吗 【归纳总结】引导学生从铁钉所处环境的不同总结出铁生绣的条件。【板书】钢铁的锈蚀条件 【思考、讨论、交流】学生思考,回答【活动与探究】 学生分小组进行探究实验,并在探究开始时、一天后、三天后、一周后观察现象,并做好实验记录。可谈教学中,各小组展示实验报告。 【交流讨论】分组交流、讨论、归纳、总结、小组汇报。【思考、交流、总结】铁在空气的锈蚀,实际上是铁与与氧气,水等物质相互作用,发生生一系列复杂的化学反应,使铁转化为铁的化合物的过程,铁锈主要成分是氧化铁(Fe2O3)。
设计意图:通过几个具体数据和设凝激发学生学习兴趣和欲望,培养学生分析、发现问题的能力。通过观察实验的发生和发展,培养学生观察能力,记录数据书写实验报告的能力,以及严谨的科学态度和合作精神。培养学生分析、归纳总结概括知识的能力和研究问题的科学态度。
教学内容(二) 防止金属锈蚀的方法
教师活动 学生活动
【演示实验、激发兴趣】 在切过咸菜的铁质菜刀同一面上选相近三处进行下列实验: 一处(a处)用湿棉球润湿 另一处(b处)用干布擦干。 第三处(c处)用干布擦干后,涂上一层食用油。放置一昼夜,猜猜菜刀三处表面有何变化?然后展示菜刀【提出问题】 根据以上实验,并结合日常生活中观察,你能总结出防止铁生锈的办法吗?【小结并板书】 钢铁的防锈方法。【创新应用】1、自行车是人们常用的交通工具,请按下列要求,回答问题。 (1)自行车的主要零件是由 (填“生铁”或“钢”)制造的。 (2)请写出自行车上各部分零件都采用了什么防锈方法? (3)被雨水淋湿的自行车能否直接用带油的布擦?为什么?2、如图所示,取一团光亮无锈的铁丝绒,放入一支洁净试管底部,将试管倒放在盛水的烧杯里。数天后,能观察到的现象是 。 【交流、思考、讨论】 学生通过观察实验现象,思考、讨论,分析原因。【交流、讨论】 分组交流、讨论,然后小组汇报同学们讨论的结果。钢铁的防锈方法: (1)保持铁制品表面的干燥和洁净。 (2)在铁制品表面形成保护层,如刷油漆、涂防锈油、镀锡、 铬等金属。 (3)改变铁的内部结构。如不锈钢。【思考、讨论、交流】 在教师的引导下,从铁生绣的条件分析,同学间讨论后回答,解决实际问题。
设计意图:通过对比实验,让学生知道“对比”是一种重要科学方法,并能应用金属锈蚀条件去分析,解决实际问题。通过对比实验和观察日常生活生产中防锈措施,培养学生观察、归纳知识的能力和应用化学知识解决实际问题的能力 。通过练习、培养学生对所学知识的掌握和应用能力。
教学内容(三) 废金属的回收利用
教师活动 学生活动
【创设情景】展示废旧金属的图片,引导学生思考:锈蚀和报废的金属是不是就没有用了呢?能否进行再利用呢?【创设问题】 废旧金属的回收和利用有什么意义呢? 【思考、交流、讨论】学生思考后,同学之间进行交流、讨论。【交流、讨论】 结合阅读教材128~129页,讨论废旧金属的回收、利用的意义。
设计意图:通过创设情景,激发学生的求知欲。教学中注意引导学生联系生活实际,使学生认识到废旧金属的回收利用的意义,同时使学生体会到化学与生活、社会的密切联系,学习化学的实用性。通过引导学生阅读教材,不但可以掌握必要的化学知识,也帮助学生提高学习能力。
五、参考资料:
1、 钢材的锈蚀
钢材的锈蚀是指其表面与周围介质发生化学反应而遭到的破坏过程。根据锈蚀作用的机理,钢材的锈蚀可分为化学锈蚀和电化学锈蚀两种:
(1).化学锈蚀
化学锈蚀是指钢材直接与周围介质发生化学反应而产生的锈蚀。这种锈蚀多数是氧化作用,使钢材表面形成疏松的氧化物。在常温下,钢材表面能形成一薄层起保护作用的氧化膜FeO,可以防止钢材进一步锈蚀。因而在干燥环境下,钢材锈蚀进展缓慢,但在温度和湿度较高的环境中,这种锈蚀进展加快。
(2).电化学锈蚀
电化学锈蚀是建筑钢材在存放和使用中发生锈蚀的主要形式。它是指钢材与电解质溶液接触而产生电流,形成微电池而引起的锈蚀。潮湿环境中的钢材表面会被一层电解质水膜所覆盖,而钢材含有铁、碳等多种成分,由于这些成分的电极电位不同,从而钢的表面层在电解质溶液中构成以铁素体为阳极,以渗碳体为阴极的微电池。在阳极,铁失去电子成为Fe2+进入水膜;在阴极,溶于水膜中的氧被还原生成0H—,随后两者结合生成不溶于水的Fe(OH)2,并进一步氧化成为疏松易剥落的红棕色铁锈Fe(OH)3。由于铁素体基体的逐渐锈蚀,钢组织中的渗碳体等暴露出来的越来越多,于是形成的微电池数目也越来越多,钢材的锈蚀速度也就愈益加速。
影响钢材锈蚀的主要因素是水、氧及介质中所含的酸、碱、盐等。同时钢材本身的组织成分对锈蚀影响也很大。埋于混凝土中的钢筋,由于普通混凝土的Ph值为12左右,处于碱性环境,使之表面形成一层碱性保护模,它有较强的阻止锈蚀继续发展的能力,故混凝土中的钢筋一般不易锈蚀。
2、防止钢材锈蚀的措施
(1).保护层法
通常的方法是采用在表面施加保护层,使钢材与周围介质隔离。保护层可分为金属保护层和非金属保护层两类。
非金属保护层常用的是在钢材表面刷漆,常用底漆有红丹、环氧富锌漆、铁红环氧底漆等,面漆有调和漆、醇酸磁漆、酚醛磁漆等,该方法简单易行,但不耐久。此外,还可以采用塑料保护层、沥青保护层、搪瓷保护层等。
金属保护层是用耐蚀性较好的金属,以电镀或喷镀的方法覆盖在钢材表面,如镀锌、镀锡、镀铬等。薄壁钢材可采用热浸镀锌或镀锌后加涂塑料涂层等措施。
(2).制成合金
钢材的组织及化学成分是引起锈蚀的内因。通过调整钢的基本组织或加入某些合金元素、可有效地提高钢材的抗腐蚀能力。例如,在钢中加入一定量的合金元素铬、镍、钛等,制成不锈钢,可以提高耐锈蚀能力。
锈蚀
条件
不锈钢
改变结构
刷油漆、涂防锈油、电镀等
表面形成保护层
表面的干燥、洁净
金属
金属(Fe)与氧气.水的接触
防护
方法
隔气
防水
合金
探究金属的
防锈措施
归纳金属的
防锈方法
废金属的
回收利用
形成结论:归纳
钢铁的锈蚀条件
探究:课前实验和观察钢铁锈蚀的现象
创设情景:有关钢铁锈
蚀图片及其损失信息
PAGE
3
执教者:付明义 单 位:河南省光山县槐店中学 指导者:李竞峰
一、知识提要
1、钢铁的锈蚀条件
2、防止金属锈蚀的简单方法
3、废弃金属对环境的污染、回收金属的重要性
二、知识脉络
三、教学思路
教师创设情景,学生讨论日常生活中观察到的金属锈蚀现象,总结出金属锈蚀的危害,让学生通过探究金属的锈蚀实验,归纳出金属的锈蚀条件,通过观察生活、生产中金属防锈措施,讨论、交流、总结出金属的防锈方法,通过了解、阅读资料,了解废金属对环境的影响和回收的重要性,具体教学思路如下所示:
四、教学过程
教学内容(一) 金属的锈蚀
教师活动 学生活动
【创设情景,引入新课】据估计,全世界每年生产的钢铁中,就有1/10左右被腐蚀掉,按此比例推算,我国每年有近一百亿美元的金属制品被锈蚀,用这笔钱可建五个葛洲坝水电站,造二艘核动力航空母舰,根据以上资料,你能提出两个问题吗?【设疑引入】使钢铁发生锈蚀的主要因素有哪些?(课前一周时间前,指导学生按照教材第126页设计实验方案,指导学生对钢铁生绣的条件进行探究。)教师对学生的实验进行点评【问题引导】根据所做的实验,同学们能分析、总结出使铁钉生锈的主要因素有哪些吗 【归纳总结】引导学生从铁钉所处环境的不同总结出铁生绣的条件。【板书】钢铁的锈蚀条件 【思考、讨论、交流】学生思考,回答【活动与探究】 学生分小组进行探究实验,并在探究开始时、一天后、三天后、一周后观察现象,并做好实验记录。可谈教学中,各小组展示实验报告。 【交流讨论】分组交流、讨论、归纳、总结、小组汇报。【思考、交流、总结】铁在空气的锈蚀,实际上是铁与与氧气,水等物质相互作用,发生生一系列复杂的化学反应,使铁转化为铁的化合物的过程,铁锈主要成分是氧化铁(Fe2O3)。
设计意图:通过几个具体数据和设凝激发学生学习兴趣和欲望,培养学生分析、发现问题的能力。通过观察实验的发生和发展,培养学生观察能力,记录数据书写实验报告的能力,以及严谨的科学态度和合作精神。培养学生分析、归纳总结概括知识的能力和研究问题的科学态度。
教学内容(二) 防止金属锈蚀的方法
教师活动 学生活动
【演示实验、激发兴趣】 在切过咸菜的铁质菜刀同一面上选相近三处进行下列实验: 一处(a处)用湿棉球润湿 另一处(b处)用干布擦干。 第三处(c处)用干布擦干后,涂上一层食用油。放置一昼夜,猜猜菜刀三处表面有何变化?然后展示菜刀【提出问题】 根据以上实验,并结合日常生活中观察,你能总结出防止铁生锈的办法吗?【小结并板书】 钢铁的防锈方法。【创新应用】1、自行车是人们常用的交通工具,请按下列要求,回答问题。 (1)自行车的主要零件是由 (填“生铁”或“钢”)制造的。 (2)请写出自行车上各部分零件都采用了什么防锈方法? (3)被雨水淋湿的自行车能否直接用带油的布擦?为什么?2、如图所示,取一团光亮无锈的铁丝绒,放入一支洁净试管底部,将试管倒放在盛水的烧杯里。数天后,能观察到的现象是 。 【交流、思考、讨论】 学生通过观察实验现象,思考、讨论,分析原因。【交流、讨论】 分组交流、讨论,然后小组汇报同学们讨论的结果。钢铁的防锈方法: (1)保持铁制品表面的干燥和洁净。 (2)在铁制品表面形成保护层,如刷油漆、涂防锈油、镀锡、 铬等金属。 (3)改变铁的内部结构。如不锈钢。【思考、讨论、交流】 在教师的引导下,从铁生绣的条件分析,同学间讨论后回答,解决实际问题。
设计意图:通过对比实验,让学生知道“对比”是一种重要科学方法,并能应用金属锈蚀条件去分析,解决实际问题。通过对比实验和观察日常生活生产中防锈措施,培养学生观察、归纳知识的能力和应用化学知识解决实际问题的能力 。通过练习、培养学生对所学知识的掌握和应用能力。
教学内容(三) 废金属的回收利用
教师活动 学生活动
【创设情景】展示废旧金属的图片,引导学生思考:锈蚀和报废的金属是不是就没有用了呢?能否进行再利用呢?【创设问题】 废旧金属的回收和利用有什么意义呢? 【思考、交流、讨论】学生思考后,同学之间进行交流、讨论。【交流、讨论】 结合阅读教材128~129页,讨论废旧金属的回收、利用的意义。
设计意图:通过创设情景,激发学生的求知欲。教学中注意引导学生联系生活实际,使学生认识到废旧金属的回收利用的意义,同时使学生体会到化学与生活、社会的密切联系,学习化学的实用性。通过引导学生阅读教材,不但可以掌握必要的化学知识,也帮助学生提高学习能力。
五、参考资料:
1、 钢材的锈蚀
钢材的锈蚀是指其表面与周围介质发生化学反应而遭到的破坏过程。根据锈蚀作用的机理,钢材的锈蚀可分为化学锈蚀和电化学锈蚀两种:
(1).化学锈蚀
化学锈蚀是指钢材直接与周围介质发生化学反应而产生的锈蚀。这种锈蚀多数是氧化作用,使钢材表面形成疏松的氧化物。在常温下,钢材表面能形成一薄层起保护作用的氧化膜FeO,可以防止钢材进一步锈蚀。因而在干燥环境下,钢材锈蚀进展缓慢,但在温度和湿度较高的环境中,这种锈蚀进展加快。
(2).电化学锈蚀
电化学锈蚀是建筑钢材在存放和使用中发生锈蚀的主要形式。它是指钢材与电解质溶液接触而产生电流,形成微电池而引起的锈蚀。潮湿环境中的钢材表面会被一层电解质水膜所覆盖,而钢材含有铁、碳等多种成分,由于这些成分的电极电位不同,从而钢的表面层在电解质溶液中构成以铁素体为阳极,以渗碳体为阴极的微电池。在阳极,铁失去电子成为Fe2+进入水膜;在阴极,溶于水膜中的氧被还原生成0H—,随后两者结合生成不溶于水的Fe(OH)2,并进一步氧化成为疏松易剥落的红棕色铁锈Fe(OH)3。由于铁素体基体的逐渐锈蚀,钢组织中的渗碳体等暴露出来的越来越多,于是形成的微电池数目也越来越多,钢材的锈蚀速度也就愈益加速。
影响钢材锈蚀的主要因素是水、氧及介质中所含的酸、碱、盐等。同时钢材本身的组织成分对锈蚀影响也很大。埋于混凝土中的钢筋,由于普通混凝土的Ph值为12左右,处于碱性环境,使之表面形成一层碱性保护模,它有较强的阻止锈蚀继续发展的能力,故混凝土中的钢筋一般不易锈蚀。
2、防止钢材锈蚀的措施
(1).保护层法
通常的方法是采用在表面施加保护层,使钢材与周围介质隔离。保护层可分为金属保护层和非金属保护层两类。
非金属保护层常用的是在钢材表面刷漆,常用底漆有红丹、环氧富锌漆、铁红环氧底漆等,面漆有调和漆、醇酸磁漆、酚醛磁漆等,该方法简单易行,但不耐久。此外,还可以采用塑料保护层、沥青保护层、搪瓷保护层等。
金属保护层是用耐蚀性较好的金属,以电镀或喷镀的方法覆盖在钢材表面,如镀锌、镀锡、镀铬等。薄壁钢材可采用热浸镀锌或镀锌后加涂塑料涂层等措施。
(2).制成合金
钢材的组织及化学成分是引起锈蚀的内因。通过调整钢的基本组织或加入某些合金元素、可有效地提高钢材的抗腐蚀能力。例如,在钢中加入一定量的合金元素铬、镍、钛等,制成不锈钢,可以提高耐锈蚀能力。
锈蚀
条件
不锈钢
改变结构
刷油漆、涂防锈油、电镀等
表面形成保护层
表面的干燥、洁净
金属
金属(Fe)与氧气.水的接触
防护
方法
隔气
防水
合金
探究金属的
防锈措施
归纳金属的
防锈方法
废金属的
回收利用
形成结论:归纳
钢铁的锈蚀条件
探究:课前实验和观察钢铁锈蚀的现象
创设情景:有关钢铁锈
蚀图片及其损失信息
PAGE
3
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
