碳酸钠的性质与应用[上学期]
图片预览





文档简介
课件13张PPT。碳酸钠的性质与应用主要知识点:一.碳酸钠的物理、 化学性质二.碳酸钠与碳酸氢钠的比较三.碳酸钠的应用和工业制法碳酸钠俗称纯碱或苏打或口碱(soda)碳酸钠属于盐类,白色粉末,是钠盐,可溶于水,水溶液呈碱性,晶体含结晶水, Na2CO3·10H2O,易失去结晶水变成白色粉末 。一.碳酸钠的物理性质 实验1实验2实验3现象:都有白色沉淀现象:气球鼓起来,有气体产生实验4现象:PH试纸变蓝,碱性现象:油污被去除二、化学性质碳酸钠+酸 → ? + ?
碳酸钠+碱 → ? + ?
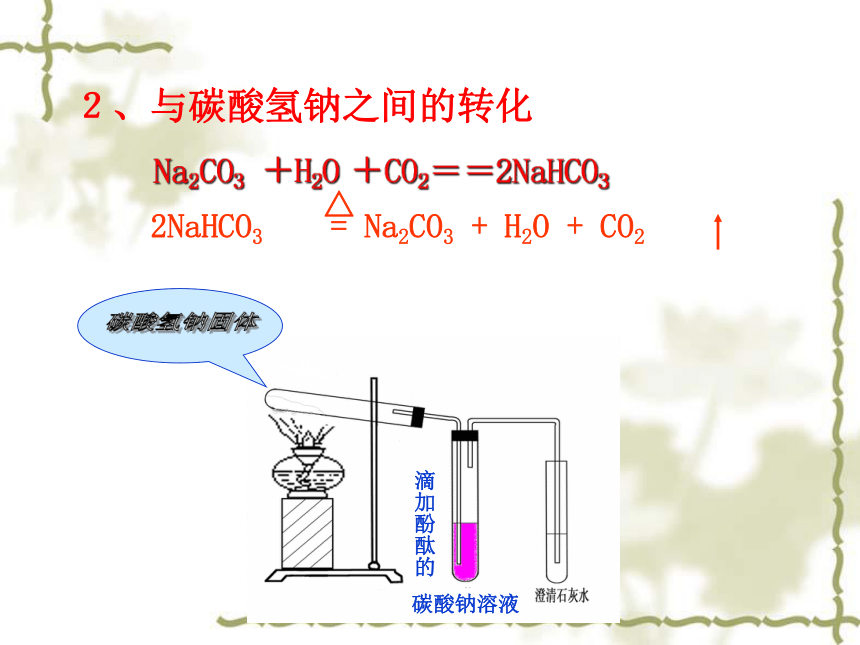
碳酸钠+盐 → ? + ?1、盐类的性质2、与碳酸氢钠之间的转化Na2CO3 +H2O +CO2==2NaHCO3
滴加酚酞的碳酸钠溶液三、碳酸钠与碳酸氢钠的比较苏打、纯碱,白色粉末小苏打,白色晶体碱 碱易溶于水 溶于水受热不分解 受热分解反应较快 反应剧烈CO32- + 2H+
=CO2↑ + H2O HCO3- + H+
=CO2↑+ H2O不与OH-离子反应 HCO3- + OH-
= CO32- + H2O设计区别固体Na2CO3和NaHCO3的方法?热稳定性不同
和酸反应生成气体的速率的差异
BaCl2或CaCl2(极稀溶液)
能不能用Ba(OH)2 、 Ca(OH)2 ?讨论:(1)向饱和Na2CO3中通入CO2会有何现象?(2)如何除去下列物质中所含的少量杂质?
⑴ 碳酸氢钠溶液中的少量碳酸钠;
⑵ 碳酸钠固体中的少量碳酸氢钠;
⑶ 二氧化碳中的少量氯化氢。通入CO2加热通过NaHCO3饱和溶液三、碳酸钠的应用和工业制法1、应用(书本52页)2、工业制法实验室中,用侯氏制碱原理制Na2CO3和NH4Cl的步骤为:⑴ ③过滤所得晶体1的名称是_________。滤液1中主要含有的溶质是_________。 操作③中使用玻棒的作用是________________________。
⑵ 操作①②的顺序_______(填能或不能)颠倒, 其原因为
________________________________________。
⑶ 连续化生产的循环步骤是 _____(填操作序号) 。碳酸氢钠NH4Cl引流不能 CO2在水中溶解度比NH3在水中溶解度小得多,而CO2在氨水中被吸收的量比在水中大。请回答:⑥谢谢
碳酸钠+碱 → ? + ?
碳酸钠+盐 → ? + ?1、盐类的性质2、与碳酸氢钠之间的转化Na2CO3 +H2O +CO2==2NaHCO3
滴加酚酞的碳酸钠溶液三、碳酸钠与碳酸氢钠的比较苏打、纯碱,白色粉末小苏打,白色晶体碱 碱易溶于水 溶于水受热不分解 受热分解反应较快 反应剧烈CO32- + 2H+
=CO2↑ + H2O HCO3- + H+
=CO2↑+ H2O不与OH-离子反应 HCO3- + OH-
= CO32- + H2O设计区别固体Na2CO3和NaHCO3的方法?热稳定性不同
和酸反应生成气体的速率的差异
BaCl2或CaCl2(极稀溶液)
能不能用Ba(OH)2 、 Ca(OH)2 ?讨论:(1)向饱和Na2CO3中通入CO2会有何现象?(2)如何除去下列物质中所含的少量杂质?
⑴ 碳酸氢钠溶液中的少量碳酸钠;
⑵ 碳酸钠固体中的少量碳酸氢钠;
⑶ 二氧化碳中的少量氯化氢。通入CO2加热通过NaHCO3饱和溶液三、碳酸钠的应用和工业制法1、应用(书本52页)2、工业制法实验室中,用侯氏制碱原理制Na2CO3和NH4Cl的步骤为:⑴ ③过滤所得晶体1的名称是_________。滤液1中主要含有的溶质是_________。 操作③中使用玻棒的作用是________________________。
⑵ 操作①②的顺序_______(填能或不能)颠倒, 其原因为
________________________________________。
⑶ 连续化生产的循环步骤是 _____(填操作序号) 。碳酸氢钠NH4Cl引流不能 CO2在水中溶解度比NH3在水中溶解度小得多,而CO2在氨水中被吸收的量比在水中大。请回答:⑥谢谢
