碳酸钠的性质与运用[上学期]
图片预览






文档简介
课件28张PPT。碳酸钠的性质与应用专题二 从海水中获得的化学物质碳酸钠俗称纯碱或苏打(soda)碳酸钠属于盐类,具有盐类化合物的通性,是钠盐,可溶于水,溶液呈碱性。 【实验一】
澄清的石灰水、氯化钙溶液中滴加碳酸钠溶液
【实验二】碳酸钠溶液中滴加盐酸
【实验三】用PH试纸测PH
【实验四】水溶液呈碱性,加热碱性增强油污被去除
实验四水溶液呈碱性PH试纸变蓝实验三Na2CO3 + 2HCl = 2NaCl+H2O+CO2↑气球鼓起来,有气体产生实验二Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
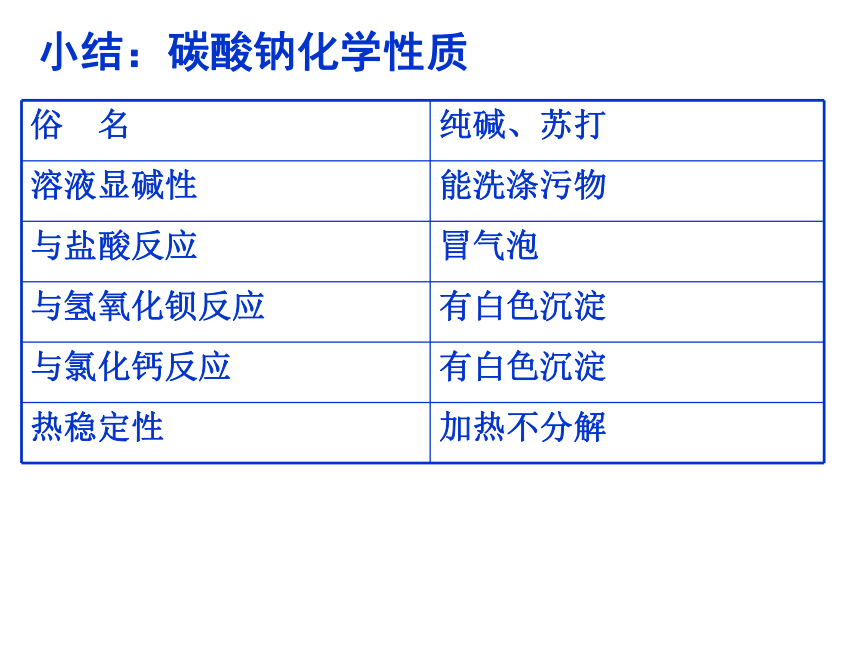
Na2CO3 + CaCl2= CaCO3 ↓ + 2NaCl都有白色沉淀实验一化学方程式实验现象小结:碳酸钠化学性质
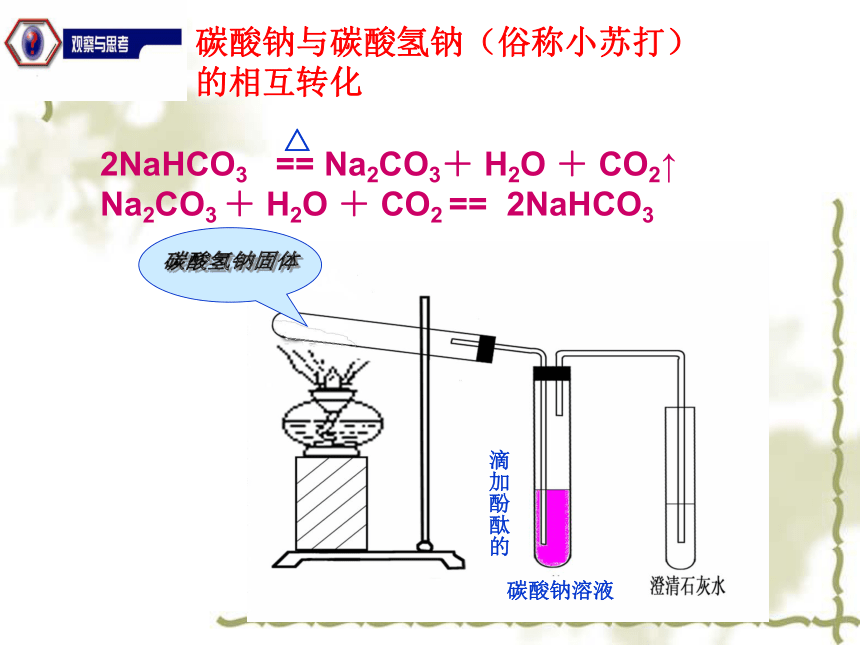
2NaHCO3 == Na2CO3+ H2O + CO2↑
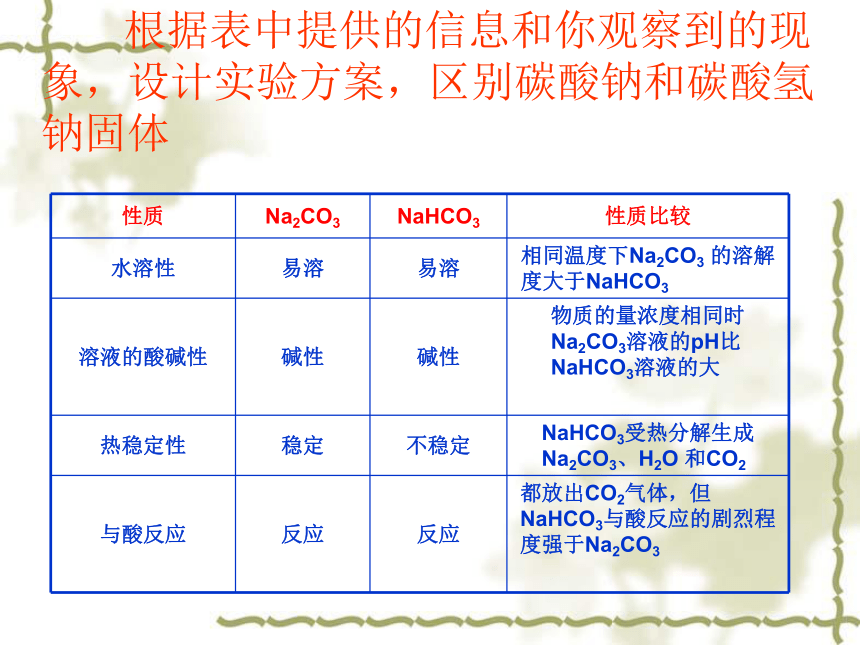
Na2CO3 + H2O + CO2 == 2NaHCO3 △滴加酚酞的碳酸钠溶液碳酸钠与碳酸氢钠(俗称小苏打) 的相互转化 根据表中提供的信息和你观察到的现象,设计实验方案,区别碳酸钠和碳酸氢钠固体Na2CO3和NaHCO3的实验探究
1、溶解度是否一样?
2、相同浓度溶液的PH值是否相同?
3、热稳定性有何不同?
4、能否与酸反应?
5、能否与碱反应?
6、能否与氯化钙反应?如何检验碳酸钠和碳酸氢钠?
(P51) 用pH试纸分别测定同浓度Na2CO3和NaHCO3溶液的pH。实验一: 物质的量浓度相同时,碱性强的是碳酸钠。实验结论: 在两干燥试管里分别放入少量Na2CO3和NaHCO3固体,接好装置,使导管末端伸入澄清石灰水中,加热,观察现象。
实验二:实验结论:很稳定的是Na2CO3;
不稳定的是Na2CO3在两支有Na2CO3和NaHCO3溶液洁净的试管中分别以同样的速度加入1mLHCl溶液,观察现象。实验三:实验结论:NaHCO3、 Na2CO3均能与盐酸反应,反应更剧烈的是NaHCO3一步完成二步完成现象分析:Na2CO3与酸反应过程:Na2CO3+HCl =
NaHCO3 + NaCl总:
Na2CO3+2HCl =
CO2↑+H2O+2NaClNaHCO3+HCl =
CO2↑+H2O+NaCl 在两支洁净的试管中分别加入1~2mLCa(OH)2溶液,再分别加入Na2CO3和NaHCO3溶液,观察现象。实验四:实验结论:NaHCO3、 Na2CO3均能与Ca(OH)2反应产生白色沉淀,不能区别与碱反应2NaHCO3+Ca(OH)2=Na2CO3+CaCO3↓+2 H2O 在两支洁净的试管中分别加入1~2mL Na2CO3和NaHCO3溶液,再分别滴入少量CaCl2溶液,观察现象。实验五:实验结论:能与CaCl2反应产生白色沉淀的是Na2CO3,而不能的 是NaHCO3与盐反应Na2CO3+CaCl 2=CaCO3 ↓ +2NaCl
NaHCO3 +CaCl 2×区别碳酸钠和碳酸氢钠固体分别加热NaHCO3固体和Na2CO3固体用PH试纸测量相同浓度的碳酸钠溶液和碳酸氢钠溶液的PH溶液的PH不一样溶液 碱性强的是Na2CO3一个受热分解,一个受热不易分解
稳定的是Na2CO3
受热易分解是
NaHCO3向盛有Na2CO3、NaHCO3固体的试管中分别滴加相同浓度的盐酸NaHCO3与盐酸反应比Na2CO3剧烈,都放出气体 与盐酸反应剧烈的是NaHCO3产生白色沉淀的是Na2CO3 纯碱是重要的化工原料,有广泛的用途。全世界纯碱产量的一半被用于制造玻璃,其余的在制肥皂、造纸、软化硬水、石油精炼、纺织和多种化学制造业中被广泛使用。碳酸钠易溶于水,它的水溶液有碱性,在日常生活中可以用来去掉发面团中的酸味儿,还可以用它的水溶液来洗涤油污的碗碟、衣物等。 碳酸钠晶体碳酸钠的用途:P52 碳酸钠又称为苏打(soda),是白色粉末。俗称纯碱,属于盐类物质,因其水溶液显弱碱性而称纯碱。制玻璃纺织等 玻璃纤维制 药灭 火 剂发 酵 剂纳米自净玻璃制 皂纺 织造 纸苏打小苏打白色粉末白色晶体易溶易溶相同温度下Na2CO3 的溶解度大于NaHCO3碱性碱性物质的量浓度相同时Na2CO3溶液的pH比NaHCO3溶液的大稳定不稳定NaHCO3受热分解生成Na2CO3、H2O 和CO2反应反应都放出CO2气体,但NaHCO3与酸反应的剧烈程度强于Na2CO3小结思考:1.如何除去Na2CO3固体中少量的NaHCO3?3.如何除去NaHCO3溶液中少量的Na2CO3?2.如何除去Na2CO3溶液中少量的NaHCO3?加热到固体质量不再改变为止或不再产生气体为止。通入过量的CO2加入适量的NaOH思考4、有五瓶失去标签的无色溶液 :澄清的石灰水、氯化钙溶液、盐酸、 酚酞试液、碳酸钠溶液, 不用其它试剂,怎样将它们区别开来?5 、 你能用多少种方法鉴别碳酸钠和碳酸氢钠固体?
6、 金属钠在空气中长时间放置最终将转化为什么?银白色
金属光泽 灰暗
失去光泽NaNa2O白色固体
易潮解NaOH析出
晶体Na2CO3?
10H2OO2H2OCO2-H2OA.加热
B.两者分别与同浓度的稀盐酸反应
C.溶于水,比较其溶解性
D.两者分别加入石灰水或Ba(OH)2
E.加BaCl2或CaCl2溶液解析:好的方法的一般衡量标准:一是操作方法简便;二是现象明显;三是所选用的试剂为常用廉价药品。6:设计区别固体Na2CO3和NaHCO3的方法?ABCE均可以,其中 AE 为最佳选择谢谢
澄清的石灰水、氯化钙溶液中滴加碳酸钠溶液
【实验二】碳酸钠溶液中滴加盐酸
【实验三】用PH试纸测PH
【实验四】水溶液呈碱性,加热碱性增强油污被去除
实验四水溶液呈碱性PH试纸变蓝实验三Na2CO3 + 2HCl = 2NaCl+H2O+CO2↑气球鼓起来,有气体产生实验二Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
Na2CO3 + CaCl2= CaCO3 ↓ + 2NaCl都有白色沉淀实验一化学方程式实验现象小结:碳酸钠化学性质
2NaHCO3 == Na2CO3+ H2O + CO2↑
Na2CO3 + H2O + CO2 == 2NaHCO3 △滴加酚酞的碳酸钠溶液碳酸钠与碳酸氢钠(俗称小苏打) 的相互转化 根据表中提供的信息和你观察到的现象,设计实验方案,区别碳酸钠和碳酸氢钠固体Na2CO3和NaHCO3的实验探究
1、溶解度是否一样?
2、相同浓度溶液的PH值是否相同?
3、热稳定性有何不同?
4、能否与酸反应?
5、能否与碱反应?
6、能否与氯化钙反应?如何检验碳酸钠和碳酸氢钠?
(P51) 用pH试纸分别测定同浓度Na2CO3和NaHCO3溶液的pH。实验一: 物质的量浓度相同时,碱性强的是碳酸钠。实验结论: 在两干燥试管里分别放入少量Na2CO3和NaHCO3固体,接好装置,使导管末端伸入澄清石灰水中,加热,观察现象。
实验二:实验结论:很稳定的是Na2CO3;
不稳定的是Na2CO3在两支有Na2CO3和NaHCO3溶液洁净的试管中分别以同样的速度加入1mLHCl溶液,观察现象。实验三:实验结论:NaHCO3、 Na2CO3均能与盐酸反应,反应更剧烈的是NaHCO3一步完成二步完成现象分析:Na2CO3与酸反应过程:Na2CO3+HCl =
NaHCO3 + NaCl总:
Na2CO3+2HCl =
CO2↑+H2O+2NaClNaHCO3+HCl =
CO2↑+H2O+NaCl 在两支洁净的试管中分别加入1~2mLCa(OH)2溶液,再分别加入Na2CO3和NaHCO3溶液,观察现象。实验四:实验结论:NaHCO3、 Na2CO3均能与Ca(OH)2反应产生白色沉淀,不能区别与碱反应2NaHCO3+Ca(OH)2=Na2CO3+CaCO3↓+2 H2O 在两支洁净的试管中分别加入1~2mL Na2CO3和NaHCO3溶液,再分别滴入少量CaCl2溶液,观察现象。实验五:实验结论:能与CaCl2反应产生白色沉淀的是Na2CO3,而不能的 是NaHCO3与盐反应Na2CO3+CaCl 2=CaCO3 ↓ +2NaCl
NaHCO3 +CaCl 2×区别碳酸钠和碳酸氢钠固体分别加热NaHCO3固体和Na2CO3固体用PH试纸测量相同浓度的碳酸钠溶液和碳酸氢钠溶液的PH溶液的PH不一样溶液 碱性强的是Na2CO3一个受热分解,一个受热不易分解
稳定的是Na2CO3
受热易分解是
NaHCO3向盛有Na2CO3、NaHCO3固体的试管中分别滴加相同浓度的盐酸NaHCO3与盐酸反应比Na2CO3剧烈,都放出气体 与盐酸反应剧烈的是NaHCO3产生白色沉淀的是Na2CO3 纯碱是重要的化工原料,有广泛的用途。全世界纯碱产量的一半被用于制造玻璃,其余的在制肥皂、造纸、软化硬水、石油精炼、纺织和多种化学制造业中被广泛使用。碳酸钠易溶于水,它的水溶液有碱性,在日常生活中可以用来去掉发面团中的酸味儿,还可以用它的水溶液来洗涤油污的碗碟、衣物等。 碳酸钠晶体碳酸钠的用途:P52 碳酸钠又称为苏打(soda),是白色粉末。俗称纯碱,属于盐类物质,因其水溶液显弱碱性而称纯碱。制玻璃纺织等 玻璃纤维制 药灭 火 剂发 酵 剂纳米自净玻璃制 皂纺 织造 纸苏打小苏打白色粉末白色晶体易溶易溶相同温度下Na2CO3 的溶解度大于NaHCO3碱性碱性物质的量浓度相同时Na2CO3溶液的pH比NaHCO3溶液的大稳定不稳定NaHCO3受热分解生成Na2CO3、H2O 和CO2反应反应都放出CO2气体,但NaHCO3与酸反应的剧烈程度强于Na2CO3小结思考:1.如何除去Na2CO3固体中少量的NaHCO3?3.如何除去NaHCO3溶液中少量的Na2CO3?2.如何除去Na2CO3溶液中少量的NaHCO3?加热到固体质量不再改变为止或不再产生气体为止。通入过量的CO2加入适量的NaOH思考4、有五瓶失去标签的无色溶液 :澄清的石灰水、氯化钙溶液、盐酸、 酚酞试液、碳酸钠溶液, 不用其它试剂,怎样将它们区别开来?5 、 你能用多少种方法鉴别碳酸钠和碳酸氢钠固体?
6、 金属钠在空气中长时间放置最终将转化为什么?银白色
金属光泽 灰暗
失去光泽NaNa2O白色固体
易潮解NaOH析出
晶体Na2CO3?
10H2OO2H2OCO2-H2OA.加热
B.两者分别与同浓度的稀盐酸反应
C.溶于水,比较其溶解性
D.两者分别加入石灰水或Ba(OH)2
E.加BaCl2或CaCl2溶液解析:好的方法的一般衡量标准:一是操作方法简便;二是现象明显;三是所选用的试剂为常用廉价药品。6:设计区别固体Na2CO3和NaHCO3的方法?ABCE均可以,其中 AE 为最佳选择谢谢
