必修二专题一第一单元元素周期律课件[上下学期通用]
文档属性
| 名称 | 必修二专题一第一单元元素周期律课件[上下学期通用] |

|
|
| 格式 | rar | ||
| 文件大小 | 22.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-09-14 00:00:00 | ||
图片预览



文档简介
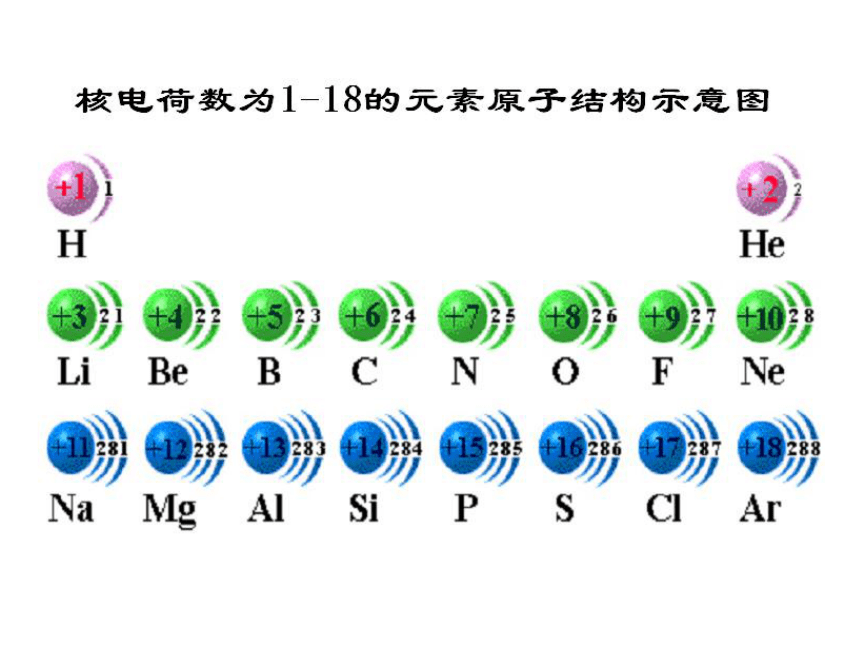
课件24张PPT。第一单元 核外电子排布与周期律专题1 微观结构与物质的多样性(二)元素周期律嘉兴市第四高级中学夏宾 原子序数
人们按核电荷数由小到大的顺序给元素编号,这种编号叫做原子序数。
原子序数==核电荷数==核内质子数
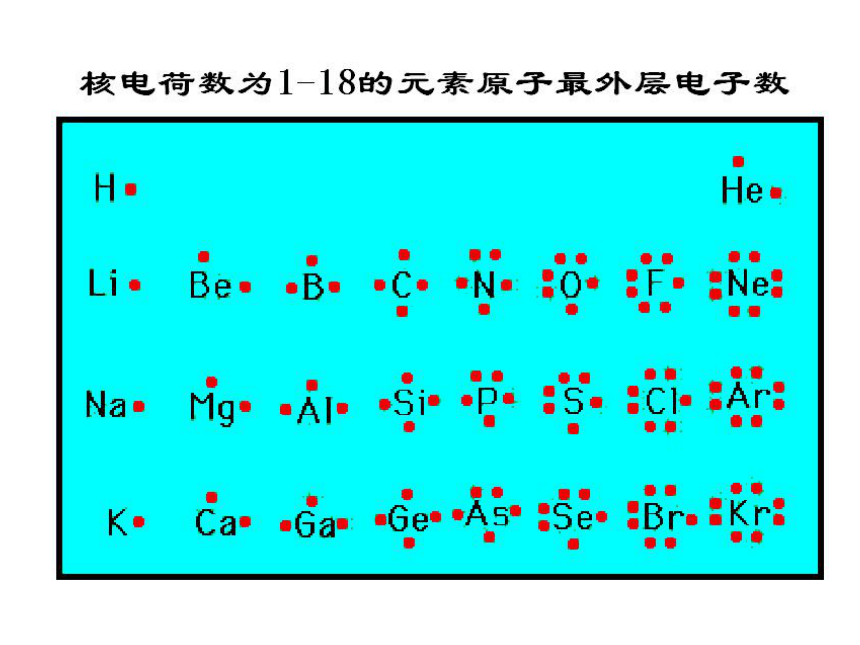
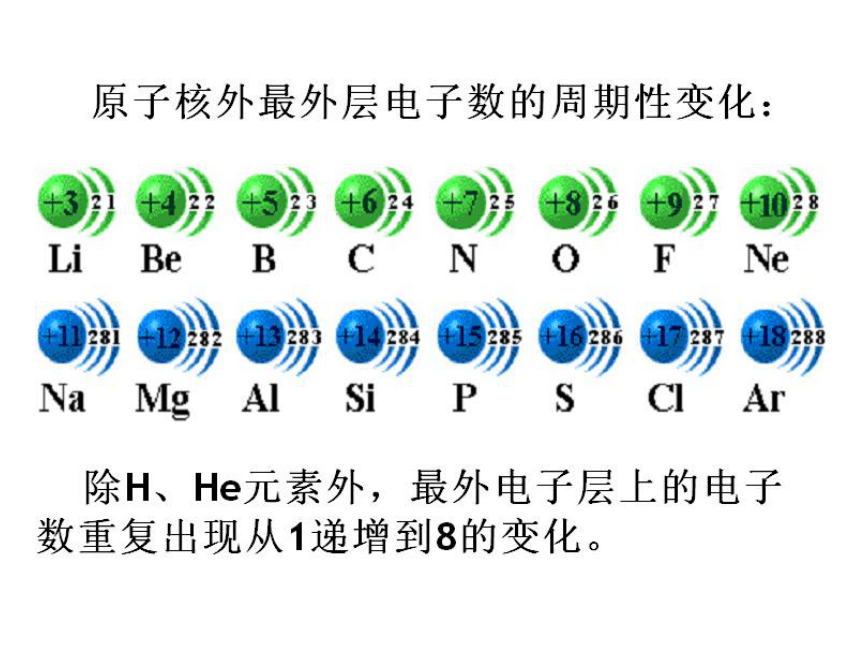
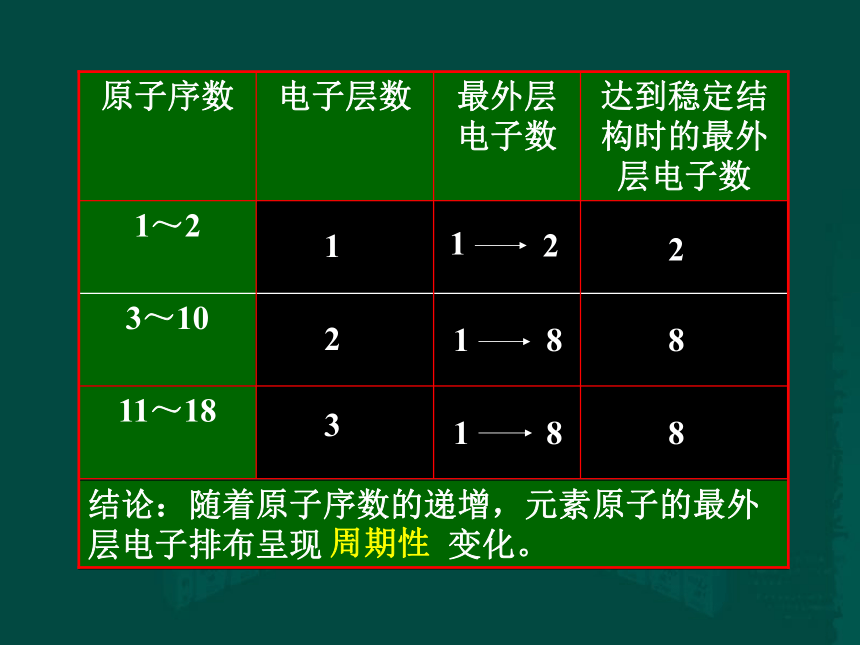
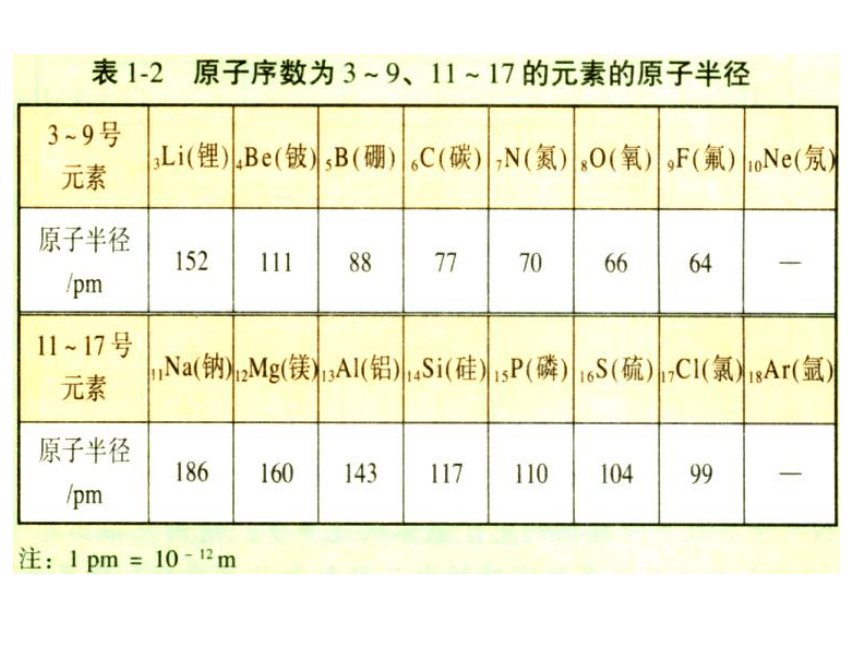
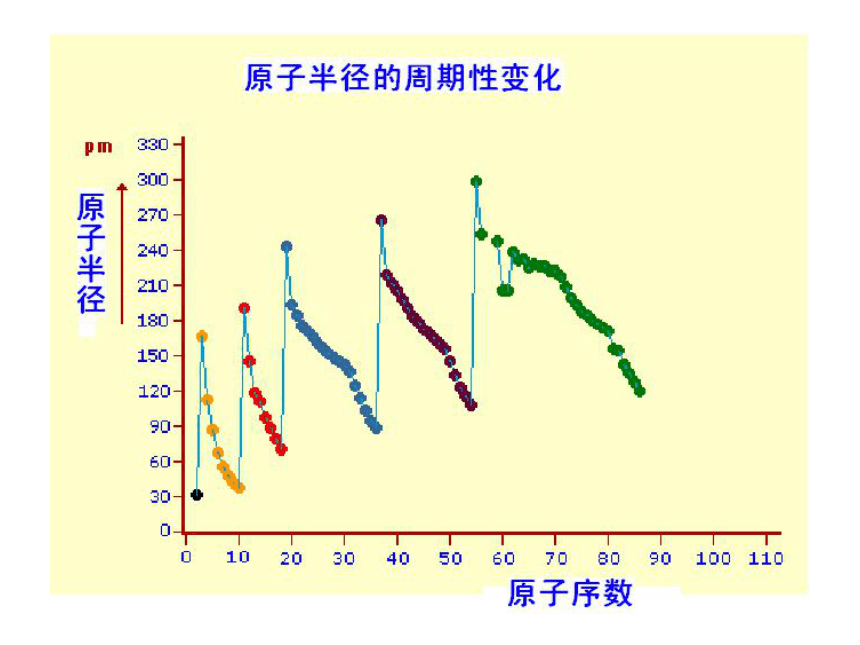
==原子的核外电子数结论:随着原子序数的递增,元素原子的最外层电子排布呈现 变化。 11~18 3~10 1~2 达到稳定结构时的最外层电子数 最外层电子数 电子层数 原子序数 123882周期性原子半径结论:随着原子序数的递增,元素原子半径呈现 变化。 11~17 3~10 原子半径的变化 原子序数 逐渐减小逐渐减小周期性? 随着原子序数的递增
元素原子的核外电子排布呈现周期性变化
元素原子半径呈现周期性变化
元素的性质是否呈现周期性变化?判断元素金属性强弱的方法判断元素非金属性强弱的方法元素的金属性、非金属性强弱判断:1、单质还原性强弱;1、单质氧化性强弱;钠、镁、铝和水的反应 金属性
Na>Mg 向盛有已擦去表面氧化膜的镁条和铝片的试管中,各加入2mL 1mol/L的盐酸。镁、铝和盐酸的反应镁、铝和盐酸的反应 金属性
Mg > Al11~18号元素性质的变化中得出如下的结论:元素化合价最高正价 = 最外层电子数
最高正价+|最低负价| = 8 元素周期律同学们
再见!
人们按核电荷数由小到大的顺序给元素编号,这种编号叫做原子序数。
原子序数==核电荷数==核内质子数
==原子的核外电子数结论:随着原子序数的递增,元素原子的最外层电子排布呈现 变化。 11~18 3~10 1~2 达到稳定结构时的最外层电子数 最外层电子数 电子层数 原子序数 123882周期性原子半径结论:随着原子序数的递增,元素原子半径呈现 变化。 11~17 3~10 原子半径的变化 原子序数 逐渐减小逐渐减小周期性? 随着原子序数的递增
元素原子的核外电子排布呈现周期性变化
元素原子半径呈现周期性变化
元素的性质是否呈现周期性变化?判断元素金属性强弱的方法判断元素非金属性强弱的方法元素的金属性、非金属性强弱判断:1、单质还原性强弱;1、单质氧化性强弱;钠、镁、铝和水的反应 金属性
Na>Mg 向盛有已擦去表面氧化膜的镁条和铝片的试管中,各加入2mL 1mol/L的盐酸。镁、铝和盐酸的反应镁、铝和盐酸的反应 金属性
Mg > Al11~18号元素性质的变化中得出如下的结论:元素化合价最高正价 = 最外层电子数
最高正价+|最低负价| = 8 元素周期律同学们
再见!
