共价键(新课)[下学期]
图片预览








文档简介
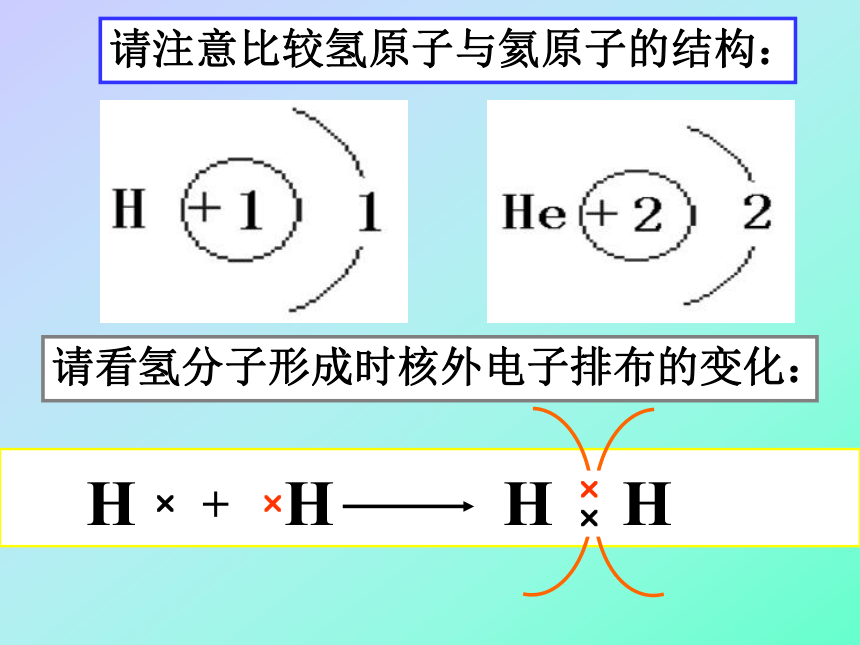
课件52张PPT。化学键(第二课时)徐州高级中学 姚斌 H?+HH?H请注意比较氢原子与氦原子的结构:请看氢分子形成时核外电子排布的变化:?? 两个氢原子结合成氢分子时电子云的变化上 一 张下 一 张返 回结 束 请同学们根据氯原子、氢原子的电子式和 原子在化合时力求达到稳定的事实,探讨氯化氢分子的形成过程,并用电子式表示之。一、共价键的形成及概念:
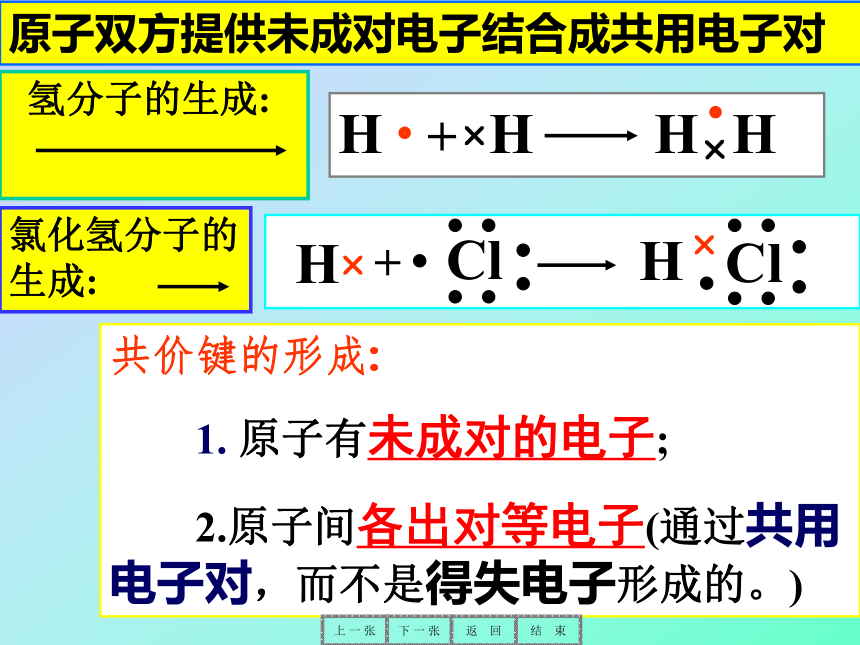
两个氢原子各提供一个电子,通过共用电子对使两原子产生了强烈的相互作用,这种: “ 原子间通过共用电子对所形成的化学键,叫做共价键。”完全由共价键构成的化合物叫共价化合物。如HCl,H2O等.共价键的形成:
1. 原子有未成对的电子;
2.原子间各出对等电子(通过共用电子对,而不是得失电子形成的。)H?H??HH?+Cl??????H? ?Cl??????H??+上 一 张下 一 张返 回结 束氯化氢分子的生成:原子双方提供未成对电子结合成共用电子对 氢分子的生成:
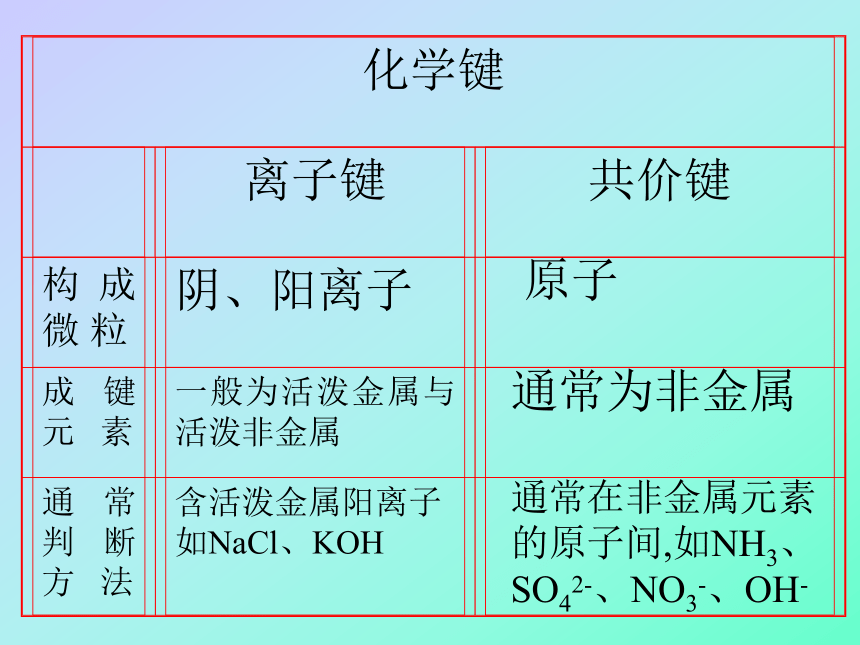
原子通常为非金属通常在非金属元素
的原子间,如NH3、
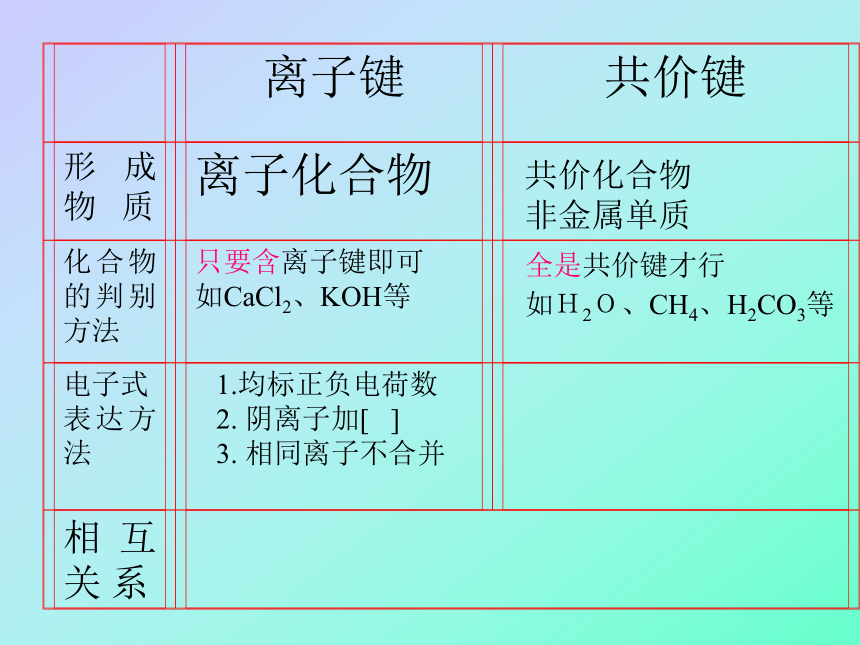
SO42-、NO3-、OH- 共价化合物
非金属单质全是共价键才行
如H2O、CH4、H2CO3等 下列关于化学键的叙述中正确的是
A、离子化合物可以含有共价键
B、共价化合物可能含有离子键
C、离子化合物中只含有离子键
D、共价化合物中不含有离子键判断下列化合物的类型
NaOH、H2S、MgCl2、H2SO4、KNO3、CO2
离子化合物
共价化合物
含共价键的离子化合物 请同学们用电子式写出H2、Cl2分子的形成过程。
以共价键形成的分子的电子式的
书写规律:1.每个原子均应达到稳定的结构
2.不加中括号[ ],不标正负电荷数
3.原子最外层电子数距8电子稳定结构差几个电子,就提供几个电子,并在此原子周围形成几对共用电子(即几个共价键) 共价化合物
非金属单质全是共价键才行
如H2O、CH4、H2CO3等 1.原子全稳定
2.不标电荷和[ ]
3.差几拿几成几
在化学上常用一根短线
表示一对共用电子,例H-H
O=O、Cl-Cl、H-Cl,其余的
电子不标出。这样的式子叫
结构式。 根据甲烷的电子式,指出分子内直接相邻的原子 分子内非直接相邻的原子 。由此可知分子内直
接相邻的原子实质上是 (填成键原子或非成键原子),非直接相邻的原子通常是 (填成键原子或非成键原子)上述两类原子间存在相互作用的是 , 相互作用比较强烈的是 ,这种强烈的相互作用又称 。 共价化合物
非金属单质全是共价键才行
如H2O、CH4、H2CO3等 1.原子全稳定
2.不标电荷和[ ]
3.差几拿几成几
共价键 离子键电子对的偏移程度
H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl
化学反应的过程
分子原子观点
分解 重新组合
物质 原子 新物质 旧键断裂 新键生成
化学键的观点
练习:用电子式写出下列共价分子的形成过程:Br2、HBr、H2O、NH3
上 一 张下 一 张返 回结 束答案:Br???????+Br???????Br????????Br??????H+Br???????H??Br??????H?+O??????+H?HO??????? ?HN?????H?++H?H?N????H??H??H?+上 一 张下 一 张返 回结 束共价键通常表示形式:
1.用电子式表示:
2.用结构式表示:
如:
H??HH? ?Cl??????HHHClClClNN如:NN? ??????? ? ?上 一 张下 一 张返 回结 束又如:例:
例:
共价键的类型极性共价键
(极性键)H??H非极性共价键
(非极性键)H? ????????+?-Cl?+?-?+?-上 一 张下 一 张返 回结 束二、共价键的性质1.键长:
在分子中,两个成键的原子的核间距离叫做键长。上 一 张下 一 张返 回结 束 一般说来,两个原子间所形成的键越短,键就越强,越牢固。上 一 张下 一 张结 束返 回2.键能:
拆开1mol某种键所需要吸收的能量,叫做键能。例如:H2 + 436KJ ? H + H
Cl2+247KJ ? Cl + Cl
N2+946KJ ? N + N键能的单位为: KJ/mol上 一 张下 一 张返 回结 束上 一 张下 一 张结 束返 回一般来说,键能越大,表示化学键越牢固,含有该键的分子越稳定。
参考下表中化学键的键能数据,下列分子中,受热时最稳定的是( )A.氢气 B.氟化氢 C.氯化氢 D.溴化氢B上 一 张下 一 张返 回结 束 在含有多个共价键的分子中, 相邻共价键之间存在一定的夹角,如H2O分子:上 一 张下 一 张返 回结 束CO2分子的键角
CH4分子的键角3.键角:
在分子中键和键之间的夹角叫做键角。上 一 张下 一 张返 回结 束甲烷(CH4)分子的空间结构
C—H键之间的夹角为109o28’上 一 张下 一 张结 束返 回 本节我们学习了以下内容: 1.共价键是怎样形成的
(形成条件;形成过程)
2.共价键的表示方法
(电子式;结构式)
3.共价键的性质
(键长;键能;键角)上 一 张下 一 张返 回结 束下列电子式中,书写错误的是
A、H O H B、N N
C、[ O H ]- D、[ S ]2- 最近科学家研制出一种新的分子,它具有类似足球的空心结构,化学式为C60,下列说法中,不正确的是
A、C60是一种新型化合物
B、C60分子中存在共价键
C、C60分子中存在离子键
D、C60相对分子质量为720下列变化中,有新的化学键形成的是
A、水和酒精混合
B、碘单质受热升华
C、钠块放入水中
D、铜在氯气中燃烧1、请你分别写出氮原子和氨气的电
子式;1、请你分别写出氮原子和氨气的电
子式;N H N H
H1、请你分别写出氮原子和氨气的电
子式;N H N H
H2、已知氯化铵为离子化合物,其电
子式如下,请分析其中所含有的化学
键: H
[H N H]+[ Cl ]-
H
请用电子式表示出下列物质:
Cl2、 N2、H2S、CH4、
K2S、Ca(OH)2、Na2O2
上 一 张下 一 张返 回结 束
答案:C????????HHH????????OH[ ]-Ca2+??O??????H[ ]-????O????Na+??O????[ ]2-Na+? ???????ClCl??????NN? ??????? ? ?HH????? ?S??
K+? ?? ?2-K[S+]????上 一 张下 一 张返 回结 束H写出H2O、CO2、NaOH,MgCl2的电子式根据下列物质的结构式写出相应电子式:
H—O—Cl 、 H—O—O—H
H—C ≡C—H书写电子式注意:
1.分清键型(是离子键还是共价键)
2.形成离子键时,要标电荷;形成共价键时不标电荷
3.成键后的原子或离子,一般为8电子稳定结构上 一 张下 一 张返 回结 束
两个氢原子各提供一个电子,通过共用电子对使两原子产生了强烈的相互作用,这种: “ 原子间通过共用电子对所形成的化学键,叫做共价键。”完全由共价键构成的化合物叫共价化合物。如HCl,H2O等.共价键的形成:
1. 原子有未成对的电子;
2.原子间各出对等电子(通过共用电子对,而不是得失电子形成的。)H?H??HH?+Cl??????H? ?Cl??????H??+上 一 张下 一 张返 回结 束氯化氢分子的生成:原子双方提供未成对电子结合成共用电子对 氢分子的生成:
原子通常为非金属通常在非金属元素
的原子间,如NH3、
SO42-、NO3-、OH- 共价化合物
非金属单质全是共价键才行
如H2O、CH4、H2CO3等 下列关于化学键的叙述中正确的是
A、离子化合物可以含有共价键
B、共价化合物可能含有离子键
C、离子化合物中只含有离子键
D、共价化合物中不含有离子键判断下列化合物的类型
NaOH、H2S、MgCl2、H2SO4、KNO3、CO2
离子化合物
共价化合物
含共价键的离子化合物 请同学们用电子式写出H2、Cl2分子的形成过程。
以共价键形成的分子的电子式的
书写规律:1.每个原子均应达到稳定的结构
2.不加中括号[ ],不标正负电荷数
3.原子最外层电子数距8电子稳定结构差几个电子,就提供几个电子,并在此原子周围形成几对共用电子(即几个共价键) 共价化合物
非金属单质全是共价键才行
如H2O、CH4、H2CO3等 1.原子全稳定
2.不标电荷和[ ]
3.差几拿几成几
在化学上常用一根短线
表示一对共用电子,例H-H
O=O、Cl-Cl、H-Cl,其余的
电子不标出。这样的式子叫
结构式。 根据甲烷的电子式,指出分子内直接相邻的原子 分子内非直接相邻的原子 。由此可知分子内直
接相邻的原子实质上是 (填成键原子或非成键原子),非直接相邻的原子通常是 (填成键原子或非成键原子)上述两类原子间存在相互作用的是 , 相互作用比较强烈的是 ,这种强烈的相互作用又称 。 共价化合物
非金属单质全是共价键才行
如H2O、CH4、H2CO3等 1.原子全稳定
2.不标电荷和[ ]
3.差几拿几成几
共价键 离子键电子对的偏移程度
H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl H H
Cl Cl
化学反应的过程
分子原子观点
分解 重新组合
物质 原子 新物质 旧键断裂 新键生成
化学键的观点
练习:用电子式写出下列共价分子的形成过程:Br2、HBr、H2O、NH3
上 一 张下 一 张返 回结 束答案:Br???????+Br???????Br????????Br??????H+Br???????H??Br??????H?+O??????+H?HO??????? ?HN?????H?++H?H?N????H??H??H?+上 一 张下 一 张返 回结 束共价键通常表示形式:
1.用电子式表示:
2.用结构式表示:
如:
H??HH? ?Cl??????HHHClClClNN如:NN? ??????? ? ?上 一 张下 一 张返 回结 束又如:例:
例:
共价键的类型极性共价键
(极性键)H??H非极性共价键
(非极性键)H? ????????+?-Cl?+?-?+?-上 一 张下 一 张返 回结 束二、共价键的性质1.键长:
在分子中,两个成键的原子的核间距离叫做键长。上 一 张下 一 张返 回结 束 一般说来,两个原子间所形成的键越短,键就越强,越牢固。上 一 张下 一 张结 束返 回2.键能:
拆开1mol某种键所需要吸收的能量,叫做键能。例如:H2 + 436KJ ? H + H
Cl2+247KJ ? Cl + Cl
N2+946KJ ? N + N键能的单位为: KJ/mol上 一 张下 一 张返 回结 束上 一 张下 一 张结 束返 回一般来说,键能越大,表示化学键越牢固,含有该键的分子越稳定。
参考下表中化学键的键能数据,下列分子中,受热时最稳定的是( )A.氢气 B.氟化氢 C.氯化氢 D.溴化氢B上 一 张下 一 张返 回结 束 在含有多个共价键的分子中, 相邻共价键之间存在一定的夹角,如H2O分子:上 一 张下 一 张返 回结 束CO2分子的键角
CH4分子的键角3.键角:
在分子中键和键之间的夹角叫做键角。上 一 张下 一 张返 回结 束甲烷(CH4)分子的空间结构
C—H键之间的夹角为109o28’上 一 张下 一 张结 束返 回 本节我们学习了以下内容: 1.共价键是怎样形成的
(形成条件;形成过程)
2.共价键的表示方法
(电子式;结构式)
3.共价键的性质
(键长;键能;键角)上 一 张下 一 张返 回结 束下列电子式中,书写错误的是
A、H O H B、N N
C、[ O H ]- D、[ S ]2- 最近科学家研制出一种新的分子,它具有类似足球的空心结构,化学式为C60,下列说法中,不正确的是
A、C60是一种新型化合物
B、C60分子中存在共价键
C、C60分子中存在离子键
D、C60相对分子质量为720下列变化中,有新的化学键形成的是
A、水和酒精混合
B、碘单质受热升华
C、钠块放入水中
D、铜在氯气中燃烧1、请你分别写出氮原子和氨气的电
子式;1、请你分别写出氮原子和氨气的电
子式;N H N H
H1、请你分别写出氮原子和氨气的电
子式;N H N H
H2、已知氯化铵为离子化合物,其电
子式如下,请分析其中所含有的化学
键: H
[H N H]+[ Cl ]-
H
请用电子式表示出下列物质:
Cl2、 N2、H2S、CH4、
K2S、Ca(OH)2、Na2O2
上 一 张下 一 张返 回结 束
答案:C????????HHH????????OH[ ]-Ca2+??O??????H[ ]-????O????Na+??O????[ ]2-Na+? ???????ClCl??????NN? ??????? ? ?HH????? ?S??
K+? ?? ?2-K[S+]????上 一 张下 一 张返 回结 束H写出H2O、CO2、NaOH,MgCl2的电子式根据下列物质的结构式写出相应电子式:
H—O—Cl 、 H—O—O—H
H—C ≡C—H书写电子式注意:
1.分清键型(是离子键还是共价键)
2.形成离子键时,要标电荷;形成共价键时不标电荷
3.成键后的原子或离子,一般为8电子稳定结构上 一 张下 一 张返 回结 束
