二氧化硅与信息材料[上学期]
图片预览



文档简介
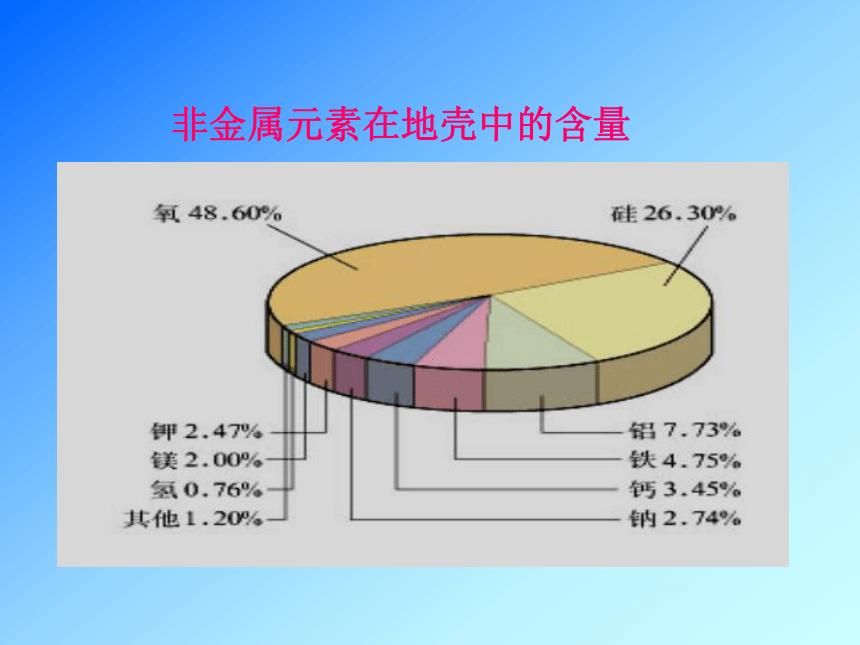
课件13张PPT。硅、二氧化硅与信息材料江苏省宿迁中学高一化学组非金属元素在地壳中的含量硅的氧化物及硅酸盐构成了地壳中大部分的岩石、沙子和土壤、约占地壳总量的90%以上。
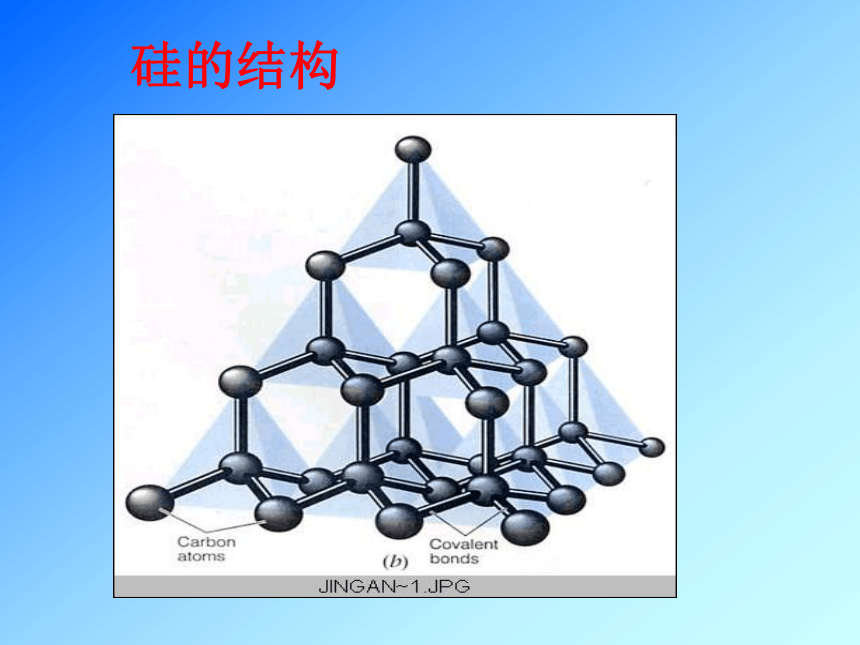
硅的结构1、物理性质熔、沸点高,硬度大,常作为半导体
以化合态存在于自然界,有两种同素异形体:晶体硅和无定形硅.2、化学性质碳单质在常温下化学性质稳定,高温时可与氧气等活泼非金属反应.常作为还原剂.
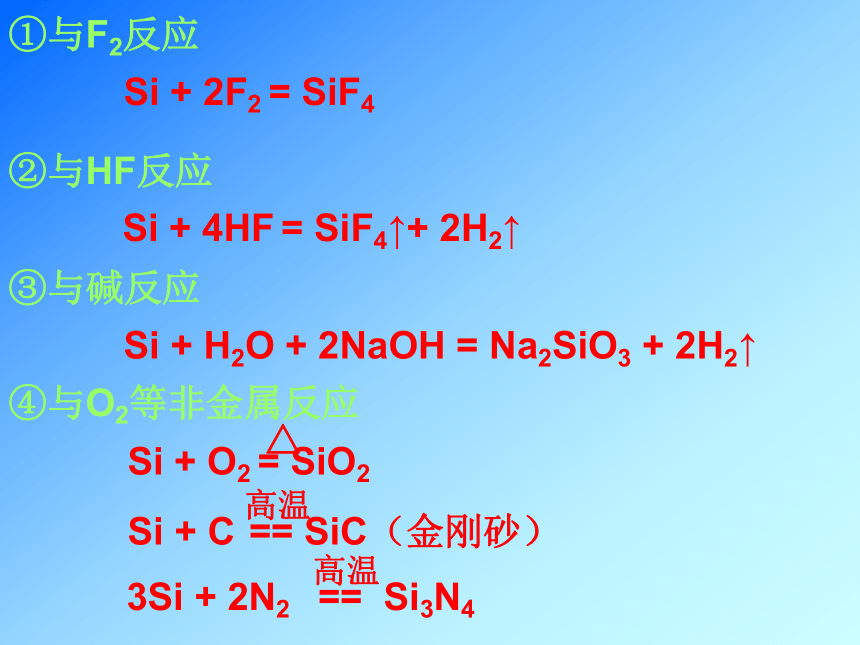
硅单质在常温下化学性质稳定.一、硅(Si)①与F2反应②与HF反应③与碱反应④与O2等非金属反应Si + 2F2 = SiF4Si + 4HF = SiF4↑+ 2H2↑Si + H2O + 2NaOH = Na2SiO3 + 2H2↑3、硅的制法4、硅的用途半导体
光电池(将光能转化为电能)
硅芯片(用于计算机)
半导体晶体管及芯片的出现,
促进了信息技术革命集成电路 晶体管二、二氧化硅(SiO2)1、物理性质二氧化硅是一种坚硬难熔的固体,不溶于水. 为什么在实验室中盛放NaOH 溶液的试剂瓶用橡皮塞而不用玻璃塞? 2、SiO2的化学性质(很不活泼)(1)与HF的反应 ( SiO2的特性)
SiO2 + 4HF = SiF4↑+ 2H2O
*用途:雕刻玻璃(2)与碱性氧化物反应生成盐(酸性氧化物的性质)
SiO2+ CaO == CaSiO3
(3)与强碱反应生成盐和水
SiO2 + 2NaOH = Na2SiO3 +H2O
硅酸钠
高温想一想水玻璃(有粘性)玻璃中的SiO2 与NaOH 反应生成有粘性的硅酸钠SiO2是不溶于水的酸性氧化物,能与氢氟酸反应SiO2+4HF=SiF4+2H2O不反应不反应CO2+H2O = H2CO3SiO2+2NaOH=
Na2SiO3 +H2OCO2+2NaOH=
Na2CO3 +H2OCO2+Na2O = Na2CO3SiO2与CO2的比较一、二氧化硅
**小知识:自然界的二氧化硅(水晶、玛瑙) 水晶玛瑙石英光导纤维
以化合态存在于自然界,有两种同素异形体:晶体硅和无定形硅.2、化学性质碳单质在常温下化学性质稳定,高温时可与氧气等活泼非金属反应.常作为还原剂.
硅单质在常温下化学性质稳定.一、硅(Si)①与F2反应②与HF反应③与碱反应④与O2等非金属反应Si + 2F2 = SiF4Si + 4HF = SiF4↑+ 2H2↑Si + H2O + 2NaOH = Na2SiO3 + 2H2↑3、硅的制法4、硅的用途半导体
光电池(将光能转化为电能)
硅芯片(用于计算机)
半导体晶体管及芯片的出现,
促进了信息技术革命集成电路 晶体管二、二氧化硅(SiO2)1、物理性质二氧化硅是一种坚硬难熔的固体,不溶于水. 为什么在实验室中盛放NaOH 溶液的试剂瓶用橡皮塞而不用玻璃塞? 2、SiO2的化学性质(很不活泼)(1)与HF的反应 ( SiO2的特性)
SiO2 + 4HF = SiF4↑+ 2H2O
*用途:雕刻玻璃(2)与碱性氧化物反应生成盐(酸性氧化物的性质)
SiO2+ CaO == CaSiO3
(3)与强碱反应生成盐和水
SiO2 + 2NaOH = Na2SiO3 +H2O
硅酸钠
高温想一想水玻璃(有粘性)玻璃中的SiO2 与NaOH 反应生成有粘性的硅酸钠SiO2是不溶于水的酸性氧化物,能与氢氟酸反应SiO2+4HF=SiF4+2H2O不反应不反应CO2+H2O = H2CO3SiO2+2NaOH=
Na2SiO3 +H2OCO2+2NaOH=
Na2CO3 +H2OCO2+Na2O = Na2CO3SiO2与CO2的比较一、二氧化硅
**小知识:自然界的二氧化硅(水晶、玛瑙) 水晶玛瑙石英光导纤维
