制取氧气[上学期]
图片预览






文档简介
课件14张PPT。课题3 制取氧气工业用氧医用氧实验用氧一、工业制取大量氧气的方法分离液态空气法
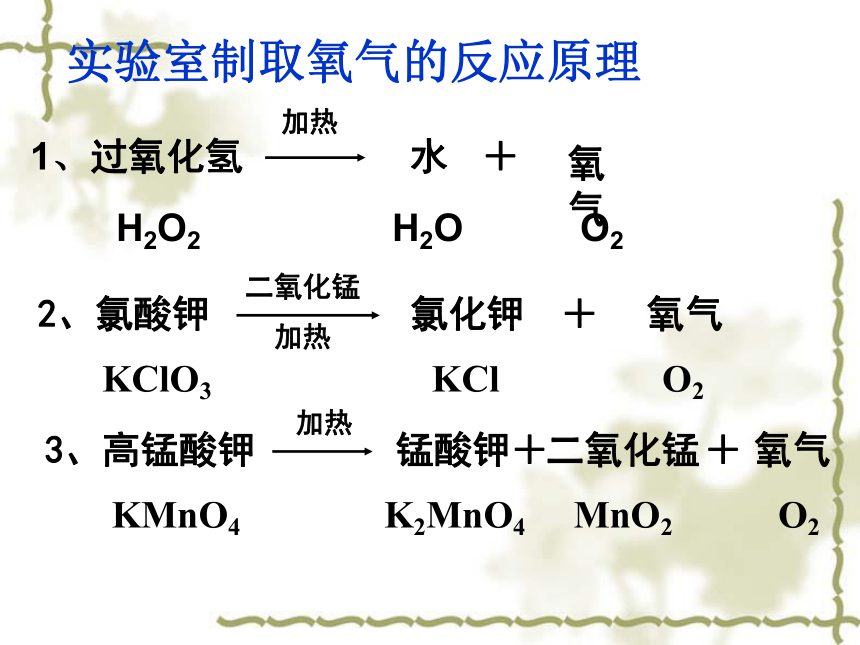
加压空气液态空气降温、加压 蒸发氮气液氧氮气和氧气沸点不同贮存在蓝色钢瓶中── 物理变化活动一:制取氧气原理的探究实验室制取氧气的反应原理1、过氧化氢2、氯酸钾二氧化锰加热3、高锰酸钾加热 H2O2 H2O O2加热水氧气+KClO3 KCl O2氯化钾+氧气 KMnO4 K2MnO4 MnO2 O2锰酸钾+二氧化锰+氧气二、实验室制取氧气的原理1.分解反应:由一种反应物生成两种或两种以上其他物质的反应。(一变多)反应型式:ABA + B【小结】 2.反应3中是生成物,反应1和2是催化剂。活动二:催化剂和化学反应速率的探究活动要求:
1.各小组同学认真观察并记录实验现象。
2.各小组同学认真组织讨论讲学稿上的三个问题。
3.各小组推荐代表汇报观察的现象、三个问题的思考。
4.你谈谈对催化剂的认识。1.催化剂:在化学反应里能改变其他物质的反应速率,而本身的质量和化学性质在反应前后都没有改变的物质叫做催化剂。(一变二不变)2.催化作用:催化剂在化学反应中所起的作用叫催化作用。【小结】 炼制石油合成氨化工制药催化剂在化工生产中的作用活动三:实验室制取O2装置的探究二、实验室制取气体收集装置的选择──考虑气体的溶解性、是否与水反应、密度与空气密度的相对大小等因素排水法── O2不易溶于水,
且不与水反应
排水法向上排空气法── 气体密度比空气大向上排空气法向下排空气法── 气体密度比空气小向下排空气法 【实验与观察】 1.加药品
2.加热
3.收集(用排水法、向上排空气法)
4.检验与验满 按照课本P38 的图和实验〔2-7〕的要求,加热KClO3和MnO2的混合物制取并检验O2,并观看录像。本节课你学到了什么?
加压空气液态空气降温、加压 蒸发氮气液氧氮气和氧气沸点不同贮存在蓝色钢瓶中── 物理变化活动一:制取氧气原理的探究实验室制取氧气的反应原理1、过氧化氢2、氯酸钾二氧化锰加热3、高锰酸钾加热 H2O2 H2O O2加热水氧气+KClO3 KCl O2氯化钾+氧气 KMnO4 K2MnO4 MnO2 O2锰酸钾+二氧化锰+氧气二、实验室制取氧气的原理1.分解反应:由一种反应物生成两种或两种以上其他物质的反应。(一变多)反应型式:ABA + B【小结】 2.反应3中是生成物,反应1和2是催化剂。活动二:催化剂和化学反应速率的探究活动要求:
1.各小组同学认真观察并记录实验现象。
2.各小组同学认真组织讨论讲学稿上的三个问题。
3.各小组推荐代表汇报观察的现象、三个问题的思考。
4.你谈谈对催化剂的认识。1.催化剂:在化学反应里能改变其他物质的反应速率,而本身的质量和化学性质在反应前后都没有改变的物质叫做催化剂。(一变二不变)2.催化作用:催化剂在化学反应中所起的作用叫催化作用。【小结】 炼制石油合成氨化工制药催化剂在化工生产中的作用活动三:实验室制取O2装置的探究二、实验室制取气体收集装置的选择──考虑气体的溶解性、是否与水反应、密度与空气密度的相对大小等因素排水法── O2不易溶于水,
且不与水反应
排水法向上排空气法── 气体密度比空气大向上排空气法向下排空气法── 气体密度比空气小向下排空气法 【实验与观察】 1.加药品
2.加热
3.收集(用排水法、向上排空气法)
4.检验与验满 按照课本P38 的图和实验〔2-7〕的要求,加热KClO3和MnO2的混合物制取并检验O2,并观看录像。本节课你学到了什么?
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
