人教版高中物理选修3-5 18.2 原子的核式结构模型 课件:26张PPT
文档属性
| 名称 | 人教版高中物理选修3-5 18.2 原子的核式结构模型 课件:26张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 842.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2018-11-11 00:00:00 | ||
图片预览






文档简介
课件26张PPT。18.2原子的核式结构模型
电子是原子的组成部分,由于电子是带负电的,而原子又是中性的,因此推断出原子中还有带正电的物质,几乎占有原子的全部质量。
me=9.109×10-31Kg
e=1.602×10-19C
历史回顾J.J.汤姆孙,1857-1940,英国物理学家,电子的发现者。
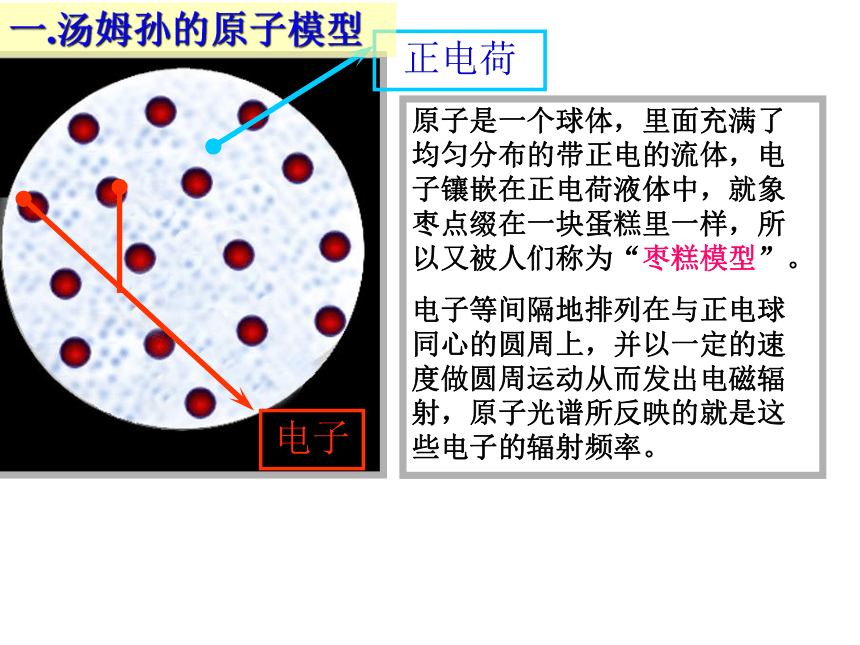
因通过气体电传导性的研究,测出电子的电荷与质量的比值,1906年获诺贝尔物理学奖。思考:那么,这两种物质是怎样构成原子的呢?电子原子是一个球体,里面充满了均匀分布的带正电的流体,电子镶嵌在正电荷液体中,就象枣点缀在一块蛋糕里一样,所以又被人们称为“枣糕模型”。
电子等间隔地排列在与正电球同心的圆周上,并以一定的速度做圆周运动从而发出电磁辐射,原子光谱所反映的就是这些电子的辐射频率。一.汤姆孙的原子模型 以汤姆孙为首的英国剑桥学派,在原子物理学上所取得的这些惊人成就,使欧洲大陆上的物理学家都拜倒在他们的脚下。他的学生卢瑟福也接受了汤姆孙的原子模型,1909年卢瑟福建议其学生兼助手盖革和罗斯顿用α粒子轰击金箔去验证汤姆孙原子模型。让我们来认识一下卢瑟福吧!从经典物理学的角度看,汤姆孙的模型是很成功的。 解释原子是电中性的,电子在原子里是怎样分布的,解释原子为什么会发光,能估计出原子的大小约为一亿分之一厘米。1895年在新西兰大学毕业后,获得英国剑桥大学的奖学金进入卡文迪许实验室,成为汤姆孙的研究生。提出原子结构的核式模型,为原子结构的研究做出很大的贡献。 1898年,在汤姆孙的推荐下,担任加拿大麦吉尔大学的物理教授。 1907年返回英国出任曼彻斯特大学的物理系主任。 1919年接替退休的汤姆孙,担任卡文迪许实验室主任。 1925年当选为英国皇家学会主席。1931年受封为纳尔逊男爵。 1937年10月19日因病在剑桥逝世,与牛顿和法拉第并排安葬,享年66岁。欧内斯特·卢瑟福 1871年8月30日生于新西兰纳尔逊的一个手工业工人家庭。并在新西兰长大。他进入新西兰的坎特伯雷学院学习。 23岁时获得了三个学位(文学学士、文学硕士、理学学士)。科学成就
1、他关于放射性的研究确立了放射性是发自原子内部的变化。为开辟原子物理学做了开创性的工作。
2、1909年起,卢瑟福根据a粒子散射试验现象提出原子核式结构模型。把原子结构的研究引上了正确的轨道,被誉为原子物理学之父。
3、1919年,卢瑟福做了用α粒子轰击氮核的实验,从而发现了质子。?
4、用粒子或γ射线轰击原子核来引起核反应实现人工核反应,成为人们研究原子核和应用核技术的重要手段。桃李满天下
在卢瑟福的悉心培养下,他的学生和助手有多人获得了诺贝尔奖金:
1921年,卢瑟福的助手索迪获诺贝尔化学奖;
1922年,卢瑟福的学生阿斯顿获诺贝尔化学奖;
1922年,卢瑟福的学生玻尔获诺贝尔物理奖;
1927年,卢瑟福的助手威尔逊获诺贝尔物理奖;
1935年,卢瑟福的学生查德威克获诺贝尔物理奖;
1948年,卢瑟福的助手布莱克特获诺贝尔物理奖;
1951年,卢瑟福的学生科克拉夫特和瓦耳顿,共同 获得诺贝尔物理奖;
1978年,卢瑟福的学生卡皮茨获诺贝尔物理奖。
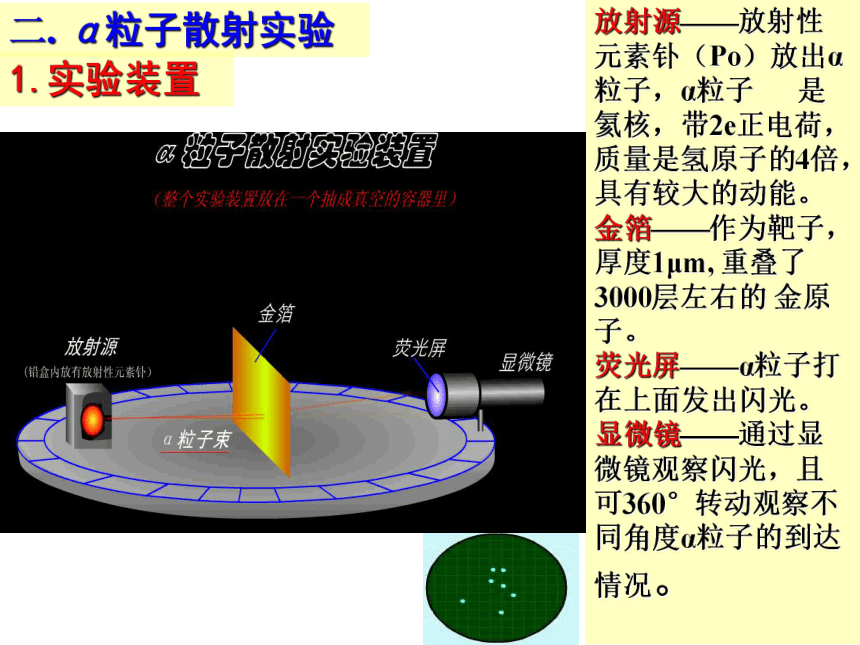
二. α粒子散射实验1.实验装置放射源——放射性元素钋(Po)放出α粒子,α粒子 是氦核,带2e正电荷,质量是氢原子的4倍,具有较大的动能。
金箔——作为靶子,厚度1μm, 重叠了3000层左右的 金原子。
荧光屏——α粒子打在上面发出闪光。
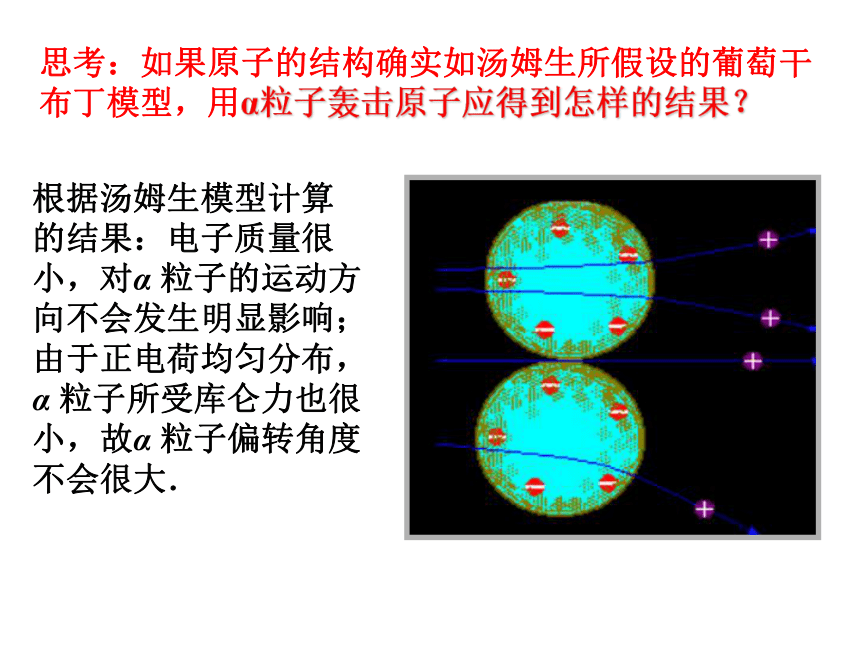
显微镜——通过显微镜观察闪光,且可360°转动观察不同角度α粒子的到达情况。思考:如果原子的结构确实如汤姆生所假设的葡萄干布丁模型,用α粒子轰击原子应得到怎样的结果?根据汤姆生模型计算的结果:电子质量很小,对α 粒子的运动方向不会发生明显影响;由于正电荷均匀分布,α 粒子所受库仑力也很小,故α 粒子偏转角度不会很大.二. α粒子散射实验2.实验现象绝大多数α粒子穿过金箔后仍沿原来方向前进,
少数α粒子(约占8000分之一)发生了较大的偏转,
极少数α粒子的偏转超过了90°,有的甚至几乎被撞了回来。二. α粒子散射实验卢瑟福根据他的导师汤姆生模型计算的结果:
电子质量很小,对α粒子的运动方向不会发生明显影响;由于正电荷均匀分布,α粒子所受库仑力也很小,散射角不超过零点几度,发生大角度偏转的几率几乎是零.实验结果与之前预测完全不一致,所以原子结构模型必须重新构思!
实验结果却是有八千分之一的粒子发生了大角度偏转 !!!
3.实验分析卢瑟福思考 1微米厚的金箔内含3000层原子层,绝大多数α粒子穿过金箔仍沿原方向前进说明什么?
少数α粒子的大角度偏转甚至反弹是怎么造成的?1.在原子的中心有一个很小的核,叫做原子核.
2.原子的全部正电荷和几乎全部质量都集中在原子核里.
3.带负电的电子在核外空间绕着核旋转.三. 原子的核式结构的提出 1. 原子的核式结构模型 α粒子穿过原子时,电子对α粒子运动的影响很小,影响α粒子运动的主要是带正电的原子核。
而绝大多数的α粒子穿过原子时离核较远,受到的库仑斥力很小,运动方向几乎没有改变,只有极少数α粒子可能与核十分接近,受到较大的库仑斥力,才会发生大角度的偏转 。三. 原子的核式结构的提出 2. 对α粒子散射实验现象解释 1919年,卢瑟福用粒子轰击氮核,得到了质子,进而猜想原子核内存在不带电的中子,这一猜想被他的学生查德威克用实验证实,并得到公认.质子中子核子质子数电荷数根据卢瑟福的原子核式模型和α粒子散射的实验数据,可以推算出各种元素原子核的电荷数,还可以估计出原子核的大小。
(1)原子的半径约为10-10m、原子核半径约是10-15m,原子核的体积只占原子的体积的万亿分之一。
(2)原子核所带正电荷数与核外电子数以及该元素在周期表内的原子序数相等。
四.原子核的电荷与尺度 根据卢瑟福的原子结构模型,原子内部是十分“空旷”的,举一个简单的例子:露珠和体育场体育场原子四.原子核的电荷与尺度 - 成功解释了?粒子散射实验, 为人类认识原子结构增添了光辉的一页。-正确地回答了原子的组成问题;【卢瑟福有核原子模型的优越性】
1 .α粒子散射实验装置、现象、意义
2.卢瑟福原子核式结构模型
3.原子核与原子大小的数量级
课堂小结你掌握了吗?课堂练习:1、提出原子核式结构模型的科学家是( )
A、汤姆孙 B、法拉第
C、卢瑟福 D、奥斯特 C2.在用α粒子轰击金箔的实验中,卢瑟福观察到的α粒子的运动情况是( )
A、全部α粒子穿过金属箔后仍按原来的方向前进
B、绝大多数α粒子穿过金属箔后仍按原来的方向前进,少数发生较大偏转,极少数甚至被弹回
C、少数α粒子穿过金属箔后仍按原来的方向前进,绝大多数发生较大偏转,甚至被弹回
D、全部α粒子都发生很大偏转B3、卢瑟福α粒子散射实验的结果( )
A、证明了质子的存在
B、证明了原子核是由质子和中子组成的
C、说明原子的全部正电荷和几乎全部质量都集中在一个很小的核上
D、说明原子的电子只能在某些不连续的轨道上运动C4、当α粒子被重核散射时,如图所示的运动轨迹哪些是不可能存在的( )
BC
5.在α粒子散射实验中,没有考虑α粒子跟电子的碰撞,其原因是( )
A.α粒子不跟电子发生相互作用.
B.α粒子跟电子相碰时,损失的能量极少,可忽略.
C.电子的体积很小,α粒子不会跟电子相碰.
D.由于电子是均匀分布的,α粒子所受电子作用的合力为零.B
6、卢瑟福原子核式结构理论的主要内容有( )
A、原子的中心有个核,叫做原子核
B、原子的正负电荷都均匀分布在整个原子中
C、原子的全部正电荷和几乎全部质量都集中在原子核里
D、带负电的电子在核外绕核旋转ACD 7 在卢瑟福的 粒子散射实验中,有少数 粒子发生大角度偏转,其原因是( )
A、原子的正电荷和绝大部分质量集中在一个很小的核上
B、正电荷在原子中是均匀分布的
C、原子中存在着带负电的电子
D、原子只能处于一系列不连续的能量状态中A
电子是原子的组成部分,由于电子是带负电的,而原子又是中性的,因此推断出原子中还有带正电的物质,几乎占有原子的全部质量。
me=9.109×10-31Kg
e=1.602×10-19C
历史回顾J.J.汤姆孙,1857-1940,英国物理学家,电子的发现者。
因通过气体电传导性的研究,测出电子的电荷与质量的比值,1906年获诺贝尔物理学奖。思考:那么,这两种物质是怎样构成原子的呢?电子原子是一个球体,里面充满了均匀分布的带正电的流体,电子镶嵌在正电荷液体中,就象枣点缀在一块蛋糕里一样,所以又被人们称为“枣糕模型”。
电子等间隔地排列在与正电球同心的圆周上,并以一定的速度做圆周运动从而发出电磁辐射,原子光谱所反映的就是这些电子的辐射频率。一.汤姆孙的原子模型 以汤姆孙为首的英国剑桥学派,在原子物理学上所取得的这些惊人成就,使欧洲大陆上的物理学家都拜倒在他们的脚下。他的学生卢瑟福也接受了汤姆孙的原子模型,1909年卢瑟福建议其学生兼助手盖革和罗斯顿用α粒子轰击金箔去验证汤姆孙原子模型。让我们来认识一下卢瑟福吧!从经典物理学的角度看,汤姆孙的模型是很成功的。 解释原子是电中性的,电子在原子里是怎样分布的,解释原子为什么会发光,能估计出原子的大小约为一亿分之一厘米。1895年在新西兰大学毕业后,获得英国剑桥大学的奖学金进入卡文迪许实验室,成为汤姆孙的研究生。提出原子结构的核式模型,为原子结构的研究做出很大的贡献。 1898年,在汤姆孙的推荐下,担任加拿大麦吉尔大学的物理教授。 1907年返回英国出任曼彻斯特大学的物理系主任。 1919年接替退休的汤姆孙,担任卡文迪许实验室主任。 1925年当选为英国皇家学会主席。1931年受封为纳尔逊男爵。 1937年10月19日因病在剑桥逝世,与牛顿和法拉第并排安葬,享年66岁。欧内斯特·卢瑟福 1871年8月30日生于新西兰纳尔逊的一个手工业工人家庭。并在新西兰长大。他进入新西兰的坎特伯雷学院学习。 23岁时获得了三个学位(文学学士、文学硕士、理学学士)。科学成就
1、他关于放射性的研究确立了放射性是发自原子内部的变化。为开辟原子物理学做了开创性的工作。
2、1909年起,卢瑟福根据a粒子散射试验现象提出原子核式结构模型。把原子结构的研究引上了正确的轨道,被誉为原子物理学之父。
3、1919年,卢瑟福做了用α粒子轰击氮核的实验,从而发现了质子。?
4、用粒子或γ射线轰击原子核来引起核反应实现人工核反应,成为人们研究原子核和应用核技术的重要手段。桃李满天下
在卢瑟福的悉心培养下,他的学生和助手有多人获得了诺贝尔奖金:
1921年,卢瑟福的助手索迪获诺贝尔化学奖;
1922年,卢瑟福的学生阿斯顿获诺贝尔化学奖;
1922年,卢瑟福的学生玻尔获诺贝尔物理奖;
1927年,卢瑟福的助手威尔逊获诺贝尔物理奖;
1935年,卢瑟福的学生查德威克获诺贝尔物理奖;
1948年,卢瑟福的助手布莱克特获诺贝尔物理奖;
1951年,卢瑟福的学生科克拉夫特和瓦耳顿,共同 获得诺贝尔物理奖;
1978年,卢瑟福的学生卡皮茨获诺贝尔物理奖。
二. α粒子散射实验1.实验装置放射源——放射性元素钋(Po)放出α粒子,α粒子 是氦核,带2e正电荷,质量是氢原子的4倍,具有较大的动能。
金箔——作为靶子,厚度1μm, 重叠了3000层左右的 金原子。
荧光屏——α粒子打在上面发出闪光。
显微镜——通过显微镜观察闪光,且可360°转动观察不同角度α粒子的到达情况。思考:如果原子的结构确实如汤姆生所假设的葡萄干布丁模型,用α粒子轰击原子应得到怎样的结果?根据汤姆生模型计算的结果:电子质量很小,对α 粒子的运动方向不会发生明显影响;由于正电荷均匀分布,α 粒子所受库仑力也很小,故α 粒子偏转角度不会很大.二. α粒子散射实验2.实验现象绝大多数α粒子穿过金箔后仍沿原来方向前进,
少数α粒子(约占8000分之一)发生了较大的偏转,
极少数α粒子的偏转超过了90°,有的甚至几乎被撞了回来。二. α粒子散射实验卢瑟福根据他的导师汤姆生模型计算的结果:
电子质量很小,对α粒子的运动方向不会发生明显影响;由于正电荷均匀分布,α粒子所受库仑力也很小,散射角不超过零点几度,发生大角度偏转的几率几乎是零.实验结果与之前预测完全不一致,所以原子结构模型必须重新构思!
实验结果却是有八千分之一的粒子发生了大角度偏转 !!!
3.实验分析卢瑟福思考 1微米厚的金箔内含3000层原子层,绝大多数α粒子穿过金箔仍沿原方向前进说明什么?
少数α粒子的大角度偏转甚至反弹是怎么造成的?1.在原子的中心有一个很小的核,叫做原子核.
2.原子的全部正电荷和几乎全部质量都集中在原子核里.
3.带负电的电子在核外空间绕着核旋转.三. 原子的核式结构的提出 1. 原子的核式结构模型 α粒子穿过原子时,电子对α粒子运动的影响很小,影响α粒子运动的主要是带正电的原子核。
而绝大多数的α粒子穿过原子时离核较远,受到的库仑斥力很小,运动方向几乎没有改变,只有极少数α粒子可能与核十分接近,受到较大的库仑斥力,才会发生大角度的偏转 。三. 原子的核式结构的提出 2. 对α粒子散射实验现象解释 1919年,卢瑟福用粒子轰击氮核,得到了质子,进而猜想原子核内存在不带电的中子,这一猜想被他的学生查德威克用实验证实,并得到公认.质子中子核子质子数电荷数根据卢瑟福的原子核式模型和α粒子散射的实验数据,可以推算出各种元素原子核的电荷数,还可以估计出原子核的大小。
(1)原子的半径约为10-10m、原子核半径约是10-15m,原子核的体积只占原子的体积的万亿分之一。
(2)原子核所带正电荷数与核外电子数以及该元素在周期表内的原子序数相等。
四.原子核的电荷与尺度 根据卢瑟福的原子结构模型,原子内部是十分“空旷”的,举一个简单的例子:露珠和体育场体育场原子四.原子核的电荷与尺度 - 成功解释了?粒子散射实验, 为人类认识原子结构增添了光辉的一页。-正确地回答了原子的组成问题;【卢瑟福有核原子模型的优越性】
1 .α粒子散射实验装置、现象、意义
2.卢瑟福原子核式结构模型
3.原子核与原子大小的数量级
课堂小结你掌握了吗?课堂练习:1、提出原子核式结构模型的科学家是( )
A、汤姆孙 B、法拉第
C、卢瑟福 D、奥斯特 C2.在用α粒子轰击金箔的实验中,卢瑟福观察到的α粒子的运动情况是( )
A、全部α粒子穿过金属箔后仍按原来的方向前进
B、绝大多数α粒子穿过金属箔后仍按原来的方向前进,少数发生较大偏转,极少数甚至被弹回
C、少数α粒子穿过金属箔后仍按原来的方向前进,绝大多数发生较大偏转,甚至被弹回
D、全部α粒子都发生很大偏转B3、卢瑟福α粒子散射实验的结果( )
A、证明了质子的存在
B、证明了原子核是由质子和中子组成的
C、说明原子的全部正电荷和几乎全部质量都集中在一个很小的核上
D、说明原子的电子只能在某些不连续的轨道上运动C4、当α粒子被重核散射时,如图所示的运动轨迹哪些是不可能存在的( )
BC
5.在α粒子散射实验中,没有考虑α粒子跟电子的碰撞,其原因是( )
A.α粒子不跟电子发生相互作用.
B.α粒子跟电子相碰时,损失的能量极少,可忽略.
C.电子的体积很小,α粒子不会跟电子相碰.
D.由于电子是均匀分布的,α粒子所受电子作用的合力为零.B
6、卢瑟福原子核式结构理论的主要内容有( )
A、原子的中心有个核,叫做原子核
B、原子的正负电荷都均匀分布在整个原子中
C、原子的全部正电荷和几乎全部质量都集中在原子核里
D、带负电的电子在核外绕核旋转ACD 7 在卢瑟福的 粒子散射实验中,有少数 粒子发生大角度偏转,其原因是( )
A、原子的正电荷和绝大部分质量集中在一个很小的核上
B、正电荷在原子中是均匀分布的
C、原子中存在着带负电的电子
D、原子只能处于一系列不连续的能量状态中A
