原子的构成[上学期]
图片预览









文档简介
课件30张PPT。蘑菇云——原子弹爆炸原子的构成为什么“原子的爆炸”会产生如此巨大的能量呢?
原子可以再分吗?请你分析 公元前5世纪,希腊哲学家德谟克利特等人认为 :
万物是由大量的不可分割的微粒构成的,即原子。有关原子的假设之一古代19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。有关原子的假设之二近代有关原子的假设之三:汤姆逊原子模型——葡萄干
面包模型。他认为原子是一个带正电的球(面包),
在这个球里面散布着很小的带负电的电子(葡萄干),
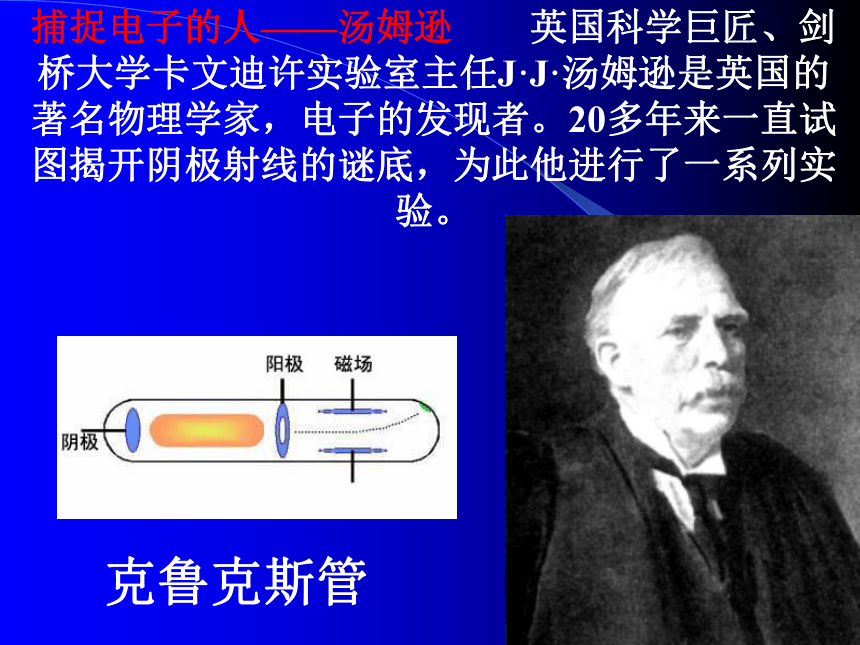
这些电子排成一层一层的环。1897年,英国科学家汤姆生发现了电子。捕捉电子的人——汤姆逊 英国科学巨匠、剑桥大学卡文迪许实验室主任J·J·汤姆逊是英国的著名物理学家,电子的发现者。20多年来一直试图揭开阴极射线的谜底,为此他进行了一系列实验。克鲁克斯管汤姆森原子模型按照汤姆森的原子模型,原子就好像一个大西瓜,里面分散了许多西瓜子,其中西瓜子是带负电的电子,西瓜肉是带正电的物质。
有关原子的假设之四:卢瑟福提出了一个更完整的原子模型:原子结构模型.swf
1、原子的中央是由很重的带正电的质子构成的核。2、远离这个核的是很轻的带负电的电子。
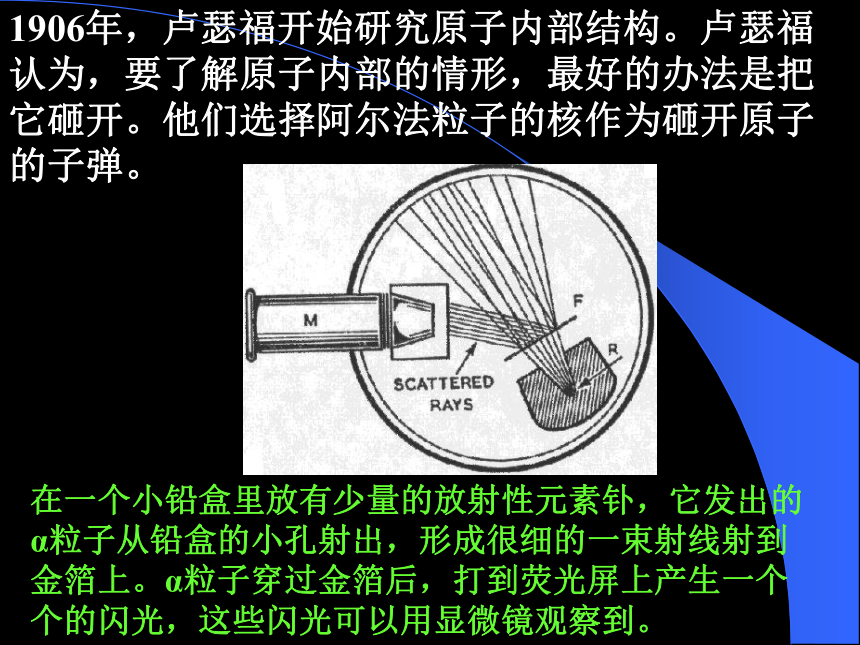
3、电子绕着核转,像行星绕着太阳转一样。 1906年,卢瑟福开始研究原子内部结构。卢瑟福认为,要了解原子内部的情形,最好的办法是把它砸开。他们选择阿尔法粒子的核作为砸开原子的子弹。在一个小铅盒里放有少量的放射性元素钋,它发出的α粒子从铅盒的小孔射出,形成很细的一束射线射到金箔上。α粒子穿过金箔后,打到荧光屏上产生一个个的闪光,这些闪光可以用显微镜观察到。 根据汤姆逊的原子模型,将阿尔法粒子打向金原子表面,就象你想要用一颗小石弹(阿尔法粒子)击向一张巨大的弹子台上紧紧地堆在一起的弹子(金原子),你想会怎么样?你也许会认为石弹一定会穿不过,这原本是卢瑟福他们所预计的实验结果。
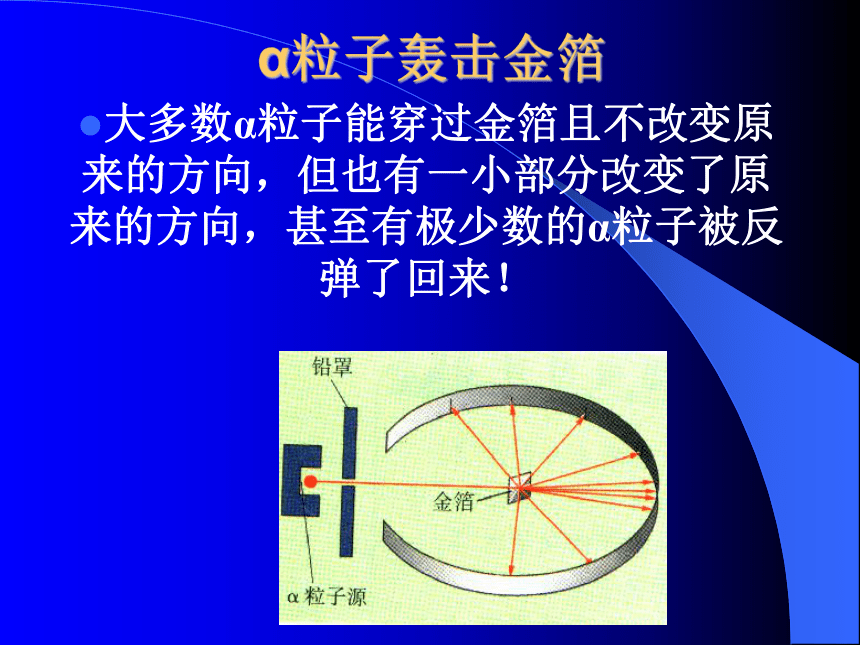
可是,这却不是卢瑟福和盖革在这个试验里所得到的答案。他们照样看到了荧光屏上的闪光,阿尔法粒子能够穿过去!其中绝大部分是笔直穿过去的。但是,有极少数的粒子偏移过大。α粒子轰击金箔大多数α粒子能穿过金箔且不改变原来的方向,但也有一小部分改变了原来的方向,甚至有极少数的α粒子被反弹了回来! 卢瑟福认为,原子是由原子核和核外电
子构成的。电子在原子核外一个相对较大
的空间里随意围绕着一个带正电的很小的
原子核运动。原子结构模型.swf 原来原子的大部分是一个空壳,这就说明了阿尔法粒子为什么能够穿透金箔。交流共享1、为什么大多数的α粒子能够顺利穿过金箔,而只有极少数被反弹回来?
2、 这极少数的α粒子碰到的阻力是大还是小?这种阻力会是来自质量很小的西瓜子(电子)吗?练习册24页3 在金原子中,原子核的半径为原子半径的十万分之一,原子核的体积只占原子体积的几千亿分之一。这样小的原子核却能把轰击它的高速子弹( α粒子)反弹回来,这说明了什么?金原子原子核的质量相对α粒子的质量是很大还是很小?原子核内有什么?1919年,卢瑟福和他的助手用α粒子轰击了氮原子核等,发现原子核里面有质子,一个质子带一个单位正电荷。
1920年,卢瑟福又预言:原子核中有不带电的中性粒子。
1932年,经过不少科学家反复实验后确实发现,原子核里面有中子,中子不带电,中子的质量与质子的质量几乎相等。卢瑟福的预言被证实。质子、中子、电子的电性和电量怎样? 质子(一个 质子带一个单位正电核)
原子核
(带正电)
原子 中子(不带电)原子结构模型.swf
(不显电性)
核外电子(一个电子带一个单位负电荷)重点一:原子结构在化学变化中不能再分,但用其他的方法是可以再分的。核电荷数:原子核所带的电荷数(由原子核内的质子 提供)决定原子的种类。学习笔记几种原子的构成1、由于核内的 数与核外的 数相等,
所以原子不显电性。
2、不同种类的原子,核内 数不同,
核外的 数也不同。核内的质子数不一定等于核内的中子数质子电子质子电子核电荷数=核内质子数=核外电子数11、不同种类的原子,质子数不同。2、原子的质子数等于电子数。3、氢原子没有中子。
4、中子数不一定等于质子数。
5、质子数==核电荷数==电子数
6、质子数决定原子种类。结论不同的原子所含的质子、中子、电子数目不同,所以它们的质量不同,1个氢原子为1.67 ×10-27 kg, 1个氧原子为2.657 ×10-26 kg,可见,原子质量数值太小,书写和使用都不方便。原子的质量又该怎样衡量呢?相对原子质量:指对12C原子(原子核内有6个质子和6个中子的碳原子)
质量的1/12(1. 661 × 10 -27 kg )为标准,其他原子的质
量跟它相比较所得的比,作为这种原子的相对原子质量。 跟质子、中子相比,电子质量很小,通常忽略不计,
原子的质量主要集中在原子核上。质子和中子的质量跟
相对原子质量标准相比较,均约等于1 。相对原子质量=质子数+中子数请记住下面的等量关系:
核内质子数 = 核外电子数 = 核电荷数 (实用于原子)三、相对原子质量以一种碳原子的质量的1/12(约1.66/×10 –27kg)
作为标准,其他原子的质量跟它比较所得的值。
公式: 一个原子的相对原子质量 = M/m
M:一个原子的真实的质量
m:一种碳原子的质量的1/12=质子数+中子数张青莲教授相对原子质量
国际规定以一种碳原子的质量的1/12(约1.66/×10 –27
kg)作为标准,其他原子的质量跟它比较所得的值。
公式: M相= M实/m标
M相:某原子的相对原子质量
M实:被求原子的真实的质量(变)
m标:一种碳原子的质量的1/12(定)
几种原子的构成:11166128816111123171735核电荷数=核内质子数=核外电子数
相对原子质量=质子数+中子数【练习】
1、在分子、原子、原子核、质子、中子、电子等粒子中,
找出符合下列条件的微粒,填在相应的横线上:
(1)能直接构成纯净物的是 (2)能保持 物质化学性质的是 (3)是化学变化中最小微
粒的是 (4)带正电荷 的 是
(5)带负电荷 的是 (6)不显电性的是
(7)质量与氢原子质量近似相等的是
(8)质 量最小的 是 (9)在同一原子中数 目相等的是
分子、原子 分子 原子质子、原子核核外电子中子原子、分子质子中子 电子 质子、电子 143 923、下列有关原子、分子的叙述中,正确的是( )
A 原子是化学变化中的最小粒子
B 原子是不能再分的最小粒子
C 分子是保持物质性质的一种粒子
D 分子的大小及质量都比原子大 A 4、一个氧分子是由两个氧原子构成的,则一个氧分子内含有的质子数是( )
A.8 B.16 C.32 D.64
B二、判断题
5.原子核是由电子和质子组成的。( )
6.在原子里,质子数一定等于中子数和电子数。( )
7.原子核中的中子数可以大于、等于或小于其中的质子数。( )
8.氧化汞中含有氧分子,受热分解可放出氧气。( )
9.相对原子质量就是一个原子的质量。( )
B在线测试1、下列关于原子核的叙述:
(1)通常是由中子和电子构成;(2)通常是由质子和中子构成;(3)带正电荷;(4)不显电性;(5)不能再分;(6)跟原子比较体积很小,但却集中了原子的主要质量。
其中正确的是 ( )
A.(2)(4)(6) B.(2)(3)(6)
C.(1)(3)(5) D.(1)(4)(5)挑战自我道尔顿认为:“一切物质都是由数量巨大的、极微小的粒子构成的,这些粒子间通过引力互相结合,我们不能创造原子,不能分裂原子,我们能实现的变化,无非是把原先结合在一起的原子分开,或原先分开的原子结合起来。”
你同意他的观点吗?请你谈谈对这段话的看法。
原子可以再分吗?请你分析 公元前5世纪,希腊哲学家德谟克利特等人认为 :
万物是由大量的不可分割的微粒构成的,即原子。有关原子的假设之一古代19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。有关原子的假设之二近代有关原子的假设之三:汤姆逊原子模型——葡萄干
面包模型。他认为原子是一个带正电的球(面包),
在这个球里面散布着很小的带负电的电子(葡萄干),
这些电子排成一层一层的环。1897年,英国科学家汤姆生发现了电子。捕捉电子的人——汤姆逊 英国科学巨匠、剑桥大学卡文迪许实验室主任J·J·汤姆逊是英国的著名物理学家,电子的发现者。20多年来一直试图揭开阴极射线的谜底,为此他进行了一系列实验。克鲁克斯管汤姆森原子模型按照汤姆森的原子模型,原子就好像一个大西瓜,里面分散了许多西瓜子,其中西瓜子是带负电的电子,西瓜肉是带正电的物质。
有关原子的假设之四:卢瑟福提出了一个更完整的原子模型:原子结构模型.swf
1、原子的中央是由很重的带正电的质子构成的核。2、远离这个核的是很轻的带负电的电子。
3、电子绕着核转,像行星绕着太阳转一样。 1906年,卢瑟福开始研究原子内部结构。卢瑟福认为,要了解原子内部的情形,最好的办法是把它砸开。他们选择阿尔法粒子的核作为砸开原子的子弹。在一个小铅盒里放有少量的放射性元素钋,它发出的α粒子从铅盒的小孔射出,形成很细的一束射线射到金箔上。α粒子穿过金箔后,打到荧光屏上产生一个个的闪光,这些闪光可以用显微镜观察到。 根据汤姆逊的原子模型,将阿尔法粒子打向金原子表面,就象你想要用一颗小石弹(阿尔法粒子)击向一张巨大的弹子台上紧紧地堆在一起的弹子(金原子),你想会怎么样?你也许会认为石弹一定会穿不过,这原本是卢瑟福他们所预计的实验结果。
可是,这却不是卢瑟福和盖革在这个试验里所得到的答案。他们照样看到了荧光屏上的闪光,阿尔法粒子能够穿过去!其中绝大部分是笔直穿过去的。但是,有极少数的粒子偏移过大。α粒子轰击金箔大多数α粒子能穿过金箔且不改变原来的方向,但也有一小部分改变了原来的方向,甚至有极少数的α粒子被反弹了回来! 卢瑟福认为,原子是由原子核和核外电
子构成的。电子在原子核外一个相对较大
的空间里随意围绕着一个带正电的很小的
原子核运动。原子结构模型.swf 原来原子的大部分是一个空壳,这就说明了阿尔法粒子为什么能够穿透金箔。交流共享1、为什么大多数的α粒子能够顺利穿过金箔,而只有极少数被反弹回来?
2、 这极少数的α粒子碰到的阻力是大还是小?这种阻力会是来自质量很小的西瓜子(电子)吗?练习册24页3 在金原子中,原子核的半径为原子半径的十万分之一,原子核的体积只占原子体积的几千亿分之一。这样小的原子核却能把轰击它的高速子弹( α粒子)反弹回来,这说明了什么?金原子原子核的质量相对α粒子的质量是很大还是很小?原子核内有什么?1919年,卢瑟福和他的助手用α粒子轰击了氮原子核等,发现原子核里面有质子,一个质子带一个单位正电荷。
1920年,卢瑟福又预言:原子核中有不带电的中性粒子。
1932年,经过不少科学家反复实验后确实发现,原子核里面有中子,中子不带电,中子的质量与质子的质量几乎相等。卢瑟福的预言被证实。质子、中子、电子的电性和电量怎样? 质子(一个 质子带一个单位正电核)
原子核
(带正电)
原子 中子(不带电)原子结构模型.swf
(不显电性)
核外电子(一个电子带一个单位负电荷)重点一:原子结构在化学变化中不能再分,但用其他的方法是可以再分的。核电荷数:原子核所带的电荷数(由原子核内的质子 提供)决定原子的种类。学习笔记几种原子的构成1、由于核内的 数与核外的 数相等,
所以原子不显电性。
2、不同种类的原子,核内 数不同,
核外的 数也不同。核内的质子数不一定等于核内的中子数质子电子质子电子核电荷数=核内质子数=核外电子数11、不同种类的原子,质子数不同。2、原子的质子数等于电子数。3、氢原子没有中子。
4、中子数不一定等于质子数。
5、质子数==核电荷数==电子数
6、质子数决定原子种类。结论不同的原子所含的质子、中子、电子数目不同,所以它们的质量不同,1个氢原子为1.67 ×10-27 kg, 1个氧原子为2.657 ×10-26 kg,可见,原子质量数值太小,书写和使用都不方便。原子的质量又该怎样衡量呢?相对原子质量:指对12C原子(原子核内有6个质子和6个中子的碳原子)
质量的1/12(1. 661 × 10 -27 kg )为标准,其他原子的质
量跟它相比较所得的比,作为这种原子的相对原子质量。 跟质子、中子相比,电子质量很小,通常忽略不计,
原子的质量主要集中在原子核上。质子和中子的质量跟
相对原子质量标准相比较,均约等于1 。相对原子质量=质子数+中子数请记住下面的等量关系:
核内质子数 = 核外电子数 = 核电荷数 (实用于原子)三、相对原子质量以一种碳原子的质量的1/12(约1.66/×10 –27kg)
作为标准,其他原子的质量跟它比较所得的值。
公式: 一个原子的相对原子质量 = M/m
M:一个原子的真实的质量
m:一种碳原子的质量的1/12=质子数+中子数张青莲教授相对原子质量
国际规定以一种碳原子的质量的1/12(约1.66/×10 –27
kg)作为标准,其他原子的质量跟它比较所得的值。
公式: M相= M实/m标
M相:某原子的相对原子质量
M实:被求原子的真实的质量(变)
m标:一种碳原子的质量的1/12(定)
几种原子的构成:11166128816111123171735核电荷数=核内质子数=核外电子数
相对原子质量=质子数+中子数【练习】
1、在分子、原子、原子核、质子、中子、电子等粒子中,
找出符合下列条件的微粒,填在相应的横线上:
(1)能直接构成纯净物的是 (2)能保持 物质化学性质的是 (3)是化学变化中最小微
粒的是 (4)带正电荷 的 是
(5)带负电荷 的是 (6)不显电性的是
(7)质量与氢原子质量近似相等的是
(8)质 量最小的 是 (9)在同一原子中数 目相等的是
分子、原子 分子 原子质子、原子核核外电子中子原子、分子质子中子 电子 质子、电子 143 923、下列有关原子、分子的叙述中,正确的是( )
A 原子是化学变化中的最小粒子
B 原子是不能再分的最小粒子
C 分子是保持物质性质的一种粒子
D 分子的大小及质量都比原子大 A 4、一个氧分子是由两个氧原子构成的,则一个氧分子内含有的质子数是( )
A.8 B.16 C.32 D.64
B二、判断题
5.原子核是由电子和质子组成的。( )
6.在原子里,质子数一定等于中子数和电子数。( )
7.原子核中的中子数可以大于、等于或小于其中的质子数。( )
8.氧化汞中含有氧分子,受热分解可放出氧气。( )
9.相对原子质量就是一个原子的质量。( )
B在线测试1、下列关于原子核的叙述:
(1)通常是由中子和电子构成;(2)通常是由质子和中子构成;(3)带正电荷;(4)不显电性;(5)不能再分;(6)跟原子比较体积很小,但却集中了原子的主要质量。
其中正确的是 ( )
A.(2)(4)(6) B.(2)(3)(6)
C.(1)(3)(5) D.(1)(4)(5)挑战自我道尔顿认为:“一切物质都是由数量巨大的、极微小的粒子构成的,这些粒子间通过引力互相结合,我们不能创造原子,不能分裂原子,我们能实现的变化,无非是把原先结合在一起的原子分开,或原先分开的原子结合起来。”
你同意他的观点吗?请你谈谈对这段话的看法。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
