质量守恒定律[上学期]
图片预览






文档简介
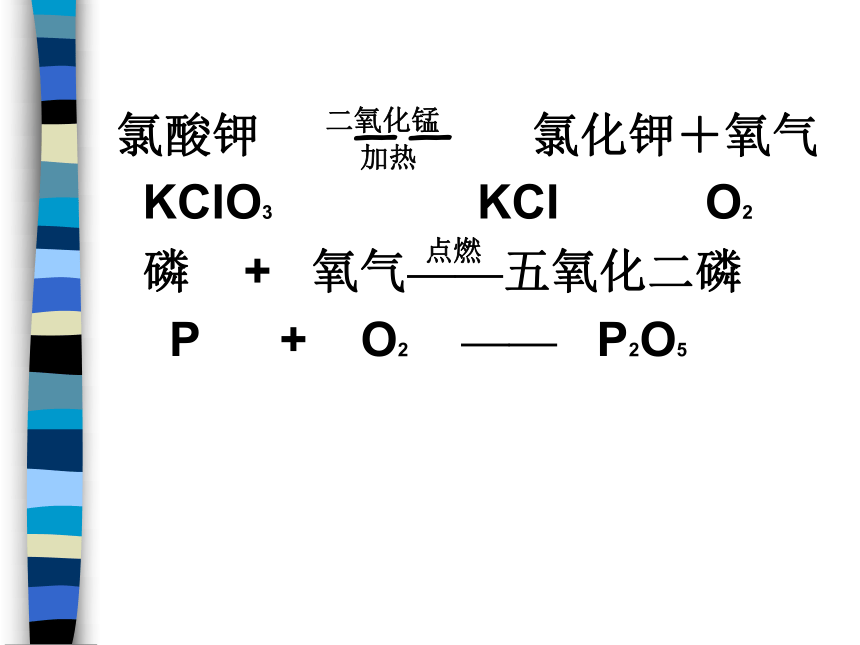
课件24张PPT。5-1质量守恒定律根河一中 闫丽红氯酸钾 —— 氯化钾+氧气
KCIO3 KCI O2
磷 + 氧气——五氧化二磷
P + O2 —— P2O5二氧化锰加热点燃结论:
化学反应前后物质种类、分子种类、物质状态、颜色等发生了变化;
原子种类、元素种类没发生变化;
对于化学反应前后物质的总质量是否发生变化?
实验思考题托盘天平只能用于粗略称量,能称准到 ,称量前应先把游码放在标尺的 ,称量时把 放在左 盘, 放在右盘。
[实验要求]
(1)观察反应物的颜色、状态;
(2)混合后有什么现象?
(3)反应前和反应后物质的总质量有没有变化?一、质量守恒定律:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律就叫质量守恒定律这是从上面两个实验得出的结果!思考:
现有一反应A+B—C,有10克A和5克B反应,反应结束后,还剩3克A,B无剩余,则生成C的质量为多少克?我们可以在锥形瓶中看到有 4 个磷原子和10 个氧原子。玻璃棒锥形瓶反 应容 器结论:因为反应前后原子种类、原子个数都没有改变,原子的质量也没有变化。所以在化学反应前后各物质的质量总和相等。从分子和原子观点来看一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。1、如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果?讨论:2、碳酸钠与盐酸的反应中,若使天平平衡,此试验应怎样改进,谈谈你的方案。
请想一想?本节总结 通过本节课的学习,你有何体会和感受?1,加热10克氯酸钾和二氧化锰的混合物,反应后称得残留物的质量总和为9.52克,则生成氧气的质量为——
2、植物在进行光合作用时,可表示为:二氧化碳+水 光 淀粉+氧气 由此可推知淀粉组成中一定含有 ( )元素,可能含有( )元素。.
3,已知一反应:2A2+3B2→2C,A,B为两元素符号,则C的化学式为
( )
(A)AB (B)A2B2
(C)A3B2 (D)A2B3
根据质量守恒定律解释下列现象:
1、蜡烛燃烧后,质量会减轻。
课后思考题:
铜在空气中易生锈,生成一种叫 “铜绿”的物质,其化学式为Cu2(OH)2CO3,
它由碳、氢、氧、铜四种组成。小明设计了一个实验,证明铜生锈仅是由铜、氧气和水共同作用的结果。
(1)你认为小明的结论正确吗?为什么?
(2)你猜测铜生锈还可能有什么物质参加反应?
(3)怎样防止铜生锈?
使用质量守恒定律注意事项:
1、质量守恒定律的适用范围仅限于化学反应。
2、质量守恒定律的“守恒”,是指质量守恒,而不是体积、反应物的分子个数守恒。
3、参加化学反应的各物质的质量总和并不是各物质的任意质量之和,不参加反应的物质的质量不能计算在内。
?? ?
思考:
方案一的实验中,如锥形瓶口不系小气球,会怎样?7、判断:
1)、10克水变成10克水蒸气,这一变化遵守质量守恒定律。
2)、质量守恒定律的“守恒”包括分子个数的守恒。4,在化学反应A+B=C中,5克A与足量的B反应生成8克C,则参加反应的B的质量是——
A 8克 B 5克, C 3克 D 2克
2、高锰酸钾受热分解后,剩余固 体的质量比原反应物的质量变小。
KCIO3 KCI O2
磷 + 氧气——五氧化二磷
P + O2 —— P2O5二氧化锰加热点燃结论:
化学反应前后物质种类、分子种类、物质状态、颜色等发生了变化;
原子种类、元素种类没发生变化;
对于化学反应前后物质的总质量是否发生变化?
实验思考题托盘天平只能用于粗略称量,能称准到 ,称量前应先把游码放在标尺的 ,称量时把 放在左 盘, 放在右盘。
[实验要求]
(1)观察反应物的颜色、状态;
(2)混合后有什么现象?
(3)反应前和反应后物质的总质量有没有变化?一、质量守恒定律:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律就叫质量守恒定律这是从上面两个实验得出的结果!思考:
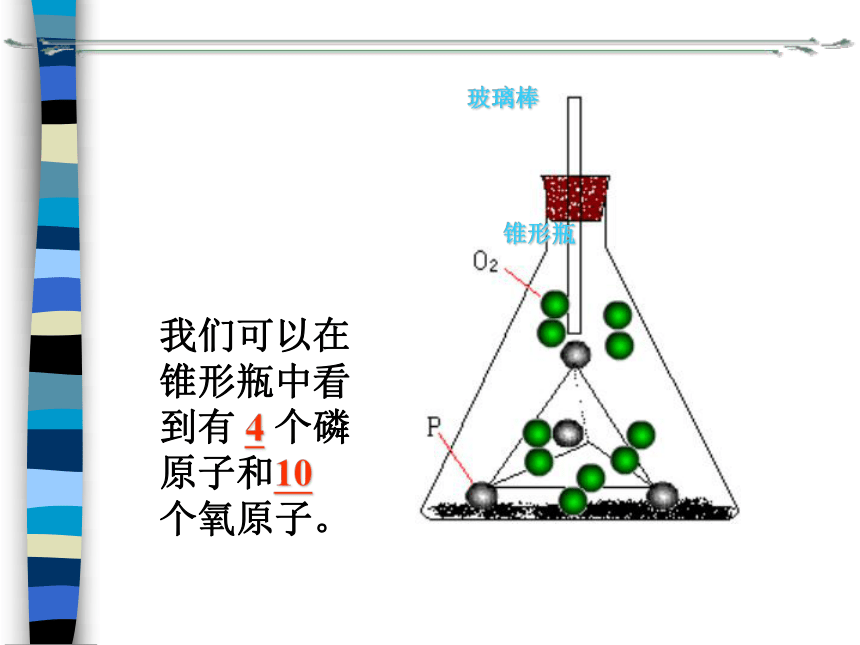
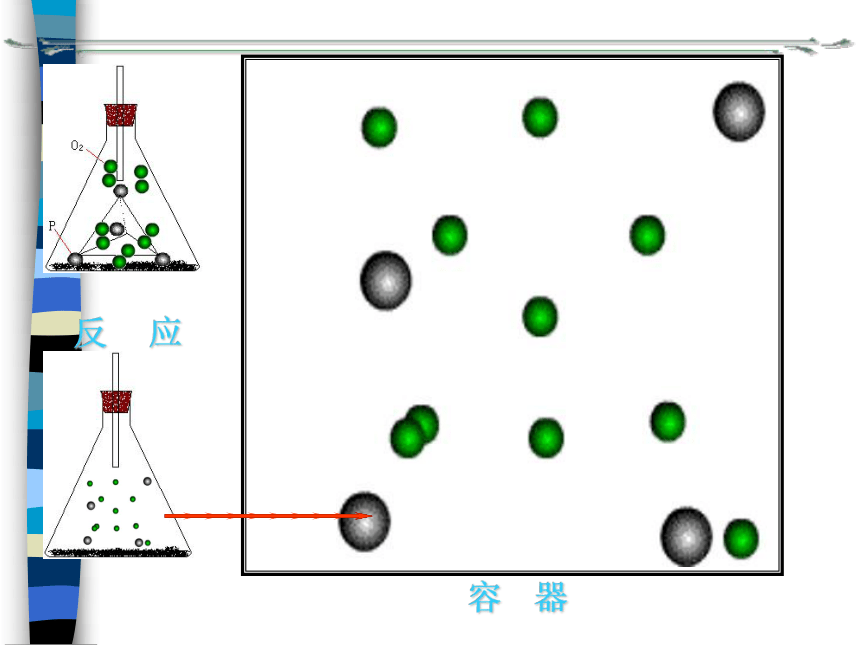
现有一反应A+B—C,有10克A和5克B反应,反应结束后,还剩3克A,B无剩余,则生成C的质量为多少克?我们可以在锥形瓶中看到有 4 个磷原子和10 个氧原子。玻璃棒锥形瓶反 应容 器结论:因为反应前后原子种类、原子个数都没有改变,原子的质量也没有变化。所以在化学反应前后各物质的质量总和相等。从分子和原子观点来看一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。1、如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果?讨论:2、碳酸钠与盐酸的反应中,若使天平平衡,此试验应怎样改进,谈谈你的方案。
请想一想?本节总结 通过本节课的学习,你有何体会和感受?1,加热10克氯酸钾和二氧化锰的混合物,反应后称得残留物的质量总和为9.52克,则生成氧气的质量为——
2、植物在进行光合作用时,可表示为:二氧化碳+水 光 淀粉+氧气 由此可推知淀粉组成中一定含有 ( )元素,可能含有( )元素。.
3,已知一反应:2A2+3B2→2C,A,B为两元素符号,则C的化学式为
( )
(A)AB (B)A2B2
(C)A3B2 (D)A2B3
根据质量守恒定律解释下列现象:
1、蜡烛燃烧后,质量会减轻。
课后思考题:
铜在空气中易生锈,生成一种叫 “铜绿”的物质,其化学式为Cu2(OH)2CO3,
它由碳、氢、氧、铜四种组成。小明设计了一个实验,证明铜生锈仅是由铜、氧气和水共同作用的结果。
(1)你认为小明的结论正确吗?为什么?
(2)你猜测铜生锈还可能有什么物质参加反应?
(3)怎样防止铜生锈?
使用质量守恒定律注意事项:
1、质量守恒定律的适用范围仅限于化学反应。
2、质量守恒定律的“守恒”,是指质量守恒,而不是体积、反应物的分子个数守恒。
3、参加化学反应的各物质的质量总和并不是各物质的任意质量之和,不参加反应的物质的质量不能计算在内。
?? ?
思考:
方案一的实验中,如锥形瓶口不系小气球,会怎样?7、判断:
1)、10克水变成10克水蒸气,这一变化遵守质量守恒定律。
2)、质量守恒定律的“守恒”包括分子个数的守恒。4,在化学反应A+B=C中,5克A与足量的B反应生成8克C,则参加反应的B的质量是——
A 8克 B 5克, C 3克 D 2克
2、高锰酸钾受热分解后,剩余固 体的质量比原反应物的质量变小。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
