人教版高中化学选修五第三章《烃的含氧衍生物》单元测试题(解析版)
文档属性
| 名称 | 人教版高中化学选修五第三章《烃的含氧衍生物》单元测试题(解析版) |

|
|
| 格式 | zip | ||
| 文件大小 | 328.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-11-12 00:00:00 | ||
图片预览




文档简介
第三章《烃的含氧衍生物》单元测试题
一、选择题(每小题只有一个正确答案)
1.塑化剂DEHP的作用类似于人工荷尔蒙,会危害男性生殖能力并促使女性性早熟,长期大量摄取会导致肝癌.其毒性远高于三聚氰胺,会造成免疫力及生殖力下降.下列关于塑化剂邻苯二甲酸二正丁酯说法不正确的是( )
A. 分子式为C16H22O4,可由石油化工原料通过取代,氧化,酯化反应制得
B. 白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
C. 用核磁共振氢谱分析有6个吸收峰
D. 邻苯二甲酸二正丁酯能发生加成,取代和氧化反应
2.白蚁分泌的蚁酸的化学性质与盐酸相似,能腐蚀很多建筑材料,下列材料中最不容易被白蚁蛀蚀的是( )
A. 钢 B. 铜 C. 大理石 D. 生铁
3.下列说法错误的是( )
A. 乙醇和乙酸都是常用调味品的主要成分
B. 乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高
C. 乙醇和乙酸都能发生氧化反应
D. 乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应
4.某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之
比为( )
A. 1∶1∶1 B. 2∶4∶1 C. 1∶2∶1 D. 1∶2∶2
5.下列说法正确的是( )
A. 苯酚与乙醇的官能团都是羟基
B. 炔烃的官能团是碳碳双键
C. 官能团是反应一类化合物物理性质的原子或原子团
D. 饱和一元羧酸的通式为CnH2n+2O2E. 饱和一元羧酸的通式为CnH2n+2O2
6.化学式为C4H8O3的有机物,在浓硫酸存在和加热时,有如下性质:
①能分别与CH3CH2OH和CH3COOH反应,②脱水生成一种能使溴水褪色的物质,此物质只存在一种结构简式,③能生成一种分子式为C4H6O2的五元环状化合物,则C4H8O3的结构简式为( )
A. HOCH2COOCH2CH3 B. CH3CH(OH)CH2COOH
C. HOCH2CH2CH2COOH D. CH3CH2CH(OH)COOH
7.下列说法正确的是( )
A. 室温下,在水中的溶解度:丙三醇>苯酚>1﹣氯丁烷
B. 用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3
C. 用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3
D. 油脂在酸性或碱性条件下均可发生水解反应,且产物相同
8.某含碳、氢、氧的有机物A能发生如图所示的变化:已知
C、D、E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,则A的同分异构体是( )
A. 乙酸 B. 甲酸乙酯 C. 甲酸甲酯 D. 乙酸甲酯
9.实验室用乙酸、乙醇、浓硫酸制取乙酸乙酯,加热蒸馏后,在饱和碳酸钠溶液的上面得到无色油状液体,振荡混合液,有气泡产生,原因是( )
A. 产品中有被蒸馏出的硫酸 B. 有部分未反应的乙醇被蒸馏出来
C. 有部分未反应的乙酸被蒸馏出来 D. 有部分乙醇跟浓硫酸反应
10.下列有关化学实验的叙述不正确的是( )
A. 苯酚俗名石炭酸,向苯酚稀溶液中滴入石蕊试液变浅红色
B. 1﹣戊炔和裂化汽油都能使溴水褪色,且褪色原理相同
C. 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高于铝
D. 将SO2通入Ba(NO3)2溶液中,有白色沉淀生成,且有气体放出
11.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生反应的类型和条件都正确的是( )
A. 答案A B. 答案B C. 答案C D. 答案D
12.由短周期前10号元素组成的物质T和X,有如图所示的转化.X不稳定,易分解.为使得下列转化能够成功进行,方框内不可能加入的反应试剂是( )
A. Ag(NH3)2OH B. 溴水 C. 酸性KMnO4溶液 D. NaOH溶液
13.下列说法中,正确的是( )
A. 实验室可以用氢氧化钠溶液出去乙酸乙酯中的乙酸杂质
B. 乙烯和聚乙烯都可以和溴水发生加成反应
C. 汽油、柴油和植物油的主要成分都是碳氢化合物
D. 分子式同为C3H7Cl,但沸点不同的分子共有两种
14.苯酚()在一定条件下能与氢气加成得到环己醇(),下面关于这两种有机物的叙述中,错误的是( )
A. 都能发生取代反应
B. 都能与金属钠反应放出氢气
C. 苯酚是比碳酸更强的酸,环己醇则显中性
D. 苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液中无明显现象
15.某学生为研究乙二酸(HOOC﹣COOH)的化学性质,进行如下实验:向盛有硫酸酸化的高锰酸钾溶液的试管中滴入适量乙二酸饱和溶液,振荡,观察到试管中溶液由紫红色变为无色,由此可知,乙二酸具有( )
A. 氧化性 B. 还原性 C. 酸性 D. 碱性
二、填空题
16.吃水果能帮助消化,当我们把苹果切开后,不久果肉上便会产生一层咖啡色的物质,好像生了“锈”一般,其原因是果肉里的酚在空气中转变为二醌,这些二醌很快聚合成为咖啡色的聚合物。
(1)这一变化(酚变为二醌)的反应类型为(填字母) 。
a.氧化反应 b.还原反应
c.加成反应 d.取代反应
(2)若要避免苹果“生锈”,请你选择一种保存切开的苹果的方法: ,其原因是 。
17.在①苯酚②甲苯③氯乙烷④乙烯⑤乙醇中,选择编号填写:
(1)能和金属钠反应放出H2的有;(2)能与NaOH溶液反应的有 ;
(3)常温下能与浓溴水反应的有 ;(4)用于制取TNT的是 ;
(5)遇氯化铁溶液呈紫色的是 ;(6)能使酸性KMnO4溶液褪色的烃有 。
18.菠萝酯是一种具有菠萝香气的食用香料,是化合物甲与苯氧乙酸发生酯化反应的产物。
(1)甲一定含有的官能团的名称是________。
(2)5.8 g甲完全燃烧可产生0.3 mol CO2和0.3 mol H2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是____________________________。
(3)菠萝酯的结构简式是____________________________________。
19.已知下列信息:
Ⅰ.在一定条件下甲苯可与Br2发生反应,生成邻溴甲苯与对溴甲苯;
Ⅱ.C6H5—SO3H可发生水解反应生成苯:
C6H5—SO3H+H2O―→C6H6+H2SO4
欲以甲苯为原料合成邻溴甲苯,设计的合成路线如下:
根据以上合成路线回答下列问题:
(1)设计步骤①的目的是____________________________________________________
________________________________________________________________________。
(2)写出反应②的化学方程式:_____________________________________________
________________________________________________________________________。
20.用化学方程式回答下列问题:
(1)在苯酚与水的浊液中加入氢氧化钠溶液后变澄清: ;
(2)实验室通常用电石与水反应制备乙炔: ;
(3)红热的铁跟水蒸气反应: 。
三、实验题
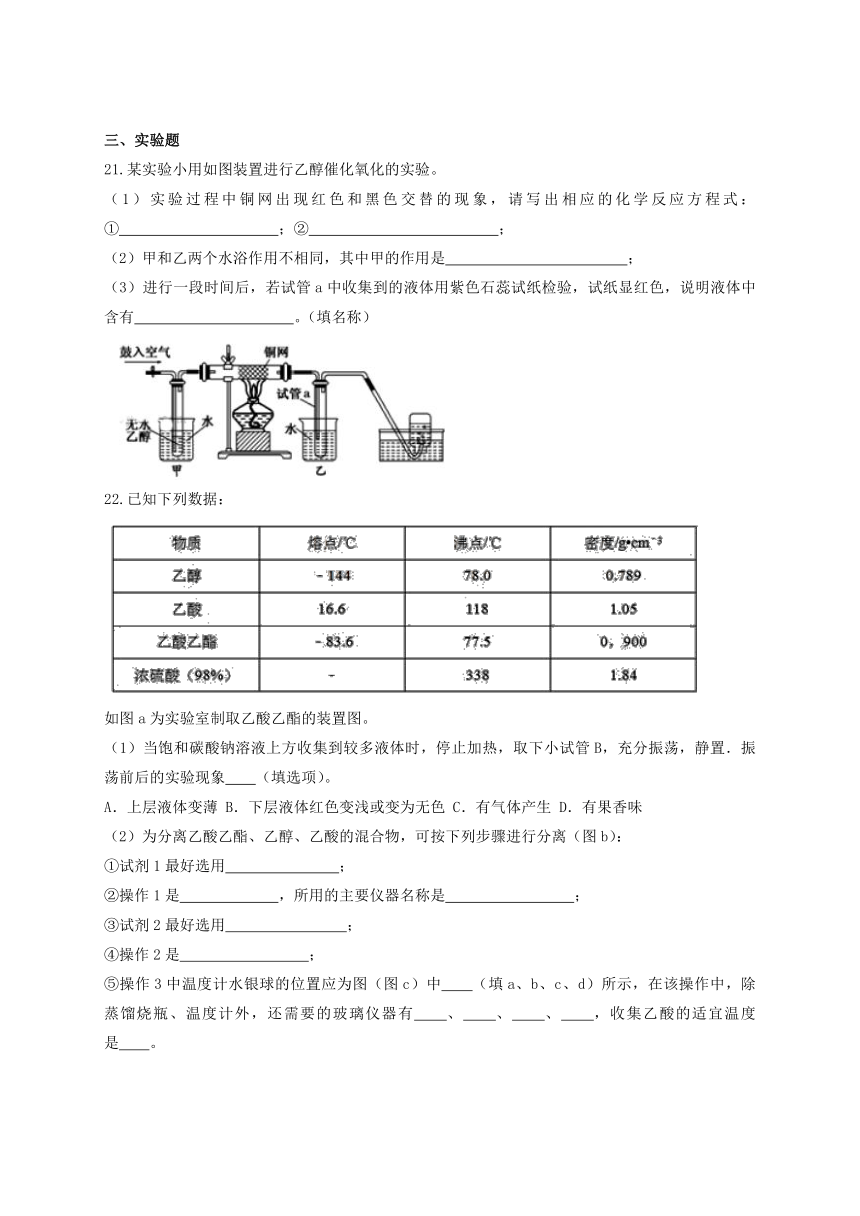
21.某实验小用如图装置进行乙醇催化氧化的实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式: ① ;② ;
(2)甲和乙两个水浴作用不相同,其中甲的作用是 ;
(3)进行一段时间后,若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中含有 。(填名称)
22.已知下列数据:
如图a为实验室制取乙酸乙酯的装置图。
(1)当饱和碳酸钠溶液上方收集到较多液体时,停止加热,取下小试管B,充分振荡,静置.振荡前后的实验现象 (填选项)。
A.上层液体变薄 B.下层液体红色变浅或变为无色 C.有气体产生 D.有果香味
(2)为分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行分离(图b):
①试剂1最好选用 ;
②操作1是 ,所用的主要仪器名称是 ;
③试剂2最好选用 ;
④操作2是 ;
⑤操作3中温度计水银球的位置应为图(图c)中 (填a、b、c、d)所示,在该操作中,除蒸馏烧瓶、温度计外,还需要的玻璃仪器有 、 、 、 ,收集乙酸的适宜温度是 。
四、推断题
23.根据下述转化关系,回答问题:
已知:①+CH3BrCH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
24.食用香料A分子中无支链,B分子中无甲基.B能使Br2的CCl4溶液褪色,1molB与足量Na反应生成0.5molH2,各物质间有如图1转化。
回答下列问题:
(1)在一定条件下能与C发生反应的是 ;
a.Na b.Na2CO3c.Br2/CCl4d.CH3COOH
(2)D分子中的官能团名称是 ,E的结构简式是;
(3)B与F反应生成A的化学方程式是;
(4)F的某种同分异构体甲能发生水解反应,其中的一种产物能发生银镜反应;另一产物在光照条件下的一氯取代物只有两种,且催化氧化后的产物也能发生银镜反应.则甲的结构简式是;
(5)已知醇与某类环醚类之间在和固体碱共热的环境下会有如图2反应:从反应机理分析,该反应类型可称为 ;
(6)工业上由乙出发可以合成有机溶剂戊(C7H14O3),流程图示见图3,
已知:①乙是C的同系物,其催化氧化产物在常温下为气态;②丁分子中有2个甲基,推测戊的结构简式是 。
五、计算题
25.已知NH4+与甲醛(HCHO)在水溶液中有如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O,实验室中有一瓶脱落标签的铵盐,取2.0g样品溶于水,加入足量的HCHO溶液配成100mL溶液,取出10mL,加入0.1mol/L的NaOH溶液,当加入25mL时,溶液恰好呈中性,求铵盐中氮元素的质量分数。
26.两种饱和一元脂肪醛的混合物,其平均相对分子质量为51。取4.08 g混合物与足量银氨溶液共热,生成银21.6 g。试通过计算判断这两种醛是什么醛,并求它们各自的物质的量。
答案解析
1.【答案】B
【解析】A.由结构简式可知,该物质的分子式是C16H22O4,苯通过取代反应生成邻二甲苯、邻二甲苯氧化得到邻苯二甲酸,邻苯二甲酸发生酯化反应得到产物,故A正确;
B.塑化剂溶解在白酒中,不能通过过滤方法除去,故B错误;
C.该物质中含有6个氢原子,用核磁共振氢谱分析有6个吸收峰,故C正确;
D.邻苯二甲酸二正丁酯中含有苯环,能发生加成,取代和氧化反应,故D正确。
2.【答案】B
【解析】因为蚁酸与盐酸性质类似,凡能与盐酸反应的物质也一定能与蚁酸反应,所以四种物质中钢与生铁的主要成分是铁都能与蚁酸反应,大理石的主要成分是碳酸钙也能与蚁酸反应,只有铜不能与蚁酸反应,故选B。
3.【答案】D
【解析】A.料酒的主要成分是乙醇,食醋的主要成分是乙酸,故A正确;
B.乙醇分子之间、乙酸分子之间都存在氢键,乙醇和乙酸常温下为液体,C2H6、C2H4常温下为气体,乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高,故B正确;
C.乙醇可以发生催化氧化,乙醇与乙酸都可以燃烧,燃烧属于氧化反应,故C正确;
D.乙醇和乙酸之间发生酯化反应生成乙酸乙酯,皂化反应是在碱性条件下进行的水解反应生成高级脂肪酸盐与水,与酯化反应的条件不同,物质不同,二者不互为逆反应,故D错误。
4.【答案】B
【解析】金属钠可以与M中的酚羟基、羧基发生反应,氢氧化钠溶液能使酯基水解,溴原子水解,也能与酚羟基和羧基反应,碳酸氢钠溶液只能与羧基发生反应,因此1 mol M消耗的钠、氢氧化钠、碳酸氢钠的物质的量分别为2 mol、4 mol、1 mol。
5.【答案】A
【解析】A.乙醇的结构简式为CH3CH2OH,是乙基和羟基连接形成的,官能团名称为羟基,化学式为:﹣OH;苯酚的结构简式为:,官能团是羟基,羟基与苯环上的碳原子直接相连,又叫“酚羟基”,化学式为:﹣OH,故A正确;
B.分子里含有碳碳三键的不饱和链烃叫炔烃,官能团是碳碳三键,故B错误;
C.决定有机物性质的原子或原子团为官能团,且官能团为电中性,常见官能团有碳碳双键、羟基、醛基、羧基以及酯基、肽键等,故C错误;
D.由羧基和烷基相连而构成的化合物为饱和一元羧酸,饱和一元羧酸通式为CnH2nO2,(n≥1),故D错误。
6.【答案】C
【解析】①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应,说明分子中含有﹣OH和﹣COOH;
②脱水生成一种能使溴水褪色的物质,此物质只存在一种结构简式,则﹣OH邻位上的C原子上有H原子,其只生成一种烯烃,说明应含有﹣CH2OH基团;
③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物,可知﹣OH应分别在4号C原子上,结合有机物的分子式C4H8O3,可知其结构简式为HOCH2CH2CH2COOH,故选C。
7.【答案】A
【解析】A.含﹣OH越多,溶解性越大,卤代烃不溶于水,则室温下,在水中的溶解度:丙三醇>苯酚>1﹣氯丁烷,故A正确;
B.HCOOCH3中两种H,HCOOCH2CH3中有三种H,则用核磁共振氢谱能区分HCOOCH3和HCOOCH2CH3,故B错误;
C.CH3COOH与碳酸钠溶液反应气泡,而Na2CO3溶液与CH3COOCH2CH3会分层,因此可以用Na2CO3溶液能区分CH3COOH和CH3COOCH2CH3,故C错误;
D.油脂在酸性条件下水解产物为高级脂肪酸和甘油,碱性条件下水解产物为高级脂肪酸盐和甘油,水解产物不相同,故D错误。
8.【答案】A
【解析】根据转化图可知,A是酯类,C是羧酸钠,B是醇,D是醛,E是羧酸.又因为A、C、D、E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,因此A是甲酸甲酯,根据同分异构体是分子式相同结构式不同的化合物来判断,A和乙酸互为同分异构体,故选A。
9.【答案】C
【解析】A、浓硫酸是难挥发性酸,在该温度下不会被蒸馏出来,产品中不会有被蒸馏出的硫酸,故A错误;
B、乙醇易挥发,蒸馏出的乙酸乙酯含有乙醇,但由于乙醇不与碳酸钠反应,不会产生气泡,故B错误;
C、由于乙酸易挥发,制备的乙酸乙酯含有乙酸,而乙酸与碳酸钠反应生成了二氧化碳,故C正确;
D、有部分乙醇跟浓硫酸反应,该温度下浓硫酸与乙醇不会生成气体,故D错误。
10.【答案】A
【解析】A.苯酚酸性很弱,向苯酚稀溶液中滴入石蕊试液溶液不变色,故A错误;
B.1﹣戊炔和裂化汽油都能与溴水发生加成反应而褪色,褪色原理相同,故B正确;
C.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高于铝,故C正确;
D.二氧化硫在酸性溶液中被硝酸根离子氧化为硫酸,生成硫酸钡沉淀,硝酸根离子还原成一氧化氮,所以有白色沉淀生成,且有气体放出,故D正确。
12.【答案】D
【解析】由球棍模型可知,T为HCHO,X不稳定,易分解,则X为H2CO3,则方框内物质为氧化剂;
A.Ag(NH3)2OH为弱氧化剂,Ag(NH3)2OH溶液能氧化HCHO生成碳酸,故A错误;
B.溴水中含有HBrO,HBrO能氧化HCHO生成碳酸,故B错误;
C.KMnO4为强氧化剂,酸性KMnO4溶液能氧化HCHO生成碳酸,故C错误;
D.NaOH溶液与HCHO不反应,即方框内物质一定不为NaOH溶液,故D正确。
13.【答案】D
【解析】A.乙酸乙酯在NaOH溶液中彻底水解生成醋酸钠与乙醇,实验室通常用饱和的碳酸钠溶液除去乙酸乙酯中的乙酸杂质,故A错误;
B.乙烯含有C=C双键,可以和溴水发生加成反应,聚乙烯不含C=C双键,不能和溴水发生加成反应,故B错误;
C.汽油、柴油的成分属于碳氢化合物,植物油是高级脂肪酸与甘油形成的酯,故C错误;
D.C3H7Cl的同分异构体有:CH3CH2CH2Cl、CH3CH(Cl)CH3,故分子式为C3H7Cl,沸点不同的分子有2种,故D正确。
14.【答案】C
【解析】A、苯环能发生取代反应,羟基能发生取代反应,所以苯酚、环己醇都能发生取代反应,故A正确;
B、根据醇羟基与酚羟基都能与金属钠反应放出氢气,所以苯酚、环己醇都能与金属钠反应放出氢气,故B正确;
C、根据苯酚的酸性比碳酸弱,环己醇显中性,故C错误;
D、根据酚遇FeCl3溶液作用显紫色,而醇无此性质,所以苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液中无明显现象,故D正确。
15.【答案】B
【解析】根据高锰酸钾由紫红色变为无色,说明高锰酸钾被还原剂还原,所以草酸具有还原性,虽然草酸具有酸性,但从实验现象无法得到,故选B。
16.【答案】(1)a (2)放入水中(其他合理答案也可) 切开的苹果易被氧化,放入水中,使果肉不与空气接触,减缓氧化速率
【解析】根据有机化学中氧化反应的概念:从有机物分子中去掉氢原子的反应称为氧化反应。该变化过程符合这一特点,故属于氧化反应。
17.【答案】(1)①⑤ (2)①③ (3)①④ (4)② (5)① (6)②④
【解析】(1)①苯酚、⑤乙醇能与钠反应放出H2;故答案为:①⑤;
(2)①苯酚、③氯乙烷能与NaOH溶液反应;故答案为:①③;
(3)①苯酚、④乙烯常温下能与浓溴水反应;故答案为:①④;
(4)甲苯能与浓硝酸在浓硫酸的作用下反应生成三硝基甲苯,即TNT;故答案为:②;
(5)苯酚遇氯化铁溶液呈紫色;故答案为:①;
(6)②甲苯、④乙烯是能使酸性KMnO4溶液褪色的烃;故答案为:②④.
18.【答案】(1)羟基
(2)CH2=CH—CH2—OH
(3)OCH2COOCH2CHCH2
【解析】根据酯化反应需要羟基和羧基,甲中肯定含有羟基;先计算出分子式,根据结构特征推导出结构简式是CH2=CH—CH2—OH,菠萝汁的结构简式为OCH2COOCH2CHCH2
19.【答案】(1)在—CH3的对位引入—SO3H,防止在这个位置上引入溴原子而生成副产物对溴甲苯
【解析】合成的最终结果为仅在甲基的邻位引入了一个溴原子。根据信息Ⅰ,如果让甲苯与溴直接反应,将生成邻溴甲苯与对溴甲苯,而对溴甲苯并不是我们需要的产物。为使之不生成对溴甲苯,利用题给信息,可让甲苯与浓硫酸先发生反应,在甲基对位引入一个—SO3H,从而把甲基的对位占据,下一步与溴反应时溴原子只能取代甲基邻位上的一个H原子,最后根据信息Ⅱ将—SO3H去掉即可。
(2)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,配平即可,方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑;
22.【答案】(1)ABCD (2)① 饱和Na2CO3溶液 ②分液 分液漏斗 ③稀硫酸
④蒸馏 ⑤b 酒精灯 冷凝管 牛角管 锥形瓶 略高于118℃
【解析】解:(1)反应物中乙醇、乙酸的沸点较低,制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,碳酸钠水解呈碱性,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,有香味,振荡时乙酸和碳酸钠反应而使溶液红色变浅;
(2)①制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,所以试剂1最好选用饱和Na2CO3溶液;
②乙酸乙酯不溶于碳酸钠溶液,所以混合液会分层,可以通过分液操作分离出乙酸乙酯,使用到的主要仪器为分液漏斗;
③根据流程可知,加入加硫酸能将乙酸钠转化为乙酸,且硫酸难挥发,不影响下步的蒸馏;
④通过操作1得到乙酸乙酯、碳酸钠、乙酸钠、乙醇的混合液,B为乙酸、乙醇、碳酸钠的混合液,通过蒸馏得到乙醇E,然后加入稀硫酸,再蒸馏得到乙酸;
⑤蒸馏的原理:通过控制沸点的不同来实现物质的分离,所以温度计水银球要靠近蒸馏烧瓶支管口,在蒸馏实验中除蒸馏烧瓶、温度计、冷凝管外,还需要的玻璃仪器有酒精灯、牛角管、锥形瓶,乙酸的沸点为118℃,所以收集乙酸的适宜温度是略高于118℃。
23.【答案】(1)1,2-二溴乙烷
(2)取代反应 NaOH醇溶液、加热
【解析】由C比甲苯多两个碳原子,结合反应①条件及信息可知:A为乙烯,B为1,2?二溴乙烷。因C的苯环上一卤代物只有两种,故两个取代基处于对位,C的结构为:。C→D→E为卤代烃的水解(得到醇),再氧化得到酸。比较C、G的分子式可知:C—F→G,为卤代烃消去反应,再加聚反应,得到高分子化合物。
(5)根据题意一分子1,2?二溴乙烷与两分子甲苯发生所给信息的反应,且均为甲基对位氢参与反应。
【解析】F能与NaHCO3反应生成CO2,应含有﹣COOH,由F分子式可知属于饱和一元羧酸,且不存在支链,应为CH3(CH2)4COOH,B和F反应生成A,由分子式可只B中应含有3个C原子,B分子中无甲基,B能使Br2的CCl4溶液褪色,说明含有C=C,1molB与足量Na反应生成0.5molH2,说明分子中含有1个﹣OH,则B应为CH2=CHCH2OH,故A为CH3(CH2)4COOCH2CH=CH2,B与氢气发生加成反应生成C为CH3CH2CH2OH,C氧化生成D为CH3CH2CHO,D进一步氧化生成E为CH3CH2COOH;
(1)C为CH3CH2CH2OH,含有羟基,能与钠、羧酸反应,不能与碳酸钠、溴的四氯化碳溶液反应;
(2)D为CH3CH2CHO,含有官能团为:醛基,E的结构简式是CH3CH2COOH;
(3)B与F反应生成A的化学方程式是(4)F为CH3(CH2)4COOH,F的同分异构体甲能发生水解反应,属于酯类物质,其中的一种产物能发生银镜反应,应为甲酸酯;另一产物在浓H2SO4存在条件下受热不能产生使Br2的CCl4溶液褪色的有机物,说明不能发生消去反应,则﹣OH邻位C原子上不含H原子,但其催化氧化后的产物也能发生银镜反应,说明含有﹣CH2OH,则该有机物的结构简式应为:HCOOCH2C(CH3)3;
(5)从反应机理分析,该反应类型可称为加成反应;
(6)中乙是C的同系物,属于醇类物质,催化氧化产物为醛类,在常温下为气态,则为甲醛,所以乙是甲醇,E为CH3CH2COOH,与丁反应得到戊,根据戊的分子式可以推得丙为:,则丁为:CH3OCH2CH2OH,所以戊的结构简式是:CH3CH2COOCH(CH3)CH2OCH3。
25.【答案】35%
【解析】设铵盐的化学式为(NH4)xR,其相对分子质量为M,由各物质间的定量关系为: 1mol(NH4)xR~xmolNH4+~xmolH+~xmolNaOH 得(2.0/M)×x=0.025,则M/x=80。若为一价铵盐,则该盐的相对分子质量为80,为硝酸铵,其含N量为35%;若为二价铵盐,则该盐的相对分子质量为160,无此铵盐,依此类推。最后确定此铵盐只能为硝酸铵。
26.【答案】甲醛和丙醛,物质的量分别是0.02 mol和0.06 mol
【解析】混合醛的物质的量=4.08 g÷51 g·mol-1=0.08 mol,生成银的物质的量=21.6 g÷108 g·mol-1=0.2 mol>0.08 mol×2,由此可知:混合物中必含有甲醛。设甲醛的物质的量为x,另一种醛A的物质的量为y。
?
MA==58 g·mol-1
根据题意,醛A应符合通式CnH2nO:12n+2n+16=58,
n=3,所以A为丙醛。
综上可知,这两种醛是甲醛和丙醛,物质的量分别是
0.02 mol和0.06 mol。
一、选择题(每小题只有一个正确答案)
1.塑化剂DEHP的作用类似于人工荷尔蒙,会危害男性生殖能力并促使女性性早熟,长期大量摄取会导致肝癌.其毒性远高于三聚氰胺,会造成免疫力及生殖力下降.下列关于塑化剂邻苯二甲酸二正丁酯说法不正确的是( )
A. 分子式为C16H22O4,可由石油化工原料通过取代,氧化,酯化反应制得
B. 白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
C. 用核磁共振氢谱分析有6个吸收峰
D. 邻苯二甲酸二正丁酯能发生加成,取代和氧化反应
2.白蚁分泌的蚁酸的化学性质与盐酸相似,能腐蚀很多建筑材料,下列材料中最不容易被白蚁蛀蚀的是( )
A. 钢 B. 铜 C. 大理石 D. 生铁
3.下列说法错误的是( )
A. 乙醇和乙酸都是常用调味品的主要成分
B. 乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高
C. 乙醇和乙酸都能发生氧化反应
D. 乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应
4.某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之
比为( )
A. 1∶1∶1 B. 2∶4∶1 C. 1∶2∶1 D. 1∶2∶2
5.下列说法正确的是( )
A. 苯酚与乙醇的官能团都是羟基
B. 炔烃的官能团是碳碳双键
C. 官能团是反应一类化合物物理性质的原子或原子团
D. 饱和一元羧酸的通式为CnH2n+2O2E. 饱和一元羧酸的通式为CnH2n+2O2
6.化学式为C4H8O3的有机物,在浓硫酸存在和加热时,有如下性质:
①能分别与CH3CH2OH和CH3COOH反应,②脱水生成一种能使溴水褪色的物质,此物质只存在一种结构简式,③能生成一种分子式为C4H6O2的五元环状化合物,则C4H8O3的结构简式为( )
A. HOCH2COOCH2CH3 B. CH3CH(OH)CH2COOH
C. HOCH2CH2CH2COOH D. CH3CH2CH(OH)COOH
7.下列说法正确的是( )
A. 室温下,在水中的溶解度:丙三醇>苯酚>1﹣氯丁烷
B. 用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3
C. 用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3
D. 油脂在酸性或碱性条件下均可发生水解反应,且产物相同
8.某含碳、氢、氧的有机物A能发生如图所示的变化:已知
C、D、E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,则A的同分异构体是( )
A. 乙酸 B. 甲酸乙酯 C. 甲酸甲酯 D. 乙酸甲酯
9.实验室用乙酸、乙醇、浓硫酸制取乙酸乙酯,加热蒸馏后,在饱和碳酸钠溶液的上面得到无色油状液体,振荡混合液,有气泡产生,原因是( )
A. 产品中有被蒸馏出的硫酸 B. 有部分未反应的乙醇被蒸馏出来
C. 有部分未反应的乙酸被蒸馏出来 D. 有部分乙醇跟浓硫酸反应
10.下列有关化学实验的叙述不正确的是( )
A. 苯酚俗名石炭酸,向苯酚稀溶液中滴入石蕊试液变浅红色
B. 1﹣戊炔和裂化汽油都能使溴水褪色,且褪色原理相同
C. 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高于铝
D. 将SO2通入Ba(NO3)2溶液中,有白色沉淀生成,且有气体放出
11.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生反应的类型和条件都正确的是( )
A. 答案A B. 答案B C. 答案C D. 答案D
12.由短周期前10号元素组成的物质T和X,有如图所示的转化.X不稳定,易分解.为使得下列转化能够成功进行,方框内不可能加入的反应试剂是( )
A. Ag(NH3)2OH B. 溴水 C. 酸性KMnO4溶液 D. NaOH溶液
13.下列说法中,正确的是( )
A. 实验室可以用氢氧化钠溶液出去乙酸乙酯中的乙酸杂质
B. 乙烯和聚乙烯都可以和溴水发生加成反应
C. 汽油、柴油和植物油的主要成分都是碳氢化合物
D. 分子式同为C3H7Cl,但沸点不同的分子共有两种
14.苯酚()在一定条件下能与氢气加成得到环己醇(),下面关于这两种有机物的叙述中,错误的是( )
A. 都能发生取代反应
B. 都能与金属钠反应放出氢气
C. 苯酚是比碳酸更强的酸,环己醇则显中性
D. 苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液中无明显现象
15.某学生为研究乙二酸(HOOC﹣COOH)的化学性质,进行如下实验:向盛有硫酸酸化的高锰酸钾溶液的试管中滴入适量乙二酸饱和溶液,振荡,观察到试管中溶液由紫红色变为无色,由此可知,乙二酸具有( )
A. 氧化性 B. 还原性 C. 酸性 D. 碱性
二、填空题
16.吃水果能帮助消化,当我们把苹果切开后,不久果肉上便会产生一层咖啡色的物质,好像生了“锈”一般,其原因是果肉里的酚在空气中转变为二醌,这些二醌很快聚合成为咖啡色的聚合物。
(1)这一变化(酚变为二醌)的反应类型为(填字母) 。
a.氧化反应 b.还原反应
c.加成反应 d.取代反应
(2)若要避免苹果“生锈”,请你选择一种保存切开的苹果的方法: ,其原因是 。
17.在①苯酚②甲苯③氯乙烷④乙烯⑤乙醇中,选择编号填写:
(1)能和金属钠反应放出H2的有;(2)能与NaOH溶液反应的有 ;
(3)常温下能与浓溴水反应的有 ;(4)用于制取TNT的是 ;
(5)遇氯化铁溶液呈紫色的是 ;(6)能使酸性KMnO4溶液褪色的烃有 。
18.菠萝酯是一种具有菠萝香气的食用香料,是化合物甲与苯氧乙酸发生酯化反应的产物。
(1)甲一定含有的官能团的名称是________。
(2)5.8 g甲完全燃烧可产生0.3 mol CO2和0.3 mol H2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是____________________________。
(3)菠萝酯的结构简式是____________________________________。
19.已知下列信息:
Ⅰ.在一定条件下甲苯可与Br2发生反应,生成邻溴甲苯与对溴甲苯;
Ⅱ.C6H5—SO3H可发生水解反应生成苯:
C6H5—SO3H+H2O―→C6H6+H2SO4
欲以甲苯为原料合成邻溴甲苯,设计的合成路线如下:
根据以上合成路线回答下列问题:
(1)设计步骤①的目的是____________________________________________________
________________________________________________________________________。
(2)写出反应②的化学方程式:_____________________________________________
________________________________________________________________________。
20.用化学方程式回答下列问题:
(1)在苯酚与水的浊液中加入氢氧化钠溶液后变澄清: ;
(2)实验室通常用电石与水反应制备乙炔: ;
(3)红热的铁跟水蒸气反应: 。
三、实验题
21.某实验小用如图装置进行乙醇催化氧化的实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式: ① ;② ;
(2)甲和乙两个水浴作用不相同,其中甲的作用是 ;
(3)进行一段时间后,若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中含有 。(填名称)
22.已知下列数据:
如图a为实验室制取乙酸乙酯的装置图。
(1)当饱和碳酸钠溶液上方收集到较多液体时,停止加热,取下小试管B,充分振荡,静置.振荡前后的实验现象 (填选项)。
A.上层液体变薄 B.下层液体红色变浅或变为无色 C.有气体产生 D.有果香味
(2)为分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行分离(图b):
①试剂1最好选用 ;
②操作1是 ,所用的主要仪器名称是 ;
③试剂2最好选用 ;
④操作2是 ;
⑤操作3中温度计水银球的位置应为图(图c)中 (填a、b、c、d)所示,在该操作中,除蒸馏烧瓶、温度计外,还需要的玻璃仪器有 、 、 、 ,收集乙酸的适宜温度是 。
四、推断题
23.根据下述转化关系,回答问题:
已知:①+CH3BrCH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
24.食用香料A分子中无支链,B分子中无甲基.B能使Br2的CCl4溶液褪色,1molB与足量Na反应生成0.5molH2,各物质间有如图1转化。
回答下列问题:
(1)在一定条件下能与C发生反应的是 ;
a.Na b.Na2CO3c.Br2/CCl4d.CH3COOH
(2)D分子中的官能团名称是 ,E的结构简式是;
(3)B与F反应生成A的化学方程式是;
(4)F的某种同分异构体甲能发生水解反应,其中的一种产物能发生银镜反应;另一产物在光照条件下的一氯取代物只有两种,且催化氧化后的产物也能发生银镜反应.则甲的结构简式是;
(5)已知醇与某类环醚类之间在和固体碱共热的环境下会有如图2反应:从反应机理分析,该反应类型可称为 ;
(6)工业上由乙出发可以合成有机溶剂戊(C7H14O3),流程图示见图3,
已知:①乙是C的同系物,其催化氧化产物在常温下为气态;②丁分子中有2个甲基,推测戊的结构简式是 。
五、计算题
25.已知NH4+与甲醛(HCHO)在水溶液中有如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O,实验室中有一瓶脱落标签的铵盐,取2.0g样品溶于水,加入足量的HCHO溶液配成100mL溶液,取出10mL,加入0.1mol/L的NaOH溶液,当加入25mL时,溶液恰好呈中性,求铵盐中氮元素的质量分数。
26.两种饱和一元脂肪醛的混合物,其平均相对分子质量为51。取4.08 g混合物与足量银氨溶液共热,生成银21.6 g。试通过计算判断这两种醛是什么醛,并求它们各自的物质的量。
答案解析
1.【答案】B
【解析】A.由结构简式可知,该物质的分子式是C16H22O4,苯通过取代反应生成邻二甲苯、邻二甲苯氧化得到邻苯二甲酸,邻苯二甲酸发生酯化反应得到产物,故A正确;
B.塑化剂溶解在白酒中,不能通过过滤方法除去,故B错误;
C.该物质中含有6个氢原子,用核磁共振氢谱分析有6个吸收峰,故C正确;
D.邻苯二甲酸二正丁酯中含有苯环,能发生加成,取代和氧化反应,故D正确。
2.【答案】B
【解析】因为蚁酸与盐酸性质类似,凡能与盐酸反应的物质也一定能与蚁酸反应,所以四种物质中钢与生铁的主要成分是铁都能与蚁酸反应,大理石的主要成分是碳酸钙也能与蚁酸反应,只有铜不能与蚁酸反应,故选B。
3.【答案】D
【解析】A.料酒的主要成分是乙醇,食醋的主要成分是乙酸,故A正确;
B.乙醇分子之间、乙酸分子之间都存在氢键,乙醇和乙酸常温下为液体,C2H6、C2H4常温下为气体,乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高,故B正确;
C.乙醇可以发生催化氧化,乙醇与乙酸都可以燃烧,燃烧属于氧化反应,故C正确;
D.乙醇和乙酸之间发生酯化反应生成乙酸乙酯,皂化反应是在碱性条件下进行的水解反应生成高级脂肪酸盐与水,与酯化反应的条件不同,物质不同,二者不互为逆反应,故D错误。
4.【答案】B
【解析】金属钠可以与M中的酚羟基、羧基发生反应,氢氧化钠溶液能使酯基水解,溴原子水解,也能与酚羟基和羧基反应,碳酸氢钠溶液只能与羧基发生反应,因此1 mol M消耗的钠、氢氧化钠、碳酸氢钠的物质的量分别为2 mol、4 mol、1 mol。
5.【答案】A
【解析】A.乙醇的结构简式为CH3CH2OH,是乙基和羟基连接形成的,官能团名称为羟基,化学式为:﹣OH;苯酚的结构简式为:,官能团是羟基,羟基与苯环上的碳原子直接相连,又叫“酚羟基”,化学式为:﹣OH,故A正确;
B.分子里含有碳碳三键的不饱和链烃叫炔烃,官能团是碳碳三键,故B错误;
C.决定有机物性质的原子或原子团为官能团,且官能团为电中性,常见官能团有碳碳双键、羟基、醛基、羧基以及酯基、肽键等,故C错误;
D.由羧基和烷基相连而构成的化合物为饱和一元羧酸,饱和一元羧酸通式为CnH2nO2,(n≥1),故D错误。
6.【答案】C
【解析】①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应,说明分子中含有﹣OH和﹣COOH;
②脱水生成一种能使溴水褪色的物质,此物质只存在一种结构简式,则﹣OH邻位上的C原子上有H原子,其只生成一种烯烃,说明应含有﹣CH2OH基团;
③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物,可知﹣OH应分别在4号C原子上,结合有机物的分子式C4H8O3,可知其结构简式为HOCH2CH2CH2COOH,故选C。
7.【答案】A
【解析】A.含﹣OH越多,溶解性越大,卤代烃不溶于水,则室温下,在水中的溶解度:丙三醇>苯酚>1﹣氯丁烷,故A正确;
B.HCOOCH3中两种H,HCOOCH2CH3中有三种H,则用核磁共振氢谱能区分HCOOCH3和HCOOCH2CH3,故B错误;
C.CH3COOH与碳酸钠溶液反应气泡,而Na2CO3溶液与CH3COOCH2CH3会分层,因此可以用Na2CO3溶液能区分CH3COOH和CH3COOCH2CH3,故C错误;
D.油脂在酸性条件下水解产物为高级脂肪酸和甘油,碱性条件下水解产物为高级脂肪酸盐和甘油,水解产物不相同,故D错误。
8.【答案】A
【解析】根据转化图可知,A是酯类,C是羧酸钠,B是醇,D是醛,E是羧酸.又因为A、C、D、E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,因此A是甲酸甲酯,根据同分异构体是分子式相同结构式不同的化合物来判断,A和乙酸互为同分异构体,故选A。
9.【答案】C
【解析】A、浓硫酸是难挥发性酸,在该温度下不会被蒸馏出来,产品中不会有被蒸馏出的硫酸,故A错误;
B、乙醇易挥发,蒸馏出的乙酸乙酯含有乙醇,但由于乙醇不与碳酸钠反应,不会产生气泡,故B错误;
C、由于乙酸易挥发,制备的乙酸乙酯含有乙酸,而乙酸与碳酸钠反应生成了二氧化碳,故C正确;
D、有部分乙醇跟浓硫酸反应,该温度下浓硫酸与乙醇不会生成气体,故D错误。
10.【答案】A
【解析】A.苯酚酸性很弱,向苯酚稀溶液中滴入石蕊试液溶液不变色,故A错误;
B.1﹣戊炔和裂化汽油都能与溴水发生加成反应而褪色,褪色原理相同,故B正确;
C.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高于铝,故C正确;
D.二氧化硫在酸性溶液中被硝酸根离子氧化为硫酸,生成硫酸钡沉淀,硝酸根离子还原成一氧化氮,所以有白色沉淀生成,且有气体放出,故D正确。
12.【答案】D
【解析】由球棍模型可知,T为HCHO,X不稳定,易分解,则X为H2CO3,则方框内物质为氧化剂;
A.Ag(NH3)2OH为弱氧化剂,Ag(NH3)2OH溶液能氧化HCHO生成碳酸,故A错误;
B.溴水中含有HBrO,HBrO能氧化HCHO生成碳酸,故B错误;
C.KMnO4为强氧化剂,酸性KMnO4溶液能氧化HCHO生成碳酸,故C错误;
D.NaOH溶液与HCHO不反应,即方框内物质一定不为NaOH溶液,故D正确。
13.【答案】D
【解析】A.乙酸乙酯在NaOH溶液中彻底水解生成醋酸钠与乙醇,实验室通常用饱和的碳酸钠溶液除去乙酸乙酯中的乙酸杂质,故A错误;
B.乙烯含有C=C双键,可以和溴水发生加成反应,聚乙烯不含C=C双键,不能和溴水发生加成反应,故B错误;
C.汽油、柴油的成分属于碳氢化合物,植物油是高级脂肪酸与甘油形成的酯,故C错误;
D.C3H7Cl的同分异构体有:CH3CH2CH2Cl、CH3CH(Cl)CH3,故分子式为C3H7Cl,沸点不同的分子有2种,故D正确。
14.【答案】C
【解析】A、苯环能发生取代反应,羟基能发生取代反应,所以苯酚、环己醇都能发生取代反应,故A正确;
B、根据醇羟基与酚羟基都能与金属钠反应放出氢气,所以苯酚、环己醇都能与金属钠反应放出氢气,故B正确;
C、根据苯酚的酸性比碳酸弱,环己醇显中性,故C错误;
D、根据酚遇FeCl3溶液作用显紫色,而醇无此性质,所以苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液中无明显现象,故D正确。
15.【答案】B
【解析】根据高锰酸钾由紫红色变为无色,说明高锰酸钾被还原剂还原,所以草酸具有还原性,虽然草酸具有酸性,但从实验现象无法得到,故选B。
16.【答案】(1)a (2)放入水中(其他合理答案也可) 切开的苹果易被氧化,放入水中,使果肉不与空气接触,减缓氧化速率
【解析】根据有机化学中氧化反应的概念:从有机物分子中去掉氢原子的反应称为氧化反应。该变化过程符合这一特点,故属于氧化反应。
17.【答案】(1)①⑤ (2)①③ (3)①④ (4)② (5)① (6)②④
【解析】(1)①苯酚、⑤乙醇能与钠反应放出H2;故答案为:①⑤;
(2)①苯酚、③氯乙烷能与NaOH溶液反应;故答案为:①③;
(3)①苯酚、④乙烯常温下能与浓溴水反应;故答案为:①④;
(4)甲苯能与浓硝酸在浓硫酸的作用下反应生成三硝基甲苯,即TNT;故答案为:②;
(5)苯酚遇氯化铁溶液呈紫色;故答案为:①;
(6)②甲苯、④乙烯是能使酸性KMnO4溶液褪色的烃;故答案为:②④.
18.【答案】(1)羟基
(2)CH2=CH—CH2—OH
(3)OCH2COOCH2CHCH2
【解析】根据酯化反应需要羟基和羧基,甲中肯定含有羟基;先计算出分子式,根据结构特征推导出结构简式是CH2=CH—CH2—OH,菠萝汁的结构简式为OCH2COOCH2CHCH2
19.【答案】(1)在—CH3的对位引入—SO3H,防止在这个位置上引入溴原子而生成副产物对溴甲苯
【解析】合成的最终结果为仅在甲基的邻位引入了一个溴原子。根据信息Ⅰ,如果让甲苯与溴直接反应,将生成邻溴甲苯与对溴甲苯,而对溴甲苯并不是我们需要的产物。为使之不生成对溴甲苯,利用题给信息,可让甲苯与浓硫酸先发生反应,在甲基对位引入一个—SO3H,从而把甲基的对位占据,下一步与溴反应时溴原子只能取代甲基邻位上的一个H原子,最后根据信息Ⅱ将—SO3H去掉即可。
(2)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,配平即可,方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑;
22.【答案】(1)ABCD (2)① 饱和Na2CO3溶液 ②分液 分液漏斗 ③稀硫酸
④蒸馏 ⑤b 酒精灯 冷凝管 牛角管 锥形瓶 略高于118℃
【解析】解:(1)反应物中乙醇、乙酸的沸点较低,制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,碳酸钠水解呈碱性,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,有香味,振荡时乙酸和碳酸钠反应而使溶液红色变浅;
(2)①制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,所以试剂1最好选用饱和Na2CO3溶液;
②乙酸乙酯不溶于碳酸钠溶液,所以混合液会分层,可以通过分液操作分离出乙酸乙酯,使用到的主要仪器为分液漏斗;
③根据流程可知,加入加硫酸能将乙酸钠转化为乙酸,且硫酸难挥发,不影响下步的蒸馏;
④通过操作1得到乙酸乙酯、碳酸钠、乙酸钠、乙醇的混合液,B为乙酸、乙醇、碳酸钠的混合液,通过蒸馏得到乙醇E,然后加入稀硫酸,再蒸馏得到乙酸;
⑤蒸馏的原理:通过控制沸点的不同来实现物质的分离,所以温度计水银球要靠近蒸馏烧瓶支管口,在蒸馏实验中除蒸馏烧瓶、温度计、冷凝管外,还需要的玻璃仪器有酒精灯、牛角管、锥形瓶,乙酸的沸点为118℃,所以收集乙酸的适宜温度是略高于118℃。
23.【答案】(1)1,2-二溴乙烷
(2)取代反应 NaOH醇溶液、加热
【解析】由C比甲苯多两个碳原子,结合反应①条件及信息可知:A为乙烯,B为1,2?二溴乙烷。因C的苯环上一卤代物只有两种,故两个取代基处于对位,C的结构为:。C→D→E为卤代烃的水解(得到醇),再氧化得到酸。比较C、G的分子式可知:C—F→G,为卤代烃消去反应,再加聚反应,得到高分子化合物。
(5)根据题意一分子1,2?二溴乙烷与两分子甲苯发生所给信息的反应,且均为甲基对位氢参与反应。
【解析】F能与NaHCO3反应生成CO2,应含有﹣COOH,由F分子式可知属于饱和一元羧酸,且不存在支链,应为CH3(CH2)4COOH,B和F反应生成A,由分子式可只B中应含有3个C原子,B分子中无甲基,B能使Br2的CCl4溶液褪色,说明含有C=C,1molB与足量Na反应生成0.5molH2,说明分子中含有1个﹣OH,则B应为CH2=CHCH2OH,故A为CH3(CH2)4COOCH2CH=CH2,B与氢气发生加成反应生成C为CH3CH2CH2OH,C氧化生成D为CH3CH2CHO,D进一步氧化生成E为CH3CH2COOH;
(1)C为CH3CH2CH2OH,含有羟基,能与钠、羧酸反应,不能与碳酸钠、溴的四氯化碳溶液反应;
(2)D为CH3CH2CHO,含有官能团为:醛基,E的结构简式是CH3CH2COOH;
(3)B与F反应生成A的化学方程式是(4)F为CH3(CH2)4COOH,F的同分异构体甲能发生水解反应,属于酯类物质,其中的一种产物能发生银镜反应,应为甲酸酯;另一产物在浓H2SO4存在条件下受热不能产生使Br2的CCl4溶液褪色的有机物,说明不能发生消去反应,则﹣OH邻位C原子上不含H原子,但其催化氧化后的产物也能发生银镜反应,说明含有﹣CH2OH,则该有机物的结构简式应为:HCOOCH2C(CH3)3;
(5)从反应机理分析,该反应类型可称为加成反应;
(6)中乙是C的同系物,属于醇类物质,催化氧化产物为醛类,在常温下为气态,则为甲醛,所以乙是甲醇,E为CH3CH2COOH,与丁反应得到戊,根据戊的分子式可以推得丙为:,则丁为:CH3OCH2CH2OH,所以戊的结构简式是:CH3CH2COOCH(CH3)CH2OCH3。
25.【答案】35%
【解析】设铵盐的化学式为(NH4)xR,其相对分子质量为M,由各物质间的定量关系为: 1mol(NH4)xR~xmolNH4+~xmolH+~xmolNaOH 得(2.0/M)×x=0.025,则M/x=80。若为一价铵盐,则该盐的相对分子质量为80,为硝酸铵,其含N量为35%;若为二价铵盐,则该盐的相对分子质量为160,无此铵盐,依此类推。最后确定此铵盐只能为硝酸铵。
26.【答案】甲醛和丙醛,物质的量分别是0.02 mol和0.06 mol
【解析】混合醛的物质的量=4.08 g÷51 g·mol-1=0.08 mol,生成银的物质的量=21.6 g÷108 g·mol-1=0.2 mol>0.08 mol×2,由此可知:混合物中必含有甲醛。设甲醛的物质的量为x,另一种醛A的物质的量为y。
?
MA==58 g·mol-1
根据题意,醛A应符合通式CnH2nO:12n+2n+16=58,
n=3,所以A为丙醛。
综上可知,这两种醛是甲醛和丙醛,物质的量分别是
0.02 mol和0.06 mol。
