课题2金属的化学性质-新人教[上学期]
文档属性
| 名称 | 课题2金属的化学性质-新人教[上学期] |  | |
| 格式 | rar | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-12-23 14:52:00 | ||
图片预览






文档简介
课件23张PPT。金属的化学性质课件制作:古南中学 叶洪福第八单元 课题2 实验探究:Ⅰ、金属与氧气的反应Ⅱ、金属与酸反应的探究Ⅲ、金属与盐溶液反应的探究动手与动脑1、镁和铝在常温下就能和空气中的氧气发生氧化反应。一、金属与氧气的反应4Al+3O2==2Al2O3 2Mg+O2==2MgO 2、铜片和铁丝在高温时能与氧气反应3、金不能和氧气反应铁丝在氧气中燃烧真金不怕火炼说明金属的活动性: _______________________镁带在空气中燃烧(1)铝在常温下能与氧气反应,那么我们用的铝制餐
具怎么不易被腐蚀? 铝在常温下发生缓慢氧化:Al+3O2=2Al2O3; 形成一层致密的氧化膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性。(2)为何不宜用钢刷来擦洗铝制餐具呢? 若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。思考:返主页二、金属和酸的反应1、实验现象及反应方程式。
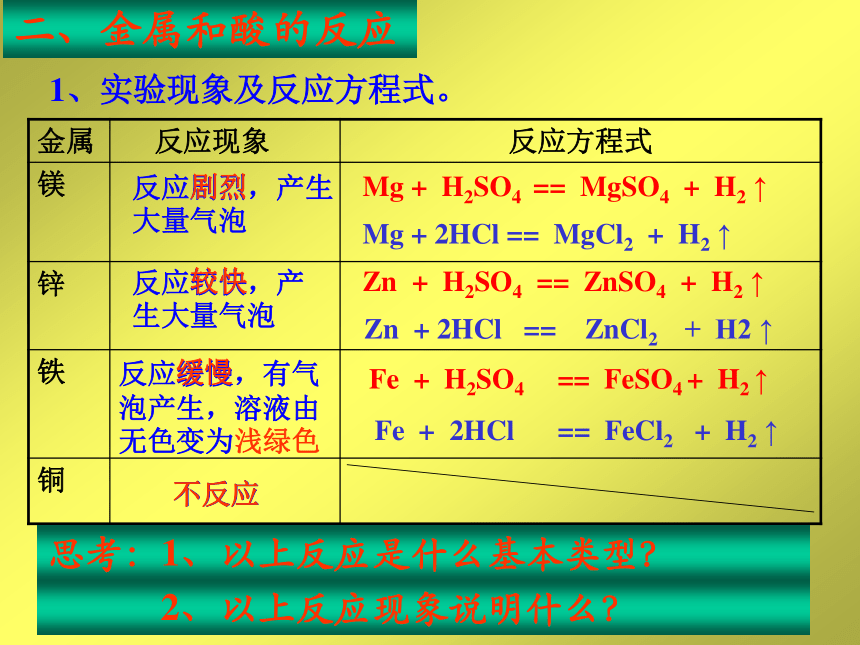
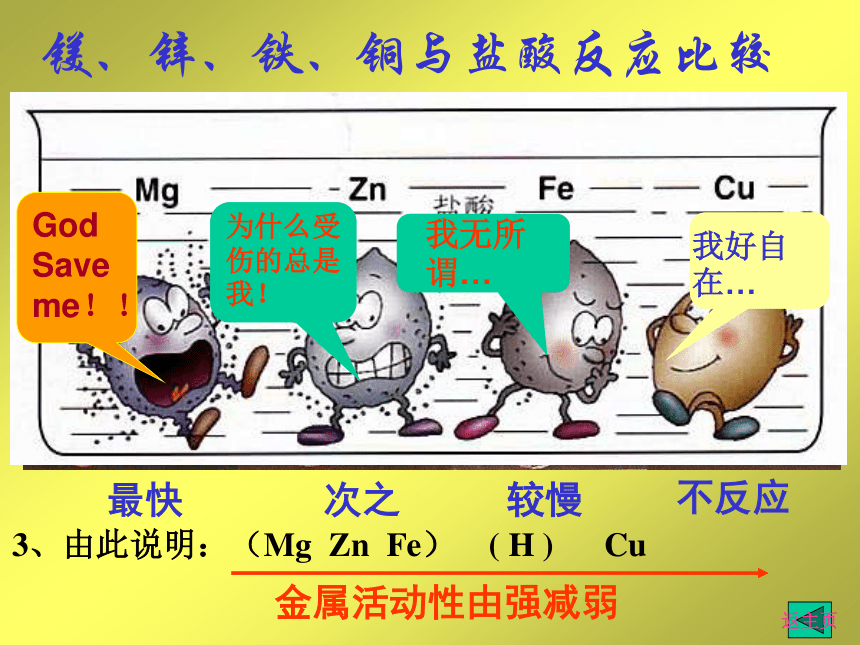
Mg + H2SO4 == MgSO4 + H2 ↑Mg + 2HCl == MgCl2 + H2 ↑Zn + H2SO4 == ZnSO4 + H2 ↑Zn + 2HCl == ZnCl2 + H2 ↑Fe + H2SO4 == FeSO4 + H2 ↑Fe + 2HCl == FeCl2 + H2 ↑反应剧烈,产生大量气泡反应较快,产生大量气泡反应缓慢,有气泡产生,溶液由无色变为浅绿色不反应缓慢较快剧烈不反应思考:1、以上反应是什么基本类型? 2、以上反应现象说明什么? 表达式:ABCAABC2、什么是置换反应?如何用字母表示其反应式?一种_____和一种______反应,生成另一种_____和另一种 _____ 的反应叫做置换反 应单质化合物单质化合物D镁、锌、铁、铜与盐酸反应比较3、由此说明:(Mg Zn Fe) ( H ) Cu返主页说明:铁能把铜从硫酸铜溶液中置换出来,这也是比较金属活动性的依据之一。现象:___________________________________________________________
将铁钉投入到硫酸铜溶液中有何现象? 铁钉表面出现红色物质,液会从蓝色变为浅绿色。Fe + CuSO4 = Cu + FeSO4 该反应的化学方程式:回忆:活动性:Fe﹥Cu看一看三、金属和盐溶液的反应《铝丝与硫酸铜》的反应:实验现象:
铝丝表面出现红色固体,溶液由蓝色变成无色。323实验结论:金属活动性 。Al > Cu三、金属和盐溶液的反应《铜丝与硝酸银》的反应:实验现象:
铜丝表面出现银白色固体,溶液由无色变成蓝色。实验结论:金属活动性 。三、金属和盐溶液的反应Cu>Ag铝丝表面出现红色固体
溶液由蓝色变成无色铜丝表面出现银白色固体,溶液由无色逐渐变成蓝色2Al + 3 CuSO4 == Al2( SO4)3+ 3CuCu + 2AgNO3 ==
Cu(NO3)2 + 2Ag无明显现象2、结论:金属活动性顺序_______________________Al>Cu>Ag三、金属和盐溶液的反应1、实验现象与反应方程式 K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au?
1.在金属活动性顺序中,金属的位置越靠 ,
它的活动性越 。
2.在金属活动性顺序中,位于 前面的金属能置换出盐酸、稀硫酸中的 。
3.在金属活动性顺序中,位于 的金属能把位于 的金属从它们化合物的溶液里置换出来四、金属活动性顺序:(熟记)(K、Ca、Na除外!)(浓硫酸、硝酸无H2 产生)前强氢前面后面氢金属的化学性质一. 金属与氧气的反应4Al+3O2=2Al2O3 2Mg+O2=2MgO 3Fe+2 O2 点燃 Fe3 O4 二.金属与稀盐酸、稀硫酸反应Fe + 2HCl == FeCl2 + H2 ↑
Fe + H2SO4 == FeSO4 + H2 ↑
Zn + 2HCl == ZnCl2 + H2 ↑
Zn + H2SO4 == ZnSO4 + H2 ↑
Mg + 2HCl == MgCl2 + H2 ↑
Mg + H2SO4 == MgSO4 + H2 ↑三.金属与某些化合物
溶液反应2Al + 3 CuSO4 == Al2(SO4 )3 + 3Cu
Cu + 2AgNO3 == Cu (NO3 )2 + 2Ag四.置换反应:由单质和化合物反应,生成单质和化合物的反应。
A+ BC = B + AC 五.金属活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
[例题1].下列金属与酸能发生置换反应而生成氢气的是( )。
A、Fe 和稀H2SO4 B、Ag 和 稀 HCl
C、Zn 和稀HNO3 D、Al 和浓H2SO4A[例题2]. 有X Y Z三种金属,如果把X和Y分别放入稀硫酸中, X 溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,
在Y的表面有银析出,而Z无变化.根据以上事实,判断X Y Z的金属活动顺序. 答: 金属活动性顺序X>Y>Z(1)X>H>Y(2)Y>Ag>Z经典题型:[例题3]:下列方程式中,正确的是( )
A、Cu + 2AgCl = 2Ag + CuCl2
B、Zn + 2AgNO3 = 2Ag + Zn(NO3)2
C、Zn +MgSO4 = Mg + Zn SO4
D、2Fe + 3CuCl2 = 2FeCl3 + 3Cu[例题4]:将一定质量的铁粉放入足量的Cu(NO3)2 和AgNO3的混合溶液中,充分反应后过滤,测得滤渣中只有一种金属,该金属是( )
A、Fe B、Cu C、Ag D、不能确定(例2)B(练习二)C经典题型:1.实验室的废酸液不能直接倒入下水道,是因为 ;
工人师傅在切割钢板时,常用硫酸铜溶液画线是因为 。
2.小兰家中收藏一件清末的铝制佛像,该佛像至今保存十分完好。其主要原因是( )
A.铝不易发生化学反应
B.铝的氧化物容易发生还原反应
C.铝不易被氧化
D.铝易氧化但氧化铝具有保护内部铝的作用练习与实践:D酸易与下水道中的铁或石灰石反应Fe+ CuSO4 = FeSO4 + Cu3.填写下列表格,除去括号内的杂质:Fe+2HCl=FeCl2+H2↑Fe+CuSO4=FeSO4+Cu 溶解、过滤、洗涤溶解、过滤4.判断下列物质能否发生反应?若能,写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
化学方程式:(2) Zn + CuSO4 = Cu + ZnSO4(4) Al +3AgNO3 = Al(NO3)3 + 3Ag(6) Mg + FeSO4 = MgSO4 +Fe√××√×√5、将铁片放入下列溶液中,溶液的质量减少 的是( )
A、稀H2SO4 B、FeSO4溶液
C、CuSO4溶液 D、稀HClC6、一根质量为10g的铁钉,投入一定量的CuSO4溶液中,过一段时间后取出铁钉,洗净干燥后称其质量11g。请计算生成的Cu的质量为多少?解:设生成的Cu的质量为X:
Fe+ CuSO4 = FeSO4 + Cu5664△m811g-10g=1gX164:8=X:1gX =8g答:生成的Cu的质量为8g。拓展探究一一些不法商贩常常用铝制的假银元坑害消费者,小明在市场上买了一枚银元,请你帮他鉴别一下这枚银元,是真?是假?方案一:测密度 (铝的密度小 )方案二:与稀盐酸反应 (铝能反应银不能 )方案三:与硫酸铜溶液反应 (铝能反应银不能 )拓展探究 二现有铁片、铜片、硝酸汞溶液和盐酸几种物质
欲确定Fe、 Cu 、Hg、 H 的活动性顺序,
有如下三种方案:
A. Fe +HCl Fe + Hg(NO3)2 Cu +HCl
B. Fe + HCl Cu + HCl Cu + Hg(NO3)2
C. Fe + HCl Fe + Hg(NO3)2 Cu + Hg(NO3)2
试评价这三种方案:
你认为合理的方案是 ,
理由是: 。B能判断出活动性顺序为Fe﹥H ﹥Cu ﹥Hg 某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,将其分成A、B两份,各加入一定量的锌粉,充分反应后,过滤洗涤,分别得到滤渣和滤液。1.将A得到的滤渣加入到稀盐酸中有气泡产生,则该滤渣中含有的物是 ;
2.往B得到的滤液中滴加稀盐酸,有白色沉淀产生,则对应的滤渣中含有 ,滤液中含有的溶质 。拓展探究 三Zn Cu Ag AgAg(NO3)2 Cu(NO3)2 Zn(NO3)2 化学就象你头顶上的果实,只要肯稍作努力,成功的甜蜜就属于你!
祝你成功!Good Bye!再见
具怎么不易被腐蚀? 铝在常温下发生缓慢氧化:Al+3O2=2Al2O3; 形成一层致密的氧化膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性。(2)为何不宜用钢刷来擦洗铝制餐具呢? 若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。思考:返主页二、金属和酸的反应1、实验现象及反应方程式。
Mg + H2SO4 == MgSO4 + H2 ↑Mg + 2HCl == MgCl2 + H2 ↑Zn + H2SO4 == ZnSO4 + H2 ↑Zn + 2HCl == ZnCl2 + H2 ↑Fe + H2SO4 == FeSO4 + H2 ↑Fe + 2HCl == FeCl2 + H2 ↑反应剧烈,产生大量气泡反应较快,产生大量气泡反应缓慢,有气泡产生,溶液由无色变为浅绿色不反应缓慢较快剧烈不反应思考:1、以上反应是什么基本类型? 2、以上反应现象说明什么? 表达式:ABCAABC2、什么是置换反应?如何用字母表示其反应式?一种_____和一种______反应,生成另一种_____和另一种 _____ 的反应叫做置换反 应单质化合物单质化合物D镁、锌、铁、铜与盐酸反应比较3、由此说明:(Mg Zn Fe) ( H ) Cu返主页说明:铁能把铜从硫酸铜溶液中置换出来,这也是比较金属活动性的依据之一。现象:___________________________________________________________
将铁钉投入到硫酸铜溶液中有何现象? 铁钉表面出现红色物质,液会从蓝色变为浅绿色。Fe + CuSO4 = Cu + FeSO4 该反应的化学方程式:回忆:活动性:Fe﹥Cu看一看三、金属和盐溶液的反应《铝丝与硫酸铜》的反应:实验现象:
铝丝表面出现红色固体,溶液由蓝色变成无色。323实验结论:金属活动性 。Al > Cu三、金属和盐溶液的反应《铜丝与硝酸银》的反应:实验现象:
铜丝表面出现银白色固体,溶液由无色变成蓝色。实验结论:金属活动性 。三、金属和盐溶液的反应Cu>Ag铝丝表面出现红色固体
溶液由蓝色变成无色铜丝表面出现银白色固体,溶液由无色逐渐变成蓝色2Al + 3 CuSO4 == Al2( SO4)3+ 3CuCu + 2AgNO3 ==
Cu(NO3)2 + 2Ag无明显现象2、结论:金属活动性顺序_______________________Al>Cu>Ag三、金属和盐溶液的反应1、实验现象与反应方程式 K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au?
1.在金属活动性顺序中,金属的位置越靠 ,
它的活动性越 。
2.在金属活动性顺序中,位于 前面的金属能置换出盐酸、稀硫酸中的 。
3.在金属活动性顺序中,位于 的金属能把位于 的金属从它们化合物的溶液里置换出来四、金属活动性顺序:(熟记)(K、Ca、Na除外!)(浓硫酸、硝酸无H2 产生)前强氢前面后面氢金属的化学性质一. 金属与氧气的反应4Al+3O2=2Al2O3 2Mg+O2=2MgO 3Fe+2 O2 点燃 Fe3 O4 二.金属与稀盐酸、稀硫酸反应Fe + 2HCl == FeCl2 + H2 ↑
Fe + H2SO4 == FeSO4 + H2 ↑
Zn + 2HCl == ZnCl2 + H2 ↑
Zn + H2SO4 == ZnSO4 + H2 ↑
Mg + 2HCl == MgCl2 + H2 ↑
Mg + H2SO4 == MgSO4 + H2 ↑三.金属与某些化合物
溶液反应2Al + 3 CuSO4 == Al2(SO4 )3 + 3Cu
Cu + 2AgNO3 == Cu (NO3 )2 + 2Ag四.置换反应:由单质和化合物反应,生成单质和化合物的反应。
A+ BC = B + AC 五.金属活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
[例题1].下列金属与酸能发生置换反应而生成氢气的是( )。
A、Fe 和稀H2SO4 B、Ag 和 稀 HCl
C、Zn 和稀HNO3 D、Al 和浓H2SO4A[例题2]. 有X Y Z三种金属,如果把X和Y分别放入稀硫酸中, X 溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,
在Y的表面有银析出,而Z无变化.根据以上事实,判断X Y Z的金属活动顺序. 答: 金属活动性顺序X>Y>Z(1)X>H>Y(2)Y>Ag>Z经典题型:[例题3]:下列方程式中,正确的是( )
A、Cu + 2AgCl = 2Ag + CuCl2
B、Zn + 2AgNO3 = 2Ag + Zn(NO3)2
C、Zn +MgSO4 = Mg + Zn SO4
D、2Fe + 3CuCl2 = 2FeCl3 + 3Cu[例题4]:将一定质量的铁粉放入足量的Cu(NO3)2 和AgNO3的混合溶液中,充分反应后过滤,测得滤渣中只有一种金属,该金属是( )
A、Fe B、Cu C、Ag D、不能确定(例2)B(练习二)C经典题型:1.实验室的废酸液不能直接倒入下水道,是因为 ;
工人师傅在切割钢板时,常用硫酸铜溶液画线是因为 。
2.小兰家中收藏一件清末的铝制佛像,该佛像至今保存十分完好。其主要原因是( )
A.铝不易发生化学反应
B.铝的氧化物容易发生还原反应
C.铝不易被氧化
D.铝易氧化但氧化铝具有保护内部铝的作用练习与实践:D酸易与下水道中的铁或石灰石反应Fe+ CuSO4 = FeSO4 + Cu3.填写下列表格,除去括号内的杂质:Fe+2HCl=FeCl2+H2↑Fe+CuSO4=FeSO4+Cu 溶解、过滤、洗涤溶解、过滤4.判断下列物质能否发生反应?若能,写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
化学方程式:(2) Zn + CuSO4 = Cu + ZnSO4(4) Al +3AgNO3 = Al(NO3)3 + 3Ag(6) Mg + FeSO4 = MgSO4 +Fe√××√×√5、将铁片放入下列溶液中,溶液的质量减少 的是( )
A、稀H2SO4 B、FeSO4溶液
C、CuSO4溶液 D、稀HClC6、一根质量为10g的铁钉,投入一定量的CuSO4溶液中,过一段时间后取出铁钉,洗净干燥后称其质量11g。请计算生成的Cu的质量为多少?解:设生成的Cu的质量为X:
Fe+ CuSO4 = FeSO4 + Cu5664△m811g-10g=1gX164:8=X:1gX =8g答:生成的Cu的质量为8g。拓展探究一一些不法商贩常常用铝制的假银元坑害消费者,小明在市场上买了一枚银元,请你帮他鉴别一下这枚银元,是真?是假?方案一:测密度 (铝的密度小 )方案二:与稀盐酸反应 (铝能反应银不能 )方案三:与硫酸铜溶液反应 (铝能反应银不能 )拓展探究 二现有铁片、铜片、硝酸汞溶液和盐酸几种物质
欲确定Fe、 Cu 、Hg、 H 的活动性顺序,
有如下三种方案:
A. Fe +HCl Fe + Hg(NO3)2 Cu +HCl
B. Fe + HCl Cu + HCl Cu + Hg(NO3)2
C. Fe + HCl Fe + Hg(NO3)2 Cu + Hg(NO3)2
试评价这三种方案:
你认为合理的方案是 ,
理由是: 。B能判断出活动性顺序为Fe﹥H ﹥Cu ﹥Hg 某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,将其分成A、B两份,各加入一定量的锌粉,充分反应后,过滤洗涤,分别得到滤渣和滤液。1.将A得到的滤渣加入到稀盐酸中有气泡产生,则该滤渣中含有的物是 ;
2.往B得到的滤液中滴加稀盐酸,有白色沉淀产生,则对应的滤渣中含有 ,滤液中含有的溶质 。拓展探究 三Zn Cu Ag AgAg(NO3)2 Cu(NO3)2 Zn(NO3)2 化学就象你头顶上的果实,只要肯稍作努力,成功的甜蜜就属于你!
祝你成功!Good Bye!再见
同课章节目录
