课题3 溶液的浓度(共38张PPT)
图片预览











文档简介
课件38张PPT。【课前回顾】1.大多数固体物质溶解度随温度升高而 ,如 。
将其从溶液中分离出来,常采用 的方法。3.极少数固体物质溶解度随温度升高而 ,如 。
将其接近饱和的溶液变成饱和溶液的方法有: 。
。 增大KNO3降温结晶2.少数固体物质溶解度受温度影响 ,如 。
将其从溶液中分离出来,常采用 的方法。不大NaCl蒸发结晶减小Ca(OH)2增加Ca(OH)2蒸发水分或升高温度5.气体的溶解度随温度升高而 ,随压强的增大而 。减小增大4.影响固体物质的溶解度主要因素有: 。 溶质和溶剂的性质 。 与溶质、溶剂的质量 。 温度6. 0℃时,氮气的溶解度为0.024的涵义是: 。
。 在0℃,氮气压强为101kPa时,1体积水最多能溶解0. 024体积氮气无关7.天气闷热时,鱼塘里的鱼为什么总是在接近水面游动? 天气闷热时,气压低、温度高,气体的溶解度随气压的降低而减小,随温度的升高而减小,所以,水中溶解的氧气减少,鱼就浮在水面呼吸。第 九 单 元课题3 溶质的质量分数1.酒精度为52%(V/V)(多见于饮用酒)11.5%(V/V)
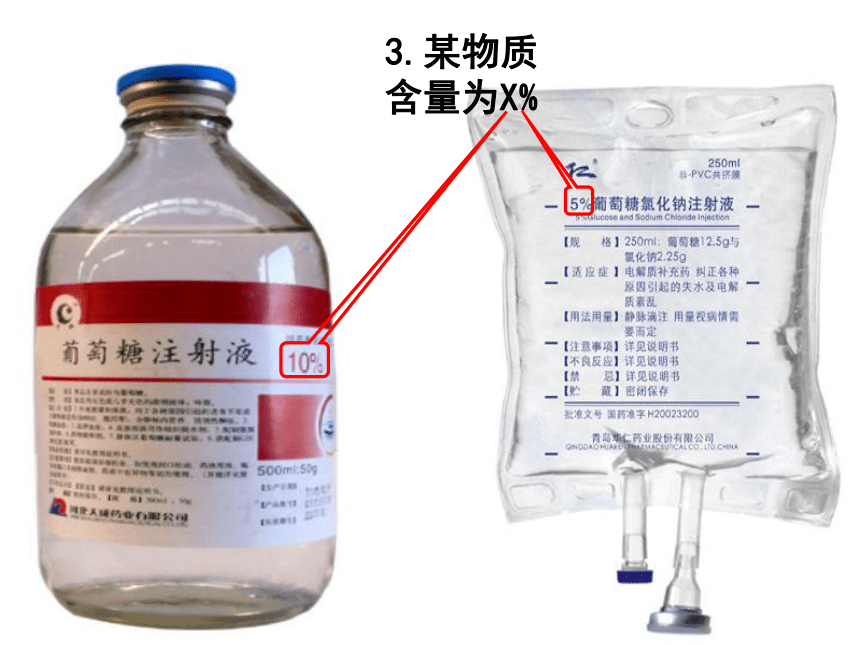
750mL2.100mL中有某物质多少毫克(多见于各种饮料)酱油中某物质含量6mg/100mL(见商标)3.某物质含量为X%展示收集到的有关浓度的商标: 3.某物质含量为2.0%; 大致有:2.100 ml中有某物质多少毫克(多见于各种饮料)1.酒精度为4%(V/V)(多见于饮用酒);
……生理盐水喷洒农药药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木.颜色:淡蓝 蓝色 深蓝【实验9-5】在三支试管中各加入10mL水,然后分别加入约0.5g、1g、1.5g固体硫酸铜。比较三种溶液的颜色。【实验9-5】浅较深深10g10g10g0.5g1g1.5g10.5g11g11.5g同质量的溶剂中,硫酸铜加的越多,溶液颜色越深,此时浓度越大。溶液的浓与稀是指溶质含量的相对多少,它不能准确的表明一定量的溶液中所含溶质的多少。怎样确切的表示一定量的溶液中含多少溶质呢?溶质的质量分数1、概念:2计算公式:溶质质量与溶液质量之比。千万别丢下我啊! 谢谢噢!想一想:上述实验配制的溶液中氯化钠的质量分数是多少?10g20g90g80g10%20%【实验9-6】【实验9-5】在三支试管中各加入10mL水,然后分别加入约0.5g、1g、1.5g固体硫酸铜。比较三种溶液的颜色。4.8%9.1%13.0%只要知道了“溶液的质量”“溶质的质量”“溶剂的质量”以及“溶质的质量分数”四个量中的任何两个,我们就可以求出另外两个。涉及的公式:m(质)+m(剂)=m(液)公式变形:6010015%25%20%5040245023664减少 每份溶液作不同操作的情况分析减少 减少 减少 减少 减少 减少 减少 减少 不变 不变 不变 不变 不变 增大 增大 增大 增大 增大 增大 例1:在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150Kg这种溶液,需要氯化钠和水的质量各是多少?解:
需要氯化钠的质量需要水的质量答:需要氯化钠24Kg和水126Kg。实验室要配制500mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水各多少克?解:需要氢氧化钠的质量需要水的质量氢氧化钠溶液的质量答:需要氢氧化钠55Kg和水495Kg。【练习】例:据《南湖晚报》报道:今年7月20日,浙江嘉善一农民蔡某,因用自己全部家当种植的十亩果树“离奇”死亡而伤心过度,蔡某自尽而亡。 据家人介绍,蔡某本人不太识字,7月18日从农技站买来250千克(溶质质量分数为40%)的液体肥料,蔡某掺了1000千克水后进行喷洒。两天后,十亩果树“离奇”死亡。 请通过计算帮助分析,果树死亡的原因,是不是所用肥料的浓度不符合使用说明呢? (该液体肥料的标签注明:该种液体肥料施花时宜用2%,施蔬菜瓜果时宜用0.5—1%,施果树不能超过3%,否则,叶片会大面积死亡。)解:稀释前、后溶质的质量为 =250 Kg×40%=100Kg
加水后,ω==8%>3%所以,果树是因为喷洒了过浓的液体肥料而死亡的。用这250Kg液体肥料喷洒果树,实际需要水 Kg。3083.3 例题2: 化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?分析:解决这道题的关键是什么?解:稀释前溶质的质量=稀释后溶质的质量如果把50g换成50mL,还需要什么条件?设稀释后溶液的质量为x50g×98%=X ×20% 需要水的质量=245g-50g=195g答:需要水的质量为195g。 解得:X=245g 变式: 化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50mL质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?解:浓硫酸的质量=50cm3×1.84g/cm3=92g92g×98%=X ×20% 需要水的质量=450.8g-92g=358.8g答:需要水的质量为358.8g。解得:X=450.8g 设稀释后溶液的质量为x关于溶液稀释问题的计算公式:m液=ρ· Vm浓×ω浓 = m稀×ω稀配制500mL20%的硫酸需要98%的硫酸多少毫升?设需98%的硫酸的体积为xx × 1.84g/cm3 × 98%=500 cm3 × 1.14g/cm3 × 20%解得:x = 63.2 cm3答:配制500mL20%的硫酸需要63.2mL98% 的硫酸。解:【变式练习】溶解度与溶质的质量分数概念间有什么区别和联系? KNO3溶液的溶质的质量分数31.6% 是指: 200C时KNO3溶解度31.6g是指: 100g这种硝酸钾溶液中含有31.6gKNO3。在200C 时,100g水最多溶解31.6gKNO3。溶解度与溶质的质量分数的比较意义表示物质溶解性的度量,受外界温度、压强等影响。 表示溶液中溶质质量的多少,不受外界条件限制。一定100克 不一定 不一定 不一定一定达到饱和 克 — 饱和溶液的溶质质量分数与溶解度S的联系: 饱和溶液中溶质的质量分数=20℃时,氯化钠的溶解度为36g。⑴将50g氯化钠加入20℃的100g水中,充分搅拌,所得溶液的溶质质量分数为 。⑵20℃时,氯化钠溶液的最大溶质质量分数为 。26.5%26.5%【练习】1.有100g溶质质量分数为10%的氯化钠溶液,若将其溶质质量分数减小至5%,若采用加水稀释的方法,需加水的质量是多少?2.有100g溶质质量分数为10%的硝酸钾溶液,若将其溶质质量分数增加到20%,若采用蒸发溶剂的方法,需蒸发掉水的质量是多少?将某溶液加水稀释,使其溶质的质量分数变为原来的一半,需加水的质量等于原溶液的质量。将某溶液蒸发浓缩,使其溶质的质量分数变为原来的2倍,需蒸发掉水的质量等于原溶液质量的一半。需加水的质量为100g。【规律性结论】【规律性结论】需蒸发掉水的质量为50g。【练习】配制步骤:用氯化钠固体和水配制50g溶质质量分数为6%的氯化钠溶液。⑴计算:⑵称量:用玻璃棒搅拌, 使氯化钠充分溶解。需食盐质量=50 g× 6% = 3 g , 用天平称量 3 g食盐,倒入烧杯中。⑶溶解:盖好瓶塞并贴上标签,放到试剂柜中。⑷装瓶,贴标签:【实验9-7】需水质量=50 g– 3 g= 47 g,需水体积= 47 mL.用量筒量取47mL水,倒入盛有氯化钠的烧杯中。将配好的溶液装入试剂瓶中,氯化钠溶液
6%1.用固体配制一定溶质质量分数的溶液的步骤有: 2.用固体配制一定溶质质量分数的溶液时常用仪器有:⑴计算⑵称量(称取和量取)⑶溶解⑷装瓶,贴标签3.若用浓溶液配制稀溶液,操作步骤还是一样吗?玻璃棒烧杯、胶头滴管、量筒、托盘天平、药匙、4.若用浓溶液配制稀溶液,所用的仪器也一样吗?答;不一样,其步骤为:⑴计算⑵量取⑶溶解⑷装瓶,贴标签答;不一样,所用仪器中没有托盘天平和药匙。【思考后归纳】下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误。⑴药品使用错误,错用了氯化钾;⑵取下的瓶塞没有倒放;⑶药品和砝码在托盘上放反了;⑷倾倒水时,量筒没有紧挨烧杯壁;⑸用温度计搅拌。答:错误有:【练习】哪些原因会造成所配制溶液的质量分数偏小?⑴天平未调平,指针向左偏时,就开始称量;讨论②倾倒水后,量筒中有少量水未倒干净;⑷计算错误,溶质算少了(或溶剂算多了);⑺用来配制溶液的烧杯不干燥;⑸倾倒氯化钠时,有氯化钠撒落在烧杯外;⑻量取水时,仰视量筒。⑹药品不纯;③装瓶时,有溶液洒落瓶外。下面两种情况会造成所配制溶液的质量分数偏小吗?⑶使用了游码称量时,砝码和称量物放颠倒了;⑵称量时,左盘放纸,右盘未放纸;①倾倒水时,有少量水溅出烧杯外;用固体溶质配制一定质量分数的溶液时,阅读 家庭小实验 ‘自制汽水’ 回答下列问题:2.产生二氧化碳的物质主要是什么?3.为了加快溶解,能否用开水代替凉开水呢?为什么?1.自制汽水主要用到的物品有哪些?4.所使用的小苏打和柠檬酸为什么必须是食品级的?物品有:小苏打、柠檬酸、凉开水、果汁、白糖、饮料瓶等。小苏打和柠檬酸反应产生二氧化碳。不能。气体的溶解度随温度的升高而减小,所以,热的开水中,二氧化碳溶解的少。防止非食品级的小苏打和柠檬酸中含有有害物质。 第九单元知识点检测(1)1.从微观的角度看,溶液的形成过程是溶质的 均匀扩散到溶剂分子之间的过程。2.硫酸铜溶液是 色的,是因为溶液中含有 离子;硫酸亚铁溶液是 色的,因为溶液中有 (填符号)。3.稀硫酸中 是溶质, 是溶剂。足量的锌加入稀硫酸中,所得溶液的溶质是 ,溶剂是 。4.石灰水中 是溶质, 是溶剂。足量的铜加入硝酸银溶液中,所得溶液的溶质是 ,溶剂是 。5. 75%的酒精溶液中 (填化学式,下同)是溶质, 是溶剂。6.①用汽油洗去油污是利用了 的原理。
②用洗涤剂去油污,是因为洗涤剂具有 功能。7.溶于水,①放热的物质可以是 ,②吸热的可以是 ,③温度没有改变的可以是 ,④与水反应放热的物质可以是 。某化学样品由氯化钠和碳酸钠组成。取该样品6g放于烧杯中,用44g水完全溶解,再向烧杯中滴加稀盐酸至不再有气泡产生,共用去稀盐酸20g,这时溶液质量为67.8g。计算:涉及化学反应的质量分数的有关计算(1)所加入的稀盐酸的质量分数,
(2)所取样品中氯化钠的质量分数,
(3)反应后所得溶液中溶质的质量分数。解:生成CO2的质量=6g+44g+20g - 67.8g=2.2g106 73 117 44x y z 2.2g设参加反应的Na2CO3、HCl质量分别为x、y,生成NaCl质量为z.Na2CO3+2HCl = 2NaCl+H2O+CO2↑解得:x=5.3g解得:y=3.65g解得:z=5.85g(1)稀盐酸的质量分数=(2)样品中氯化钠的质量=6g - 5.3g=0.7g 样品中氯化钠的质量分数= (3)反应后所得溶液中溶质的质量分数为:答:稀盐酸的质量分数为:18.25%,样品中氯化钠的质量分数为:11.7%,反应后所得溶液中溶质的质量分数为:9.7%。取20.4g Na2CO3和NaCl组成的固体混合物样品,倒入烧杯中,再向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:(1) 固体样品中NaCl的质量分数;
(2) 当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液,通过计算求出其中溶质的质量分数。【练习】
将其从溶液中分离出来,常采用 的方法。3.极少数固体物质溶解度随温度升高而 ,如 。
将其接近饱和的溶液变成饱和溶液的方法有: 。
。 增大KNO3降温结晶2.少数固体物质溶解度受温度影响 ,如 。
将其从溶液中分离出来,常采用 的方法。不大NaCl蒸发结晶减小Ca(OH)2增加Ca(OH)2蒸发水分或升高温度5.气体的溶解度随温度升高而 ,随压强的增大而 。减小增大4.影响固体物质的溶解度主要因素有: 。 溶质和溶剂的性质 。 与溶质、溶剂的质量 。 温度6. 0℃时,氮气的溶解度为0.024的涵义是: 。
。 在0℃,氮气压强为101kPa时,1体积水最多能溶解0. 024体积氮气无关7.天气闷热时,鱼塘里的鱼为什么总是在接近水面游动? 天气闷热时,气压低、温度高,气体的溶解度随气压的降低而减小,随温度的升高而减小,所以,水中溶解的氧气减少,鱼就浮在水面呼吸。第 九 单 元课题3 溶质的质量分数1.酒精度为52%(V/V)(多见于饮用酒)11.5%(V/V)
750mL2.100mL中有某物质多少毫克(多见于各种饮料)酱油中某物质含量6mg/100mL(见商标)3.某物质含量为X%展示收集到的有关浓度的商标: 3.某物质含量为2.0%; 大致有:2.100 ml中有某物质多少毫克(多见于各种饮料)1.酒精度为4%(V/V)(多见于饮用酒);
……生理盐水喷洒农药药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木.颜色:淡蓝 蓝色 深蓝【实验9-5】在三支试管中各加入10mL水,然后分别加入约0.5g、1g、1.5g固体硫酸铜。比较三种溶液的颜色。【实验9-5】浅较深深10g10g10g0.5g1g1.5g10.5g11g11.5g同质量的溶剂中,硫酸铜加的越多,溶液颜色越深,此时浓度越大。溶液的浓与稀是指溶质含量的相对多少,它不能准确的表明一定量的溶液中所含溶质的多少。怎样确切的表示一定量的溶液中含多少溶质呢?溶质的质量分数1、概念:2计算公式:溶质质量与溶液质量之比。千万别丢下我啊! 谢谢噢!想一想:上述实验配制的溶液中氯化钠的质量分数是多少?10g20g90g80g10%20%【实验9-6】【实验9-5】在三支试管中各加入10mL水,然后分别加入约0.5g、1g、1.5g固体硫酸铜。比较三种溶液的颜色。4.8%9.1%13.0%只要知道了“溶液的质量”“溶质的质量”“溶剂的质量”以及“溶质的质量分数”四个量中的任何两个,我们就可以求出另外两个。涉及的公式:m(质)+m(剂)=m(液)公式变形:6010015%25%20%5040245023664减少 每份溶液作不同操作的情况分析减少 减少 减少 减少 减少 减少 减少 减少 不变 不变 不变 不变 不变 增大 增大 增大 增大 增大 增大 例1:在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150Kg这种溶液,需要氯化钠和水的质量各是多少?解:
需要氯化钠的质量需要水的质量答:需要氯化钠24Kg和水126Kg。实验室要配制500mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水各多少克?解:需要氢氧化钠的质量需要水的质量氢氧化钠溶液的质量答:需要氢氧化钠55Kg和水495Kg。【练习】例:据《南湖晚报》报道:今年7月20日,浙江嘉善一农民蔡某,因用自己全部家当种植的十亩果树“离奇”死亡而伤心过度,蔡某自尽而亡。 据家人介绍,蔡某本人不太识字,7月18日从农技站买来250千克(溶质质量分数为40%)的液体肥料,蔡某掺了1000千克水后进行喷洒。两天后,十亩果树“离奇”死亡。 请通过计算帮助分析,果树死亡的原因,是不是所用肥料的浓度不符合使用说明呢? (该液体肥料的标签注明:该种液体肥料施花时宜用2%,施蔬菜瓜果时宜用0.5—1%,施果树不能超过3%,否则,叶片会大面积死亡。)解:稀释前、后溶质的质量为 =250 Kg×40%=100Kg
加水后,ω==8%>3%所以,果树是因为喷洒了过浓的液体肥料而死亡的。用这250Kg液体肥料喷洒果树,实际需要水 Kg。3083.3 例题2: 化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?分析:解决这道题的关键是什么?解:稀释前溶质的质量=稀释后溶质的质量如果把50g换成50mL,还需要什么条件?设稀释后溶液的质量为x50g×98%=X ×20% 需要水的质量=245g-50g=195g答:需要水的质量为195g。 解得:X=245g 变式: 化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50mL质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?解:浓硫酸的质量=50cm3×1.84g/cm3=92g92g×98%=X ×20% 需要水的质量=450.8g-92g=358.8g答:需要水的质量为358.8g。解得:X=450.8g 设稀释后溶液的质量为x关于溶液稀释问题的计算公式:m液=ρ· Vm浓×ω浓 = m稀×ω稀配制500mL20%的硫酸需要98%的硫酸多少毫升?设需98%的硫酸的体积为xx × 1.84g/cm3 × 98%=500 cm3 × 1.14g/cm3 × 20%解得:x = 63.2 cm3答:配制500mL20%的硫酸需要63.2mL98% 的硫酸。解:【变式练习】溶解度与溶质的质量分数概念间有什么区别和联系? KNO3溶液的溶质的质量分数31.6% 是指: 200C时KNO3溶解度31.6g是指: 100g这种硝酸钾溶液中含有31.6gKNO3。在200C 时,100g水最多溶解31.6gKNO3。溶解度与溶质的质量分数的比较意义表示物质溶解性的度量,受外界温度、压强等影响。 表示溶液中溶质质量的多少,不受外界条件限制。一定100克 不一定 不一定 不一定一定达到饱和 克 — 饱和溶液的溶质质量分数与溶解度S的联系: 饱和溶液中溶质的质量分数=20℃时,氯化钠的溶解度为36g。⑴将50g氯化钠加入20℃的100g水中,充分搅拌,所得溶液的溶质质量分数为 。⑵20℃时,氯化钠溶液的最大溶质质量分数为 。26.5%26.5%【练习】1.有100g溶质质量分数为10%的氯化钠溶液,若将其溶质质量分数减小至5%,若采用加水稀释的方法,需加水的质量是多少?2.有100g溶质质量分数为10%的硝酸钾溶液,若将其溶质质量分数增加到20%,若采用蒸发溶剂的方法,需蒸发掉水的质量是多少?将某溶液加水稀释,使其溶质的质量分数变为原来的一半,需加水的质量等于原溶液的质量。将某溶液蒸发浓缩,使其溶质的质量分数变为原来的2倍,需蒸发掉水的质量等于原溶液质量的一半。需加水的质量为100g。【规律性结论】【规律性结论】需蒸发掉水的质量为50g。【练习】配制步骤:用氯化钠固体和水配制50g溶质质量分数为6%的氯化钠溶液。⑴计算:⑵称量:用玻璃棒搅拌, 使氯化钠充分溶解。需食盐质量=50 g× 6% = 3 g , 用天平称量 3 g食盐,倒入烧杯中。⑶溶解:盖好瓶塞并贴上标签,放到试剂柜中。⑷装瓶,贴标签:【实验9-7】需水质量=50 g– 3 g= 47 g,需水体积= 47 mL.用量筒量取47mL水,倒入盛有氯化钠的烧杯中。将配好的溶液装入试剂瓶中,氯化钠溶液
6%1.用固体配制一定溶质质量分数的溶液的步骤有: 2.用固体配制一定溶质质量分数的溶液时常用仪器有:⑴计算⑵称量(称取和量取)⑶溶解⑷装瓶,贴标签3.若用浓溶液配制稀溶液,操作步骤还是一样吗?玻璃棒烧杯、胶头滴管、量筒、托盘天平、药匙、4.若用浓溶液配制稀溶液,所用的仪器也一样吗?答;不一样,其步骤为:⑴计算⑵量取⑶溶解⑷装瓶,贴标签答;不一样,所用仪器中没有托盘天平和药匙。【思考后归纳】下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误。⑴药品使用错误,错用了氯化钾;⑵取下的瓶塞没有倒放;⑶药品和砝码在托盘上放反了;⑷倾倒水时,量筒没有紧挨烧杯壁;⑸用温度计搅拌。答:错误有:【练习】哪些原因会造成所配制溶液的质量分数偏小?⑴天平未调平,指针向左偏时,就开始称量;讨论②倾倒水后,量筒中有少量水未倒干净;⑷计算错误,溶质算少了(或溶剂算多了);⑺用来配制溶液的烧杯不干燥;⑸倾倒氯化钠时,有氯化钠撒落在烧杯外;⑻量取水时,仰视量筒。⑹药品不纯;③装瓶时,有溶液洒落瓶外。下面两种情况会造成所配制溶液的质量分数偏小吗?⑶使用了游码称量时,砝码和称量物放颠倒了;⑵称量时,左盘放纸,右盘未放纸;①倾倒水时,有少量水溅出烧杯外;用固体溶质配制一定质量分数的溶液时,阅读 家庭小实验 ‘自制汽水’ 回答下列问题:2.产生二氧化碳的物质主要是什么?3.为了加快溶解,能否用开水代替凉开水呢?为什么?1.自制汽水主要用到的物品有哪些?4.所使用的小苏打和柠檬酸为什么必须是食品级的?物品有:小苏打、柠檬酸、凉开水、果汁、白糖、饮料瓶等。小苏打和柠檬酸反应产生二氧化碳。不能。气体的溶解度随温度的升高而减小,所以,热的开水中,二氧化碳溶解的少。防止非食品级的小苏打和柠檬酸中含有有害物质。 第九单元知识点检测(1)1.从微观的角度看,溶液的形成过程是溶质的 均匀扩散到溶剂分子之间的过程。2.硫酸铜溶液是 色的,是因为溶液中含有 离子;硫酸亚铁溶液是 色的,因为溶液中有 (填符号)。3.稀硫酸中 是溶质, 是溶剂。足量的锌加入稀硫酸中,所得溶液的溶质是 ,溶剂是 。4.石灰水中 是溶质, 是溶剂。足量的铜加入硝酸银溶液中,所得溶液的溶质是 ,溶剂是 。5. 75%的酒精溶液中 (填化学式,下同)是溶质, 是溶剂。6.①用汽油洗去油污是利用了 的原理。
②用洗涤剂去油污,是因为洗涤剂具有 功能。7.溶于水,①放热的物质可以是 ,②吸热的可以是 ,③温度没有改变的可以是 ,④与水反应放热的物质可以是 。某化学样品由氯化钠和碳酸钠组成。取该样品6g放于烧杯中,用44g水完全溶解,再向烧杯中滴加稀盐酸至不再有气泡产生,共用去稀盐酸20g,这时溶液质量为67.8g。计算:涉及化学反应的质量分数的有关计算(1)所加入的稀盐酸的质量分数,
(2)所取样品中氯化钠的质量分数,
(3)反应后所得溶液中溶质的质量分数。解:生成CO2的质量=6g+44g+20g - 67.8g=2.2g106 73 117 44x y z 2.2g设参加反应的Na2CO3、HCl质量分别为x、y,生成NaCl质量为z.Na2CO3+2HCl = 2NaCl+H2O+CO2↑解得:x=5.3g解得:y=3.65g解得:z=5.85g(1)稀盐酸的质量分数=(2)样品中氯化钠的质量=6g - 5.3g=0.7g 样品中氯化钠的质量分数= (3)反应后所得溶液中溶质的质量分数为:答:稀盐酸的质量分数为:18.25%,样品中氯化钠的质量分数为:11.7%,反应后所得溶液中溶质的质量分数为:9.7%。取20.4g Na2CO3和NaCl组成的固体混合物样品,倒入烧杯中,再向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:(1) 固体样品中NaCl的质量分数;
(2) 当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液,通过计算求出其中溶质的质量分数。【练习】
同课章节目录
