溶解度[下学期]
图片预览










文档简介
课件30张PPT。 第九单元 溶液
课题2 溶解度
前提测评:写出下列溶液的溶质的化学式:
1、食盐水 2、盐酸 ;
3、石灰水 4、稀硫酸 ;
5、酒精溶液 .NaClHClCa(OH)2H2SO4C2H5OH2、下列物质溶于水时,使溶液的温度明显升高的是 ( ),溶液的温度明显降低的是 ( )。
A、蔗糖 B、食盐
C、硝酸铵 D、氢氧化钠
1、把少量的下列各物质分别放入水里,充分振荡后可形成溶液的是( )
A、葡萄糖 B、面粉
C、花生油 D、冰块
ADC3、现有一瓶蓄电池用的稀硫酸,从上半部分取出少量,测得其密度为1.2g/cm3,若从底部取出少量测定其密度,则测得底部的稀硫酸的密度值为 ( )
A、大于1.2/cm3 B、小于1.2/cm3
C、等于1.2/cm3 D、无法确定C注明:稀硫酸是溶液,溶液是均一的,即各部分性质相同。1)饱和溶液:在一定温度下,向
一定量溶剂里加入某种溶质,当溶
质不能继续溶解时,所得的溶液.2)不饱和溶液:还能继续溶解的溶液3) 提醒:只有指明“在一定量溶剂里”和“在一定温度下”,溶液的“饱和”和“不饱和”才有意义。不饱和
溶液增加溶质、降低温度、饱和
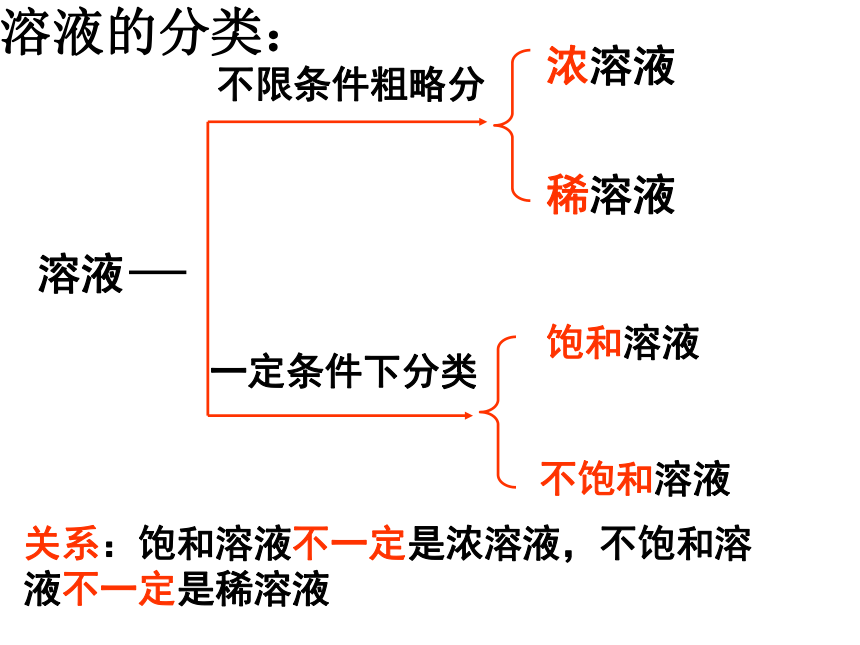
溶液增加溶剂、升高温度蒸发溶剂 饱和溶液与不饱和溶液的转化溶液不限条件粗略分一定条件下分类浓溶液稀溶液饱和溶液不饱和溶液
关系:饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液
溶液的分类:1、下列关于饱和溶液的说法中,错误的是( )
A、在温度不变时,KNO3的饱和溶液不能再溶解KNO3
B、当温度升高时,饱和溶液一定能继续溶解溶质
C、稀溶液一定是不饱和溶液,浓溶液一定是饱和溶液
D、改变温度可以使不饱和溶液变成饱和溶液B、C巩固练习2、某课外小组需一定浓度的KNO3溶液做实验,怎样使KNO3固体较快地溶于水中?说明理由。
建议1:溶解时加热,粒子扩散速度加快,使溶解速度加快
建议2;溶解时不断的搅拌,使粒子运动速度加快,迅速扩散到溶剂中去。
建议3:溶解前先将固体研碎,增大固体与水的接触面积,使溶解速度加快3、室温下,向一定质量的氯化钠溶液中加入10克氯化钠固体,充分搅拌后,尚有部分未溶解,加入10克水后,固体全部溶解。下列判断正确的是( )
A、加水前一定是饱和溶液
B、加水前可能是饱和溶液
C、加水后一定是饱和溶液
D、加水后一定是不饱和溶液
A4、在一定温度下,将一瓶接近饱几的硝酸钾溶液转化成饱和溶液的方法( )①升高温度②降低温度③增加溶质④增加溶剂⑤蒸发溶剂
A、①②③
B、②③⑤
C、②③④
D、③④⑤
B5、使20℃的饱和食盐溶液变成不饱和溶液,可采取的措施是( )
A、加水
B、取出一些食盐溶液
C、加食盐
D、蒸发水A6、在一定温度下,一定量的水中,不断加入食盐晶体,能正确表示溶解的食盐质量m与时间t的关系的图象的是 ( )
D7. 下列说法正确的是( )
A、凡是均一、稳定的液体都是溶液B、饱和溶液所含的溶质一定比不饱和溶液的多
C、析出晶体后的溶液一定是饱和溶液D、某物质的溶液达到饱和后应不能再溶解任何物质
C8、下列有关从海水中提取食盐晶体的说法,错误的是( )A、属于化学变化
B、属于物理变化
C、得到纯净的食盐晶体
D、得到不纯净的食盐晶体
AC一、概念:P36溶解度五大理解要点:
①条件:在一定温度下
②标准:100g溶剂
③状态:达到饱和状态
④单位:溶解的质量,单位为克
“定温百克剂,饱和单位克”固体的溶解度的学习要点:20℃时NaCl的溶解度为36g,其含义是什么?①在20℃时,NaCl在100g水中达到饱和状态时,溶解溶质的质量是36g。或②在20℃时,NaCl在100g溶剂中最多能溶解36g。(1)20℃时,36g NaCl能溶解在100g水中,所以说, 20℃时NaCl的溶解度为36g
(2)36g NaCl溶解在100g水中,达到饱和状态,所以说, NaCl的溶解度为36g(3)20℃时,36g NaCl溶解在50g水中,所以说, 20℃时NaCl的溶解度为36g
(4)20℃时,36g NaCl溶解在100g水中, 所以说, 20℃时NaCl的溶解度为36
判断下列说法是否正确,说明理由。难溶0.01g1g微溶10g可 溶易溶溶解性20℃时
溶解度①20℃时溶解度大于10g的物质为易溶物②20℃时溶解度在1g~10g的物质为可溶物
③20℃时溶解度在0.01g~1g的物质为微溶物
④20℃时溶解度小于0.01g的物质为难溶物或不溶物
1、在200C,NaCl的溶解度是36g。在200C时,把20g NaCl投入50g水中,充分溶解后,下列有关说法不正确的是( )
A、制成了70g饱和溶液
B、制成了68g饱和溶液
C、有18g NaCl发生溶解
D、还剩余2g固体NaCl未溶解A2、在200C,NaCl的溶解度是36g。 NaCl属于( )
A、易溶物
B、微溶物
C、可溶物
D、难溶物
A溶解度(克)温度(0C)ABC0二、溶解度曲线的意义P37活动与探究2、多数固体的溶解度随着温度的升高而增大(曲线陡);少数固体的溶解度受温度影响不大(曲线平缓);极少数固体的溶解度随着温度升高反而减少(曲线向下)。4、(1)物质的溶解度受温度变化的影响大小
(2)某一物质在某温度时的溶解度(3)同一物质在不同温度时的溶解度(4)不同物质在同一温度时的溶解度 (5)有些物质在同一温度下溶解度相等ABCMNSOtt1t2
1、t10C时,A、B、C的溶解度由大到小的顺序为 ;2、当三种物质饱和溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可达到饱和的是 ;3、M点的意义是 ;20g4、N点的意义为 ;A、B、CA A、B两物质在 t10C时溶解度相等
A物质在 t20C时溶解度
为20g
气体的溶解度1、概念:在压强为101KPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积2、气体的溶解度受压强和温度影响压强越大,气体的溶解度越大
例如:制汽水时加大压强使更多的二氧化碳溶于水中温度越高,气体的溶解度越小
例如:煮水至将开时,有许多气泡冒出P38讨论:1、压强
2、温度
3、将气体通入澄清石灰水中,若变浑浊,证明是二氧化碳
习题答案:
3、因为溶解度与温度有关,不同温度下同一物质的溶解度不同
4、可以看出,多数因体的溶解度随温度的升高而增大,如硝酸铵,硝酸钾,氯化铵等,少数固体的溶解度受温度影响不大,如氯化钠;但也有少数固体的溶解度随温度的升高反而减小,如熟石灰。
5、汗水中含有一些盐分,因此有咸味。被汗水浸湿的衣服干后,水分蒸发了,但盐分仍留在衣服上,就形成白色斑迹。
6、把一滴试样滴在玻璃片上,晾干或烘干。有白色痕迹的是氯化钾溶液。无痕迹的水。
7、在水中溶解有一些空气等气体,冷水受热时,温度升高,气体的溶解度减小,不能溶解的气体便逸出水面形成气泡。天气闷热时,水温度高,水中氧气的溶解度变小,溶解的氧气少了,而水面与空气接触,溶解的氧气相对多些,因此鱼总是接近水面游动。
8、氨水应密封保存在氨水罐中,氨水罐应放在阴凉处。
课题2 溶解度
前提测评:写出下列溶液的溶质的化学式:
1、食盐水 2、盐酸 ;
3、石灰水 4、稀硫酸 ;
5、酒精溶液 .NaClHClCa(OH)2H2SO4C2H5OH2、下列物质溶于水时,使溶液的温度明显升高的是 ( ),溶液的温度明显降低的是 ( )。
A、蔗糖 B、食盐
C、硝酸铵 D、氢氧化钠
1、把少量的下列各物质分别放入水里,充分振荡后可形成溶液的是( )
A、葡萄糖 B、面粉
C、花生油 D、冰块
ADC3、现有一瓶蓄电池用的稀硫酸,从上半部分取出少量,测得其密度为1.2g/cm3,若从底部取出少量测定其密度,则测得底部的稀硫酸的密度值为 ( )
A、大于1.2/cm3 B、小于1.2/cm3
C、等于1.2/cm3 D、无法确定C注明:稀硫酸是溶液,溶液是均一的,即各部分性质相同。1)饱和溶液:在一定温度下,向
一定量溶剂里加入某种溶质,当溶
质不能继续溶解时,所得的溶液.2)不饱和溶液:还能继续溶解的溶液3) 提醒:只有指明“在一定量溶剂里”和“在一定温度下”,溶液的“饱和”和“不饱和”才有意义。不饱和
溶液增加溶质、降低温度、饱和
溶液增加溶剂、升高温度蒸发溶剂 饱和溶液与不饱和溶液的转化溶液不限条件粗略分一定条件下分类浓溶液稀溶液饱和溶液不饱和溶液
关系:饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液
溶液的分类:1、下列关于饱和溶液的说法中,错误的是( )
A、在温度不变时,KNO3的饱和溶液不能再溶解KNO3
B、当温度升高时,饱和溶液一定能继续溶解溶质
C、稀溶液一定是不饱和溶液,浓溶液一定是饱和溶液
D、改变温度可以使不饱和溶液变成饱和溶液B、C巩固练习2、某课外小组需一定浓度的KNO3溶液做实验,怎样使KNO3固体较快地溶于水中?说明理由。
建议1:溶解时加热,粒子扩散速度加快,使溶解速度加快
建议2;溶解时不断的搅拌,使粒子运动速度加快,迅速扩散到溶剂中去。
建议3:溶解前先将固体研碎,增大固体与水的接触面积,使溶解速度加快3、室温下,向一定质量的氯化钠溶液中加入10克氯化钠固体,充分搅拌后,尚有部分未溶解,加入10克水后,固体全部溶解。下列判断正确的是( )
A、加水前一定是饱和溶液
B、加水前可能是饱和溶液
C、加水后一定是饱和溶液
D、加水后一定是不饱和溶液
A4、在一定温度下,将一瓶接近饱几的硝酸钾溶液转化成饱和溶液的方法( )①升高温度②降低温度③增加溶质④增加溶剂⑤蒸发溶剂
A、①②③
B、②③⑤
C、②③④
D、③④⑤
B5、使20℃的饱和食盐溶液变成不饱和溶液,可采取的措施是( )
A、加水
B、取出一些食盐溶液
C、加食盐
D、蒸发水A6、在一定温度下,一定量的水中,不断加入食盐晶体,能正确表示溶解的食盐质量m与时间t的关系的图象的是 ( )
D7. 下列说法正确的是( )
A、凡是均一、稳定的液体都是溶液B、饱和溶液所含的溶质一定比不饱和溶液的多
C、析出晶体后的溶液一定是饱和溶液D、某物质的溶液达到饱和后应不能再溶解任何物质
C8、下列有关从海水中提取食盐晶体的说法,错误的是( )A、属于化学变化
B、属于物理变化
C、得到纯净的食盐晶体
D、得到不纯净的食盐晶体
AC一、概念:P36溶解度五大理解要点:
①条件:在一定温度下
②标准:100g溶剂
③状态:达到饱和状态
④单位:溶解的质量,单位为克
“定温百克剂,饱和单位克”固体的溶解度的学习要点:20℃时NaCl的溶解度为36g,其含义是什么?①在20℃时,NaCl在100g水中达到饱和状态时,溶解溶质的质量是36g。或②在20℃时,NaCl在100g溶剂中最多能溶解36g。(1)20℃时,36g NaCl能溶解在100g水中,所以说, 20℃时NaCl的溶解度为36g
(2)36g NaCl溶解在100g水中,达到饱和状态,所以说, NaCl的溶解度为36g(3)20℃时,36g NaCl溶解在50g水中,所以说, 20℃时NaCl的溶解度为36g
(4)20℃时,36g NaCl溶解在100g水中, 所以说, 20℃时NaCl的溶解度为36
判断下列说法是否正确,说明理由。难溶0.01g1g微溶10g可 溶易溶溶解性20℃时
溶解度①20℃时溶解度大于10g的物质为易溶物②20℃时溶解度在1g~10g的物质为可溶物
③20℃时溶解度在0.01g~1g的物质为微溶物
④20℃时溶解度小于0.01g的物质为难溶物或不溶物
1、在200C,NaCl的溶解度是36g。在200C时,把20g NaCl投入50g水中,充分溶解后,下列有关说法不正确的是( )
A、制成了70g饱和溶液
B、制成了68g饱和溶液
C、有18g NaCl发生溶解
D、还剩余2g固体NaCl未溶解A2、在200C,NaCl的溶解度是36g。 NaCl属于( )
A、易溶物
B、微溶物
C、可溶物
D、难溶物
A溶解度(克)温度(0C)ABC0二、溶解度曲线的意义P37活动与探究2、多数固体的溶解度随着温度的升高而增大(曲线陡);少数固体的溶解度受温度影响不大(曲线平缓);极少数固体的溶解度随着温度升高反而减少(曲线向下)。4、(1)物质的溶解度受温度变化的影响大小
(2)某一物质在某温度时的溶解度(3)同一物质在不同温度时的溶解度(4)不同物质在同一温度时的溶解度 (5)有些物质在同一温度下溶解度相等ABCMNSOtt1t2
1、t10C时,A、B、C的溶解度由大到小的顺序为 ;2、当三种物质饱和溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可达到饱和的是 ;3、M点的意义是 ;20g4、N点的意义为 ;A、B、CA A、B两物质在 t10C时溶解度相等
A物质在 t20C时溶解度
为20g
气体的溶解度1、概念:在压强为101KPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积2、气体的溶解度受压强和温度影响压强越大,气体的溶解度越大
例如:制汽水时加大压强使更多的二氧化碳溶于水中温度越高,气体的溶解度越小
例如:煮水至将开时,有许多气泡冒出P38讨论:1、压强
2、温度
3、将气体通入澄清石灰水中,若变浑浊,证明是二氧化碳
习题答案:
3、因为溶解度与温度有关,不同温度下同一物质的溶解度不同
4、可以看出,多数因体的溶解度随温度的升高而增大,如硝酸铵,硝酸钾,氯化铵等,少数固体的溶解度受温度影响不大,如氯化钠;但也有少数固体的溶解度随温度的升高反而减小,如熟石灰。
5、汗水中含有一些盐分,因此有咸味。被汗水浸湿的衣服干后,水分蒸发了,但盐分仍留在衣服上,就形成白色斑迹。
6、把一滴试样滴在玻璃片上,晾干或烘干。有白色痕迹的是氯化钾溶液。无痕迹的水。
7、在水中溶解有一些空气等气体,冷水受热时,温度升高,气体的溶解度减小,不能溶解的气体便逸出水面形成气泡。天气闷热时,水温度高,水中氧气的溶解度变小,溶解的氧气少了,而水面与空气接触,溶解的氧气相对多些,因此鱼总是接近水面游动。
8、氨水应密封保存在氨水罐中,氨水罐应放在阴凉处。
同课章节目录
