溶液的形成课件(共30张PPT)
图片预览








文档简介
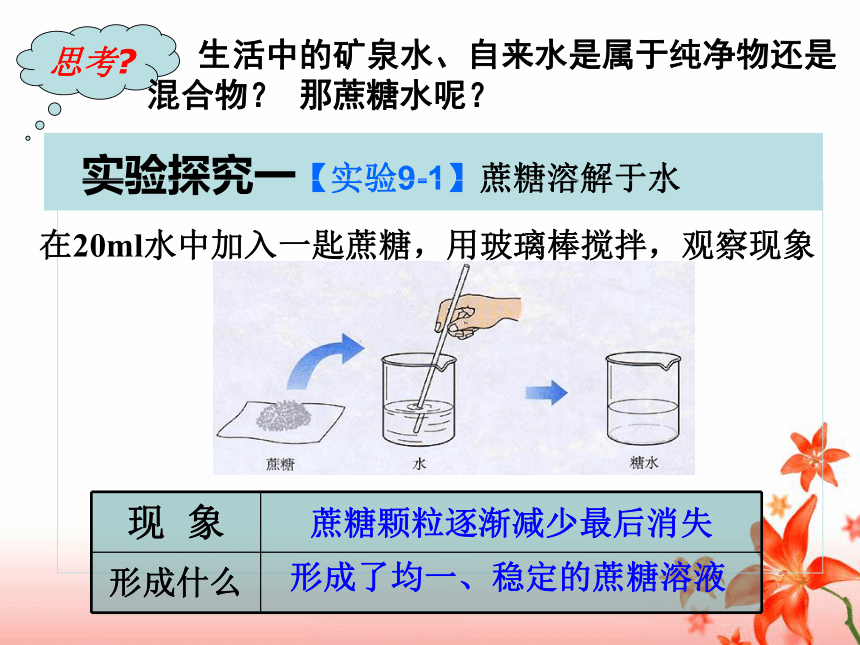
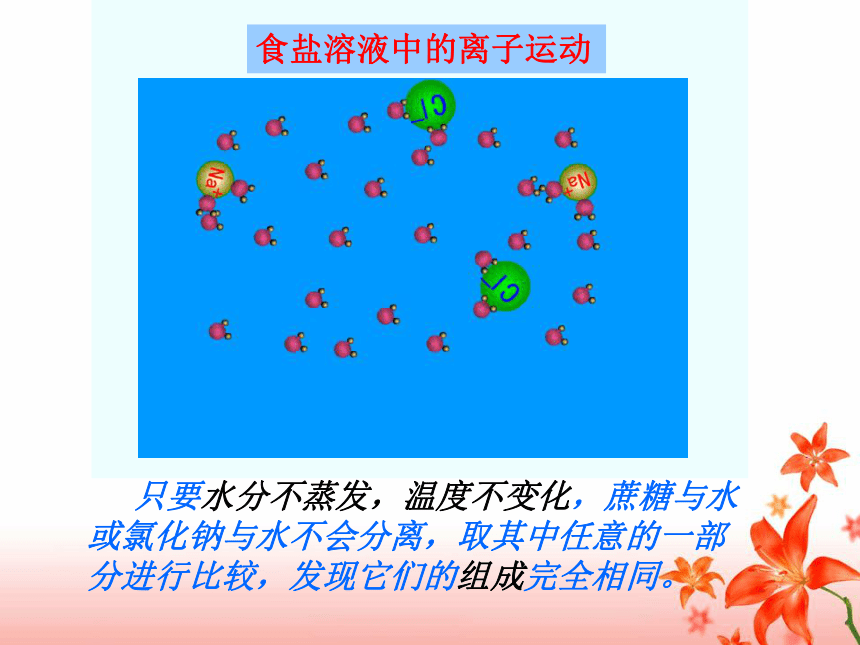
课件30张PPT。成形液溶溶 液 形 成第1课时的第九单元 溶液目标1 了解溶液、溶质、溶剂的概念目标2 认识溶液的基本特征目标3 了解溶液在生产生活中的应用日常生活中的溶液 实验探究一【实验9-1】蔗糖溶解于水 蔗糖颗粒逐渐减少最后消失形成了均一、稳定的蔗糖溶液在20ml水中加入一匙蔗糖,用玻璃棒搅拌,观察现象思考? 生活中的矿泉水、自来水是属于纯净物还是混合物? 那蔗糖水呢?蔗糖在水中为什么会“消失”呢?思考: 同学们都喝过糖水,糖水是甜的,但在糖水中为什么看不到糖呢?食盐溶液中的离子运动 只要水分不蒸发,温度不变化,蔗糖与水或氯化钠与水不会分离,取其中任意的一部分进行比较,发现它们的组成完全相同。一种或几种物质分散到另一种物质 里,形成均一的、稳定的混合物。 溶液的特征:(1)(2)1、定义:(密度、浓度、颜色等)一、溶液均一性:指溶液任一部分的组成和性质相同稳定性:在外界条件不变时,溶液稳定存在(溶质不会从溶剂分离出来)【溶剂】能溶解其他物质的物质叫做溶剂。如:水【溶质】被溶解的物质叫做溶质。如:蔗糖、食盐NaCl溶质H2O溶剂溶液(混合物)溶液的组成2、溶液的组成 m溶液 = m溶质 + m溶剂 V溶液 ≠ V溶质 + V溶剂溶液 硫酸铜溶液 碘 酒硫酸溶液 稀盐酸 溶质(溶解前的状态) 溶剂硫酸铜(固体) 碘(固体) 硫酸(液体) 氯化氢 (气体) (状态)水(液态)酒精(液态)水(液态)水(液态)我会填医用酒精 乙醇 (液体) 水(液态)【思考】水是不是可以溶解所有的物质呢?是不是只有水能做溶剂呢?水是最常用的溶剂,除此之外,汽油、酒精等也可作溶剂。如:碘酒。探讨:
怎样确定溶液中谁是溶质?谁是溶剂?溶液的名称:一般溶质的名称在前,溶剂的名称在后(通常溶剂“水”隐去)。如:硫酸铜溶液、碘酒、溴的四氯化碳溶液1.溶质的状态可以为固体液体气体2.液体与液体互溶量多---溶剂;量少---溶质在未指明溶剂时,溶剂一般为水。但如果其中有一种是水,不
管多少,一般把水叫做溶剂。固体、气体溶于液体,形成溶液时;固体和气体一般作溶质,液体作溶剂。溶液组成的判断P28 判断下列溶液中的溶质和溶剂NaOHH2OCa(OH)2NaClH2OH2O汽油酒精 H2O植物油说一说-关于溶液的认识
(1)均一、稳定的液体一定是溶液吗?
(2)溶液一定是无色透明的吗?
(3)将蔗糖溶液和NaCl溶液混合后还是
溶液吗?
(4)溶液里的溶质只能是一种物质吗?均一、透明、稳定的液体不一定是溶液,如水.溶液不一定是无色的:
硫酸铜溶液(蓝色)—— Cu2+
氯化铁溶液(黄色)——Fe3+
氯化亚铁、硫酸亚铁溶液(浅绿色)——Fe2+
高锰酸钾溶液(紫红色)—— MnO4-注意:3、溶液的用途生活中医疗上农业上实验室中实验探究二:溶质与溶剂的关系 在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。 [实验]9-2 不同溶质在不同溶剂中的溶解性几乎不溶(溶液略显棕黄色) 溶解,溶液呈紫红色溶解,溶液呈棕色几乎不溶【结论】:物质的溶解能力与溶质和溶剂的性质有关。同一种溶质在不同的溶剂中溶解能力不同;
不同的溶质在同一种溶剂中的溶解能力也不同。实验现象纪录实验探究三:[实验9-3] 水和乙醇能够互溶吗?分层混合均匀不分层乙醇与水互溶注意:乙醇能与水以任意比例互溶练习1:烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B B: ?A < ?B
C:?A= ?B D: 不能确定ABC练习2:当水分不蒸发,温度不改变时,KNO3溶液放置一年时间后,KNO3将( )
A:会沉降下来 B:不会分离出来
C:会浮上水面 D:不能确定B 洗涤剂为什么能除去餐具上的油污呢?液体分层形成乳状
浑浊液体液体分层液体分层形成乳状
浑浊液体,有泡 液体不分层 否 是[实验9-4] 乳化作用二、浊液:小液滴分散到液体里形成的混合物3、特征:三、洗涤剂的乳化功能不均一、不稳定 洗涤剂去污原理:洗涤剂具有乳化功能,能将油滴分散成无数细小的液滴,随水流走。区别: 汽油(或酒精)去污原理:汽油(或酒精)能溶解油污。1、乳浊液:2、悬浊液:固体小颗粒分散到液体里形成的混合物4、用途:医药上的钡餐是BaSO4的悬浊液;粉刷墙的涂料也是悬浊液;农业上,把农药配成乳浊液或悬浊液节约农药,提高药效(如,波尔多药是悬浊液).探究实验: 溶液、悬浊液和乳浊液的区别液体小液滴分散到另一种液体里形成不均一、不稳定的混合物。固体小颗粒分散到液体里形成不均一、不稳定的混合物。一种或几种物质分散到另一种物质里形成均一、稳定的混合物。均一
稳定不均一
不稳定不均一
不稳定混
合
物混
合
物混
合
物食盐水
糖水
稀盐酸
石灰水泥浆水
洪水油水练习3、可以作为溶质的( )
A、只有固体 B、只有液体
C、只有气体 D、气、液、固体都可以
练习4、把少量物质加入水中充分搅拌可以得到溶液的有( )
A、泥沙 B、酒精 C、汽油 D、蔗糖
练习5、下列关于溶液的说法正确的是( )
A、溶液一定是无色的
B、均一稳定的液体是溶液
C、溶液中的溶质可是固体、液体,也可是气体
D、溶液中的溶质只能是一种物质CB DD活动与探究 现有试管、烧杯、玻璃棒、温度计等仪器和固态NaCl、NH4NO3、NaOH(你还可选用其他仪器和药品),试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。1.实验方案:2.实验简图:根据实验记录实验结果,完成第30页表格.(1)分别向三只烧杯中倒入等体积的水,然后测出水温(2)分别将等质量的三种固体放入上述三只烧杯中,搅拌并测出温度(3)比较前后温度变化四、溶解时的吸热或放热现象1、溶解过程的两种变化:吸收热量放出热量2、几种表现:(1)扩散过程吸收的热量小于水合过程放出的热量:表现为放热,温度升高.(2)扩散过程吸收的热量大于水合过程放出的热量:表现为吸热,温度降低.(3)扩散过程吸收的热量等于水合过程放出的热量:表现为温度不变.溶解过程扩散过程
(吸热)水合过程
(放热)吸热>放热
(溶液温度降低)
例如:NH4NO3固体溶于水吸热 = 放热
(溶液温度不变)
例如:NaCl固体溶于水吸热<放热
(溶液温度升高)
例如:NaOH固体和浓硫酸
(H2SO4)溶于水[小结]练习与巩固:右图所示,向小试管中加入一定量的下列物质,
U形管液面右侧未发生改变,该物质是( )
U形管液面右侧升高,该物质是( )
U形管液面右侧降低,该物质是( )
A、浓硫酸 B、烧碱 C、生石灰
D、蔗糖 E、硝酸铵 F、氯化钠DFABCE一种或几
种物质另一种
物质均一、稳定的
混合物溶剂溶质溶液液体固体气体液-液互溶:量多的是溶剂通常:水是
溶剂【小结】分散被溶解能溶解【溶液和乳浊液区别】溶液是均一、稳定的;
乳浊液不稳定,静置会分层
怎样确定溶液中谁是溶质?谁是溶剂?溶液的名称:一般溶质的名称在前,溶剂的名称在后(通常溶剂“水”隐去)。如:硫酸铜溶液、碘酒、溴的四氯化碳溶液1.溶质的状态可以为固体液体气体2.液体与液体互溶量多---溶剂;量少---溶质在未指明溶剂时,溶剂一般为水。但如果其中有一种是水,不
管多少,一般把水叫做溶剂。固体、气体溶于液体,形成溶液时;固体和气体一般作溶质,液体作溶剂。溶液组成的判断P28 判断下列溶液中的溶质和溶剂NaOHH2OCa(OH)2NaClH2OH2O汽油酒精 H2O植物油说一说-关于溶液的认识
(1)均一、稳定的液体一定是溶液吗?
(2)溶液一定是无色透明的吗?
(3)将蔗糖溶液和NaCl溶液混合后还是
溶液吗?
(4)溶液里的溶质只能是一种物质吗?均一、透明、稳定的液体不一定是溶液,如水.溶液不一定是无色的:
硫酸铜溶液(蓝色)—— Cu2+
氯化铁溶液(黄色)——Fe3+
氯化亚铁、硫酸亚铁溶液(浅绿色)——Fe2+
高锰酸钾溶液(紫红色)—— MnO4-注意:3、溶液的用途生活中医疗上农业上实验室中实验探究二:溶质与溶剂的关系 在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。 [实验]9-2 不同溶质在不同溶剂中的溶解性几乎不溶(溶液略显棕黄色) 溶解,溶液呈紫红色溶解,溶液呈棕色几乎不溶【结论】:物质的溶解能力与溶质和溶剂的性质有关。同一种溶质在不同的溶剂中溶解能力不同;
不同的溶质在同一种溶剂中的溶解能力也不同。实验现象纪录实验探究三:[实验9-3] 水和乙醇能够互溶吗?分层混合均匀不分层乙醇与水互溶注意:乙醇能与水以任意比例互溶练习1:烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B B: ?A < ?B
C:?A= ?B D: 不能确定ABC练习2:当水分不蒸发,温度不改变时,KNO3溶液放置一年时间后,KNO3将( )
A:会沉降下来 B:不会分离出来
C:会浮上水面 D:不能确定B 洗涤剂为什么能除去餐具上的油污呢?液体分层形成乳状
浑浊液体液体分层液体分层形成乳状
浑浊液体,有泡 液体不分层 否 是[实验9-4] 乳化作用二、浊液:小液滴分散到液体里形成的混合物3、特征:三、洗涤剂的乳化功能不均一、不稳定 洗涤剂去污原理:洗涤剂具有乳化功能,能将油滴分散成无数细小的液滴,随水流走。区别: 汽油(或酒精)去污原理:汽油(或酒精)能溶解油污。1、乳浊液:2、悬浊液:固体小颗粒分散到液体里形成的混合物4、用途:医药上的钡餐是BaSO4的悬浊液;粉刷墙的涂料也是悬浊液;农业上,把农药配成乳浊液或悬浊液节约农药,提高药效(如,波尔多药是悬浊液).探究实验: 溶液、悬浊液和乳浊液的区别液体小液滴分散到另一种液体里形成不均一、不稳定的混合物。固体小颗粒分散到液体里形成不均一、不稳定的混合物。一种或几种物质分散到另一种物质里形成均一、稳定的混合物。均一
稳定不均一
不稳定不均一
不稳定混
合
物混
合
物混
合
物食盐水
糖水
稀盐酸
石灰水泥浆水
洪水油水练习3、可以作为溶质的( )
A、只有固体 B、只有液体
C、只有气体 D、气、液、固体都可以
练习4、把少量物质加入水中充分搅拌可以得到溶液的有( )
A、泥沙 B、酒精 C、汽油 D、蔗糖
练习5、下列关于溶液的说法正确的是( )
A、溶液一定是无色的
B、均一稳定的液体是溶液
C、溶液中的溶质可是固体、液体,也可是气体
D、溶液中的溶质只能是一种物质CB DD活动与探究 现有试管、烧杯、玻璃棒、温度计等仪器和固态NaCl、NH4NO3、NaOH(你还可选用其他仪器和药品),试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。1.实验方案:2.实验简图:根据实验记录实验结果,完成第30页表格.(1)分别向三只烧杯中倒入等体积的水,然后测出水温(2)分别将等质量的三种固体放入上述三只烧杯中,搅拌并测出温度(3)比较前后温度变化四、溶解时的吸热或放热现象1、溶解过程的两种变化:吸收热量放出热量2、几种表现:(1)扩散过程吸收的热量小于水合过程放出的热量:表现为放热,温度升高.(2)扩散过程吸收的热量大于水合过程放出的热量:表现为吸热,温度降低.(3)扩散过程吸收的热量等于水合过程放出的热量:表现为温度不变.溶解过程扩散过程
(吸热)水合过程
(放热)吸热>放热
(溶液温度降低)
例如:NH4NO3固体溶于水吸热 = 放热
(溶液温度不变)
例如:NaCl固体溶于水吸热<放热
(溶液温度升高)
例如:NaOH固体和浓硫酸
(H2SO4)溶于水[小结]练习与巩固:右图所示,向小试管中加入一定量的下列物质,
U形管液面右侧未发生改变,该物质是( )
U形管液面右侧升高,该物质是( )
U形管液面右侧降低,该物质是( )
A、浓硫酸 B、烧碱 C、生石灰
D、蔗糖 E、硝酸铵 F、氯化钠DFABCE一种或几
种物质另一种
物质均一、稳定的
混合物溶剂溶质溶液液体固体气体液-液互溶:量多的是溶剂通常:水是
溶剂【小结】分散被溶解能溶解【溶液和乳浊液区别】溶液是均一、稳定的;
乳浊液不稳定,静置会分层
同课章节目录
