物质的量第二节[上学期]
图片预览








文档简介
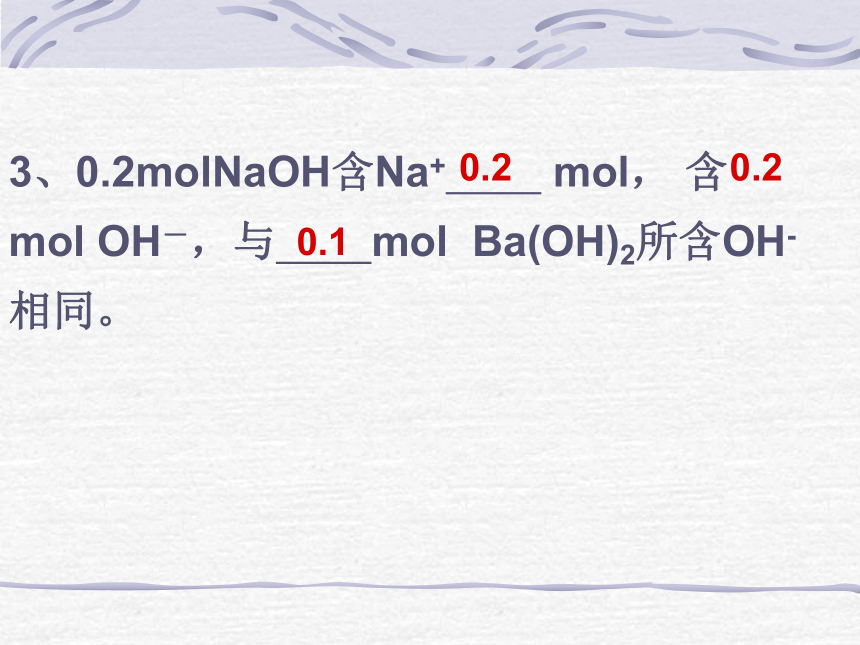
课件29张PPT。3、0.2molNaOH含Na+??? ?????mol, 含 mol OH-,与??? ????mol? Ba(OH)2所含OH- 相同。
?0.20.10.2在HCl、MgCl2、MgSO4三种物质配成的混合溶液中,已知H+为0.1mol, Mg2+为0.35mol,Cl-为0. 3mol,则SO42-为 mol
0.25在无土栽培中,需配制一定量含50molNH4Cl、16molKCl和24molK2SO4的营养液。若用KCl、 (NH4)2SO4和 NH4Cl三种固体为原料来配制,三者的物质的量依次为 二、摩尔质量[提问]
取一杯水,怎样知道这杯水里有多少个水分子? ?五 摩尔质量1.定义:单位物质的量的物质所具有的质量2.符号:M3.单位:g·mol-14. M = mn 1mol任何物质的质量。 C + O2 ==== CO2 微观 一个C原子 一个O2分子 一个CO2分子↓扩大6.02×1023 ↓扩大6.02×102 ↓扩大6.02×1023 1 mol C 原子 1 mol O2 分子 1 mol CO2 分子
(宏观) ↓ ↓ ↓质量 0.012 kg=12 g x g y g
相对原子质量或
相对分子质 12 32 44 因为元素原子的质量比=元素相对原子质量比,
所以可求出: x=32g y=44g 由此可见:1 mol任何物质的质量,若以克为单位,在数值上与微粒的相对原子质量,或相对分子质量相等。意义 物质的量是把微观粒子和宏观物质联系起来的 一座桥梁。1、a.1 mol H2O的质量是 g
b.1 mol NaCl的质量是 g 2、 a.Na的摩尔质量
b.NaCl的摩尔质量
c.SO的摩尔质量
c.1 mol Na+的质量是 g
d.1 mol S的质量是 g练习一摩尔质量概念的计算 例1、483 g Na2SO4·10H2O中所含的Na+和SO42-的物质的量各是多少?所含H2O分子的数目是多少?
(请同学们阅读课本P.7例题1)[问题解决1]
1、参考下列解题方式,完成下列计算:
(1)9.8 g H2SO4的物质的量 。
(2)10.6 g Na2CO3的物质的量 。
(3)0.25 mol CaCO3的质量 。
(4)2.0 mol H2O的质量 。
(0.1 mol)(0.1 mol)
(25 g)(36 g)[问题解决3]
3、写出下列反应的化学方程式,并说明反应中反应物和生成物的物质的量的关系。
(1)氢氧化钠和硫酸的反应。
(2)氧化铁在高温下与一氧化碳的反应。
(3)氯酸钾(KClO3)加热分解生成氧气和氯化钾的反应。
(4)过氧化氢(H2O2)分解成氧气和水的反应。
[问题解决3参考答案]
(1)2NaOH+H2SO4=Na2SO4+2H2O 反应物与生成物的物质的量之比为:2∶1∶1∶2
(2)Fe2O3+3CO 2Fe+3CO2 反应物与生成物的物质的量之比为:1∶3∶2∶3
(3)2KClO3 2KCl+3O2↑ 反应物与生成物的物质的量之比为:2∶2∶3
(4)2H2O2 2H2O+O2 反应物与生成物的物质的量之比为:2∶2∶1 1、下列说法正确的是 [ ]。
A.氮原子的质量在数值上等于它的摩
尔质量
B.NaOH的摩尔质量是40g
C.氩气的摩尔质量在数值上等于它的
相对原子质量
D.CaCO3的摩尔质量是100kg/molC练习二 2、质量相同的下列物质中,含分子数最多的是 [ ]。
A.O2 B.NH3
C.CO D.CH4
D 3、下列相同质量的气体中,含分子个数相同的是 [ ];含分子个数相差1倍的是 [ ]
A.O2和SO2 B.SO2和SO3
C.N2O和CO2 D.CO和CO2
CA 4、质量相同的Mg、Cl2、NH3、CH4、SO2、H3PO4所含原子数多少,由大到小排列的顺序是什么?
CH4>NH3>H3PO4>SO2>Mg>Cl2 5、 胆矾晶体的化学式CuSO4·nH2O。50g胆矾晶体在蒸发皿里加热(CuSO4不分解)至质量不再减轻为止,剩余无水盐32g。试求n值是多少?10kg胆矾的物质的量是多少?n值为5;10kg胆矾的物质的量为40mol。 6、3.01×1022个 OH- 的物质的量为0.05mol,
质量为 ,
含有质子的物质的量为 ,
含有电子的物质的量为 ,
这些 OH- 与 NH3的质量相同,
这些 OH- 和 Na+含有的离子数相同。
0.85g0.45mol0.5mol0.05mol1.15g3.01×1022个H2O 的物质的量为 ,
质量为 ,
含有电子的物质的量为 ,
这些 H20 与 g H3PO4所含的氢原子数相同,
0.9g0. 5mol3.270.05mol5、将4g NaOH溶于多少克水中,才能使每100个H2O分子溶有一个Na+? 6、设NA代表阿伏加德罗常数,下列说法正确的
是( )
(A)2.3g金属钠全部变成钠离子时失去的电子数目
为0.2NA
(B)2g氢气所含原子数目为NA
(C)17gNH3 所含的电子数为10NA
(D)NA个氧分子和NA个氢分子的质量比等于16 :1
C、D7、设一个12C原子的质量为ag,一个R原
子的质量为bg,阿伏加德罗常数为NA,
则R的相对原子质量可以表示为( )
(A) (B)
(C) bNA (D) aNA
B、C
1:有15gA与10.8gB物质恰好完全反应,生成7.2gC,1.8gD和0.3molE,求E的摩尔质量?作业2、38 g某二价金属氯化物RCl2中含Cl-0.8mol,求RCl2的摩尔质量?R的相对原子质量?3:有A、B、C三种一元碱,它们的相对分子质量之比为:3:5:7,如果把7 mol的A,5 mol的B、3 mol的C均匀混合。取5.36g混合物恰好能中和0.15mol的HCl,求A、B、C的相对分子质量?
同学们
再见!
?0.20.10.2在HCl、MgCl2、MgSO4三种物质配成的混合溶液中,已知H+为0.1mol, Mg2+为0.35mol,Cl-为0. 3mol,则SO42-为 mol
0.25在无土栽培中,需配制一定量含50molNH4Cl、16molKCl和24molK2SO4的营养液。若用KCl、 (NH4)2SO4和 NH4Cl三种固体为原料来配制,三者的物质的量依次为 二、摩尔质量[提问]
取一杯水,怎样知道这杯水里有多少个水分子? ?五 摩尔质量1.定义:单位物质的量的物质所具有的质量2.符号:M3.单位:g·mol-14. M = mn 1mol任何物质的质量。 C + O2 ==== CO2 微观 一个C原子 一个O2分子 一个CO2分子↓扩大6.02×1023 ↓扩大6.02×102 ↓扩大6.02×1023 1 mol C 原子 1 mol O2 分子 1 mol CO2 分子
(宏观) ↓ ↓ ↓质量 0.012 kg=12 g x g y g
相对原子质量或
相对分子质 12 32 44 因为元素原子的质量比=元素相对原子质量比,
所以可求出: x=32g y=44g 由此可见:1 mol任何物质的质量,若以克为单位,在数值上与微粒的相对原子质量,或相对分子质量相等。意义 物质的量是把微观粒子和宏观物质联系起来的 一座桥梁。1、a.1 mol H2O的质量是 g
b.1 mol NaCl的质量是 g 2、 a.Na的摩尔质量
b.NaCl的摩尔质量
c.SO的摩尔质量
c.1 mol Na+的质量是 g
d.1 mol S的质量是 g练习一摩尔质量概念的计算 例1、483 g Na2SO4·10H2O中所含的Na+和SO42-的物质的量各是多少?所含H2O分子的数目是多少?
(请同学们阅读课本P.7例题1)[问题解决1]
1、参考下列解题方式,完成下列计算:
(1)9.8 g H2SO4的物质的量 。
(2)10.6 g Na2CO3的物质的量 。
(3)0.25 mol CaCO3的质量 。
(4)2.0 mol H2O的质量 。
(0.1 mol)(0.1 mol)
(25 g)(36 g)[问题解决3]
3、写出下列反应的化学方程式,并说明反应中反应物和生成物的物质的量的关系。
(1)氢氧化钠和硫酸的反应。
(2)氧化铁在高温下与一氧化碳的反应。
(3)氯酸钾(KClO3)加热分解生成氧气和氯化钾的反应。
(4)过氧化氢(H2O2)分解成氧气和水的反应。
[问题解决3参考答案]
(1)2NaOH+H2SO4=Na2SO4+2H2O 反应物与生成物的物质的量之比为:2∶1∶1∶2
(2)Fe2O3+3CO 2Fe+3CO2 反应物与生成物的物质的量之比为:1∶3∶2∶3
(3)2KClO3 2KCl+3O2↑ 反应物与生成物的物质的量之比为:2∶2∶3
(4)2H2O2 2H2O+O2 反应物与生成物的物质的量之比为:2∶2∶1 1、下列说法正确的是 [ ]。
A.氮原子的质量在数值上等于它的摩
尔质量
B.NaOH的摩尔质量是40g
C.氩气的摩尔质量在数值上等于它的
相对原子质量
D.CaCO3的摩尔质量是100kg/molC练习二 2、质量相同的下列物质中,含分子数最多的是 [ ]。
A.O2 B.NH3
C.CO D.CH4
D 3、下列相同质量的气体中,含分子个数相同的是 [ ];含分子个数相差1倍的是 [ ]
A.O2和SO2 B.SO2和SO3
C.N2O和CO2 D.CO和CO2
CA 4、质量相同的Mg、Cl2、NH3、CH4、SO2、H3PO4所含原子数多少,由大到小排列的顺序是什么?
CH4>NH3>H3PO4>SO2>Mg>Cl2 5、 胆矾晶体的化学式CuSO4·nH2O。50g胆矾晶体在蒸发皿里加热(CuSO4不分解)至质量不再减轻为止,剩余无水盐32g。试求n值是多少?10kg胆矾的物质的量是多少?n值为5;10kg胆矾的物质的量为40mol。 6、3.01×1022个 OH- 的物质的量为0.05mol,
质量为 ,
含有质子的物质的量为 ,
含有电子的物质的量为 ,
这些 OH- 与 NH3的质量相同,
这些 OH- 和 Na+含有的离子数相同。
0.85g0.45mol0.5mol0.05mol1.15g3.01×1022个H2O 的物质的量为 ,
质量为 ,
含有电子的物质的量为 ,
这些 H20 与 g H3PO4所含的氢原子数相同,
0.9g0. 5mol3.270.05mol5、将4g NaOH溶于多少克水中,才能使每100个H2O分子溶有一个Na+? 6、设NA代表阿伏加德罗常数,下列说法正确的
是( )
(A)2.3g金属钠全部变成钠离子时失去的电子数目
为0.2NA
(B)2g氢气所含原子数目为NA
(C)17gNH3 所含的电子数为10NA
(D)NA个氧分子和NA个氢分子的质量比等于16 :1
C、D7、设一个12C原子的质量为ag,一个R原
子的质量为bg,阿伏加德罗常数为NA,
则R的相对原子质量可以表示为( )
(A) (B)
(C) bNA (D) aNA
B、C
1:有15gA与10.8gB物质恰好完全反应,生成7.2gC,1.8gD和0.3molE,求E的摩尔质量?作业2、38 g某二价金属氯化物RCl2中含Cl-0.8mol,求RCl2的摩尔质量?R的相对原子质量?3:有A、B、C三种一元碱,它们的相对分子质量之比为:3:5:7,如果把7 mol的A,5 mol的B、3 mol的C均匀混合。取5.36g混合物恰好能中和0.15mol的HCl,求A、B、C的相对分子质量?
同学们
再见!
