钠的性质及应用[上学期]
图片预览






文档简介
课件18张PPT。 第二单元
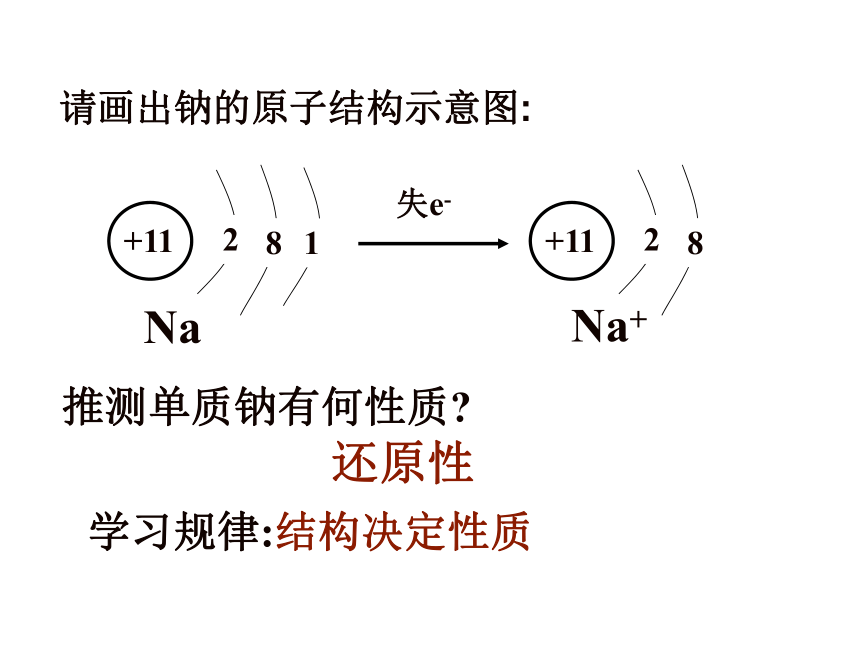
钠、镁及其化合物钠元素在自然界中分布很广,请同学们举些例子:在自然界 只能以化合态存在为什么自然界中不存在单质钠呢?金属钠的性质与应用请画出钠的原子结构示意图:NaNa+推测单质钠有何性质?还原性学习规律:结构决定性质请同学们注意观察实验并总结钠的物理性质实验1、钠的切割色状熔点硬度密度导电
导热银白色,固体低小,质软大于煤油的密度电、热的良导体观察与思考设问:我们可以看到刚切割的金属钠表面很快变暗,
这是什么原因呢?二、化学性质1、与非金属反应4Na+O2==2Na2O(白色固体)实验2、将钠块加热,观察现象现象:剧烈燃烧,发出黄光,产生淡黄色粉末结论:(淡黄色粉末)过氧化钠结论:反应条件不同,产物不同 现象:反应剧烈、产生白色的烟实验3、钠在氯气中燃烧:演示实验4、钠投入水中怎样证明产生的气体是氢气?思考:产生的是什么气体?根据反应产物书写钠与水反应的化学方程式
并标出电子转移的方向和数目2、与水反应2Na+2H2O= 2NaOH+ H2 ↑为什么将钠投入氯化铜溶液中不能置换出铜,而产生氢氧化铜沉淀呢?思考:将金属钠投入硫酸铜溶液中有何现象?
你是根据什么推断的?2Na+2H2O===2NaOH+H2↑ ………… (1)CuSO4+2NaOH==Cu(OH)2↓+Na2SO4…... (2)2Na+CuSO4+2H2O== Cu(OH)2↓+Na2SO4 +H2↑
……………(3) 钠该如何保存?
我们取用金属钠时要注意什么?
若金属钠着火了,该怎样来灭火?讨论钠 的 用途制Na2O2核反应堆导热剂高压钠灯冶炼某些贵金属总结:结构决定性质决定
用途1.关于钠的用途叙述正确的是( )
A.钠用于电光源上
B.钠是一种强还原剂,可以把钛、锆、铌、钽从其盐溶液中置换出来
C.钠和钾的合金常温下为液体,可作原子反应堆的导热剂
D.工业上可用于生产纯碱和大量制备氢氧化钠练习
D2、下列物质放置在空气中因发生氧化还原反应而变质的是( )
A.NaOH B.Na2O C.Na D.CaOC银白色变暗变白色固体结块粉末(Na)(Na2CO3)(Na2CO3· 10H2O)(NaOH)(Na2O)与O2与H2O与CO2风化成液(NaOH潮解) __D___4.将一小块金属钠投入下列溶液中时,既有气体又有沉淀的是( )ACA.MgCl2 B.Na2SO4C.FeCl3 D.Ba(NO3)25. 97.8水中加入2.3钠,充分反应后,求所得溶液的质量分数?
钠、镁及其化合物钠元素在自然界中分布很广,请同学们举些例子:在自然界 只能以化合态存在为什么自然界中不存在单质钠呢?金属钠的性质与应用请画出钠的原子结构示意图:NaNa+推测单质钠有何性质?还原性学习规律:结构决定性质请同学们注意观察实验并总结钠的物理性质实验1、钠的切割色状熔点硬度密度导电
导热银白色,固体低小,质软大于煤油的密度电、热的良导体观察与思考设问:我们可以看到刚切割的金属钠表面很快变暗,
这是什么原因呢?二、化学性质1、与非金属反应4Na+O2==2Na2O(白色固体)实验2、将钠块加热,观察现象现象:剧烈燃烧,发出黄光,产生淡黄色粉末结论:(淡黄色粉末)过氧化钠结论:反应条件不同,产物不同 现象:反应剧烈、产生白色的烟实验3、钠在氯气中燃烧:演示实验4、钠投入水中怎样证明产生的气体是氢气?思考:产生的是什么气体?根据反应产物书写钠与水反应的化学方程式
并标出电子转移的方向和数目2、与水反应2Na+2H2O= 2NaOH+ H2 ↑为什么将钠投入氯化铜溶液中不能置换出铜,而产生氢氧化铜沉淀呢?思考:将金属钠投入硫酸铜溶液中有何现象?
你是根据什么推断的?2Na+2H2O===2NaOH+H2↑ ………… (1)CuSO4+2NaOH==Cu(OH)2↓+Na2SO4…... (2)2Na+CuSO4+2H2O== Cu(OH)2↓+Na2SO4 +H2↑
……………(3) 钠该如何保存?
我们取用金属钠时要注意什么?
若金属钠着火了,该怎样来灭火?讨论钠 的 用途制Na2O2核反应堆导热剂高压钠灯冶炼某些贵金属总结:结构决定性质决定
用途1.关于钠的用途叙述正确的是( )
A.钠用于电光源上
B.钠是一种强还原剂,可以把钛、锆、铌、钽从其盐溶液中置换出来
C.钠和钾的合金常温下为液体,可作原子反应堆的导热剂
D.工业上可用于生产纯碱和大量制备氢氧化钠练习
D2、下列物质放置在空气中因发生氧化还原反应而变质的是( )
A.NaOH B.Na2O C.Na D.CaOC银白色变暗变白色固体结块粉末(Na)(Na2CO3)(Na2CO3· 10H2O)(NaOH)(Na2O)与O2与H2O与CO2风化成液(NaOH潮解) __D___4.将一小块金属钠投入下列溶液中时,既有气体又有沉淀的是( )ACA.MgCl2 B.Na2SO4C.FeCl3 D.Ba(NO3)25. 97.8水中加入2.3钠,充分反应后,求所得溶液的质量分数?
