原子构成[上学期]
图片预览






文档简介
课件19张PPT。3、原子核外电子排布规律①?电子总是尽先排布在能量最低的电子层里, 然后由往外,依次排在能量逐步升高的电子层里(能量最低原理)
先排K层,排满K层后再排L层,排满L层后再排M层②每个电子层最多只能容纳2n2个电子。
③ 最外层最多只能容纳 8个电子(K层为最外层时不能超过2个)
次外层最多只能容纳18个电子(K层为次外层时不能超过2个
倒数第三层最多只能容纳32个电子
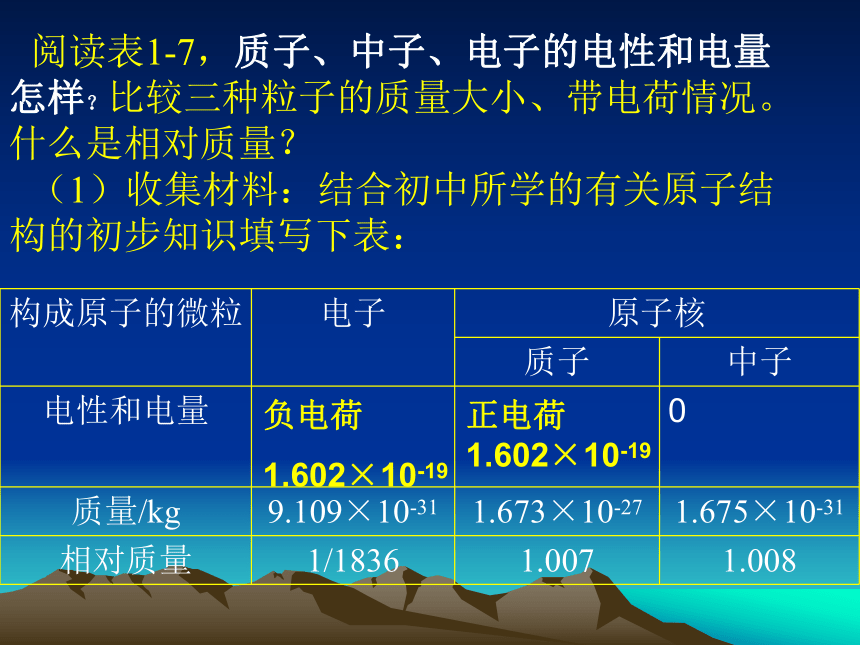
原子的构成阅读表1-7,质子、中子、电子的电性和电量怎样?比较三种粒子的质量大小、带电荷情况。什么是相对质量?
(1)收集材料:结合初中所学的有关原子结构的初步知识填写下表:负电荷
1.602×10-19正电荷
1.602×10-191 构成原子的微粒之间的数量关系
91911
231327如果忽略电子的质量,将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,我们称之为质量数。质量数(A)=质子数(Z)+中子数(N)——元素符号质量数 —— 核电荷数 ——
(核内质子数)2含义:代表一个质量数为A、质子数为Z的原子。
⑵电性关系:
原子:核电荷数(Z)=核内质子数=核外电子数
阳离子:核电荷数(Z)=核内质子数>核外电子数
核电荷数(Z)=核内电子数+电荷数
阴离子:核电荷数(Z)=核内质子数<核外电子数
核电荷数(Z)=核内电子数—电荷数A、Z、c、d、e各代表什么? A——代表质量数;
Z——代表核电荷数(质子数)
c——代表离子所带的电荷数
d——代表化合价
e——代表原子个数请指出Al、Al3+中所含的质子数和电子数。元素:具有相同质子数的同一类原子的总称。同位素:质子数相同而中子数不同的核素互称为同位素。核素:具有一定质子数和一定中子数的一种原子。HDT同位素的特点:
①天然存在的元素,各同位素在自然界的含量占该元素总量的百分比(称为“丰度”,即原子百分比)基本上是固定的。②同种元素,可以有若干种不同的核素.
(元素:112种,同位素:1800种)③同种元素是同一元素的不同核素之间的互相称谓,不指具体的原子。
同一种元素的不同同位素原子其质量数不同,核外电子层结构相同,其原子、单质及其构成的化合物化学性质几乎相同,只是某些物理性质略有差异。同位素构成的化合物是不同的化合物,H2O、D2O、T2O的物理性质不同,化学性质几乎相同
A= A1×a1%+A2×a2%+A3×a3%+……
A :元素的相对原子质量
A1 、A2、 A3、……同位素的相对原子质量
a1%、a2%、a3%、 ……同位素在自然界的含量占该元素总量的百分比(称为“丰度”,即原子百分比)或者是同位素的物质的量分数
元素的相对原子质量【例】(2005年江苏高考题)我国的“神舟”五号载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法正确的是( )
A. 42He原子核内含有4个质子
B. 32He和42He互为同位素
C. 32He原子核内含有3个中子
D.42He的最外层电子数为2,所以42He具有较强的金属性B据报道,上海某医院正在研究用放射性的一
种碘 治疗肿瘤。该碘原子的核内的中子数与核外电子数之差是A、72 B、19 C、53 D、125B某二价阴离子,核外有18个电子,质量数为32,则其中子数为:A、12 B、14 C、16 D、18CA、核外有13个电子
B、核内有6个质子,核外有7个电子
C、质量数为13,质子数为6,核外有7个电子
D、质量数为13,质子数为6,核内有7个中子
00全国高考题D⒈原子的构成是本节重点,掌握的关系式:
的含义:代表一个质量数为A、
质子数为Z的原子。
中各个字母的含义:
A:质量数;
Z:质子数;
e:原子个数;
c:电荷数
d: 化合价
⑵电性关系:
原子:核电荷数(Z)=核内质子数=核外电子数
阳离子:核电荷数(Z)=核内质子数>核外电子数
核电荷数(Z)=核内电子数+电荷数
阴离子:核电荷数(Z)=核内质子数<核外电子数
核电荷数(Z)=核内电子数—电荷数
⑶质量关系:质量数(A)=质子数(Z)+中子数(N)
⒉元素、核素、同位素和Na+具有相同质子数和电子数的微粒是:
A、NH4+ B、F - C、H2O D、NH3AB下节课评讲习题和发下去的练习
先排K层,排满K层后再排L层,排满L层后再排M层②每个电子层最多只能容纳2n2个电子。
③ 最外层最多只能容纳 8个电子(K层为最外层时不能超过2个)
次外层最多只能容纳18个电子(K层为次外层时不能超过2个
倒数第三层最多只能容纳32个电子
原子的构成阅读表1-7,质子、中子、电子的电性和电量怎样?比较三种粒子的质量大小、带电荷情况。什么是相对质量?
(1)收集材料:结合初中所学的有关原子结构的初步知识填写下表:负电荷
1.602×10-19正电荷
1.602×10-191 构成原子的微粒之间的数量关系
91911
231327如果忽略电子的质量,将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,我们称之为质量数。质量数(A)=质子数(Z)+中子数(N)——元素符号质量数 —— 核电荷数 ——
(核内质子数)2含义:代表一个质量数为A、质子数为Z的原子。
⑵电性关系:
原子:核电荷数(Z)=核内质子数=核外电子数
阳离子:核电荷数(Z)=核内质子数>核外电子数
核电荷数(Z)=核内电子数+电荷数
阴离子:核电荷数(Z)=核内质子数<核外电子数
核电荷数(Z)=核内电子数—电荷数A、Z、c、d、e各代表什么? A——代表质量数;
Z——代表核电荷数(质子数)
c——代表离子所带的电荷数
d——代表化合价
e——代表原子个数请指出Al、Al3+中所含的质子数和电子数。元素:具有相同质子数的同一类原子的总称。同位素:质子数相同而中子数不同的核素互称为同位素。核素:具有一定质子数和一定中子数的一种原子。HDT同位素的特点:
①天然存在的元素,各同位素在自然界的含量占该元素总量的百分比(称为“丰度”,即原子百分比)基本上是固定的。②同种元素,可以有若干种不同的核素.
(元素:112种,同位素:1800种)③同种元素是同一元素的不同核素之间的互相称谓,不指具体的原子。
同一种元素的不同同位素原子其质量数不同,核外电子层结构相同,其原子、单质及其构成的化合物化学性质几乎相同,只是某些物理性质略有差异。同位素构成的化合物是不同的化合物,H2O、D2O、T2O的物理性质不同,化学性质几乎相同
A= A1×a1%+A2×a2%+A3×a3%+……
A :元素的相对原子质量
A1 、A2、 A3、……同位素的相对原子质量
a1%、a2%、a3%、 ……同位素在自然界的含量占该元素总量的百分比(称为“丰度”,即原子百分比)或者是同位素的物质的量分数
元素的相对原子质量【例】(2005年江苏高考题)我国的“神舟”五号载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法正确的是( )
A. 42He原子核内含有4个质子
B. 32He和42He互为同位素
C. 32He原子核内含有3个中子
D.42He的最外层电子数为2,所以42He具有较强的金属性B据报道,上海某医院正在研究用放射性的一
种碘 治疗肿瘤。该碘原子的核内的中子数与核外电子数之差是A、72 B、19 C、53 D、125B某二价阴离子,核外有18个电子,质量数为32,则其中子数为:A、12 B、14 C、16 D、18CA、核外有13个电子
B、核内有6个质子,核外有7个电子
C、质量数为13,质子数为6,核外有7个电子
D、质量数为13,质子数为6,核内有7个中子
00全国高考题D⒈原子的构成是本节重点,掌握的关系式:
的含义:代表一个质量数为A、
质子数为Z的原子。
中各个字母的含义:
A:质量数;
Z:质子数;
e:原子个数;
c:电荷数
d: 化合价
⑵电性关系:
原子:核电荷数(Z)=核内质子数=核外电子数
阳离子:核电荷数(Z)=核内质子数>核外电子数
核电荷数(Z)=核内电子数+电荷数
阴离子:核电荷数(Z)=核内质子数<核外电子数
核电荷数(Z)=核内电子数—电荷数
⑶质量关系:质量数(A)=质子数(Z)+中子数(N)
⒉元素、核素、同位素和Na+具有相同质子数和电子数的微粒是:
A、NH4+ B、F - C、H2O D、NH3AB下节课评讲习题和发下去的练习
